Safety of high-dose ivermectin: a systematic review and meta-analysis
J Antimicrob Chemother
Miriam Navarro 1*, Daniel Camprubı 2, Ana Requena-Mendez2, Dora Buonfrate 3, Giovanni Giorli3, Joseph Kamgno4, Jacques Gardon5, Michel Boussinesq5, Jose Munoz~2, Alejandro Krolewiecki2,6
1Department of Public Health, Science History and Gynecology, Universidad Miguel Herna ndez de Elche, Alicante, Spain; 2Barcelona Institute for Global Health (ISGlobal) Hospital Clınic – Universitat de Barcelona, Barcelona, Spain; 3Department of Infectious – Tropical Diseases and Microbiology, IRCCS Sacro Cuore Don Calabria Hospital, Negrar, Verona, Italy; 4Centre de Recherche sur les Filarioses et autres Maladies tropicales, Yaounde, Cameroon; 5Institut de Recherche pour le Developpement, Montpellier, France; 6Instituto de Investigaciones de Enfermedades Tropicales Universidad Nacional de Salta/CONICET, Ora n, Argentina
2019年11月26日受理

概要
背景
イベルメクチンは、顧みられない熱帯病を制御するための重要な駆虫薬である。集団投与によるイベルメクチンの主な適応症はオンコセルカ症とリンパ系フィラリア症であるが、疥癬、土壌伝染性蠕動、マラリアの制圧のために、より高用量の固定用量レジメンを使用することに関心が持たれている。これらの高用量レジメンの安全性データが必要である。
方法
イベルメクチンの安全性と投与量に関する系統的な文献レビューとメタアナリシスを行った。対象とした研究は患者レベルのデータを報告しており、メタアナリシスでは用量200および400 lg/kgのデータを報告している臨床試験を対象とした。有害事象の重症度と影響を受けた臓器別に比較するために、発生率比を用いた。
結果
系統的検索では6件の研究が抽出され、有害事象を経験した被験者の数には差がなかった。様々な適応症を対象としたこれらの臨床試験を記述的に分析した結果、有害事象の重症度は、イベルメクチンの標準用量(400 lg/kgまで)とそれ以上の用量の間で差がなかった。臓器系の関与では、オンコセルカ症の治療を対象とした1つの臨床試験において、高用量群で眼の事象が増加したのみで、いずれも一過性で強度は軽度から中等度であった。
結論
今回のレビューでは、高用量イベルメクチンの安全性は標準的な用量と同等であると思われるが、承認用量を超える高用量での使用を推奨するには十分なデータがない。眼の有害事象は、一過性ではあるものの、オンコセルカ症患者では懸念される。これらのデータは、プログラムマネージャーに情報を提供するとともに、イベルメクチンの使用に関する新しいアプローチを評価する際のオペレーションリサーチ活動の指針となる。
はじめに
オンコセルカ症やリンパ系フィラリア症(LF)の制圧、土壌伝染性蠕虫症(STH)やシストソーマ症の制圧を目的としたプログラムでは、罹患率や有病率が最も高い地域に安全で有効な薬剤を提供することが強力な手段であることが実証されている2-4。
イベルメクチンは、おそらく最も注目されている駆虫薬であり、その有効性と安全性から、これらの疾患の制圧に最も適したツールとなっている6。また、フィラリア線虫に対するミクロフィラリア活性だけでなく、ベンゾイミダゾール系薬剤との併用によるTrichuris trichiuraに対する顕著な活性、疥癬に対する有効性、アノフェレス蚊に対する殺虫活性によるマラリア対策への可能性など、その視野は広がっている7。 -10 Strongyloides stercoralis感染症の治療薬として選択されているイベルメクチンは、STHに対する意識の高まりとともに需要が拡大している11,12。LFの場合、アルベンダゾール、イベルメクチン、クエン酸ジエチルカルバマジンの3剤併用療法が優れた効果を示すことから、WHOの最新のLF治療ガイドラインで推奨されている13,14。
イベルメクチンの使用拡大の主な障害は、その供給量が限られていることと、ロア糸状虫との重複感染患者が経験した重篤な有害事象(脳症)であった15-17。これらの問題にもかかわらず、広く使用されているイベルメクチンは、頻度が低くほとんどが軽度の有害事象であり、非常に安全な薬剤であることが実証されている5,18。現在、イベルメクチンは、ほとんどのフィラリアおよびS. stercoralis感染症に対して150〜200 lg/kgの用量で処方されており、Wuchereria bancrofti感染症に対しては最大400 lg/kgの用量で承認されている19,20。イベルメクチンのSTHやマラリア対策などの新効能では、より高いピークを達成することで有効性を向上させたり、薬剤レベルを検出できる間隔を延長する目的で、400 lg/kgを超える用量が評価されている21。高用量イベルメクチンは、適切な安全性プロファイルを示すことができれば、わずか数回、あるいは1回のイベルメクチンの合剤投与で、大規模な人口集団を十分に治療することができる。本研究の目的は、高用量イベルメクチンの安全性プロファイルを系統的に検討し、本剤の使用拡大の可能性を探ることにある。
試験方法
本研究のプロトコルは 2017年11月11日にProspero International Prospective Register of Systematic Reviewsに登録された(CRD42017078101)。
レビューの質問は、治療期間に関わらず、200および400lg/kg/dayを超える用量で使用した場合のイベルメクチンのヒトにおける安全性を評価することであった。
検索戦略と選択基準
創刊から 2018年1月まで、複数のデータベースで系統的な文献検索を行った。以下のデータベースで関連する研究を検索した。MEDLINE (PubMed); Web of Science Core Collection; Cumulative Index to Nursing and Allied Health Literature (CINAHL data-base); Tropical Diseases Bulletin; CAB Direct; Scopus (Elsevier API); Science Direct; International Pharmaceutical Abs (Ovid); and Conference Papers Index (CSA) (ProQuest XML)である。
言語や出版状況(発表済み、未発表、出版中、進行中)にかかわらず、すべての関連研究をレビューした。また、関連する可能性のある他の研究や著者の個人的なコレクション(灰色文献)についても、すべての対象研究の参考文献リストを確認した。
検索用語
以下の3つの用語を組み合わせて検索を行った。(i)イベルメクチン、(ii)投与量400,600,700,800,高用量、高投与量、(iii)副作用、副作用。研究は、ヒトの研究のみを含むようにフィルタリングされた(Table S1, JAC OnlineでSupplementary dataとして入手可能)。最近発表されたアブストラクトや出版中の原稿の著者に連絡を取り、完全な論文を入手した。
研究の選択
2名の審査員(M.N.とD.C.)が、検索で得られたタイトルと要旨を独自にレビューし、本レビューの対象基準を満たす可能性のあるすべての研究を特定した。その後、各研究が組み入れ基準を満たしているかどうかを、適格性評価フォームを用いて独自に評価した。レビューアの間で意見が一致しなかった場合は、3人目のレビューア(A.R.-M.)が最終的な組み入れの判断を行った。除外されたすべての研究は、その理由とともに文書化された。
ヒトにおけるイベルメクチンの安全性を評価した研究は、症例対照研究を含めてすべて対象とした。高用量のイベルメクチンを他の薬剤と併用して投与したことを評価した研究については、データの分離を試みるか、研究著者に連絡して分離したデータを要求した。システマティックレビューでは、適応症にかかわらず、イベルメクチンを投与された患者に関するすべての研究を対象としたが、基礎疾患は記録した。また、免疫抑制状態の患者を対象とした研究も対象とした。さらに、高用量を投与されている被験者群と対照群(標準用量を投与されている被験者)を比較した研究を含めて、メタアナリシスを行った。
データ抽出およびデータ解析
2人の査読者(M.N.とD.C.)が、事前に作成したデータ抽出フォームを用いて独立してデータ抽出を行った。データ抽出に関して意見の相違があった場合は、2人のレビュアー間で協議して解決した。必要に応じて、第3の査読者(A.R.-M.)が、合意が得られるまで議論を進めた。抽出されたデータは、Excelデータベース(Microsoft, Redmond, WA, USA)に入力された。
研究デザイン、研究対象者(人数、患者か健常者かを含む)除外基準、統計手法に関するデータを収集した。解析は、200 lg/kgを超える用量を使用している者と400 lg/kgを超える用量を使用している者に層別して行われた。参照基準はイベルメクチンの用量が150~200lg/kgのものとした。主要評価項目は、200 lg/kg超および400 lg/kg超のイベルメクチンの有害事象を基準用量と比較した。
メタアナリシスでは、以下の情報が得られた研究のみを対象とした。メタ解析では、以下の情報が得られた研究のみを対象とした:(i)標準用量と高用量で治療した患者の絶対数、(ii)標準用量群と高用量群の両方で何らかの有害事象を経験した患者の絶対数。報告された 有害事象 は、論文中に他の原因に起因すると明確に記載されていない限り、薬剤に関連するものとした。有害事象 の種類(眼、神経、皮膚、その他の 有害事象)とグレード(軽度、中等度、重度、生命を脅かす)、イベルメクチンの適応、年齢(15 歳以上/15 歳未満)、異なる試験環境(地理的大陸別)、クリアリングドーズ(高用量投与の 3 ヶ月前に標準的な 150 lg/kg を投与、眼窩ミクロフィラリア密度が高い被験者における眼の 有害事象 のリスクを低減するため)、単回投与と複数回投与に関連して、記述的分析を行った。
品質評価
メタアナリシスの対象となった研究はすべて無作為化臨床試験(RCT)であった。これらの研究の方法論的な質は、RCT のための NICE 方法論チェックリストを用いて評価した23。バイアスの危険性があり、情報が不足している研究については、共著者に連絡して、不足しているデータの入手を試み、不明瞭な方法論を明らかにした。2名の審査員が、メタアナリシスに含まれる研究の質を独立して評価した(M.N.およびD.C.)。システマティックレビューの報告は、有害事象を含むシステマティックレビューに特化したPRISMA-harmチェックリストに従った(Table S2)。
統計解析およびデータ統合
考慮したすべての研究から、各治療群における薬物使用に関連したあらゆる 有害事象 の絶対度数を抽出した。まず、各研究において、任意の 有害事象 とイベルメクチンの高用量投与との関連について OR を算出し、それに対応する 95% CI を算出した。次に、ランダム効果を用いた Cochran-Mantel-H有害事象nszel 法を用いて、高用量投与の効果のプール推定値を求めた。また、I2やDerSimonian-Laird estimator for s2などの異質性の指標も算出した。フォレストプロットは、点推定値を95%CIとともに示すために用いられた。このようなメタアナリシスは、R バージョン 3.4.3(meta package)を用いて行った。また、有害事象 の重症度および臓器障害について投与群間で比較し、発生率比(IR)を算出した。
結果
収録試験
検索の結果、452 件の研究がヒットした(重複を除く)。著者らは、システマティックレビューに関連する情報を有する 6 つの研究を追加で確認し、適格性を評価した。239件の研究は、タイトルを読んだだけでは質問に答えられないため(他のトピックに関する研究、動物を対象とした研究、非経口イベルメクチンに関する研究)除外され、疑問が残った場合には、要旨や論文全体をスキャンした。452件の研究のうち9件が選択基準を満たした。最終的に、6つの研究がメタアナリシスの対象となった(図1)21,22,24-27。
品質評価
研究の質を評価した結果、6件の研究のうち半数は無作為化の方法が不明瞭であり22-24,十分な割り付けの隠蔽が確認されたのは3件のみであった18,24,25。18,22,24 Wimmersbergerらの研究27は単盲検RCTであり、残りの2つの試験は非盲検RCTであった(Dembele et al 24およびMunoz~ et al 22)。したがって、被験者の介入や他の交絡因子、予後因子に対する治験責任者の盲目性に起因するバイアスのリスクを考慮する必要がある。また、22,24研究のうち2つの研究では、参加者の割付に対する盲目性の欠如が検出された。
図1.系統的文献検索のPRISMAフロー図。IVM, イベルメクチン
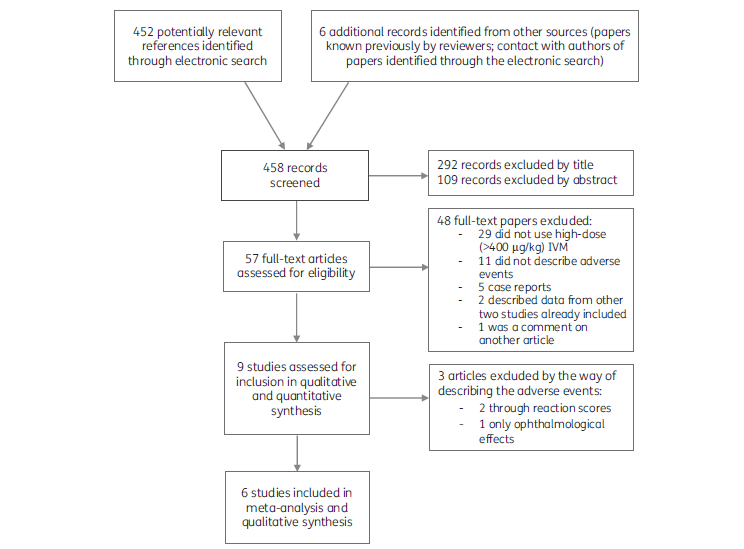
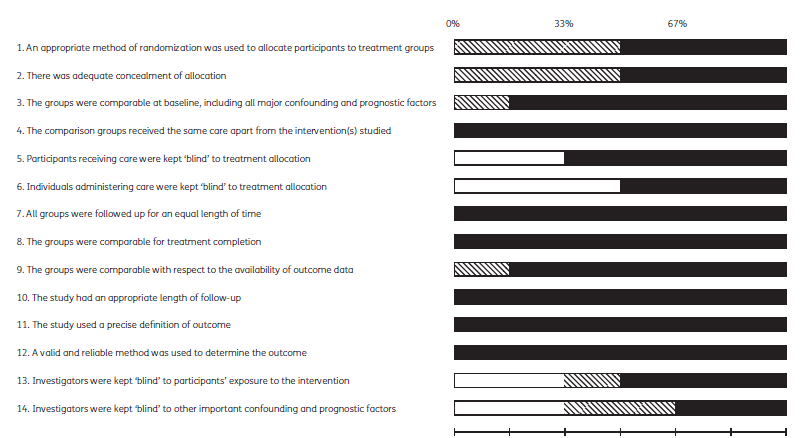
図2 NICE Methodology Checklist for RCTを用いたメタアナリシスに含まれる研究の質の評価。白は「いいえ」、縞模様の線は「不明」、黒は「はい」
1. 治療群への参加者の割り振りに適切な無作為化法が用いられている。
2. 割り付けの隠蔽が適切であった
3. すべての主要な交絡因子および予後因子を含めて、ベースラインで両群が比較可能であった。
4. 比較群は、研究された介入以外に同じケアを受けていた。
5. 治療を受けている参加者は、治療の割り当てについて「盲目」であること
6. ケアを実施する個人は、治療の割り当てについて「盲目」にされていた
7. すべてのグループが同じ期間、追跡調査を受けた
8. 治療完了までの期間が各群で同等であること
9. 結果データの入手可能性に関して、各グループが同等であった
10. フォローアップ期間が適切である
11. 正確なアウトカムの定義がなされている
12. 結果を決定するために、有効で信頼できる方法を用いた
13. 研究者は参加者が介入にさらされることを「見えない」ようにした
14. 研究者は他の重要な交絡因子や予後因子を「見えない」ようにした。
研究グループ間で受けたケアやフォローアップの長さについては、対象となった原稿のいずれにもバイアスのリスクは検出されなかった。すべての論文において、治療完了は研究グループ間で同等であった。対象となったすべての研究は、正確な結果の定義と、結果を決定するための信頼できる方法を用いていた。選択的報告バイアスのリスクについては、データが不明確なものを除き、すべての論文で結果データは研究グループ間で比較可能であった26。全体的なバイアスのリスクは、図2に示すようにグラフ化されている.
記述的解析
メタアナリシスに含まれた 4 件の試験のうち、400 lg/kg までの用量またはそれ以上の用量のものについて、有害事象 の総数、重症度、および特定の器官系への関与についても分析した(表 1).健康なボランティアを含む多様な適応症の試験を対象とした本解析では、高用量群には800 lg/kgまでの用量が含まれていた。試験参加者は複数の有害事象を経験する可能性があるため、イベルメクチンの安全性プロファイルにおいて、文献に最も頻繁に記載されている特定の器官系(眼、神経、皮膚)の関与を評価するためにIRを算出したところ、オンコセルカ症の治療を目的とした1つの臨床試験26において、眼系に関する有害事象が有意に増加したことが明らかになった(IR 2.797、95%CI:1.226-6.377)。本試験で評価した眼系有害事象は、一過性の目のかすみ、目のかゆみや痛み、色覚異常などの眼の自覚症状であった。有害事象 の重症度をみると、すべての試験で、標準投与群、高用量投与群ともに 100%が軽度または中等度と報告されており、生命を脅かすとされる重篤な 有害事象 は、標準投与群で 1 例(アナフィラキシー反応)高用量投与群で 1 例(心電図における QTc 延長、併用薬に起因する可能性が高い)が報告されたのみであった21。治療を受けた患者/被験者の年齢は2歳から60歳までで、1つの試験は小児(2~12歳)残りは成人(18歳以上)を対象に実施された。治療前にイベルメクチン150mgの清涼剤を投与した研究は1件のみであった26。
メタアナリシス
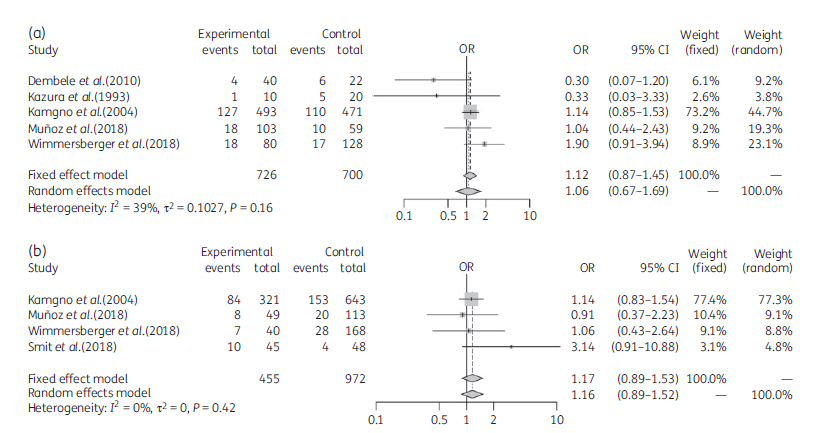
合計6つの研究が、異なるメタアナリシスの対象となった。1993年から 2018年の間に発表された5つの研究が、400 lg/kgをカットオフとしてメタ解析に含まれ、中程度のヘット不均一性(I2 = 39%)が認められた22,24-27。ランダム効果モデルは1.06(95% CI 0.67-1.69)で、研究群間に差がないことが示された(図3a)。次に、200 lg/kgまでのイベルメクチン投与量とそれ以上の投与量を比較するために、メタアナリシスを繰り返した。この場合、4つの研究21,22,26,27が含まれており、固定効果モデルとランダム効果モデルの両方によると、試験群間でORに差がないという結果が得られた。この場合、ran-dom-effectsモデルは1.16(95%CI 0.89-1.52)で、ヘット相異性は非常に低いものであった(図3b)。
考察
本研究では、ヒトにおいて経口投与により標準的なレジメンよりも高い1日投与量で使用した場合のイベルメクチンの安全性について述べている。文献のシステマティックレビューとメタアナリシスを用いた方法論により、健康なボランティアを含む異なる基礎的な臨床条件を用いて発表された異なる試験の比較と共同分析が可能となった。
図 1. 標準用量(400 lg/kgまで)と高用量(400 lg/kg以上)のイベルメクチンを比較した臨床試験における、臓器および器官別のイベルメクチンの有害事象の記述的解析
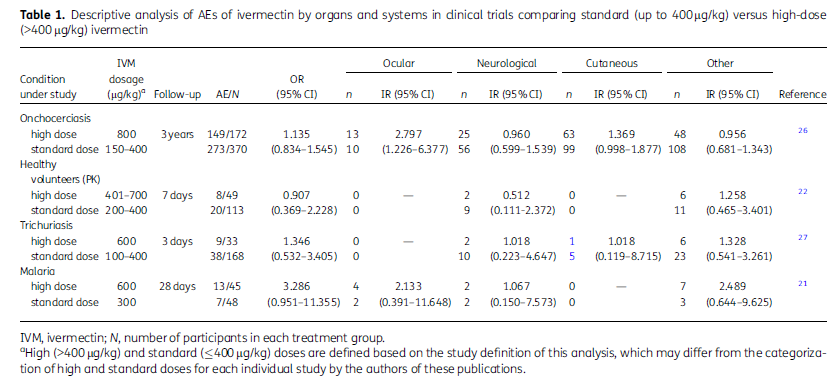
図3 標準投与量400 lg/kg(a)または200 lg/kg(b)を基準とした、有害事象と標準投与量および高投与量のイベルメクチンとの関連性に関するメタアナリシス
本試験の目的は、高用量のイベルメクチンの安全性プロファイルを理解し、より高い有効性を得るために、あるいは現在推奨されている体重ベースのアプローチに代わる投与法として固定用量での使用を検討できるようにすることであったため、比較対象としては、高用量の安全性をプラセボや無治療と比較するのではなく、よく知られている通常用量(400 lg/kgまで)での安全性を選択した。この方法では、固定用量のレジメンではlg/kgのイベルメクチンを変動させることになるため、かなりの割合の人が通常のレジメンよりも高い用量にさらされることになる。そのため、薬剤耐性の出現を予防する上で利点となりうる高用量の安全性を正しく理解する必要がある28。
メタアナリシスの目的で、治療レジメンは2つのアームに分類されたが、「高用量」アームには幅広い用量が含まれていることを考慮する必要がある。イベルメクチンの用量増加の影響をさらに解析することはできなかったが、ここでの結果は、用量の 増加に伴って 有害事象 が増加する傾向を示唆するものではなかった。オンコセルカ症患者を対象とした 1 件の研究では、イベルメクチンの高用量投与群で 有害事象 のリスクが高いことが示された 26 が、その後の解析では、これらの 有害事象 をミクロフィララエミアや疾患関連病変と関連付けることはできなかった29 。最も一般的な訴えは、一過性の目のかすみ、目のかゆみや痛み、スコトーマや閃光を見ることであり、いずれも数日間で徐々に消失した。これらの結果は、基礎疾患の種類と重症度がイベルメクチンの安全性を決定する最も関連性の高い変数であると結論づけた過去の報告と一致している30。また、オンコセルカ症患者71名を対象に、投与後24時間および48時間の血清中イベルメクチン濃度と症状との関連性を検討した結果、イベルメクチンの安全性プロファイルおよび症状は、一般的に用量とは無関係であることが示された31。オンコセルカ症の治療を目的とした臨床試験では、イベルメクチンを800 lg/kgまで増量することで、有効性と安全性の両方において同等の結果が得られた32。なお、5万人を超える治療対象者に130~200 lg/kgを投与した大規模なオンコセルカ症の介入試験では、ミクロフィラリアの負荷を補正した後の全反応の発生率とイベルメクチンの投与量との間に統計学的に有意な関係が認められたが、中等度および重度の反応についてはそのような関係はなかった33。また、レビュー対象となった試験の数が限られていたため、サブ解析(例えば、有害事象 発現における基礎疾患の影響の可能性や、試験の地理的位置の評価など)を実施することができなかった。
今回の知見は、試験数が少なく、盲検化が行われていないという制限はあるものの、800 lg/kg までの用量のイベルメクチンの安全性を示す証拠となった。このメタアナリシスでは、W. bancrofti 感染症では 400 lg/kg が MDA キャンペーンに使用されていることから、最高の標準用量として 200 lg/kg と 400 lg/kg を用いて別々の解析を行った。驚くべきことに、本解析の対象となった最大の研究であるオンコセルカ症患者を対象とした研究では、患 者の臓器別に分類された未発表のデータが記載されており、その結果、視覚に影響を及ぼす事象の IR は 2.80(95% CI:1.23~6.38)と高かった(表 1).全身、神経、皮膚に分類された事象は、各群間で有意な頻度の増加は認められなかった。今回の解析対象となった他のすべての試験では、群間で視覚障害のリスクが統計的に有意に増加することはなかった。いくつかの自覚的な眼のトラブル(一過性の目のかすみ、目のかゆみや痛み、色覚異常)が現れたが、重度の有害事象を発症した患者はおらず、有害反応のために試験を中止した患者もいなかった。これらの結果は、LF 治療における 有害事象 を評価した研究の最近のレビューと一致しており、毒性に最も関連する変数は薬剤や用量ではなく、ミクロフィララレミアのレベルであることが確認された30。
イベルメクチンは30年以上にわたって十分に使用されており、年間3億人以上が使用していることから、MDAキャンペーンでの使用を通じて、発展途上の世界で最も関連性の高い公衆衛生介入の一つとなっている36。これらの集団では安全性に関するデータが不足しているため、MDAキャンペーンの対象外となっている。しかし、最近発表されたT.trichiura感染症に対してイベルメクチンを投与した小児のPKデータでは、同用量の200 lg/kgを投与した成人よりも低い曝露プロファイルが示されており、この年齢層ではより高用量の投与が必要であることが示唆されている37。国際的なファーマコビジランスシステムのデータベースを用いた最近の分析では、L. loa 感染症では、通常の用量でも神経系の重篤な 有害事象 はまれであるが、これらの 有害事象 の他の危険因子に関する研究が必要であると結論付けられている38. イベルメクチンの PK/薬力学パラメータの理解に関連するその他の側面として、PK パラメータ(主に Cmax)と毒性の発現との関係がある.本試験では、薬物曝露に関連するパラメータ(AUC及びCmax)は、高い個体間変動係数(CV)(それぞれ37.4%及び32.5%)及び個体内変動係数(それぞれ39.6%及び33.2%)を示した22 。従って、純粋に用量と有害事象の関係に基づいた試験の結果及び結論には限界がある。
本試験では、分析単位としてイベルメクチンの複数日の累積投与量ではなく 1 日の投与量を用いたが、このアプローチは、600 lg/kg までの 3 回の連日投与におけるイベルメクチンの 1 日の Cmax の変動が少ないことに基づいている39。
結論
メタアナリシスを含む本システマティックレビューでは、800 lg/kg までのイベルメクチンを単回投与した際の 有害事象 は、現在承認されている通常用量での 有害事象 と比較して、頻度や強度に大きな違いはないことが示された。眼の症状は、一過性ではあるものの、オンコセルカ症の患者では懸念されており、その適応症でイベルメクチンを高用量で使用する場合には注意が必要であり、さらなる検討が必要である。レビューされた試験で報告された有害事象の多くは軽度または中等度であり、イベルメクチンの安全性が示唆された。そのため、イベルメクチンに関連する 有害事象 の管理について MDA キャンペーンに参加するプログラムや医療従事者に適切な情報を提供するために、他のグループ30 が提案しているように、安全性データの適切かつ標準的な報告方法についてコンセンサスを得ることが必要である.結論として、高用量でのイベルメクチンの安全性、体重15 kg未満の小児および妊婦を対象とした安全性を評価する臨床試験がさらに必要である.
