Contents
Safety and efficacy of artemisinin-piperaquine for treatment of COVID-19: an open-label, non-randomised and controlled trial
www.ncbi.nlm.nih.gov/pmc/articles/PMC7605811/
2020年11月2日
要旨
背景
コロナウイルス感染症2019(COVID-19)に有効な治療法はない。
方法
COVID-19が確認された患者41人が本試験に登録され,アルテミシニン-ピペラキン(AP)投与群(n = 23)と対照群(n = 18)の2群に分けられた。主要アウトカムは、重症急性呼吸器症候群-コロナウイルス-2(SARS-CoV-2)の検出不能レベルに達するまでの時間と、7日目、10日目、14日目、28日目に検出不能レベルのSARS-CoV-2が検出された参加者の割合であった。副次的転帰として,10日以内のCT(コンピュータ断層撮影)画像の変化,補正されたQT間隔の変化,有害事象,臨床検査値の異常を評価した。
結果
未検出のウイルスRNAに到達するまでの平均時間(平均±標準偏差)は、AP群で10.6±1.1日(95%信頼区間[CI]8.4~12.8)対照群で19.3±2.1日(95%CI 15.1~23.5)であった。7日目、10日目、14日目、21日目、28日目にウイルスRNAが検出されなかった割合は、AP群で26.1%、43.5%、78.3%、100%、対照群で5.6%、16.7%、44.4%、55.6%、72.2%であった。治療後10日以内のCT撮影では、群間の有意差は認められなかった(P>0.05)。両群とも軽度の有害事象は認められた。
結論
軽度から中等度のCOVID-19を有する患者では、検出不能なSARS-CoV-2に到達するまでの時間は、AP群では対照群に比べて有意に短かった。ただし、医師はAPを使用する前にQT間隔の変化を考慮すべきである。
キーワード
アルテミシニン、ピペラキン、COVID-19,抗マラリア薬、SARS-CoV-2
1. はじめに
コロナウイルス病2019(COVID-19)は、重症急性呼吸器症候群コロナウイルス2(SARS-CoV-2)による感染症である。2020年4月23日までに全世界で255万人の確定症例と179千人の死亡が確認されている。累積確定症例数は1,200万人を超え、死亡者数は2020年7月09日までに54万人を超えた[1]。
いくつかの研究では、COVID-19の潜伏期間は最初の接触から3~7日であると報告されている[2,3]。中国の「新型コロナウイルス肺炎診断・治療計画(トライアル第7版)」によると、COVID-19患者は通常、症状に基づいて軽症、中等症、重症、重症に分類されている。COVID-19の可能性のある薬剤の臨床試験が多数実施されている。抗ウイルス療法、細胞療法、免疫療法、漢方薬などの様々な治療法が様々な有効性を示しているが、本稿執筆時点では、COVID-19の治療薬としてFDAによって承認された薬剤や生物製剤はない[4]。ロピナビルやリトナビルなどの抗ウイルス薬は、標準治療よりも優れた抗ウイルス効果を示していない[5]。抗マラリア薬のクロロキンとヒドロキシクロロキンの使用は議論の的となっている。いくつかの臨床試験では、ヒドロキシクロロキンはCOVID-19の治療に失敗したことが示されている[6]。国立衛生研究所は、無害ではあるが、この薬剤は効果がないと報告されているため、ヒドロキシクロロキンを含む臨床試験の中止を勧告している[7]。しかし、中国からの研究では、中国のCOVID-19患者においてクロロキンの有効性と安全性が実証されている[8]。フランスの研究では、ヒドロキシクロロキンがCOVID-19患者のウイルス負荷を有意に低下させ、アジスロマイシンとの相乗的相互作用を示したことが報告されている[9]。研究者たちは、ワクチンがこのパンデミックを抑えるのに役立つと楽観視しているが、ワクチンの開発サイクルは長く、時間がかかる [10,11]。
COVID-19特異的治療法の開発を早急に進めることに加えて、他の治療戦略も試験されるべきである。そのような治療戦略の一つに、すでに異なる適応症で使用されている薬剤の使用がある。アルテミシニンとピペラキン(AP)は、新世代のアルテミシニン併用療法(ACT)をベースとした抗マラリア薬である。第一選択抗マラリア薬であるアルテミシニンおよびその誘導体は、強力な抗マラリア薬であるだけでなく、かなりの抗ウイルス特性を有している[12,13,14]。アルテミシニンは、B型肝炎ウイルス[15]、C型肝炎ウイルス[16,17]、およびヒト免疫不全ウイルス[18,19]の増殖を減少させることが報告されている。ピペラキンは、クロロキンと同様のビスキノリン系抗マラリア薬である。ピペラキンは1960年代に中国で初めて合成され、以来、中国を中心に広く使用されている。クロロキンは忍容性が高いだけでなく、ファルシパルム原虫やビバックス原虫に対しても同様の効力を持っている[20]。クロロキンは中東呼吸器症候群や非定型呼吸器症候群(SARS)の治療薬として報告されている[21]。さらに、試験管内試験実験では、クロロキンがSARS-CoV-2に対して阻害作用を有することが示されている[22]。APは第4世代のACTであり、マラリアの予防・治療に欠かせない役割を果たしている。APがCOVID-19も治療すれば、多くの国、特にマラリアの影響を受けている発展途上国が恩恵を受けることになる。
2. 方法
2.1. 研究デザイン
本試験は、武丹江医科大学附属紅旗病院の倫理委員会で承認された(登録番号:20214)。試験計画書と申請書類は、中国臨床試験登録センターにオンライン登録のために提出された(登録番号:ChiCTR2000033049)。本試験は当初、軽度から中等度のCOVID-19患者に対するAP錠の有効性と安全性をヒドロキシクロロキンと比較して比較することを目的とした非盲検、無作為化、並行群間比較試験であった。中国ではこのパンデミックが急速に抑制されていたため、患者数が試験要件を満たしていなかった。そのため、本試験は対照臨床試験に変更され、同期間に実施された。SARS-CoV-2感染が確認された患者を2群に分けた。第1群はAP錠、第2群は対照群とし、抗ウイルス剤および対症療法としてヒドロキシクロロキン/アルビドールを投与した。
2.2. 患者
除外基準は以下の通りである。1)年齢18歳以上、2)リアルタイム逆転写酵素ポリメラーゼ連鎖反応(RT-PCR)により上気道検体のSARS-CoV-2感染が確認されたこと、3)インフォームド・コンセント用紙への署名。
除外基準は以下の通り。1)年齢18歳未満、2)妊娠、3)重度の悪性腫瘍、心臓・肝臓・腎臓疾患または代謝管理不良の疾患、4)4-アミノキノリンに対するアレルギー、5)血液系疾患、6)不整脈または慢性心疾患、7)網膜疾患または難聴、8)精神疾患または皮膚疾患(発疹、皮膚炎、乾癬を含む)。
COVID-19の患者は、中国の「新型コロナウイルス肺炎診断・治療計画(トライアル第7版)」に従って以下のように分類された。
軽度:臨床症状が軽度でCT画像に肺炎症状が認められない、中等度:発熱、咳嗽、呼吸器症状等の症状があり、CT画像に肺炎症状が認められる。
2.3. 治療法
APグループ。抗ウイルス・対症療法としてAP(アルテファーム株式会社)を使用した。APは初日に2錠(アルテミシニン125mg、ピペラキン750mg)をローディング用量として経口投与し、その後6日間は1日1錠(アルテミシニン62.5mg、ピペラキン375mg)を維持用量として経口投与した。総投与量は7日間で8錠とした。
対照群とした。ヒドロキシクロロキン/アルビドールは、中国の「新型コロナウイルス肺炎診断・治療計画(第7版試行)」によると、抗ウイルス・対症療法として主に使用された。ヒドロキシクロロキン硫酸塩(上海中西製薬有限公司)を最初の3日間はローディング用量として800mg/日を経口投与し、その後5日間は維持用量として400mg/日を経口投与した。アルビドール塩酸塩(CSPC応益製薬株式会社)を600mg/日を1日3回に分けて8日間経口投与した。
薬物投与終了時に陽性の患者は対症療法を継続し、2回連続で核酸検査が陰性となった時点で退院条件を満たした。退院後は全例を14日間隔離して観察した。検査が陰性のままであれば検疫制限は解除された。
2.4. 評価
重点検査指標:各患者から毎日上気道検体を採取し、現地の疾病対策センターまたは病院でSARS-CoV-2のRT-PCRを実施した。RT-PCR試験キット(BioGerm社)[23]は、SARS-CoV-2核酸のORF1ab/N遺伝子を検出することができ、遺伝子検出の基準平均Ct値は38であった。RT-PCRのFAMチャンネル、HEX/VICチャンネル、ROXチャンネルについては、両チャンネルのCt値が38以下であれば陽性、そうでなければ陰性であった。疫学的特徴、臨床症状、徴候、有害事象は症例報告書を用いて記録した。臨床的特徴、臨床検査所見、胸部CT検査データは症例報告書と院内症例報告システムに記録した。SARS-CoV-2 RNA が 2 回連続で陰性であった患者は 14 日間隔離された。
結論は、専門の画像診断医が撮影前と撮影後の画像を比較して導き出した。主な解析基準は、各CT画像上の罹患葉数、地殻結節の存在、パッチ状/パンク状の地殻不透明度、パッチ状の圧密、繊維状の縞模様、不規則な固形結節の有無であった[24]。
‘未検出ウイルスRNAまでの時間’は、薬剤投与の初回投与からSARS-CoV-2のRT-PCRが初めて陰性となるまでの時間と定義した。薬剤投与中の7日目、10日目、14日目、21日目、28日目のRT-PCRによるSARS-CoV-2の未検出率、10日以内のCT画像結果、臨床検査値異常指数、有害事象を2つの治療法間で比較した。APの安全性を評価するために、心電図(日本製光電心電計ECG-1250C 6チャンネル自動解析12リード)を用いてAP群の治療前と3~8日後のQT変化をモニターした。QTcのアルゴリズムはBazettの式で補正した。
QTc=QT/(RR∧0.
2.5. 統計解析
質的指標は、記述的統計分析のためにパーセンテージまたは構成比で記述し、量的指標は平均と標準偏差で記述した。質的データについては、χ2,フィッシャーの厳密確率法、Wilcoxon ランクサム検定を用いた。量的データは t 検定で正規分布に適合し、Wilcoxon 位相和検定では正規分布に適合しなかった。仮説検定は一様に両側検定を用いた。P値<0.05は統計的に有意と考えられる。全体的な陰性転換確率は、患者が検出不能なウイルスRNAレベルに達するまでに要した時間を分析することにより推定した。これにはKaplan-Meier法が用いられ、所見は対数順位検定で比較された。統計解析の実行にはSPSS19.0を使用した。
3. 結果
3.1. 参加者のベースライン情報
AP群に受け入れられた25名の患者のうち、23名(92%)が治療を完了し、最終解析に含まれた。同様に、対照群22人の患者のうち、18人(82%)が治療を完了し、最終解析に含まれた(図1)。患者の人口統計学的ベースラインデータと臨床的特徴を表1
にまとめた。AP群と対照群の平均年齢はそれぞれ42.7歳と45.8歳であった。AP群では82.6%、対照群では88.9%の患者が中等度のCOVID-19と診断され、残りは軽度のCOVID-19であった。両群の患者は臨床的特徴の点で比較的バランスが取れており、臨床検査指標も有意差は認められなかった(P>0.05)。
図1 研究のフローチャート

表1 患者のベースラインの人口統計学的および臨床的特徴
| 特徴a | AP(n = 23) | コントロール(n = 18) | P値 |
|---|---|---|---|
| 年齢(年) | 42.7±11.8 | 45.8±16.3 | 0.472 |
| 男性(%) | 9(39.1) | 6(33.3) | 0.754 |
| 病気の重症度(%) | |||
| 軽度 | 4(22.2) | 2(1.1) | 0.679 |
| 中程度 | 19(82.6) | 16(88.9) | 0.679 |
| 共存条件(%) | |||
| 高血圧 | 5 | 6 | 0.489 |
| 糖尿病 | 3 | 4 | 0.679 |
| その他 | 5 | 5 | 1.000 |
| バイタルサイン | |||
| 体温(°C) | 36.6±0.5 | 36.8±0.7 | 0.321 |
| 呼吸数(呼吸/分) | 19.3±2.0 | 18.8±1.7 | 0.345 |
| 脈拍(拍/分) | 89.7±17.0 | 87.5±14.5 | 0.658 |
| 収縮期血圧(mmHg) | 136.5±20.6 | 143.7±25.0 | 0.319 |
| 拡張期血圧(mmHg) | 88.1±17.1 | 91.5±12.2 | 0.460 |
| 症状 | |||
| 呼吸困難 | 0 | 1 | 0.439 |
| 味覚障害 | 0 | 1 | 0.439 |
| 熱 | 3 | 7 | 0.075 |
| 咳 | 6 | 8 | 0.322 |
| 喀痰の生産 | 3 | 4 | 0.679 |
| 倦怠感 | 0 | 1 | 0.439 |
| 咽頭痛 | 1 | 3 | 0.303 |
| 咽頭炎 | 3 | 1 | 0.618 |
| 胸の圧迫感 | 0 | 3 | 0.077 |
| めまい | 1 | 0 | 1.000 |
| 筋肉痛 | 2 | 2 | 1.000 |
| 不眠症 | 3 | 1 | 0.618 |
| 鼻詰まり | 0 | 2 | 0.187 |
| 下痢 | 0 | 2 | 0.187 |
| 実験室パラメータ | |||
| アラニンアミノトランスフェラーゼ(U / L) | 24.48±14.00 | 28.83±21.31 | 0.436 |
| アスパラギン酸アミノトランスフェラーゼ(U / L) | 19.39±5.17 | 20.78±7.38 | 0.484 |
| 乳酸デヒドロゲナーゼ(U / L) | 171.43±41.71 | 179.94±40.66 B | 0.523 |
| 白血球数(×10 ^ 9 / L) | 6.41±1.71 | 5.99±1.84 | 0.457 |
| 好中球数(×10 ^ 9 / L) | 3.87±1.39 | 3.97±1.38 | 0.825 |
| リンパ球数(×10 ^ 9 / L) | 1.97±0.60 | 1.84±0.81 | 0.555 |
| ヘマトクリット | 0.42±0.04 | 0.39±0.05 | 0.014 |
| 血小板数(×10 ^ 9 / L) | 262.00±81.31 | 264.89±83.67 | 0.912 |
| 総ビリルビン(μmol/ L) | 16.91±6.69 | 13.12±4.95 | 0.052 |
| 尿素(mmol / L) | 3.96±0.73 | 3.77±1.37 | 0.601 |
| クレアチニン(μmol/ L) | 58.75±10.09 | 54.27±12.76 B | 0.612 |
| 尿酸(μmol/ L) | 331.17±87.98 | 278.06±95.72 | 0.072 |
| クレアチンキナーゼ(μmol/ L) | 72.22±42.71 | 54.50±33.29 | 0.241 |
| ミオグロビン(ng / mL) | 31.29±10.85 | 36.58±11.95 | 0.146 |
| トロポニン1(μg/ L) | 0.63±0.18 | 0.53±0.22 | 0.111 |
略語 AP、アルテミシニン-ピペラキン;コントロール、ヒドロキシクロロキン/アルビドール
a±値は平均値±SD。
b乳酸脱水素酵素、クレアチニンは5.6%(1/18)のデータが欠落している。
ウイルスに特異的な効果があることを証明する治療法がなかったため、倫理的要件に基づき、表2に示すリストに示すように、他の薬剤が臨床的に使用されてきた抗ウイルス効果を阻害する可能性がある。他の抗ウイルス剤の列挙は事実に基づいたものであり、有効性を評価する上で避けられない要因に影響を与える可能性がある。インターフェロンα-1b,リバビリン,ロピナビル,オセルタミビル,キャリマイシンはCOVID-19患者に一定の影響を及ぼす可能性があったが,両群間に有意な統計的差は認められなかった(P>0.05).本試験では対症療法として漢方薬を使用したが,両群間に有意差は認められなかった(P=0.030).
表2 両群の他の抗ウイルス治療法
| 治療N(%) | AP(n = 23) | コントロール(n = 18) | P値 |
|---|---|---|---|
| インターフェロンα-1b | 12(52.2) | 6(33.3) | 0.343 |
| ヒドロキシクロロキン | 0(0) | 5(27.8) | 0.011 |
| アービドール | 0(0) | 15(83.3) | <0.001 |
| カリマイシン | 0(0) | 3(16.7) | 0.077 |
| オセルタミビル | 2(8.7) | 0(0) | 0.495 |
| リバビリン | 7(30.4) | 2(11.1) | 0.254 |
| ロピナビル | 2(8.7) | 0(0) | 0.495 |
| LianhuaQingwenカプセル | 18(78.3) | 12(66.7) | 0.489 |
| ハーブ | 23(100) | 14(77.8) | 0.030 |
略語 AP、アルテミシニン-ピペラキン;対照、ヒドロキシクロロキン/アルビドール。
3.2. SARS-CoV-2 RNAの検出不能レベルに到達するまでの全時間
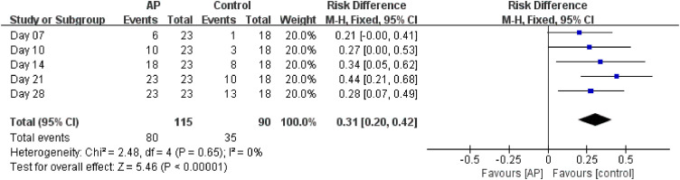
AP群のSARS-CoV-2 RNAが未検出になるまでの平均時間は、対照群に比べて有意に短かった(AP:10.6±1.1日(95%CI 8.4~12.8)対照群:19.3±2.1日(95%CI 15.1~23.5))。(P = 0.001 )であった(図 2 )。薬剤投与7日目,10日目,14日目,21日目,28日目にSARS-CoV-2が検出されなかった患者の割合は,AP群ではそれぞれ26.1%,43.5%,78.3%,100%,100%であったが,対照群ではそれぞれ5.6%,16.7%,44.4%,55.6%,72.2%であった(表3).これらのデータを解析した結果、AP群のSARS-CoV-2 RNAの消失率は対照群に比べて有意に高かった(RD = 0.28;95%CI 0.07-0.49)(図3 )。入院期間はAP群が13.3±4.8日,対照群が21.3±9.1日であった(表3).COVID-19の重症型に進行した患者はいなかった。
図2 異なる治療群における検出不能なウイルスRNAレベルを達成するのに要した時間のカプラン-マイヤー曲線

表3 患者におけるウイルスRNAの未検出までの時間。
| AP(n = 23) | コントロール(n = 18) | P値 | |
|---|---|---|---|
| 検出できないウイルスRNAまでの日数(平均±SD) | 10.6±1.1 | 19.3±2.1 | <0.005 |
| ウイルスRNAが検出されない患者、N(%) | |||
| 7日目 | 6(26.1) | 1(5.6) | 0.112 |
| 10日目 | 10(43.5) | 3(16.7) | 0.095 |
| 14日目 | 18(78.3) | 8(44.4) | 0.049 |
| 21日目 | 23(100.0) | 10(55.6) | <0.005 |
| 28日目 | 23(100.0) | 13(72.2) | 0.011 |
| 入院期間(日数、平均±SD) | 13.3±4.8 | 21.3±9.1 | <0.005 |
略語 AP、アルテミシニン-ピペラキン;対照、ヒドロキシクロロキン/アルビドール。
図3 異なる治療群における検出不能なウイルスRNAレベルを達成するのに要した全体の時間
3.3. CTイメージング
治療前、AP群の82.6%(19/23)対照群の83.3%(15/18)の患者の肺には目に見える炎症が認められた。患者のCT画像の変化を10日以内に分析した。CT画像の改善はAP群患者の36.8%(7/19)対照群患者の46.7%(7/15)に認められた。AP群では21.1%(4/19)対照群では6.7%(1/15)の患者で有意な変化は認められなかった。増悪はAP群患者の10.5%(2/19)対照群患者の13.3%(2/15)に認められた。AP群では31.6%(6/19),対照群では33.3%(5/15)の患者が10日以内に再検査を受けなかった(表4)。
表4 患者のCT画像の変化
| グループ/ケース | 前 | 後(≤10日) | |||
|---|---|---|---|---|---|
| 改善 | 大きな変化はありません | 悪化 | レビューなし | ||
| AP | 19 | 7 | 4 | 2 | 6 |
| コントロール | 15 | 7 | 1 | 2 | 5 |
略語 AP、アルテミシニン-ピペラキン;コントロール、ヒドロキシクロロキン/アルビドール。
aAP群:有意な炎症反応が認められなかった4例、対照群:有意な炎症反応が認められなかった2例、未記録の1例。
bフィッシャーの厳密確率法によるχ2検定では、P=0.669,有意な群間差は認められなかった。
3.4. 安全性の解析
副作用は両群とも軽度であり、治療後は速やかに消失した。副作用が発現したのはAP群3例(13%)対照群3例(17%)であり、AP群では吐き気、筋肉痛、倦怠感などが、対照群では吐き気、発疹などが発現した。副作用は、AP群では吐き気、筋肉痛、倦怠感など、対照群では吐き気、発疹、そう痒感などであった。AP群では、3名の患者さんでアラニンアミノトランスフェラーゼ(ALT)値>80 U/L、1名の患者さんでアスパラギン酸アミノトランスフェラーゼ(AST)値>60 U/Lでした。対照群では、2人の患者でALT値>80 U/L、1人の患者でAST値>60 U/Lであった。
AP群17例の心電図の結果、QTc間隔の平均値は治療前411.94ms、治療3~8日後433.59msであった。平均延長は治療後21.65ms(95%CI 3.58~39.71ms)であった。延長の程度が異なる患者は12人(70.59%)であった:軽度の延長(30ms未満)が6人(35.29%)中等度の延長(30~60ms)が4人(23.53%)重度の延長(>60ms)が2人(11.76%)であった。さらに、対をなす標本のt検定では、グループ間で有意な差が認められた(P < 0.05)(図4 )。
図4 アルテミシニン-ピペラキン群における補正後QT間隔変化の心電図モニタリング。
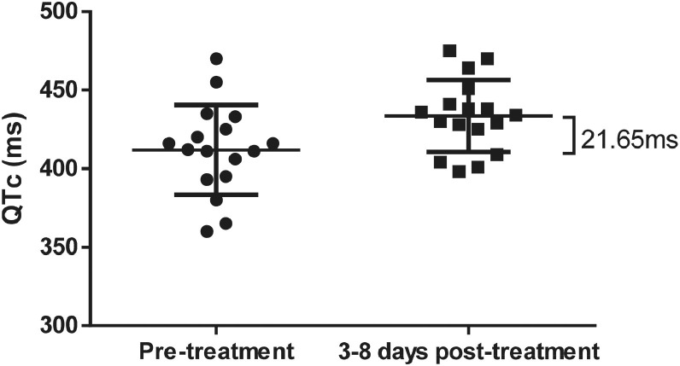
*アルテミシニン-ピペラキン(AP)群では,治療前と治療後3~8日の間に有意差が認められた(P = 0.011).
AP治療は患者にTdPやその他の不整脈を引き起こさなかった。QT 間隔が延長した患者は、治療中止後に正常に戻った。対照群の患者の心電図変化は収集されず記録されなかった。
4. 考察
本研究は、サンプル数の不足や試験デザインの不備など様々な制約があるが、喫緊の治療ニーズに応えるため、研究データを公開することとした。
AP治療において、アルテミシニンは経口吸収が速く完全であり、分布が広く、排泄が速く、半減期が短い(1.93時間)ことが報告されている[25]。しかし、ピペラキンは半減期が長く(11.7日)排泄速度が遅い[26]。APの連続投与により毒性が生じ、QT延長を引き起こす可能性がある[27]。そのため、最初に2錠を投与した後、副作用を最小限に抑え、アルテミシニンの効果を最大限に発揮させるために、1日1錠を選択した。
COVID-19患者の漢方薬であるLianhua QingwenやHuoxiang Zhengqiを用いた治療は、重篤な副作用を伴わずに患者の症状を有意に緩和し、予後を改善するが、ウイルスアッセイ所見に有意に寄与することは確認されていない[28,29,30]。このことを踏まえ、本研究では、APがSARS-CoV-2の未検出値に到達するまでの時間を有意に短縮できることに焦点を当てた。漢方薬などの対症療法手段を用いたため、臨床症状の改善については、それ以上の解析や推論は行われなかった。
COVID-19は飛沫、汚染された手や表面を介して人から人へと伝播する。SARS-CoV-2の潜伏期間は2~14日である。ほとんどの研究で推定されているこのウイルスの拡散指数は2.24~3.58で、SARSよりもわずかに高い[31]。COVID-19は軽症から重症に急速に進行する可能性がある[32]。隔離、隔離、社会的疎外、コミュニティの封じ込めなどの伝統的な公衆衛生対策は、このパンデミックを抑制する上で効果的である [33]。
この研究では、APはウイルスが体内に留まる時間を短縮することがわかった。AP服用後10日以内のCT画像検査の結果では、対照群と同様の肺の改善効果が認められた。有効な抗ウイルス薬がないため、軽度から中等度のCOVID-19患者にはAPを7日間で8錠使用することが推奨されている。また、医療施設のない地域では、患者の状態が悪化した場合には、隔離・隔離期間中もAPの使用が推奨される。COVID-19の密接な接触が疑われる患者には、予防的治療としてAP(7日以内に8錠)の投与が推奨されている。
SARS-CoV-2は内皮に直接感染し、免疫細胞の勧誘を引き起こし、その結果、広範な内皮機能障害とアポトーシスを引き起こす。これらの症状は血液をより粘性のあるものにし、血栓の形成につながる[34]。研究によると、マラリアに対するAPの成人への投与量は4錠(アルテミシニン250mgとピペラキン1500mg)で構成されており、一部の人ではQT間隔が延長することが示されている[35]。COVID-19の治療のためのAP成人の総推奨用量は8錠(アルテミシニン500mgとピペラキン3000mg)である。今回の研究では、2人の患者(11.76%)で重度の延長が認められ、2群間で有意差が認められた。AP治療は患者によってはQT間隔の延長を引き起こす可能性があるが、TdPやその他の不整脈を引き起こすことはなかった。また、QT間隔が延長した患者は、薬剤の投与を中止すると正常に戻った。しかし、SARS-CoV-2の血管への影響やAPの副作用を考慮すると、やはりAP治療中のQTセグメントの変化を綿密にモニタリングすることが推奨される。
APがCOVID-19患者の健康状態をどのように改善しているのか、そのメカニズムは現在も調査中である。
