Contents
Review of the Emerging Evidence Demonstrating the Efficacy of Ivermectin in the Prophylaxis and Treatment of COVID-19
Kory, Pierre MD1,*; Meduri, Gianfranco Umberto MD2; Varon, Joseph MD3; Iglesias, Jose DO4; Marik, Paul E. MD5
American Journal of Therapeutics 2021年5月6月-第28巻-第3号-p e299-e318
概要
背景
COVID-19が米国に出現した後、医療関係者は有効な治療法を特定するために、新たな基礎科学、トランスレーショナルデータ、および臨床データの検討を始めた。さらに、新規および再利用された多数の治療薬が経験的に使用され、臨床試験で検討された。
不確実性のある分野
中等度から重度の疾患におけるコルチコステロイドを除いて、大多数の治療薬はCOVID-19の死亡率を低下させる効果について再現性のある決定的な証拠を得ることができなかった。最近では、経口抗寄生虫剤であるイベルメクチンが、多くの抗ウイルスおよび抗炎症メカニズムを示し、試験結果で有意な転帰の改善が報告されているという証拠が出ていた。中には査読を通過していないものもあることから、Unitaid/世界保健機関をはじめとするいくつかの専門家グループは、活動中のすべての試験責任者に連絡を取り、評価やメタアナリシスの実施に必要なデータを迅速に収集するための組織的なグローバル活動を行っている。
データソース
データは、発表された査読付き研究、プレプリントサーバーに掲載された原稿、専門家によるメタ分析、イベルメクチン配布キャンペーンを行った地域の多数の疫学分析から得られたものである。
治療の進歩
大多数のイベルメクチンの無作為化比較試験および観察対照試験では、臨床転帰に大きな改善が繰り返し報告されている。数多くの予防試験では、イベルメクチンを定期的に使用することで感染が大幅に減少することが示されている。複数の大規模な自然実験が行われ、「イベルメクチンの配布」キャンペーンを開始した地域では、そのようなキャンペーンを行っていない近隣の地域と比較して、感染者数と致死率が時間的に関連してしっかりと再現可能なほど減少した。
結論
COVID-19におけるイベルメクチンの18の無作為化対照治療試験に基づくメタアナリシスでは、死亡率,臨床的回復までの時間,ウイルス除去までの時間が統計的に有意に大きく減少することが明らかになった。さらに、多数の予防対照試験の結果から、イベルメクチンを定期的に使用することでCOVID-19に感染するリスクが大幅に減少することが報告されている。最後に、イベルメクチンの配布キャンペーンが人口全体の罹患率と死亡率の急速な低下をもたらした多くの例は、COVID-19のすべての局面で有効な経口薬が特定されたことを示している。
序論
2020年初頭、パンデミックの拡大に伴い、多くの医療機関では、COVID-19に有効な治療法を特定するために、急速に出現している基礎科学、トランスレーショナルデータ、臨床データを継続的に検討し始めた。現在では、中等度から重度の疾患におけるコルチコステロイドを筆頭に、重要な臨床結果において一定の有効性を示す治療法が少数ながら増加しているが、世界は、病院や集中治療室(ICU)を再び圧倒する可能性のある危機的状況の悪化に悩まされ続けている。2020年2月21日現在、米国におけるCOVID-19に起因する死亡者数は510,248人、有効症例数は930万人を超え、これまでで最も多い数となっている。また、ヨーロッパの複数の国では、新たに制限やロックダウンが実施された。
さらに、COVID-19に有効と考えられる薬剤を用いて実施された治療に関する無作為化比較試験の結果が最近相次いで発表され、レムデシビル、ヒドロキシクロロキン、ロピナビル/リトナビル、インターフェロン、回復期血漿、モノクローナル抗体療法を用いても、入院患者の死亡率に影響を与えないことが明らかになった1。 パンデミックから 1年が経過したCOVID-19において、救命治療として「証明された」と考えられているのは、中等症から重症の患者に対する副腎皮質ホルモンの使用だけである5,6。同様に、最も懸念されるのは、外来患者において、入院を防ぐために病気の進行を防ぐ効果があると証明された薬剤がまだないという事実である。
最近では、広く使用されている抗寄生虫薬であり、抗ウイルス作用や抗炎症作用が知られているイベルメクチンの試験結果が、死亡率を含む複数の重要な臨床的およびウイルス学的アウトカムに有効であることを示している。この結論を裏付ける研究の多くが査読を通過しているが、残りの試験データの約半分は、医療用プレプリントサーバーにアップロードされた原稿によるものである。以下は、COVID-19におけるイベルメクチンの上記の効果を示す、試験管内試験、動物、臨床、実社会での試験から得られた2020年12月12日時点での有効性データの包括的なレビューである。
イベルメクチンの歴史
1975年、日本の北里研究所の大村智教授は、本州の南東海岸沿いにあるゴルフ場付近の土壌から、珍しいストレプトミセス菌を分離した。大村は、ウィリアム・キャンベルとともに、この菌の培養液が回虫Heligmosomoides polygyrusに感染したマウスを治療できることを発見した。キャンベルは、この細菌培養物から活性化合物を分離し、その化合物がマウスから虫を取り除く能力があることから、「エバーメクチン」とS. avermitilis菌と名付けた7。その後、エバーメクチンの誘導体であるイベルメクチンが革命的な効果を発揮した。1988年にオンコセルカ症(河川盲目症)の治療に使用されて以来、世界中の何十億もの人々の栄養状態や健康状態を改善していた。1988年にオンコセルカ症(河川盲目症)の治療に初めて使用されて以来、オンコセルカ症は、効果が高く、広範囲に作用し、安全性が高く、忍容性があり、投与が容易であるなど、多くの点で理想的な治療薬であることが証明された7。さまざまな内部線虫感染症の治療に使用されたが、最もよく知られているのは、2つの世界的な疾病撲滅キャンペーンの重要な柱であり、世界で最も醜い壊滅的な2つの疾病をほぼ撲滅した。Merck & Co. メルク社と北里研究所の前例のないパートナーシップと、国際的な医療機関の支援は、多くの専門家から 20世紀の最も偉大な医学的業績の一つとして認められている。イベルメクチンは、熱帯地方の何十億もの貧しい人々を苦しめてきたオンコセルカ症とリンパ系フィラリア症の制圧に貢献したことから、発見者は2015年にノーベル医学賞を受賞し、世界保健機関(WHO)の「必須医薬品リスト」にも掲載されている。さらに、他のいくつかの人間の病気を克服することにも成功しており、新たな用途が絶えず発見されている7。
SARS-CoV-2に対するイベルメクチンの前臨床試験
2012年以降、イベルメクチンが、インフルエンザ、ジカ熱、HIV、デング熱、そして最も重要なSARS-CoV-2など、ますます多くのRNAウイルスに対して抗ウイルス作用を有することが、多くの細胞研究によって明らかにされてきた9-17。Caly et al 18は、細胞培養モデルにおいてイベルメクチンがSARS-CoV-2の複製を著しく阻害することを初めて報告し、イベルメクチン投与48時間後にはすべてのウイルス物質がほぼ消失することを確認した。19,20 細胞培養モデルで効果を得るために必要な濃度は、イベルメクチンのような治療薬と相乗的に働く活発な免疫系が存在しないため、ヒトの生理機能とは似て非なるものであることに留意すべきである。さらに、長期間にわたって薬剤を投与する場合、細胞培養モデルでの短期間の投与に比べて数分の一の投与量で済む可能性がある。さらに、6つの分子モデリング研究で提案されているように、SARS-CoV-2スパイクタンパク質の宿主受容体結合領域とイベルメクチンが競合的に結合するなど、複数の共存あるいは代替作用メカニズムが、観察された臨床効果を説明していると考えられる21。 26 そのうち4つの研究では、イベルメクチンは、SARS-CoV-2のスパイクタンパクのS1結合ドメインに対する結合親和性が、何百もの分子をまとめて調べた中で最も高い、あるいは最も高いレベルにあることが確認されたが、これらの研究のうち4つでは、イベルメクチンは特に研究対象にはなっていなかった27。SARS-CoV-2スパイクタンパク質に対するイベルメクチンの高い結合活性は、ACE-2受容体またはシアル酸受容体のいずれかへの結合をそれぞれ制限し、ウイルスの細胞侵入を阻止するか、またはCOVID-19で最近提唱された病態メカニズムであるヘマグルティングを阻止する可能性がある。21,22,26-28 また、イベルメクチンは、ウイルスが複製するのに必要な複数の必須構造タンパク質および非構造タンパク質に結合したり、それらを妨害したりすることが示されている26,29。最後に、イベルメクチンは、SARS-CoV-2のRNA依存性RNAポリメラーゼ(RdRp)にも結合して、ウイルスの複製を阻害する30。
Arevaloらは、SARS-CoV-2に類似した2型ファミリーRNAコロナウイルス(マウス肝炎ウイルス)に感染したマウスモデルを用いて、イベルメクチン500μg/kgとプラセボの反応を調べた31。5日目にすべてのマウスを殺し、組織を採取して検査とウイルス量の評価を行った。イベルメクチンを投与しなかった20匹の感染マウスでは、いずれも重度の肝細胞壊死とそれを取り巻く重度のリンパ形質細胞性炎症浸潤が認められ、高い肝ウイルス量を伴っていた(52,158)のに対し、イベルメクチンを投与したマウスでは、ウイルス量ははるかに少なく(23,192; P < 0. 05)、肝細胞はわずかに残っていた。 05)イベルメクチン投与マウスの肝臓では病理組織学的な損傷を示すものはわずかで、非感染対照マウスの肝臓との差は統計的に有意ではなかった。
Dias De Meloら32は、ゴールデンハムスターにSARS-CoV-2ウイルスを経鼻接種し、感染時にイベルメクチンを0.4mg/kgの用量で1日目に単回皮下注射した研究結果を発表した。対照動物には生理食塩水のみを投与した。その結果、イベルメクチンを投与したハムスターでは、無嗅覚症が劇的に減少し(33.3%対83.3%、P=0.03)雄のハムスターでは臨床スコアが低下したのに対し、雌のハムスターでは無嗅覚症の兆候が見られないという性差も認められた。また、ウイルスの力価に明らかな差がなかったにもかかわらず、治療を受けた動物の鼻濁液と肺のサイトカイン濃度が有意に低下したことも分かった。
このように、イベルメクチンの予防および治療薬としての既存および潜在的な作用機序が明らかになったにもかかわらず、重大な研究上のギャップが残っており、これらの機序をより明確にするだけでなく、予防薬としてのイベルメクチンの役割、特に必要とされる最適な投与量と投与頻度をさらに裏付けるために、さらに多くの試験管内試験および動物実験を行う必要があることを強調しなければならない。
イベルメクチンの抗炎症作用に関する前臨床試験
COVID-19の後期にはウイルスの複製はほとんど起こらず、ウイルスを培養することもできず、ウイルスの細胞病理学的変化が認められるのは少数の剖検例に過ぎない33-35ことを考えると、最も可能性の高い病態生理学的メカニズムはLiら36が明らかにしたものであり、彼らはSARS-CoV-2の非生存RNA断片が圧倒的で傷害的な炎症反応を引き起こすことによってCOVID-19の高い死亡率と罹患率をもたらすことを示した。これらの知見と、後述する疾患末期におけるイベルメクチンの臨床的有用性に基づけば、炎症抑制剤としてのイベルメクチンの試験管内試験での特性は、これまで認識されていたよりもはるかに臨床的に強力なものであると思われる。イベルメクチンの抗炎症作用を示す研究は増え続けており、リポ多糖暴露後のサイトカイン産生を抑制する能力、NF-kBの転写をダウンレギュレートする能力、一酸化窒素とプロスタグランジンE2の産生を制限する能力などがある37-39。
イベルメクチンのCOVID-19感染防止能力に関する暴露予防試験
現在、3件の無作為化比較試験(RCT)と5件の観察対照試験(OCT)のデータに基づいて、ヒト被験者の間でCOVID-19の感染が大きく、統計的に有意に減少したことを示すデータも入手可能であり、8件のうち4件(うち2件はRCT)が専門誌に発表されている40-46。
エジプトのベンハ大学の Elgazzar ら45 は、COVID-19 を発症した患者の医療関係者および家庭内接触者 200 人を対象に、介入群では 100 人の患者に個人防護具の着用に加えて 1 日目に 0.4 mg/kg の高用量を投与し、7 日目に 2 回目の投与を行い、対照群では 100 人の接触者に個人防護具のみを着用させた。その結果、イベルメクチンを投与した場合、逆転写酵素ポリメラーゼ連鎖反応(PCR)で陽性と判定された接触者は、対照群に対して2%対10%、P<0.05と、統計的に有意に減少したことが報告された。
Shouman氏は、エジプトのZagazig大学で、PCR法でSARS-CoV-2陽性となった患者の家族340人(治療者228人、対照者112人)を対象としたRCTを実施した44。イベルメクチン(約0.25mg/kg)は、陽性反応が出た日とその72時間後の2回投与された。2週間の追跡調査の結果、イベルメクチンを投与された世帯員のCOVID-19の症状は、7.4%対58.4%、P < 0.001と、大きく統計的に有意に減少した。
最近では、バングラデシュのAlamらが、118人の患者を対象とした前向き観察研究を行い、治療群と対照群のいずれかに志願した人に均等に分けて、説得力のあるアプローチと説明している。この方法は、盲検化されていないことと相まって交絡因子をもたらしたと考えられるが、2群間の差は非常に大きく(6.7%対73.3%、P <0.001)他の予防試験の結果と同様であったため、交絡因子だけでこのような結果を説明することはできないと考えられる。
Carvalloらは、健康なボランティアにイベルメクチンとカラギーナンを28日間毎日投与し、薬を服用していない同様の健康な対照者と比較するという前向き観察試験も実施した40。28日後,イベルメクチンを投与された予防群では,SARS-COV-2の陽性反応が出た患者は一人もいなかったのに対し,対照群では11.2%であった(P < 0.001).同じグループが行った、1195人の医療従事者を対象としたより大規模な追跡調査の前向き観察対照試験では、3カ月間で、週1回イベルメクチンの予防投与を受けた788人の労働者には感染が記録されなかったのに対し、407人の対照群では58%がCOVID-19に罹患したことがわかった。40
Carvallo IVERCARプロトコルは、アルゼンチンTucumanの保健省によるプロスペクティブRCTでも検証され、介入群である234名の医療従事者が週1回12mgを服用した結果、COVID-19に感染したのは3.4%のみで、対照群では21.4%であったことがわかった(P<0.0001)46。
バングラデシュのダッカで行われた最近のRCTでは、介入群(n=58)が12mgを月1回、同様に4ヶ月間服用し、対照群と比較して感染症が6.9%対73.3%、P < 0.0001と大きく統計的に有意に減少したことが報告されていることを考えると、Carvallo試験における4ヶ月間の週1回服用の必要性はなかったかもしれない。 47
次に、インドで行われた大規模なレトロスペクティブ・ケースコントロール研究において、Beheraら41は、医療従事者の186組のケースコントロールペア(n = 372)のうち、何らかの予防措置を講じたことのある169人を特定し、そのうち115人がイベルメクチンを服用していたことを報告した。マッチドペア解析の結果、イベルメクチンを2回投与して予防した労働者では、COVID-19に感染するオッズ比が顕著に低下したことが報告された(0.27,95%信頼区間(CI)0.15-0.51)。注目すべきは、この研究では1回の投与による予防効果が認められなかったことである。All India Institute of Medical Sciencesでは、エジプトの予防研究と今回の研究結果に基づいて、医療従事者にイベルメクチン0.3mg/kgを72時間間隔で2回投与し、毎月繰り返し投与するという予防プロトコルを策定した。
イベルメクチンのCOVID-19に対する保護作用の可能性を示すデータとして、フランスの老人ホームの入居者を対象とした研究がある。この研究では、疥癬が発生し、入居者69人と職員52人全員にイベルメクチンが投与された施設で、41,この出来事の前後の期間に、入居者69人のうち7人がCOVID-19に罹患したことがわかった(10.1%)。平均年齢90歳のこのグループでは、酸素サポートが必要となった入居者は1名のみで、死亡した入居者はいなかった。また、周辺施設の入居者からなるマッチドコントロール群では、22.6%の入居者が病気になり、4.9%の入居者が死亡したとのことである。
予防薬としてのイベルメクチンの有効性を裏付ける証拠が、International Journal of Antimicrobial agentsに掲載された。研究グループは、WHOが運営する予防化学療法データバンクのデータと、ジョンズ・ホプキンス大学などが利用している公的データ集計サイトWorldometersで得られた症例数を分析した42。さらに、寄生虫感染予防のためのイベルメクチン大量投与プログラムが実施されている国のデータを比較したところ、最近プログラムが実施された国では、COVID-19の症例数が有意に少ないことがわかった(P < 0.001)。
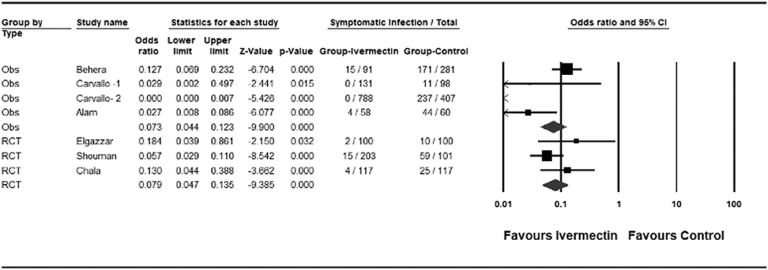
図1は、COVID-19におけるイベルメクチン予防の対照試験について、研究著者が行ったメタアナリシスを示したものである。
図1: COVID-19におけるイベルメクチン予防試験のメタアナリシス
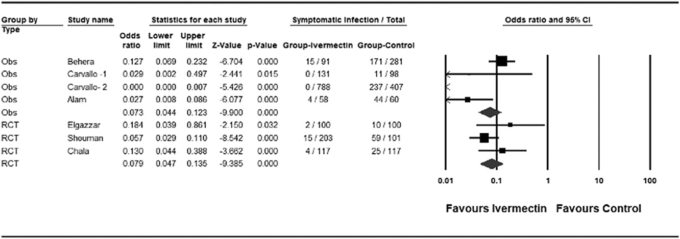
OBSは観察研究、RCTは無作為化比較試験。記号。正方形。個々の試験の治療効果を示す。大きな菱形。直上の研究デザインの要約を反映している。各記号の大きさは、治療効果の点推定値の信頼区間の大きさと相関しており、大きければ大きいほど信頼区間が正確であることを示している。
感染率の低下にイベルメクチンが貢献していることを裏付けるデータとして、南米の国々では大規模な「自然実験」が行われたと考えられている。例えば、ペルー、ブラジル、パラグアイの各地域の保健省や政府当局は、早ければ5月から、市民に対して「イベルメクチン配布」キャンペーンを開始した48。ブラジルの例では、イタジャイ市、マカパ市、ナタール市が大量のイベルメクチンを市民に配布し、ナタール市の場合は100万回分が配布された。イタジャイでは7月中旬から、ナタールでは6月30日から配布を開始し、首都アマパをはじめとする近隣のマカパでは、4月に特に大きな被害を受けた後、5月下旬から治療プロトコルにイベルメクチンを取り入れた。表1のデータは、ブラジル政府の公式サイトおよび全国報道機関から入手したものであるが、配布開始直後の3都市では、キャンペーンを行っていない近隣の都市に比べて患者数が大きく減少している。
表1 – イベルメクチンの配布キャンペーンを行った都市と行わなかった都市の症例数減少の比較
| 領域 | 二ケース | 6月 | 7月 | 8月 | 人口2020(1000) | 2020年6月から8月の新規症例の減少率 |
| 南 | イタジャイ | 2123 | 2854 | 998 | 223 | – 53% |
| シャペコ | 1760 | 1754 | 1405 | 224 | – 20% | |
| 北 | マカパ | 7966 | 2481 | 2370 | 503 | – 70% |
| アナニンデウア | 1520 | 1521 | 1014 | 535 | – 30% | |
| 潤 | ナタール | 9009 | 7554 | 1590 | 890 | – 82% |
| ジョアンペソア | 9437 | 7963 | 5384 | 817 | – 43% |
表1に示したブラジルの3都市における症例数の減少は、表2にまとめたように、死亡率の減少にも関連していた。
表2 – ブラジルの近隣地域における死亡率の変化
| 領域 | 状態 | 2週間前と比較した1週間あたりの平均死亡数の変化 |
| 南 | サンタカタリーナ | –36% |
| パラ | –3% | |
| リオグランデドスル | –5% | |
| 北 | アマパー | –75% |
| アマゾナス | –42% | |
| パラ | + 13% | |
| 潤 | リオグランデドノルテ | –65% |
| CEARÁ | + 62% | |
| パライバ | –30% |
軽症の外来患者に対するイベルメクチンの有効性に関する臨床試験
現在、7つのRCTと4つのケースシリーズからなる7つの試験が完了しており、合計3000人以上の軽度の外来患者を対象としている49-60。
最も規模の大きいMahmud49による二重盲検RCTは、バングラデシュのダッカで実施され、400人の患者を対象とし、363人の患者が研究を完了した。この研究では、レビューする他の多くの臨床研究と同様に、治療の一環としてテトラサイクリン(ドキシサイクリン)またはマクロライド系抗生物質(アジスロマイシン)が含まれてた。ドキシサイクリンやアジスロマイシンなどの抗生物質を含めることの重要性は不明であるが、テトラサイクリン系とマクロライド系の抗生物質は、いずれも抗炎症作用、免疫調節作用、さらには抗ウイルス作用が認められている(58-61)。本研究の掲載データでは、軽症の外来患者と入院患者の治療量は明記されていないが、早期改善率の増加(60.7%対44.4%、P<0.03) 臨床悪化率の減少(8.7%対17.8%、P<0.02)など、重要な臨床転帰に大きな影響を与えてた。また、軽症の外来患者が主な対象であったため、死亡例は2例のみであった(いずれも対照群)。
Ravikirti氏は、115人の患者を対象に二重盲検RCTを実施し、主要評価項目である6日目のPCR陽性率には差がなかったものの、副次評価項目である死亡率は0%対6.9%、P = 0.019でした60。ナイジェリアのBabalola氏も、62人の患者を対象に二重盲検RCTを実施し、Ravikirti氏とは対照的に、低用量治療群と高用量治療群の両方と対照群の間で、用量依存的にウイルスクリアランスに有意差があることを見出した、P = 0.006でした59。
Hashimら53がイラクのバグダッドで行った別のRCTでは、140人の患者を均等に分け、対照群には標準的な治療を、治療群には外来患者と入院患者の両方を組み合わせました。軽度から中等度の外来患者96人のうち、48人にイベルメクチン/ドキシサイクリンと標準治療を組み合わせて投与し、標準治療のみを行った48人との転帰を比較した。この試験での標準治療は、必要に応じてデキサメタゾン6mg/日またはメチルプレドニゾロン40mg/日×2回、ビタミンC1000mg/日×2回、亜鉛75~125mg/日、ビタミンD3 5000IU/日、アジスロマイシン250mg/日×5日、アセトアミノフェン500mg/日などの薬を投与した。いずれの群でも進行や死亡した患者はいなかったが、回復までの期間はイベルメクチン投与群で有意に短くなった(6.3日対13.7日、P < 0.0001)。
Chaccour氏らは、スペインで小規模な二重盲検RCTを実施し、24人の患者をイベルメクチンとプラセボに無作為に割り付けた。その結果、7日目のPCR陽性率には差がなかったが、ウイルス量、無嗅覚患者の日数(76日対158日、P<0.05)咳をした患者の日数(68日対98日、P<0.05)が統計的に有意に減少することがわかった57。
外来患者116名を対象としたイベルメクチン治療の別のRCTは、Chowdhuryらによってバングラデシュで実施され、PCR陰性化までの期間を主要評価項目として、イベルメクチン/ドキシサイクリン併用療法を受けた60名とヒドロキシクロロキン/ドキシサイクリンを受けた60名のグループを比較した54。Podderらによる62人の患者を対象とした別の小規模なRCTでも、統計的に有意に近い症状回復までの期間の短縮が認められた(10.1日対11.5日、P>0.05,95%CI,0.86-3.67)55。
ドミニカ共和国のある医療グループは、救急部で治療を受けようとしている連続した症状のある外来患者2688人のケースシリーズを報告した。患者は,0.4mg/kgの高用量イベルメクチンを1回投与し、5日間のアジスロマイシン投与を受けた。驚くべきことに、2688人の患者のうち、その後の入院が必要となったのは16人(0.59%)のみで、死亡例は1件のみでした61。
バングラデシュで100人の患者を対象に行われた別のケースシリーズでは、全員が0.2mg/kgのイベルメクチンとドキシサイクリンの組み合わせで治療を受け、入院を必要とした患者や死亡した患者はおらず、すべての患者の症状が72時間以内に改善したことがわかった62。
アルゼンチンのケースシリーズでは、イベルメクチン、アスピリン、デキサメタゾン、エノキサパリンを併用したプロトコルが報告されている。同様に、メキシコで行われたケースシリーズでは、イベルメクチンを連続して投与された28人の患者のうち、全員が回復し、完全に回復するまでの平均時間はわずか3.6日だったと報告されている58。
入院患者におけるイベルメクチンの有効性に関する臨床研究
より重症の入院患者を対象としたイベルメクチンの研究には、6件のRCT、5件のOCT、および1件のデータベース分析研究がある。
入院患者を対象とした最大のRCTは、Elgazzarらによって上述の予防試験と同時に実施された45。第1群と第2群は、軽症/中等症の患者のみを対象とし、第1群にはイベルメクチン0.4mg/kgを1回投与するとともに標準治療(SOC)を行い、第2群にはヒドロキシクロロキン400mgを1日目に2回投与した後、200mgを1日2回、5日間投与するとともに標準治療を行った。イベルメクチン投与群では、統計学的に有意に進行率が低く(1%対22%、P<0.001)死亡例はそれぞれ0例、4例であった。グループ3と4には重症患者のみが含まれ、グループ3では再び0.4mg/kgとSOCの単回投与が行われ、グループ4ではヒドロキシクロロキンとSOCの併用が行われた。この重症患者のサブグループでは、転帰の差がさらに大きくなり、進行率は4%対30%、死亡率は2%対20%であった(P < 0.001)。
上述のHashim氏による主に外来患者を対象としたRCTでは、各群に22人の入院患者が含まれていた。イベルメクチン/ドキシサイクリン投与群では、重症患者11人と重症患者11人が含まれてたが、標準治療群では、対照群に重症患者を含めることに倫理的な懸念があったため、重症患者(n = 22)のみが含まれてた(45)。この決定により、これらの入院患者群の間で重症度の著しい不均衡が生じた。しかし、グループ間の重症度の不一致や対象となった患者数の少なさにもかかわらず、アウトカムに有益な差が見られたが、すべてが統計的に有意ではなかった。例えば、病気の進行率は大きく減少し(9%対31.8%、P = 0.15)最も重要なことは、重症患者群の死亡率に大きな差があり、統計的に有意な境界線に達していたことである(0%対27.3%、P = 0.052)。また、重症患者のサブセットで死亡率が18%と比較的低かったことも重要な発見であり、全員にイベルメクチンが投与されていた。
イランからの最近のRCTは、イベルメクチンの使用により死亡率が劇的に減少することを発見した。65 複数のイベルメクチン治療群(介入群では異なるイベルメクチン投与法を採用)のうち、平均死亡率は3.3%と報告されているが、標準治療群とプラセボ群の平均死亡率は18.8%で、オッズ比(OR)は0.18(95%CI 0.06-0.55,P<0.05)であった。
Spoorthi64氏とSasanak氏は、100名の入院患者を対象とした前向き試験を行い、50名にイベルメクチンとドキシサイクリンを投与し、50名の対照群にはビタミンB6からなるプラセボを投与した。両群とも死亡例はなかったが、イベルメクチン投与群では、入院期間(LOS)が3.7日対4.7日、P = 0.03,症状が完全に消失するまでの期間が6.7日対7.9日、P = 0.01と、統計学的に有意に短かった。
入院患者を対象とした最大規模のOCT(n=280)は、フロリダ州のBroward Health HospitalsでRajterらが実施したもので、最近、主要な医学雑誌「Chest」に掲載された(43)。彼らは、280人の連続した治療を受けた患者を対象に、傾向をマッチさせたデザインでレトロスペクティブなOCTを実施し、イベルメクチンを投与した患者とそうでない患者を比較した。イベルメクチンを投与された患者は137名(160名は単回投与、13名は7日目に2回目の投与)投与されなかった患者は107名であった。63 マッチしていないコホートと傾向マッチしたコホートの両方で、イベルメクチンを投与された患者の死亡率は同様に大きく、統計的に有意に低いことがわかった(15.0%対25.2%、P =0.03)。さらに、重度の肺病変を有する患者のサブグループでは、イベルメクチンを投与した場合に死亡率が大幅に低下した(38.8%対80.7%、P = 0.001)。
バングラデシュの別の大規模なOCTは、イベルメクチンで治療された115人の患者を133人の患者からなる標準的なケアコホートと比較した。51 イベルメクチン投与群では男性患者の割合が有意に高く(すなわち、COVID で生存率が低いことが十分に説明されている)その他の点では両群はよく一致していたが、死亡率の低下は統計的に有意であった(0.9%対 6.8%、P<0.05)。
最大のOCTは、編集者へのレターとして発表され、約1500人の患者を対象としたブラジルの研究である66。主要データは提供されていないが、入院患者704人に0.15mg/kgのイベルメクチンを単回投与したところ、704人の対照群と比較して、全死亡率が低下したことが報告されている(1.4%対8.5%、HR 0.2,95%CI 0.12-0.37,P < 0.0001)。同様に、人工呼吸を行っている患者においても、死亡率が低下した(1.3% vs. 7.3%)。
イラクのバグダッドで行われた小規模な研究では、イベルメクチンを投与した16人の患者と71人の対照群を比較した52。この研究でも、イベルメクチン投与群で入院期間が有意に短縮されたことが報告されている(7.6日対13.2日、P<0.001)。インドの病院で治療を受けた最初の 1000 人の患者について報告した研究では、イベルメクチンのみで治療を受けた 34 人の患者では全員が回復して退院したのに対し、他の薬剤で治療を受けた 900 人以上の患者では全体の死亡率が 11.1%であったことが報告されている70。
上記の対照治療試験のメタアナリシスは、臨床回復までの期間と死亡率という2つの重要な臨床アウトカムに焦点を当てて、研究著者によって行われた(図2および3)。両方の試験デザインにおいて、全体的に統計的に有意な利益をもたらす一貫した再現性のあるシグナルが得られたことは、特にいくつかの試験で治療が疾患経過の後半に開始されたことを考えると、注目に値する。
図2 COVID-19におけるイベルメクチン治療の対照試験から得られた、臨床的回復までの時間に関する結果のメタ分析
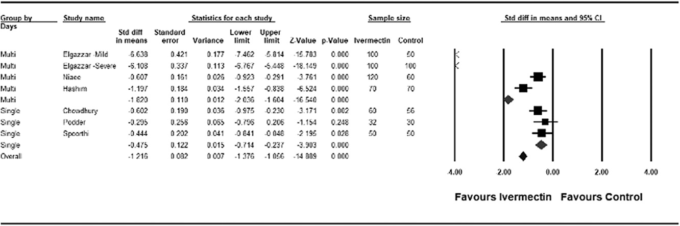
OBSは観察研究、RCTは無作為化比較試験。記号。正方形。個々の試験の治療効果を示す。大きな菱形。直上の研究デザインの概要を反映している。小さな菱形。すべての試験デザインの効果の合計。各記号の大きさは,治療効果の点推定値の信頼区間の大きさと相関しており,大きければ大きいほど信頼区間が正確であることを示している。
図3: COVID-19におけるイベルメクチン治療の対照試験から得られた死亡率というアウトカムのメタアナリシス
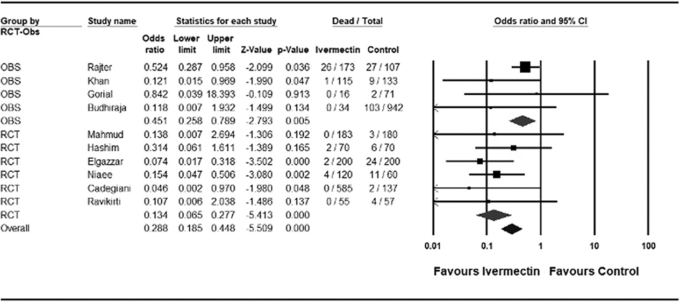
OBSは観察研究、RCTは無作為化比較試験。記号 四角。個々の研究の治療効果を示す。大きな菱形。直上の研究デザインの概要を反映している。小さな菱形。すべての試験デザインの効果の合計。各記号の大きさは、治療効果の点推定値を中心とした信頼区間の大きさと相関しており、大きければ大きいほど信頼区間が正確であることを示している。
COVID-19におけるイベルメクチンの予防試験、初期治療試験、後期治療試験の詳細は、表3に記載している。
表3 – COVID-19 の予防および治療におけるイベルメクチンの有効性を評価した臨床試験
| 予防試験著者、国、出典 | 研究デザイン、サイズ | 研究対象 | イベルメクチン投与量 | 投与頻度 | 報告された臨床転帰 |
| 予防試験 | |||||
| Shouman W、エジプトwww.clinicaltrials.gov NCT04422561 |
RCT N = 340 |
+ COVID-19PCR検査を受けたptsの世帯員 | 40〜60 kg:15 mg、60〜80 kg:18 mg、および> 80 kg:24 mg | 72時間間隔で2回投与 | 7.4%対58.4%がCOVID-19症状を発症、P <0.001 |
| Elgazzar A、エジプト ResearchSquare doi.org/10.21203/rs.3.rs-100956/v1 |
RCT N = 200 |
+ COVID-19PCRテストによるptsのヘルスケアと家庭の接触 | 0.4mg / kg | 1日目と7日目の2回投与 | 2%対10%がCOVID-19 P <0.05で陽性とテストされた |
| Chala R、アルゼンチン NCT04701710 Clinicaltrials.gov |
RCT N = 234 |
医療従事者 | 12mg | 7日ごと | 3.4%対21.4%、P = 0.0001。 |
| Carvallo H、アルゼンチン Journal of Biochemical Research andInvestigation doi.org/10.31546/2633–8653.1007 |
OCT N = 229 |
COVID-19PCR検査で陰性の健康な患者 | 0.2mg滴 | 1滴5回adx28 d | 0.0%対11.2%の契約COVID-19 P <0.001 |
| Alam MT、バングラデシュ European J Med Hlth Sciences 10.24018 / ejmed.2020.2.6.599 |
OCT N = 118 |
医療従事者 | 12mg | 毎月 | 6.9%対73.3%、P <0.05 |
| Carvallo H、アルゼンチン Journal of Biochemical Research andInvestigation doi.org/10.31546/2633–8653.1007 |
OCT N = 1195 |
医療従事者 | 12mg | 週に1回、最大10週間 | イベルメクチンを服用している788人の労働者の0.0%に対して、407人の対照の58%がCOVID-19に感染した。 |
| ベエラ P、インドmedRxiv doi.org/10.1101/2020.10.29.20222661 |
OCT N = 186のケースコントロールペア |
医療従事者 | 0.3mg / kg | 1日目と4日目 | 2回の投与でCOVID-19に感染する確率が低下した(または0.27 95%CI 0.16–0.53) |
| Bernigaud C、フランス Annales de Dermatologie et de Venereologi doi.org/10.1016/j.annder.2020.09.231 |
OCT N = 69のケースコントロールペア |
ナーシングホーム入居者 | 0.2mg / kg | 一度 | 10.1%対22.6%の居住者がCOVID-19に感染した0.0%対4.9%の死亡率 |
| Hellwig M、USAJ 抗菌剤 doi.org/10.1016/j.ijantimicag.2020.106,248 |
OCT N = 52か国 |
IVM予防プログラムの有無にかかわらず国 | わからない | 変数 | IVM予防プログラムを実施しているアフリカ諸国におけるCOVID-19の有意に低い発生率P <0.001 |
| 臨床試験–外来患者 | %イベルメクチン対%コントロール | ||||
| 予防試験著者、国、出典 | 研究デザイン、サイズ | 研究対象 | イベルメクチン投与量 | 投与頻度 | 報告された臨床転帰 |
| Mahmud R、バングラデシュwww.clinicaltrials.gov NCT0452383 |
DB-RCT N = 363 |
外来および入院 | 12 mg +ドキシサイクリン | 1回、PCR +テストから3日以内 | 初期の改善60.7%対44.4%、P <0.03,劣化8.7%対17.8%、P <0.02 |
| Chowdhury A、バングラデシュ リサーチスクエア doi.org/10.21203/rs.3.rs-38896/v1 |
RCT N = 116 |
外来患者 | 0.2 mg // kg +ドキシサイクリン | 一度 | 回復時間5。9日対9。3日(P = 0.07) |
| インド、 ラビキルティ medRxiv doi.org/10.1101/2021.01.05.21249310 |
DB-RCT N = 115 |
軽度から中等度の病気 | 12mg | 2日間毎日 | 6日目のPCRで差異なし+ 0%対6.9%の死亡率、P = 0.019 |
| Babalola OE、ナイジェリア medRxiv doi.org/10.1101/2021.01.05.21249131 |
DB-RCT N = 62 |
軽度から中等度の病気 | 6mgと12mg | 48時間ごと×2週間 | ウイルスクリアランスまでの時間:高用量4。6日対低用量6。0日対対照9。1日(P = 0.006) |
| Podder CS、バングラデシュ IMC J Med Sci 2020; 14(2) |
RCT N = 62 |
外来患者 | 0.2mg / kg | 一度 | 回復時間10.1対11。5日(NS)平均時間5.3対6.3(NS) |
| ChaccourC。スペイン リサーチスクエアdoi.org/10.21203/rs.3.rs-116547/v1 |
DB-RCT N = 24 |
外来患者 | 0.4mg / kg | 一度 | PCR + 7日目に差異はなく、ウイルス量d 4および7が低く(P <0.05)76対158ポイント。無嗅覚症のd(P <0.05)68対98ポイント。咳のd(P <0.05) |
| Morgenstern J、ドミニカ共和国 medRxiv doi.org/10.1101/2020.10.29.20222505 |
ケースシリーズ N = 3099 |
外来および入院 | 外来患者:0.4mg / kg入院患者:0.3mg / kg | 外来患者:0.3mg / kg×1回投与入院患者:0.3mg / kg、1,2,6,7日目 | 死亡率= 2688人の外来患者で0.03%、300人の非ICU入院患者で1%、111人のICU患者で30.6% |
| Carvallo H、アルゼンチンmedRxiv doi.org/10.1101/2020.09.10.20191619 |
ケースシリーズ N = 167 |
外来および入院 | 24 mg =軽度、36 mg =中程度、48 mg =重度 | 0日目と7日目 | 軽度の病気の135人全員が生き残り、1/32人(入院患者の3.1%)が死亡した |
| Alam A、バングラデシュ 大学Phys and SurgのバングラデシュJ 2020; 38:10-15 doi.org/10.3329 / jbcps.v38i0.47512 |
ケースシリーズ N = 100 |
外来患者 | 0.2 mg / kg / kg +ドキシサイクリン | 一度 | すべて72時間以内に改善 |
| Espatia-Hernandez G、メキシコ 生物医学研究 www.biomedres.info/biomedi ..- proof-of-concept-study- 14435.html |
ケースシリーズ N = 28 |
外来患者 | 6mg | 1,2,7,8日目 | すべてのポイントが平均回復時間3。6日を回復した |
| 臨床試験–入院患者 | %イベルメクチン対%コントロール | ||||
| 予防試験著者、国、出典 | 研究デザイン、サイズ | 研究対象 | イベルメクチン投与量 | 投与頻度 | 報告された臨床転帰 |
| Elgazzar A、エジプト ResearchSquare doi.org/10.21203/rs.3.rs-100956/v1 |
OL-RCT N = 400 |
入院患者 | 0.4mg / kg | 4日間毎日 | 中等度の病気:1%悪化対22%、P <0.001。重症:P <0.001で4%対30%の死亡率2%対20%の悪化 |
| Niaee S. M、リサーチスクエア doi.org/10.21203/rs.3.rs-109670/v1 |
DB-RCT N = 180 |
入院患者 | 0.2,0.3,および0.4 mg / kg(3つの投与戦略) | 1日目と1,3,5日目 | 死亡率3.3%対18.3%。または0.18,(0.06〜0.55,P <0.05) |
| Hashim H、イラクmedRxiv doi.org/10.1101/2020.10.26.20219345 | SB-RCT N = 140 | 2/3の外来患者と1/3の病院ポイント | 0.2 mg / kg +ドキシサイクリン | 2〜3日間毎日 | 回復時間6。3日対13。6日(P <0.001),0%対27.3%の重症患者の死亡率(P = 0.052) |
| Spoorthi S、インド AIAM 2020; 7(10):177-182 |
PCT N = 100 |
入院患者 | 0.2 mg / kg +ドキシサイクリン | 一度 | 短い病院LOS、3。7日対4。7日、P = 0.03,症状のより速い解決、6。7日対7。9日、P = 0.01 |
| Ahmed S. Dhaka、バングラデシュ 国際感染症ジャーナル doi.org/10.1016/j.ijid.2020.11.191 |
DB-RCT N = 72 |
入院患者 | 12mg | 5日間毎日 | より速いウイルスクリアランス9。7日対12。7日、P = 0.02 |
| Chachar AZK、パキスタン Int J Sciences doi.org/10.18483/ijSci.2378 |
DB-RCT N = 50 |
入院患者-軽度 | 12mg | 1日目2回投与と2日目1回投与 | 7日目までに64%対60%無症候性 |
| ポートマン-バラッコA、ブラジル アーチブロンコネウモル。2020 doi.org/10.1016/j.arbres.2020.06.011 |
OCT N = 1408 |
入院患者 | 0.15 mg / kg | 一度 | 全体的な死亡率1.4%対8.5%、HR 0.2,95%CI 0.12–0.37,P <0.0001 |
| Rajter JC、フロリダ チェスト2020 doi.org/10.1016/j.chest.2020.10.009 |
OCT N = 280 | 入院患者 | 0.2 mg / kg +アジスロマイシン | 必要に応じて1日目と7日目 | 全体的な死亡率15.0%対25.2%、P = 0.03,重度の病気による死亡率38.8%対80.7%、P = 0.001 |
| カーンX、バングラデシュ アーチBronconeumol。2020 doi.org/10.1016/j.arbres.2020.08.007 |
OCT N = 248 |
入院患者 | 12mg | 入場時に一度 | 死亡率0.9%対6.8%、P <0.05,LOS 9対15日、P <0.001 |
| Gorial FI、イラク medRxiv doi.org/10.1101/2020.07.07.20145979 |
OCT N = 87 |
入院患者 | 0.2 mg / kg + ヒドロキシクロロキンおよびアジスロマイシン | 入場時に一度 | LOS 7.6対13。2日、P <0.001,0 / 15対2/71死亡 |
| Budiraja S. India medRxiv doi.org/10.1101/2020.11.16.20232223 |
OCT N = 1000 IVM = 34 |
入院患者 | 該当なし | 該当なし | 100%IVMポイントはIVM未処理ポイントで11.1%の死亡率を回復した |
ポストCOVID-19症候群に対するイベルメクチンの効果
急性COVID-19から回復した後も、持続的でつらい症状、さらには障害を伴う症状が報告されることが増えており、多くの人がこの症状を「Long COVID」と呼び、患者を「Long Haulers」と呼んでおり、症例の約10%~30%に発生すると推定されている。多くの患者さんは、記憶力や集中力の低下、極度の疲労感を伴う症状を「brain fog(ブレインフォグ)」と表現しており、ウイルス感染、特にエプスタインバーウイルス感染後に発症することが報告されている筋痛性脳脊髄炎/慢性疲労症候群を強く示唆している。Long-COVIDに特異的な治療法はないが、ペルーのサンマルコス国立大学のAguirre-Changらが最近発表した論文では、このような患者に対するイベルメクチンの使用経験が報告されている74。この論文では、症状の発現から4~12週間経過した33人の患者に対し、軽度の場合は0.2mg/kgを2日間、中等度の場合は0.4mg/kgを2日間と段階的にイベルメクチンを投与し、症状が持続する場合は投与を延長した。その結果、2回の投与で87.9%の患者にすべての症状の消失が認められ、さらに7%の患者が追加投与で完全に消失したと報告している。この経験から、この厄介な症候群の有効性をよりよく検証するための対照試験の必要性が示唆された。
イベルメクチンの広範な使用が人口の症例数および症例死亡率に及ぼす影響を示す疫学データ
ブラジルの各都市がイベルメクチンを配布した直後に、キャンペーンを行わなかった近隣の都市と比較して患者数が大幅に減少したのと同様に、ペルーでは、オーストラリアのCalyらによる試験管内試験研究のみに基づいて 2020年5月8日に政府がイベルメクチンの使用を政令で承認した48 。その直後、複数の州の保健省が、当時世界で最も高かったCOVID-19の罹患率と死亡率を低下させるために、イベルメクチンの配布キャンペーンを開始した。FLCCCアライアンスのメンバーであるデータアナリストのJuan Chamie氏48は、最近、2つの重要なデータをまとめて比較した論文を発表した。1つ目は、各地域におけるイベルメクチンの介入の時期と規模を、公式発表やプレスリリース、ペルーの「Situation Room」データベースを調査して、効果的な投与の時期を確認したこと、2つ目は、地域の全死亡者数と、特定の年齢層におけるCOVID-19の症例数のデータを、National Computer System of Deaths (SINADEF)とNational Institute of Statistics and Informaticsのレジストリから抽出したことである。 48 なお、彼は、若年層の感染者数の増加との混同を避けるため、分析対象を60歳以上の国民に限定した。これらのデータをもとに、ペルーの8つの州において、COVID-19の総症例数と人口10万人当たりの超過死亡数がこの年齢層で大きく減少した時期を、それぞれの州のイベルメクチン配布キャンペーンの開始時期と比較することができた(図4参照)。
図4: ペルー8州におけるイベルメクチン大量配布キャンペーン後の60歳以上の人口におけるCOVID-19の総症例数および総死亡数/人口の減少
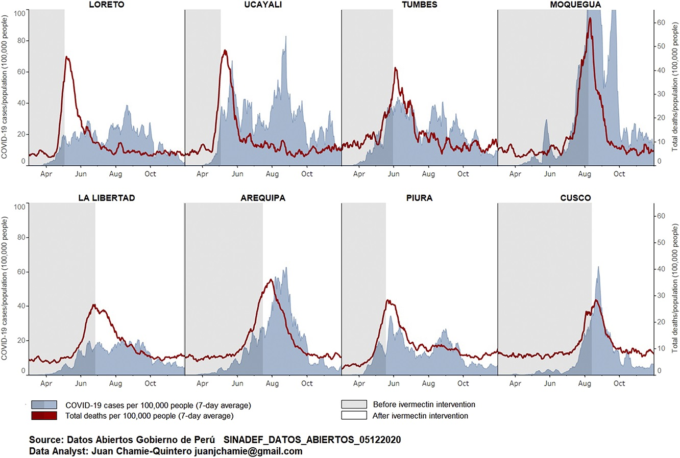
同じ研究の図5は、ペルーの8つの州における60歳以上の患者の致死率のデータを示している。COVID-19と診断された高齢患者の致死率は、イベルメクチンがこれらの地域で広く配布されるようになってから劇的に減少していることに注目してほしい。この結果は、マスク着用やロックダウンの変化では説明できない。
図5.: イベルメクチンを早期に大量投与したペルーの8州と、数カ月後にイベルメクチンを投与した首都を含むリマ州の60歳以上の患者集団におけるCOVID-19の1日あたりの総死亡者数、症例死亡者数、症例発生率
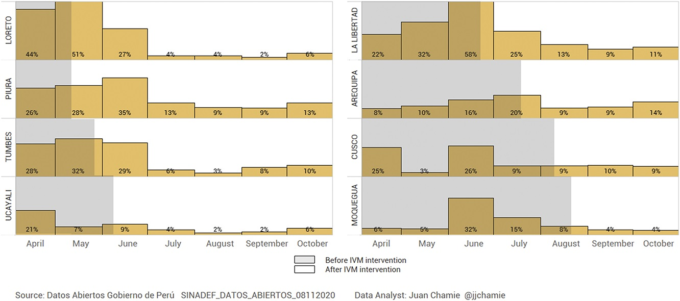
さらに、Chamie氏は、上記の8州と、同時期にイベルメクチンが配布されず、治療にも広く使われていなかったリマ市の症例数と致死率を比較している。図6は、リマ市では感染者数や死亡者数に有意な減少や持続的な減少が見られなかったことと、イベルメクチンが広く配布されていた8州では両方の結果が劇的に減少したことを比較したものである。
図6: ペルーの各州におけるイベルメクチン大量投与の有無によるCOVID-19症例死亡数と総死亡数
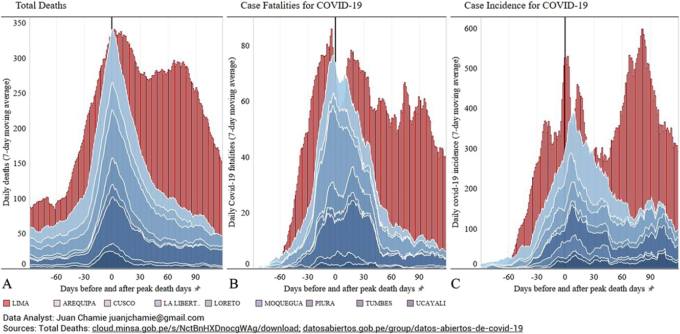
もう一つの例は、Chamie氏がまとめたパラグアイのデータから見ることができる。Chamie氏は、アルト・パラナ州の政府が9月初旬にイベルメクチンの配布キャンペーンを開始したことを指摘している。このキャンペーンは公式には「駆虫」プログラムとされているが、これはパラグアイでCOVID-19の治療にイベルメクチンを使用することを推奨している国立保健省からの叱責や対立を避けるための、地域の知事による装いであると解釈されている。プログラムは3万箱のイベルメクチンを配布することから始まり、10月15日には、図7に見られるように、州内にほとんど患者が残っていないと知事が宣言した。
図7.: パラグアイ-イベルメクチン配布開始後のAlto Parana(青の太線)におけるCOVID-19の症例数と死亡者数を他の地域と比較したもの
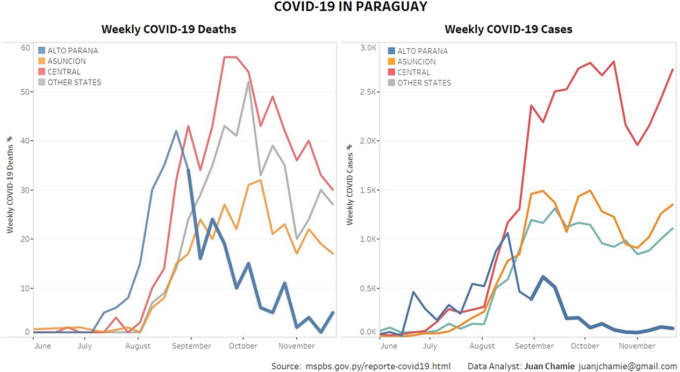
COVID-19に対するイベルメクチンのエビデンスベース
現在までに、COVID-19に対するイベルメクチンの有効性は以下のように裏付けられている。
- 2012年以降、複数の試験管内試験研究により、イベルメクチンがインフルエンザ、ジカ熱、デング熱などを含む多くのウイルスの複製を阻害することが実証されている9-17。
- イベルメクチンは、いくつかの観察および提案されたメカニズムにより、SARS-CoV-2の複製および宿主組織への結合を阻害する18。
- イベルメクチンには強力な抗炎症作用があり、試験管内試験 のデータでは、サイトカインの産生と炎症の最も強力なメディエーター である核内因子-κB (NF-κB)の転写の両方を深く阻害することが示されている37-39。
- 31,32 SARS-CoV-2または類似のコロナウイルスに感染した複数の動物モデルにおいて、イベルメクチンはウイルス量を有意に減少させ、臓器障害を防ぐ。
- イベルメクチンは、感染した患者に暴露された人のCOVID-19の感染と発症を防ぐ40-45。
- 症状が出てから早期に治療を受けた軽度から中等度の患者の回復を早め、悪化を防ぐ45,49-52,61,62
- 入院中の患者において、回復を早め、ICU への入室や死亡を回避する 45,51,53,63-66
- イベルメクチンは、COVID-19 を有する重症患者の死亡率を低下させる45,53,63
- イベルメクチンは、イベルメクチン配布キャンペーン後の地域において、時間的に関連した症例死亡率の低下をもたらす48。
- イベルメクチンの安全性、入手のしやすさ、コストは、約40年間の使用と数十億回の投与で観察された軽度でまれな副作用に加え、重要な薬物相互作用の発生率が低いことから、他に類を見ないものとなっている75。
- 世界保健機関(WHO)は、長年にわたりイベルメクチンを「必須医薬品リスト」に掲載している。
上記の対照試験で統計的に有意な結果が得られたものの概要は以下の通りである。
COVID-19 の予防に関する対照試験(8 つの試験)
- 入手可能な8つの対照試験の結果はすべて、統計的に有意な感染の減少を示している。
- 感染率が統計学的に有意に減少した3つのRCT、N=774人44-46
- 感染率を統計的に有意に減少させた5つのOCT、N=2052人の患者40-43,47
COVID-19を対象とした対照試験(19試験)
- 回復までの期間や入院期間に統計的に有意な影響を与えた5つのRCT 45,49,53,64,65
- 回復までの時間がほぼ統計的に有意に減少したRCTが1件、P=0.07,N=130.54
- 悪化率または入院率が大幅に統計的に有意に減少したRCTが1件、N=363.49
- ウイルス量、無嗅覚日数、および咳が統計的に有意に減少したRCTが2件、N=85.57,60
- 死亡率が統計的に有意に減少した3つのRCT(N=695)45,60,65
- 死亡率がほぼ統計的に有意に減少したRCTが1件、P=0.052(N=140)53
- 死亡率が統計的に有意に減少したOCTが3件(N=1688)51,63,66
イベルメクチンの安全性
多くの研究では、有害事象の発生率は低く、その多くは軽度で一過性のものであり、寄生虫の死に対する身体の炎症反応に起因するもので、かゆみ、発疹、リンパ節の腫れ、関節痛、発熱、頭痛などがある75。さらに、薬学的参照基準であるLexicompによると、イベルメクチンとの併用が禁忌とされている薬剤は、抗結核ワクチンとコレラワクチンの同時投与のみで、抗凝固剤であるワルファリンは投与量のモニタリングが必要とされている。また、免疫抑制剤や臓器移植を受けた患者で、タクロリムスやシクロスポリンなどのカルシニューリン阻害剤や免疫抑制剤のシロリムスを服用している場合、イベルメクチンを服用する際には、これらの薬剤の濃度に影響を与える相互作用があるため、注意深くモニタリングする必要がある。薬物相互作用のより詳細なリストは、drugs.comのデータベースに掲載されており、ほぼすべての相互作用がイベルメクチンの血中濃度の上昇または低下を引き起こす可能性がある。高用量のイベルメクチンを投与しても耐性があり、副作用がないという研究結果から、毒性は考えにくいが、血中濃度の低下による有効性の低下は懸念される77。
肝疾患のある患者に対する安全性の懸念は、我々の知る限り、イベルメクチンに関連して肝障害が報告されたのは2例のみであり、両例とも治療の必要なく速やかに治癒していることから、根拠のないものと考えられる78,79。イベルメクチンは神経毒性を持つ可能性があると言われているが、ある研究では、世界的な医薬品データベースを検索した結果、運動失調、意識変化、痙攣、振戦などの重篤な神経系有害事象は、約40億回の投与の中で28例しか見つからなかった80。しかし、報告された症例の総数から、このような事象は極めて稀であることが示唆されている。最後に,イベルメクチンは妊婦,小児,乳児にも安全に使用されている。
考察
現在 2020年12月14日時点で、COVID-19の予防と治療におけるイベルメクチンの安全性と有効性の両方を示すエビデンスが蓄積されている。大規模な疫学的分析により、試験管内試験、動物実験、予防、および臨床試験の結果が検証されている。イベルメクチンが広く使用されている地域の疫学データでは、症例数、入院数、死亡率が一時的に減少していることが実証されている。
イベルメクチンの長年にわたる安全性、低コスト、幅広い入手可能性に加え、感染率、入院の必要性、死亡率について一貫した再現性のある大きな結果が得られていることから、予防と治療の両方に広く使用することが提案されている。イベルメクチンの場合、(1)半数の試験が無作為化比較試験デザインを採用しており(上記レビューの24件中12件)(2)2014年に行われたこのテーマの大規模なコクランレビューで報告されているように、観察試験デザインと無作為化試験デザインは平均して同等の結論に達していることを認識する必要がある。 81 特に、(フロリダのRajter研究のように)傾向マッチング技術を用いたOCTは、冠症候群、重症患者、手術を含む多くの異なる疾患状態において、後に実施されたRCTとほぼ同じ結論を見出している82。 -同様に、予防試験(図1)と治療試験(図2,3)のメタアナリシス、および試験概要表(表3)に示されているように、OCTとRCTの両方の試験デザインで発見されたベネフィットの全体は、ベネフィットの方向性と大きさの両方で一致している。このように、世界中の様々な国やセンターで行われた様々な規模の試験デザインの中で、ベネフィットが一貫していることはユニークであり、強力な追加のサポートとなる。
COVID-19患者に対する適切な治療的介入を決定する上で、医療従事者が直面する継続的な課題は、主要な政府医療機関からより最新で適切なエビデンスに基づくガイダンスが提供されれば、大幅に緩和されるであろう。現在、米国では、COVID-19の治療ガイドラインは、米国国立衛生研究所(National Institutes of Health)が発行している。COVID-19患者へのイベルメクチンの使用に関する彼らの最新の推奨は、2021年2月11日に更新され、「COVID-19においてイベルメクチンの使用を推奨するには十分な証拠がない 」としている。主要な主要公衆衛生機関(PHA)がより決定的な勧告を出すためには、世界的な保健医療の緊急時であっても、イベルメクチンのような安全で、経口で、低コストで、広く利用でき、展開可能な介入策を考慮して、試験の質と量の両方に関するさらに多くのデータが必要であることは明らかである。
幸いなことに、2つの異なる組織がスポンサーとなっている大規模なチームがこの取り組みに着手している。1つは、ユニテイド/WHOのACTアクセラレータプログラムがスポンサーとなり、リバプール大学のシニアリサーチフェローであるアンドリュー・ヒル博士が率いるチームで、COVID-19におけるイベルメクチン治療のRCTのみに焦点を当てたシステマティックレビューとメタアナリシスを行っている。2月に17件のRCTの予備的なメタアナリシスがプレプリントサーバーに投稿されたが、2021年3月19日までに、約4500人の患者を含む約27~29件のRCTの結果がWHOガイドライン委員会に提示されることが予想され、Chamieらが上記でレビューした疫学研究は、すでに3月上旬に委員会に提示されている(アンドリュー・ヒル博士との私信)。なお、2月5日、WHOガイドライン委員会は、蓄積されたイベルメクチンのデータのレビューを開始し、4~6週間以内に独自の正式な治療勧告に到達する見込みであることを発表した。残りの臨床試験で上記のような効果が報告され続ければ、現在の支持的なエビデンスがほぼ倍増することになり、WHOやNIHなどのPHAによる使用勧告が行われることが期待される。
パンデミックの緊急性に鑑み、また、主要なPHAが驚くほど持続的な不作為を行っていることに対応して、WHOが行う標準的なガイドライン作成プロセスを用いてイベルメクチン治療ガイドラインをより迅速に策定するために、Evidence-Based Medicine Consultancy Ltd.によって英国イベルメクチン推奨開発パネルが最近コーディネートされた。このパネルは、WHOをはじめとする国内外の多くの公衆衛生機関で長年にわたり研究コンサルタントを務めてきたメンバーで構成され、運営委員会と技術ワーキンググループを招集し、システマティックレビューとメタアナリシスを実施した。2021年2月12日には、世界16カ国のほとんどの地域を代表する75名の実務家、研究者、専門家、患者代表からなる国際コンソーシアムによる会議が開催された。この勧告開発パネルには、2500人以上の患者を含む18の治療RCTと3つの予防RCTのメタ分析の結果に加えて、観察試験の概要とイベルメクチンの地域的な使用に関連する疫学的分析が提示された。討議期間の後、WHOの標準的なガイドライン作成プロセスに従って、イベルメクチンに関するデータの複数の側面について投票が行われた。パネルは、イベルメクチンの生存率に対する効果を示すエビデンスの確実性が高いと判断し、COVID-19の予防と治療に使用するために無条件に採用することを推奨した。
以上、本レビューで提示された臨床試験および疫学的エビデンスの全体像に加え、Unitaid/WHOによる治療RCTのメタアナリシスの予備的知見、およびBIRD国際会議でのガイドライン勧告に基づき、COVID-19の予防および治療にイベルメクチンを世界的かつ体系的に導入すべきであるとした。