Contents
- Potential Role of Oral Rinses Targeting the Viral Lipid Envelope in SARS-CoV-2 Infection
Potential Role of Oral Rinses Targeting the Viral Lipid Envelope in SARS-CoV-2 Infection
www.ncbi.nlm.nih.gov/pmc/articles/PMC7239187/
要旨
新たな研究により、初期のCOVID-19疾患におけるウイルス複製および感染の部位としての喉および唾液腺の重要性がますます明らかになってきている。SARS-CoV-2はエンベロープ型ウイルスであり、宿主細胞に由来する外部脂質膜を特徴とする。脂質生体膜を破壊する薬剤には非常に敏感であるが、感染防止における口腔洗浄の潜在的な役割についてはこれまで議論されていなかった。
ここでは、エタノール、クロルヘキシジン、塩化セチルピリジニウム、過酸化水素、およびポビドンヨードを含む広く入手可能な歯科用洗口剤成分によるウイルス脂質膜破壊の既知のメカニズムをレビューする。
また、これらの薬剤の濃度に基づいて、SARS-CoV-2の脂質包絡膜を破壊する潜在的な能力について既存の製剤を評価し、いくつかの薬剤は臨床評価に値すると結論づけた。我々は、コロナウイルスを含む他のエンベロープ型ウイルスに関する既に発表されている研究が、SARS-CoV-2の感染を減少させるための潜在的な方法として経口洗浄を考慮すべきであるという考えを直接支持していることを強調している。これを検証するための研究としては、既存の製剤や特別に調整された新しい製剤を、十分に設計されたウイルス不活化試験で評価した後、臨床試験を実施することが考えられる。集団ベースの介入は、有効性を判断するために結果を積極的にモニタリングしながら、入手可能な洗口剤を用いて実施することができる。これは臨床的に必要とされている未研究の領域である。
キーワード:コロナウイルス、脂質、エンベロープ、口腔咽頭、ウイルス、呼吸器
ウイルス性脂質エンベロープ
インフルエンザや単純ヘルペスなど多くのウイルスに共通して、コロナウイルスは「脂質エンベロープ」と呼ばれる脂肪層に囲まれており、その中に感染に必要なスパイク糖タンパク質が挿入されている(図1)。ウイルスのエンベロープは宿主細胞膜で獲得され、その一部は形質膜で、他の一部は核膜、小胞体、ゴルジ体などの内部細胞膜で獲得される3,4。6-12 SARS-CoV-2のエンベロープの脂質組成はまだ特徴づけられていないが、コロナウイルスは小胞体ゴルジ中間コンパートメント(ERGIC)から芽を出し、エキソサイトーシスによって輸送される前に、貨物小胞で輸送されることが知られている13,14。6-12 最近の報告では、コロナウイルス(HCoV-229E)が他の多くのウイルスと共通して、感染に応答して宿主の脂質代謝を制御していることが示された15-17 が、ウイルス脂質エンベロープの組成に関する情報は提供されておらず、その特異的な組成は実験的に決定されていない。
図1 ウイルスエンベロープに埋め込まれたSARS-CoV-2糖タンパク質と膜破壊剤の漫画表現
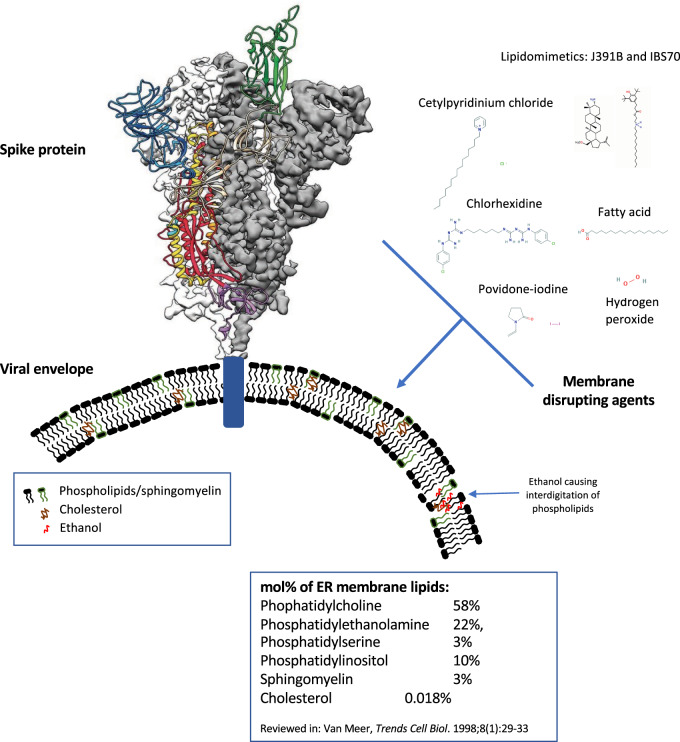
表面中和に関連する石鹸/アルコールウイルス性公衆衛生上のアドバイス
脂質エンベロープへの干渉が、多くのコロナウイルスを標的としたウイルス殺傷戦略であることは広く知られており、多くの薬剤の影響を証明する多くの研究が行われている。19-21 SARS-CoV-2に関する最近の研究もこれを支持しており、最近のプレプリントで示されているように、高濃度は非常に効果的であることが示されている。殺微生物研究において高濃度の試験のみを行ってきた歴史的な理由は、これらの試験では細菌、ウイルス、真菌に対して幅広いスペクトルの活性が得られるため、標的微生物が不明な無生物の表面/微生物への使用が常に好まれてきたことにある。コンセンサスは、ヘルペスウイルス、オルソミキソウイルス、パラミクソウイルス、コロナウイルスなどのエンベロープウイルスは、60%~70% (v/v) エタノールに対して非常に感受性が高く、ほぼ即時に不活性化されるのに対し、非エンベロープウイルスは感受性が低いか、あるいは低いというのが見解である。
最近の世界保健機関(WHO)や環境保護庁の勧告(https://apps.who.int/iris/bitstream/handle/10665/331138/WHO-WPE-GIH-2020.1-eng.pdf; www.epa.gov/pesticide-registration/list-n-disinfectants-use-against-sars-cov-2; …www.who.int/gpsc/tools/GPSC-HandRub-Wash.pdf)を含め、これらの薬剤は脂質包絡膜にダメージを与えるという見解に基づいて、SARS- Medical Journalに掲載された医療従事者を感染から保護するよう呼びかけた論文に対する最近の反応を除けば、これまで議論されたことはなかった(https://www.bmj.com/content/369/bmj.m1324/rr-5)。この問題に対処するための適切に設計された臨床試験は、現在のところ文献では不足している。在宅での SARS-CoV-2 の臨床管理に関する現在の WHO の暫定ガイダンスでは、空気感染やウイルスの直接感染のリスクを減らすために、手、衣服、表面の衛生管理に加えて、フェイスマスクなどの個人的な保護具を使用することに重点が置かれているが、口腔衛生については言及されていない(https://apps.who.int/iris/handle/10665/331133)。このように、SARS-CoV-2の環境下での有用性は体系的に検討されておらず、肯定的または否定的な頑健な臨床的証拠も不足している。
マウスウォッシュの組成は多岐にわたっているが、英国、欧州、米国では、市販されている製剤の中にはエタノールを14~27%(w/v)含有しているものもある。そこで我々は、現在のパンデミック状況において、特に脆弱な個人や医療従事者に対するウイルス感染を抑制するために、エタノールベースの洗口剤やその他のタイプの洗口剤を用いた経口治療が、ウイルス負荷を軽減または低減する戦略となり得るかどうかを確認するために、利用可能な科学的文献をレビューした。我々は、エンベロープドウイルスの不活化に対する低濃度(毒性の低い)エタノールの影響を体系的に試験したデータが少ないことを発見したが、ほとんどのデータでは、上記の高濃度の使用を繰り返すだけである。
SARS-CoV-2 におけるウイルス負荷、唾液/咽頭ウイルス、および重症度
喉はCOVID-19病におけるウイルスの主要な複製・脱落部位であり、ウイルス負荷が重要であることが認識されるようになってきている27 。ウイルス負荷は高齢と相関しており、中国南昌市で 76 人の患者を対象とした研究では、重症の SARS-CoV-2 患者は軽症の患者に比べてウイルス負荷が高く、ウイルス脱落期間が長い傾向があることが示されている30 。同様に、肺炎患者 12 人を対象とした研究では、ウイルス負荷は肺疾患の重症度と関連している31 。32 GTEX遺伝子発現データからのデータは、アンジオテンシン変換酵素(ACE2)(COVID-19の重要な受容体)の発現が肺よりも唾液腺で高いことを示しており、これらの腺が新しいウイルス粒子の主要な供給源である可能性を示唆している。移動性データとベイズ推論を用いた最近の研究では、文書化されていない感染率が高いことが SARS-CoV-2 の急速な感染拡大の原因であることが推論されている34 。ウイルス負荷と症状の重症度との関係をよりよく理解するためには、さらなる研究が必要であるが、喉や肺でのウイルスの排出量が多いことは、他の人への感染力の増加と関連していると考えられる。現在までのところ、肺とのどのウイルス負荷と重症度の関係は明らかになっておらず、のどのウイルス負荷を軽減することが、結果として生じる肺疾患やウイルス感染にどのような影響を与えるのかはわかっていない。
SARS-CoV-2 の感染経路は、現在のところ SARS-CoV と同様に呼吸器飛沫を介していると考えられており35 、ウイルス粒子はエアロゾル中で最大 3 時間生存可能である36 。36 もしそうであれば、ウイルス粒子の除去や不活性化を促進することで粘膜中の感染性ウイルス粒子の数を減らす戦略が、感染リスクの低減に貢献する可能性がある。このように、喉が初期(症状が現れる前であっても)の主要な複製部位であると仮定すると、脂質エンベロープを損傷または破壊する可能性のある薬剤を用いた口腔洗浄は、口咽頭におけるウイルス負荷を低減させる可能性がある。
現時点では、SARS-CoV-2がどのようにして喉や鼻から肺に移動するかについての情報は不完全であり、(1)ウイルスの脱落、(2)壊死細胞の破片の吸引、(3)隣接する細胞への直接感染などが考えられる。ウイルスの脱落が関与していると仮定すると、ウイルス脂質エンベロープを標的とする経口洗浄剤は、喉で生成された感染性粒子を除去/リンスするか、または不活性化するための潜在的な方法である。ヒトにおけるSARS-CoV-2の特異的な細胞内複製サイクルはまだ知られていない。24時間未満の非同期複製サイクルに基づいて、ウイルスはほぼ常に分泌されている可能性が高い37,38 。したがって、治療の持続性が重要になる。洗口剤成分が口腔内の生体膜と相互作用する能力をどのくらいの時間保持するかは不明であり、さらなる研究が必要とされている。
エタノール濃度低下による生体膜への影響
より低い(毒性がなく、より経済的な)エタノール濃度を検討する場合には、(脂質エンベロープの起源となる)哺乳類細胞の文献が近い比較対象となる。また、ホスファチジルコリンなどのリン脂質からなるモデル膜小胞の研究もレビューしたが、これらはタンパク質を含まないため、エタノールの毒性に対する非脂質成分の影響は考慮されていない。細菌病原体は、リポ多糖類やペプチドグリカンなど、脂質やタンパク質の組成が大きく異なる膜を含んでいるため、ここでは考慮していない。以下、エタノールの細胞/モデル膜への影響に関する文献をまとめてみた(表1)。
表1. 生体膜またはエンベロープされたウイルスに対するエタノールの影響を支持する試験管内試験および生体内試験のデータ
| 参照 | 研究タイプ | エタノール | 結果 |
|---|---|---|---|
| ライとロンゴ39 | 膜小胞のモデル化(膜の流動性、透過性、交互嵌合、厚さなど) | エタノール> 3.4 M(20%v:v) | 「安定」とは見なされない膜。交互嵌合; PCベシクルの急速な腫れ |
| Ahl etal。40 | SUVからの交互嵌合PLシートの形成 | 2 Mを超えるエタノール(11.8%v:v) | より大きなIFVを形成しました。小胞の内容物の漏れ |
| ハントら。41 | モデル膜の遷移段階を繰り返し循環する | エタノール86mM(0.5%v:v) | PCベシクルの溶解 |
| 小松他 42〜44 | PC、PE / PC、またはPC /コレステロールで作られたベシクルからの色素の漏出。 | 0.6〜2.1 M(3.5%〜12.3%、v / v) | カルセインは低エタノール濃度で漏れ出します。小胞の急速な腫れ。 |
| デニソン等。45 | In vitro-ヘルペス、インフルエンザ、ロタウイルス、およびアデノウイルス | エッセンシャルオイルを含む26.9%エタノール(v:v) | エンベロープウイルス(ヘルペスとインフルエンザ)は大きな影響を受けました |
| IADRアブストラクト2010 | H1N1インフルエンザパンデミック株、invitro | 21.6%エタノール、30秒すすぎ | 感染力が99.99%以上減少 |
| ロバーツとロイド46 | 3つのエンベロープウイルス:invitroでのシンドビス、単純ヘルペス-1およびワクシニア | 20%(v:v)エタノール | 完全に不活化 |
| Siddharta etal。47 | エンベロープウイルス; コロナウイルスの存在下でのinvitro感染性WHO製剤I。 | 34%(v:v)エタノールを含む希釈液の30秒間の曝露 | その後のウイルス複製を完全に防止 |
| Oh etal。48 | 哺乳類の細胞膜:角膜上皮細胞 | 20%エタノール; 30秒のインキュベーション | 生存率の40%の損失; 細胞内内容物の高レベルの漏出 |
| Sonmez etal。49 | 哺乳類の細胞膜:赤血球 | 1M(5.9%v:v)エタノール | 約10%の細胞溶解 |
| カイおよびWu 50とTyulinaら。51、52 | 哺乳類の細胞膜:赤血球 | 3〜4M(18%〜23.5%)程度の中程度の濃度。 | カリウムの漏出と溶血 |
| 王ら。53 | 哺乳類の細胞膜:腸細胞株(Caco-2) | エタノール> 5%–10%:60分の長いインキュベーション時間 | 生存能力の喪失、内容物の漏出、および密着結合の破壊。 |
| Meiller etal。54 | インビボヒト研究 | 21.6%エタノール、30秒すすぎ | 単純ヘルペスI型およびII型の回復可能なビリオンはすすぎ後0になります。30分ですべてプレリンスより低く、11/20は0のままでした |
| Meiller etal。54 | インビボヒトリピート研究 | 21.6%エタノール、30秒すすぎ | すすぎ後18/20および30分で12/20に0の回収可能なビリオン。60分ですべてベースラインよりも少ない |
| Sattar etal。(未発表データ) | 大人の指パッド; 乾燥接種物; ヒト呼吸器コロナウイルス229E | 60%および70%エタノールを20秒間さらしたハンドジェル | ウイルスの生存率は、どちらの場合も99.99%以上減少しました |
本文中で引用されている研究は、種類、エタノール量、結果の順に上記にまとめられている。これらの研究は、モデル膜の順に、ウイルスを用いた試験管内試験研究、哺乳類細胞膜を用いた研究、そして生体内試験研究の順に記載されている。エタノール濃度も記載されているが、場合によっては、v/vまたはw/vを使用したかどうかが記載されていないこともある。すべての研究において、膜に対するエタノールの影響に関する完全な情報については、一次文献 PC、ホスファチジルコリン、PE、ホスファチジルエタノールアミン。
エタノールの低濃度はモデル膜の膨潤、絡み合い、および漏れを引き起こす
1980年代から 1990年代にかけての生物物理学的研究では、モデルリン脂質膜を摂動させる能力について様々なアルコール(エタノール、メタノール、ブタノール、プロパノール)を比較している。多くは薬物送達のために脂質ベシクルの生成を最適化していたが、ほとんどの短鎖アルコールの毒性は経口投与を禁止していた。ここでは、モデル膜におけるエタノールの特性に関する報告をレビューした。溶解を直接調べた研究はほとんどなく、代わりに膜の流動性、透過性、浸潤性、膜厚、その他のパラメータに焦点を当てていた。ある研究では、エタノールを3.4M(20% v/v)以上添加した場合、膜は「安定」とはみなされなかったとされている。 55Interdigitationとは、短鎖アルコールの存在により、脂肪アシル鎖のメチル基が二重層の中面を越えて反対側の単分子膜を貫通する過程を指し、小胞の融合と漏出に先行して促進される事象であると考えられている56。これは、この濃度のエタノールが小さなリン脂質小胞を変形させ、より大きな構造の融合と形成をもたらすことを意味する。この過程で、小胞からの内容物の漏出が見られる。3つの研究では、ホスファチジルコリン単独、ホスファチジルコリン/ホスファチジルエタノールアミン混合物、ホスファチジルコリン/コレステロール混合物のいずれかで構成される膜を比較し,0.6~2.1M(3.5%~12.3%, v/v)程度のエタノール濃度ですべての膜が透過性になることを示した43。このことは、複雑な生物学的膜は非常に異なる反応を示す可能性があり、他の脂質の存在だけでなく、タンパク質の影響も考慮する必要があることを示している。それにもかかわらず、硬い表面上のウイルスの不活化のために現在推奨されている60%~70%よりもはるかに低い濃度で、また、広く入手可能な洗口剤に含まれる量で、モデル膜がエタノールに敏感であることは明らかである(セクション6)。
哺乳類細胞膜に対するエタノールの影響
また、試験管内試験での哺乳類細胞へのエタノールの影響についても検討した。コロナウイルスに直接関連するものとして、角膜上皮細胞を対象とした研究では、20%エタノールで 30 秒間インキュベートすると、生存能力が約 40%低下し、40%エタノールでは 70%まで低下することが示された。この短いインキュベーションは、炎症反応、分化、上皮マーカーの発現にも影響を与えた。Sonmezらは、約1M(5.9% v/v)で約10%の細胞溶解を引き起こすことを示しているが、それ以上の量は試験されていない。49 赤血球への影響は、3-4M(18%-23.5% v/v)程度の中等度の濃度では、カリウム漏出や溶血を含む様々な影響が示されている。50-52 最後に、腸管細胞株(Caco-2)を用いた研究では、エタノールの濃度が 5-10%を超えると、60 分間の長時間の培養で、生存能力の低下、内容物の漏出、タイトジャンクションの破壊を引き起こすことが示されている。
これまでのところ、エタノールの量を減らした場合のエンベロープされたウイルスへの影響を試験した研究を発見しただけである。いずれも試験管内で実施されたもので、ウイルスの変性に関連して肯定的な結果を示している。
- 2007,ロバーツとロイドは、20%エタノールを使用すると3種類のエンベロープウイルスが完全に不活化されることを発見した。46 不活化は、ウイルス感染力アッセイにおけるプラーク形成ユニットの阻害によって測定されたが、ウイルスエンベロープへの直接的な影響は明らかにされなかった。この研究では、土壌負荷がない場合には、かなり基本的なシステムを使用したが、これは、現在では米国試験材料協会(ASTM)委員会E35 on Pesticides, Antimicrobials and Alternative Control Agents(https://www.astm.org/Standards/E2197.htm)または英国では、同等の英国規格(BS)Norme Européenne(EN)規格(BS EN 14476:2013+A2:2019 Chemical disinfectants and antiseptics)で推奨されているものである。医療分野におけるウイルス性活性の評価のための定量的懸濁試験 試験方法と要件(フェーズ2/ステップ1)https://shop.bsigroup.com/ProductDetail?pid=000000000030401479)。また、より関連性の高い36.8℃の経口温度ではなく、変性剤の影響が大きくなる22℃で実施された。
- 2017,Siddhartaらは、コロナウイルスを含むエンベロープ型ウイルスに対するWHO推奨製剤の試験を行った。85%(v/v)エタノール,0.725%(v/v)グリセロール、および0.125%(v/v)過酸化水素を含むWHO製剤Iに焦点を当て、彼らは土壌負荷(0.5%w/vウシ血清アルブミン)の存在下で試験管内試験感染性を測定した。34%(v/v)エタノール(ニートの40%)を含む希釈液を30秒間曝露すると、その後のウイルス複製が完全に防止された47。
これらの研究は、比較的希釈したエタノールがエンベロープされたウイルスに対して非常に有効であることを示している。しかし、生物学的に関連する条件下(粘膜、口腔など)でコロナウイルスが希釈アルコールによってどのように影響を受けるか、また、非毒性の膜破壊剤と組み合わせてSARS-CoV-2の経口不活化を達成できるかどうかを決定する必要性が急務となっている。最低量のエタノール、例えば10%〜30%(v/v)のエタノールが有効であろうし、接触時間もまた、必要とされるエタノール曝露を減少させ得る重要なパラメータであろう。エタノールは、人工脂質膜の膜特性に影響を与え、完全な溶解がない場合でも内容物の漏出を引き起こす。宿主細胞に感染するウイルスの能力はまた、タンパク質の機能に影響を与えるウイルス膜への生物物理学的変化を誘導することによって変更される可能性がある。SARS-CoV-2 の感染に必要なスパイク糖タンパク質は、ウイルスエンベロープに挿入された膜貫通ドメインを有しており1 、脂質膜の生物物理的な摂動が哺乳類細胞の多くの膜貫通タンパク質の構造や機能に影響を与えることが知られている。この点で、HIV-1 の脂質膜はウイルス膜の糖タンパク質を安定化させ、抗体による中和に対する感受性を制御することが最近明らかになった62 。エタノールまたは他の薬剤が生体内でのSARS-CoV-2スパイク蛋白質の感染活性に与える影響を決定するためには、研究が必要である。
溶解を伴わない膜の摂動は、エンベロープされたウイルスの感染性を減衰させることができる
膜を乱すことでウイルスを不活性化するという概念は、膜破壊剤との関連で最近検証されており、1000種の化合物の試験管内試験スクリーニングにより、膜を変化させ、HIV-1の感染性を減衰させることができる一連の脂質模倣薬が同定された。活性剤には、コレステロール、スフィンゴシン、または宿主細胞への侵入の段階でブロックする長鎖脂肪酸を持つ脂肪族脂質が含まれていた。その影響は、脂質が膜に取り込まれ、脂質の秩序と粒子の浮力密度の変化を誘導することに起因しているように見えた。これを裏付けるように、1970年代の研究では、炭素鎖長16~18の脂肪酸とモノグリセリドが試験管内試験で非常に効果的で,0.2μMまでの濃度で単純ヘルペスウイルスの生存率を約50%まで低下させたことが示されている。
発表された研究でエンベロープウイルスに対して活性を示すマウスウォッシュ製剤
市販のマウスウォッシュが、エタノール(表1)または他の活性剤によってウイルスの脂質エンベロープを破壊する可能性を、利用可能な文献をレビューして調査した。
メリーランド大学、テキサス・ヒューストン健康科学センター、およびニューヨーク州立大学の3つの業界主催の研究では、21~26%のエタノールとエッセンシャルオイル(ユーカリプトール0.092%、メントール0.042%、サリチル酸メチル0.060%、およびチモール0.064%/v)を組み合わせた広く入手可能な処方を使用して、この試験を実施した。注目すべきは、ユーカリ油とチモールがこれらの濃度で単純ヘルペスウイルスに対して有意な抗ウイルス性を有することを示す証拠が発表されており、これはウイルスの脂質エンベロープの破壊に関連していると仮定されている64。
- エッセンシャルオイルを用いた21%(v/v)エタノールの包絡ウイルスに対する殺ウイルス作用は 2005年にヒトの生体内で報告された。具体的には、単純ヘルペスI型およびII型の感染性ウイルスを30秒のすすぎで実質的にゼロにした54。対照的に、蒸留水でのすすぎでは、30分後のすすぎでは平均値の低下がかなり少なく、30分後にはほぼベースラインに戻っていた。このことは、洗口剤がウイルスの回復に特異的かつ有意な影響を与えたことを示している。繰り返しの試験では、18/20人の被験者が30秒後のすすぎ後にゼロになり、12/20人の被験者は30分後にゼロのままであった。60分後の時点では、20人全員がベースラインよりも1-2 log10低い値でウイルスを排出しており、ウイルス力価への影響はわずかであることが示された。54 ヘルペスウイルスはコロナウイルスとは異なり、前者は神経の中に存在するところから周期的に噴出する可能性があるので、洗口剤を使用すると一時的にレベルが低下し、病変の解決を促進する可能性がある。逆に、コロナウイルスは積極的に複製すると、ほぼ常時排出される。
- 1995年に行われた研究では、26.9%エタノールに精油を加えたものを、試験管内試験でヘルペス、インフルエンザ、ロタウイルス、アデノウイルスに対して試験した。ここでは、ヘルペスとインフルエンザは有意な影響を受けたが、アデノウイルスとロタウイルス(非発生型)は影響を受けなかったことから、ウイルスの脂質エンベロープへの影響が推測されている45。
- 2010年に行われた未発表の追跡研究では、エッセンシャルオイルを用いた21.6%エタノールへの30秒間の試験管内試験曝露により、H1N1インフルエンザAパンデミック株の感染率が99.99%以上低下したことが明らかになった(https://iadr.abstractarchives.com/abstract/2010dc-131191/evaluation-of-h1n1-antiviral-properties-of-an-essential-oil-containing-mouthrinse)。
これらの研究は、21%~27%のエタノールを含むエッセンシャルオイルを含むマウスウォッシュ剤が、実験室でもヒトでも、エンベロープ化されたウイルスを不活化できるという概念を証明するものであり、そのメカニズムは脂質エンベロープへの損傷である可能性が高いと考えられている。ここでは、エッセンシャルオイルと組み合わせたエタノールが、より効果的な処方を提供する可能性がある。このように、研究は行われていないが、これらのタイプの洗口剤はSARS-CoV-2に対して有効である可能性がある。市販されている他のエタノール洗口剤は、一般的にエッセンシャルオイルを含まない低濃度のものが多いが、膜の生物学的な影響は理論的には可能であり、研究が必要である。
クロルヘキシジン
クロルヘキシジンは、英国では口腔衛生のために広く使用されており、特にグラム陽性菌に有効であるが、グラム陰性菌や真菌にはあまり効果的ではない65 。0.12%の試験管内試験での殺ウイルス効果に関する報告では、クロルヘキシジンはエンベロープされたウイルスのウイルス濃度を減少させることができるが、非エンベロープされたウイルスのウイルス濃度は減少させないことが示されている66 。クロルヘキシジンは低濃度のエタノールと一緒に製剤化されることが多く、これがそのウイルス性の影響の一端を説明しているかもしれない。コロナウイルスの文献の最近のレビューでは、使用した濃度は 0.02%と低濃度であったにもかかわらず、クロルヘキシジンを 10 分間曝露しただけで、懸濁液試験ではコロナウイルス株を弱く不活化したことが確認されている19,24。67 コロナウイルスに対する活性が低いにもかかわらず、クロルヘキシジンとアルコールの組み合わせは、より長い時間をかけてウイルスの負荷を軽減するための有用な戦略となる可能性がある。
クロルヘキシジン洗口剤は、化学療法や放射線療法を受けているがん患者の口腔内細菌叢を減少させ、感染症や粘膜炎を予防するための重要な臨床ツールとして40年以上にわたって使用されてきた68-70 。最後に、最近のメタアナリシスでは、原因菌は記載されていないが、クロルヘキシジン(リンスまたはゲル)が機械換気を受けている患者の人工呼吸器関連肺炎のリスクを低下させることが示された71。
ポビドン-ヨード
ポビドンヨード(PVP-I)洗口剤は、広範囲の抗菌・殺菌作用について広く研究されている。日本で日常的に使用されている0.23%のPVP-Iは、SARS-CoV、MERS-CoV、インフルエンザウイルスA(H1N1)およびロタウイルスを試験管内試験で迅速に不活化する72。実際、日本では、試験管内試験試験や限られた臨床試験に基づいて、厚生労働省が上気道感染症の予防策として毎日のうがいを支持している74。PVP-Iの場合にこれを支持する少数のヒト研究では、うがいを繰り返すことで細菌感染とウイルス感染(インフルエンザ)の両方の発生率が減少することが示されている72,75 ある限定的な研究では、山形市の中学校の欠席率を3ヶ月間で比較した。別の研究では、23人の患者のグループが1日4回以上うがいを2時間まで行ったところ、慢性呼吸器感染症の急性増悪が約50%減少した。1%溶液として、PVP-Iは香港、韓国、シンガポール、マレーシア、フィリピン、台湾で入手可能である。PVP-Iは、世界保健機関の必須医薬品リスト(https://www.who.int/medicines/publications/essentialmedicines/en/)に掲載されていることから、局所用の幅広い抗菌剤として高濃度のPVP-Iの重要性が示されている。まれなアレルギー反応がPVP-Iに対して報告されていることに注意すべきである。
塩素化水または高張性生理食塩水での洗浄
日本で行われた研究では、驚くべきことに塩素処理された水道水によるうがいが呼吸器感染症を減少させ、ある研究ではPVP-Iよりも優れていた。ある研究では、年齢と性別が一致した約130人のヒトを対象に3つのグループ(20mLを1日3回、少なくとも1日3回、60日間、15秒間うがいを行う)が調査された78。しかし、塩素の殺ウイルス効果に関する情報は、30 分間の接触時間を含む 試験管内試験 試験(1 試験は 30 分間の接触時間を含む)から得られたものであり、水道水のうがいによるエンベロップドウイルスに対する生体内での影響は不明である。2008年の別の試験では、約120人の被験者の2つのグループで60日間水をうがいした場合の経済性を計算し、これが上気道感染予防のための費用対効果の高い戦略であると結論づけている80 。最後に、最近の研究では、高張性生理食塩水でのうがいと鼻洗浄が、症状、発病期間、ウイルスの脱落を減少させることが示された。しかし、これは試験的な、非盲検、自己報告の研究であったため、確定的なものとは考えられない。81 ヒトコロナウイルス 229E を含むエンベロープ型および非エンベロープ型ウイルスを用いた 試験管内試験 でのフォローアップ研究では、これが細胞内の塩化物レベルとペルオキシダーゼ活性の変化に関係している可能性が示唆された。
経口洗浄とは別に、生理食塩水による鼻洗浄は、風邪やアレルギーの患者の鼻腔をきれいにするために推奨されている一般的な方法であることは注目に値する。ウイルスが鼻咽頭で回収されることを考えると、予防策としての利用も同様に考えられる。
洗口剤については、鼻洗浄が呼吸器感染症の予防にどの程度効果があるかについては、臨床研究では体系的に検討されていない。特に、沸騰していない水道水に寄生アメーバが含まれていることから、適切に洗浄しないと重症化するという報告がまれにあることから、CDC(https://www.cdc.gov/parasites/naegleria/sinus-rinsing.html)では洗浄用注射器の消毒を慎重に行うことを推奨している。
過酸化水素
過酸化水素は、無酸素ラジカルによる脂質膜の破壊を引き起こし、歯のホワイトニング剤として広く使用されている。最近のシステマティックレビューを含む研究では、コロナウイルス229Eおよびその他のエンベロープドウイルスは約0.5%の濃度で不活化されることが報告されている19,83。過酸化水素の濃度が高い(5%以上)と軟組織および硬組織の両方に損傷を引き起こすが、ホワイトニング用の洗口剤に使用される濃度が1%~3%の範囲内では損傷はほとんどないと報告されている84。口腔内環境では、唾液中の宿主や細菌由来のカタラーゼ活性や他の内因性ペルオキシダーゼの存在により、過酸化水素は急速に不活性化される。85 ペルオキシダーゼの影響は、水と一緒にプレリンゼを使用することで理論的には減少させることができるが、これまでのところ、これは試験管内試験でしか確認されていない。
第四級アンモニウム化合物
これらの化合物は、細胞表面のタンパク質や脂質成分、特にグラム陽性菌やグラム陰性菌に作用する殺菌剤として広く使用されている。79 この化合物群の中で、塩化セチルピリジニウム(CPC)は、最近、試験管内試験および生体内試験の両方で、ウイルスのエンベロープを直接攻撃することにより、インフルエンザに対して活性があることが示されており、試験管内試験でのEC50は5~20μg/mLであった89。CPCは、英国では0.025%~0.075%/v(250~750 µg/mL)の濃度で薬用経口洗浄液に使用されているが、一部の国で販売されているトローチには1.4~3.0 mgのCPCが含まれている。
歯科診療および免疫抑制患者における口腔衛生および微生物殺虫剤の使用に関する最新の方針
歯科医師はSARS-CoV-2に曝露されるリスクが高く、臨床的に洗口剤を使用することを推奨するガイドラインがある。以前に発表された歯科環境における感染制御のためのCDCガイドラインでは、あらゆる種類の空気感染性病原体の広がりを軽減するために、前もって洗口剤を使用することが有用である可能性があることが引用されている90 。実際、CPCおよびクロルヘキシジンを含むウイルス性成分が、この環境における細菌汚染の軽減にどのように効果的であるかについての研究が行われているが、ウイルスの不活化はテストされていない91,92。最後に、SARS-CoV-2 に関連して歯内療法士のためのガイドラインを提供することを目的とした最近の 2 つの論文では,0.2%の PVP-I を使用した前処置前のマウスリンスが推奨されている。
研究の緊急の必要性
口腔衛生が SARS-CoV-2 の感染を抑制するための実行可能なアプローチであるかどうかについては、多くの疑問に対処する必要があり、これに対処するための研究が必要とされている。
口腔衛生に関連して、私たちは決定する必要がある。
- 口腔内洗浄によって口腔咽頭のウイルス負荷を低減できるか?
- もし負荷を減らすことができるのであれば、どの口腔洗浄剤が臨床的に効果的なのであろうか。現在選択されているのは、20%~30%エタノール、脂質ベースの膜破壊剤、PVP-1,CPC、過酸化水素、単純塩素化水道水、またはWHO製剤Iを30%に希釈したものであるか?
- より低い量の薬剤の組み合わせの方が忍容性が高く、副作用を軽減し、効果を持続させることができるであろうか?
- どのような組み合わせや薬剤、接触時間、使用頻度で抗ウイルス活性を誘導し、SARS-CoV-2の感染性を低下させるか?
利用可能な研究アプローチには以下のようなものがある。
統計的疫学研究により、口内洗浄が SARS-CoV-2 を含む咽頭および呼吸器感染症の発生率の低下と関連しているかどうかを集団レベルで立証することができる。健康関連製品の購入データを利用して、健康との関連性をモデル化することができる。SARS-CoV-2の症状を広範囲にモニタリングするための新しいアプリケーションでは、症状や重症度との相関性を調べるために洗口剤の使用状況を把握し、無症状の人の幅広い購買行動を把握することができる。モデル化アプローチでは、洗口剤の集団使用とウイルスの拡散も考慮すべきである。
研究の裏付けとなるもの。すべての包まれたウイルスが同じというわけではなく、ヘルペス、インフルエンザ、および麻疹ウイルスは、ヒトのコロナウイルスよりも不安定であると考えられており、これらのウイルスは、無生物の表面上で最大 5 日間持続する可能性がある19,36,96 。SARS-CoV-2 リピドームの正確な組成は、リピドミクス質量分析法を用いて決定する必要がある。研究では、試験管内試験および生体内試験でのスパイク蛋白質自体の感染活性に対するエタノールまたは他の薬剤の影響を決定する必要がある。試験管内試験で試験するのに有用なウイルスは、ヒト呼吸器コロナウイルス229Eで、ヒトコロナウイルスのサロゲートとして広く使用されているが、必要なのはカテゴリー(Cat2)の手順のみで、その複製および伝播条件はすでに十分に確立されている。病原性コロナウイルスの代表格としては、Cat3 のバイオセキュリティを必要とする SARS-CoV-2 に絞る前に、これが良いと思われる。
温度と土壌負荷の影響は、ASTMまたはEU標準プロトコル(https://www.astm.org/Standards/E2197.htm)を適用した試験管内試験試験で考慮する必要がある。ここでは、投与量/組成だけでなく、病原菌活性の既知の修正可能なパラメータである薬剤との接触時間の重要な問題の影響を簡単に試験することができる。スパイクタンパク質のコンフォメーションおよび活性を決定するアッセイと一緒にエンベロープのリピドミクス分析を実施して、ウイルス性メカニズムを決定することができる。特定のエタノール濃度では完全な不活化が達成されるかもしれないが、より低い量では、ウイルスを除去するのに役立つか、または、例えば、宿主細胞上の受容体と相互作用するスパイク糖タンパク質の能力の潜在的な修飾を介して、のど細胞ウイルス感染性に影響を与える可能性のある膜損傷(透過性/漏出)につながる可能性がある。この点、HIV-1の場合、脂質膜は膜糖タンパク質を安定化させ、抗体の中和に対する感受性を調節している62 。実際、脂質模倣化合物は、脂質膜の構造や曲率に影響を与えることでウイルス感染を減衰させることができる化合物がすでに開発されている(セクション「溶解を伴わない膜の摂動は、エンベロープされたウイルス感染を減衰させることができる」で説明する)。
ほとんどのウイルス性研究は、薬剤に対する反応が異なるであろう試験管内試験モデルを使用しており、また、宿主免疫の影響を考慮に入れていない。コロナウイルス呼吸器疾患に関する動物モデル研究はないが、ヒト化ACE2遺伝子を導入したマカクとマウスが研究され始めており、SARS-CoV-2ウイルスに反応して軽度の疾患を発症することが初期の兆候として示されている(https://www.nature.com/articles/d41586-020-00698-x)。
臨床試験。最も効果的な構成の決定を含め、堅牢に設計された適切なパワーを有する生体内試験臨床試験が必要である。自己報告による、無作為化されていない、盲検化されていない研究は信頼性が低く、避ける必要がある。これらの市販薬の重要な副作用として、個人が診断用鼻咽頭/咽頭スワブを提供する前にそれらを使用する可能性がある。これは偽陰性検査の数を増やし、感染を促進する可能性がある。現在のところ、検査前にこれらの薬剤を使用しないようにするための具体的なアドバイスはない。
パニック買いやエタノールやメタノールの危険な消費は避けなければならないが、人口ベースの介入が検討される可能性がある。高リスク群が自己隔離から抜け出してくるので、彼らは利用可能な洗口剤を実際に使用した結果としての臨床的転帰を評価するための母集団となりうる。現在の社会的制限は、多くの感染リスク因子変数を減少させ、SARS-CoV-2感染、他の呼吸器感染、および副作用の点で臨床転帰を変化させるが、転帰をモニタリングすることで有用なデータが得られる可能性がある。利用者には、製品の使用に関する一般的なアドバイス、うがいのタイミングや時間を記録して後で分析できるようにしたり、対照として行動したりすることができる。同様に、感染のリスクが高い保健ワーカーにも製品を提供し、使用方法を記録して結果を報告するよう求めることができる。理想的には、検査のために喉の綿棒と血液サンプルが得られるだろう。調査の立ち上げには、物流上、倫理上、規制上の問題があるだろう。しかし、我々が検討した理論的な妥当性とデータに加え、容易に入手可能な製品と、SARS-CoV-2 感染を減少させる緊急の必要性を考えると、大発生時に集団で臨床調査を行うための対策を検討し、行動を起こすことは可能である。
宿主の炎症。化粧品や医療上の理由から、日常の口腔衛生や歯科衛生に広く利用されている洗口剤は、1 日に複数回、6 ヶ月間以上の期間使用した場合、許容可能な忍容性が実証されている。にもかかわらず、ウイルスの脂質膜は宿主の脂質膜と実質的に同じであるため、これらの薬剤を用いたすすぎによる喉組織の健康への影響を真剣に考慮する必要がある。エタノールおよび過酸化水素のようなこれらの薬剤のいくつかは、2〜3ヶ月の期間にわたって1日に数回使用すると、粘膜炎症を誘発する可能性がある。これは角膜上皮細胞を対象とした研究で観察され、炎症性サイトカイン(IL-1b、IL-6)ケモカイン(IL-8/CXCL8,CCL2)およびマトリックスメタロプロテアーゼ(MMP9)が、20%(v/v)エタノールに30秒暴露した1~3日後のmRNAレベルですべてアップレギュレートされていた48。また、感染初期の宿主の自然免疫反応もウイルスを除去するための戦略である可能性があるが、これはこれまでの研究では考慮されていない。アルコール誘発性組織傷害の分子基盤については、かなりの進歩がみられている。しかし、これらの研究は、アルコールのアセトアルデヒドと活性酸素中間体への代謝が組織の恒常性の維持に関連した様々な生理的プロセスを変化させる急性および慢性のアルコール摂取の研究に限定される傾向がある。
その他の読み物
このレビューを作成する際に参考にした、ここで引用した一次研究の情報源となった優れたレビュー記事のリストを強調している。
ウイルスの脂質膜の萌芽。SimonsとGaroff98
脂質代謝に対するウイルスの影響 サンチェスとラグノフ99
表面上のコロナウイルスの不活化のレビュー Wolffら.100
2003年のSARS-CoVの出現。Peirisら.101
エタノールの膜間消化への影響に関する2つの論文。Slatter and Huang102,103
ポビドンヨードを用いた感染症のコントロール エガース104
細胞内の脂質膜の組成のまとめ:van Meer105
検索戦略
このレビューは、基礎生化学、ウイルス学、微生物学の研究から、医学、歯科学の臨床情報まで、多くの分野をカバーしているため、複数の情報源を参照した。ほとんどの文献は、「ウイルス」、「コロナウイルス」、「脂質エンベロープ」、「アルコール」、「膜」、「クロルヘキシジン」などの検索語を使用して、PubMed、ResearchGate、またはGoogleから、単独または組み合わせて同定した。最初に特定された多くの文献は、その後、追加の出典を見つけるためにさらに調査され、その後に含まれていたオリジナルの一次研究を見つけることができた。レビューの草稿作成のアイデアは 2020年3月21日にV.B.O.によって、様々な国際的な専門家に直接連絡を取り、電話やフォローアップメールを介して意見やインプットを直接得ることによって開始された。Boots UKは、最初にアイデアを議論し、入手可能なマウスウォッシュの処方に関する情報を得るためにアプローチを受けた。Bootsの研究者と科学者は、ジョンソン・エンド・ジョンソン社に連絡を取り、ジョンソン・エンド・ジョンソン社は独自の情報を提供した。Boots の研究者(Kirkdale、Thornley、Povey、Inchley、O’Shea)は、その後、同じ用語を使用して PubMed、Google、ResearchGate でさらに検索を行った。学術および臨床の専門家は、ウイルス学(Stanton、Humphreys、Bosch)臨床/ICU(Fegan、Wise)歯科診療(Thomas)免疫学(Jones)脂質生化学(Wakelem、Murphy、Simons、O’Donnell)微生物学(Sattar、Maillard)について相談した。専門家との電話/電子メールのやりとりにより、意見、意見、追加の参考文献を確認した。参考文献のタイムラインは使用しておらず、除外された言語もない。
