journals.sagepub.com/doi/10.1177/0038038510369368

Pharmaceuticalization of Society in Context:Theoretical, Empirical and Health Dimensions
BSA Publications Ltd®Volume 44(4): 603-622
-ジョン・エイブラハムサセックス大学
概要
医薬品に対する社会学的関心が高まり、「医薬品化」に対する認識が高まっている。バイオメディカル主義、医療化、製薬産業のプロモーションとマーケティング、消費者主義、規制国家のイデオロギーや政策という5つの主要な生物社会学的説明要因を参照して、医薬品化を理解する必要があると主張する。
医薬品治療の拡大は、健康ニーズを満たすための生物医学的科学の進歩を反映しているとするバイオメディカル主義論文は、医薬品化の成長のかなりの部分が科学的証拠と矛盾しており、大きな治療進歩をもたらす医薬品イノベーションが、大きな健康ニーズの領域を含む部門全体で減少していることから、弱い説明要因になると判明している。
消費者主義のいくつかの要素は医薬品開発を弱体化させ、いくつかの治療分野では脱医薬品化を引き起こしてさえいる。しかし、消費者主義の他の側面は、産業振興、医療化、国の規制緩和政策とともに、公衆衛生のための重要な治療上の進歩から大きく外れた、あるいは最適とはいえない方法で、医薬品化を促進するものであることが明らかになった。
キーワード
バイオメディカル、コンシューマリズム、医薬品イノベーション、マーケティング、メディカライゼーション、製薬産業、規制国家
序論
概念的・方法論的フレームを構築する海洋学者は20年以上にわたって社会における医薬品を研究してきた(Abraham,1995a,2008;Braithwaite,1984;Fraser et al.)近年、この分野への注目度が高まっている(Abraham,2002a;Busfield,2006;Conrad,2005a: 145;Williams et al. 2009a)。研究者たちは、医薬品が人々の生活の中でますます大きな役割を果たしていることに気づき、「医薬品化」、「医薬品人間」、「医薬品的想像力」などに言及する者もいる(Abraham,2009;Fox and Ward,2009;Marshall,2009;Martin,2006)。
医薬品化の理論家の中には、「寝室とキッチンが医薬品のマーケティングと消費の場になっている」ことから、「家庭生活の医薬品化が進んでいる」と主張する人もいる(Fox and Ward,2009: 41)。同様に、過度の眠気のための処方薬の非医学的使用や乱用に関する報道を指摘したウィリアムズら(2009b: 37)は、「医薬品化」を「人間の状態、能力、能力を治療や強化のための医薬品的事項に変えること」と定義している。私は「医薬品化」を「社会的、行動的、身体的な状態が、医師や患者2によって医療用医薬品1によって治療される、あるいは治療が必要であるとみなされる過程」と定義している(Abraham,2009: 100)。
社会学は長い間、「医療化」-「非医療的な問題が、通常は病気や障害という観点から、医療的な問題として定義され扱われるようになる過程」(Conrad,1992: 209)という概念を認めてきた。医療化の理論家は、医療状態の拡大は、社会における医療専門家の支配と、社会的逸脱や機能不全を再定義する「病気の役割」の重要性を大きく反映していると主張している(Conrad and Schneider,1992;Freidson,1970;Parsons,1951;Zola,1972)。このような医療化は薬物治療を増加させる可能性があるが、医療化の理論家は医療従事者、患者、医療機関の間の相互作用に焦点を当て、医薬品や製薬産業にはほとんど関心を払わなかった。しかし近年、1980年代後半の「プロザック時代」以降、欧米社会では製薬企業が医療化の主要な担い手となったため、医療化理論家はもはや医療者を医療化の中心的推進者と見なすべきではないと主張している(Abraham and Lewis,2002;Conrad,2005b)。
このことは、「医薬品化」が必要な概念なのか、「医療化」に包含されるのか、という問いを提起している。重複はあるものの、この2つの現象には大きな違いがある。医薬品の使用拡大がそれ自体で医薬品化に影響を与えるのに対して、医療化の理論家の関心は、この拡大が、以前は医学の管轄外であった生活の側面が医学的問題として解釈されるようになったことをどのように反映するかにのみ向けられている。例えば、コンラッド(2005b)は、処方薬の消費者向け直接広告(DTCA)など、米国食品医薬品局(FDA)の規制の変更が、規制当局が承認した病状を超えて医師が処方する医薬品のプロモーションをいかに促進したかを強調している。さらに、こうした変化は、製薬会社が医薬品を売るための戦略として「全般性不安障害」などの疾病を売り込む動機となり、これもまたメディカライゼーションを高めたと論じている。
しかし、医療化という概念は、コンラッドが論証のために用いたいくつかの事例にはうまく対応できない。彼は、注意欠陥・多動性障害(ADHD)の子どもを治療するためのリタリンなどの薬物の販売が、過去10年間に大きく拡大したことを挙げている(Conrad,2005b: 7)。しかし、リタリンは1960年代からこの症状の治療薬として利用されていた(Conrad and Schneider,1992: 156-8)。リタリン処方の増加は、診断の増加による医療化もあるが、ADHDの既存の診断に対処するために、心理療法ではなく薬物治療を選ぶという決定から生じたものも相当数あるであろう。後者のシナリオは、製薬化ではあっても医療化ではない。もう一つの例は、以前は食事制限や手術のみで治療していた肥満の治療を、「減量」医薬品で行うことである(Padwal and Majumdar,2007;Throsby,2009)。このように、医薬品化は、医療化が拡大することなく進展することがある。なぜなら、ある医薬品は、確立された医学的状態の治療にますます使用されるようになり、非医学的問題が医学的問題へと変換されることはないからだ。
また、医薬品の選択、購入、使用において医療専門家が介在しないため、医療化とは関係なく医薬品化が起こることもある。例えば、インターネットやスーパーマーケット、薬局での一般用医薬品(OTC)などで「ライフスタイルドラッグ」(バイアグラなどの処方薬を含む)を直接購入する消費者もいる(Fox and Ward,2009;Stevenson et al.)実際、政府が処方薬のみをOTC製品として再分類することで使用が拡大する場合など、同じ一つのプロセスで医薬品化が拡大し、医療化が縮小することがある(Abraham,2009)3。
医療化論者も医薬品化論者も、医薬品の処方や使用量の拡大・増加を過度に目的論的にとらえる傾向がある。Clarkeら(2003)は、「生物医学化」の進展はアメリカ医学のブレイクスルー変革を意味するとさえ主張している。一部の医薬品分野でのこのような拡大は否定できない。しかし、成長を強調するあまり、理論家は「適応外使用」4が拡大し、市場規模が拡大した医薬品分野や医薬品に集中するようになった。医薬品化と医療化に関する社会学的な議論は、ほぼ独占的に、医療における心理社会的あるいは「ライフスタイル」分野と、それに関連した性行為、睡眠障害、社会不安、多動、注意障害、うつ病を治療する医薬品を中心に展開される。
これらの問題は重要である。2008年、世界的には、抗うつ薬、気分安定薬、抗精神病薬が売上高上位4治療薬であり、米国では、適応外使用が最も多い14の処方薬のうち、6つが双極(躁鬱)障害、1つが不安、1つがうつ、1つが睡眠障害の適応外使用だった(Scrip 2008a 2008b)。しかし、これらの現象を十分に理解するためには、医薬品分野の他の部分の動向との関連で設定する必要がある。すべての医療分野で医薬品化が進んでいるわけではない。縮小している分野を理解することで、医薬品化の性質や程度に関するさらなる洞察が得られる可能性がある。さらに、社会学的概念としての「医薬品化」が、単に社会における医薬品のプレゼンスが高まっているという観察以上のものであるならば、それは生物医学的テーゼの有効性(あるいは無効性)と関連している必要がある。それは、医薬品治療の成長は、新しい病気や確立した病気に対する医薬品の解決法を発見する生物医学の進歩的能力によって明らかになった健康ニーズの進展への対応であるという主張である。実際、生物医学的テーゼが正しいとすれば、医薬品の普及は「医薬品-医学の治療的普及」に大きく包含されることになる。生物医学のテーゼを社会学的分析に組み込むことは、健康に対する製薬化の意味合いに直接光を当てることになる–医療化と製薬化理論の奇妙に捉えどころのない特徴である(Conrad and Leiter,2008: 835;Rose,2007)。
医薬品の拡大への継続的な言及は、患者や消費者の概念化にも影響を及ぼしている。彼らの役割は、広告によって、あるいは業界のマーケティング活動と文化的期待の融合によって生み出された医薬品への渇望によって特徴づけられる消費者主義のイデオロギーの下にのみ分類される傾向がある(Applbaum,2006;Conrad,2005a: 138-40;Fox and Ward,2009;Marshall,2009: 143;Rose,2007;Williams et al.,2009a)。医薬品に対する消費者の需要と効果的なマーケティングは議論の余地がないが、医薬品とそのマーケティングに対する消費者ベースの異論が政治・法律領域に存在し、その複雑さは、医薬品化の社会学的構造全体に統合される前に「消費主義」の分解を必要とするものである。さらに、コンラッドが医療化あるいは医薬品化の進展の中心的説明としてDTCAに着目したのは、米国に限定されなければならない。しかし、彼が言及する拡大現象は、ヨーロッパ、カナダ、オーストラリアでも明らかである(House of Common Health Committee[HCHC],2005;Lexchin,2001;Lofgren,2004;Moynihan and Cassels,2005)。DTCAを超えた、より広範で根本的な規制思想や政策の転換を検討する必要があるのかもしれない。
社会学文献における医薬品化(および関連する医療化)の議論は、主に西洋社会における過去15〜20年の処方薬部門に関する発展に言及されてきた。分析の一貫性を保つため、ここでも同じ時間的・空間的焦点が採用されている。本稿では、医薬品化は5つの主要な説明要因を参照することで理解されるべきであり、それらは相互に影響し合いながらも競合するものであると主張する。すなわち、バイオメディカル主義(医薬品研究開発・イノベーションを含む)、医療化、医薬品プロモーション・マーケティング、消費者主義、規制国家のイデオロギー・政策という5つの側面である。
方法論としては、これらの要因のそれぞれが製薬会社の成長を牽引してきたと仮定することはしない。むしろ、各要因がそのような成長に貢献したという仮説の妥当性を分析する。その際、説明要因を成長だけでなく、医薬品の縮小や衰退の側面と関連付ける必要がある。Rose(2007)やMarshall(2009)は、「医療化」を社会学的分析における疑惑と含意のクリシェとして批判している。ここでの方法論は、バイオメディカル主義が競合する説明要因として明示的に含まれ、それが健康ニーズの充足と明示的に関連するため、「医薬品化」概念の同じ運命を回避することができる。相互作用的説明要因の有無にかかわらず、生物医学的テーゼがもっともらしいものであればあるほど、医薬品が健康ニーズを満たすことによって医薬品化が拡大した(「治療普及」)可能性が高くなる。逆に、生物医学的説明力を犠牲にしてでも、競合する説明要因がより妥当であればあるほど、医薬品の拡大は、商業的優先順位、政府の意図、医師や患者の誤った期待などを反映している可能性が高く、それらは健康ニーズとは大きくかけ離れたものである。
医療の医薬品化
バイオメディカル主義、医療化、マーケティング1960年から1980年代初頭まで、欧米社会における処方薬の売上はGDP比でほぼ横ばいであった。しかし、1980年代初頭から2002年までの間に、処方薬の売上高は3倍に増え、全世界で約4000億米ドル、米国では約2000億米ドルとなった(Angell,2004: 1-5)。2002年から2006年にかけて、米国の処方薬の売上は毎年平均10%ずつ増加し 2007年には世界の売上は6000億米ドルに達した(IMS Health,2008;Scrip,2008c)。医療の分野によっては、医薬品市場の拡大とともに、医薬品化が進んだものもある。1993年から2002年にかけて、選択的セロトニン再取り込み阻害薬(SSRI)として知られる抗うつ薬の英国NHSでの処方は、188万4571から1550万に、リタリンについては3500から16万1800に増加した(保健省、1994,2003)。アメリカでは、SSRIであるフルオキセチン(プロザック)の売り上げは1994年から2000年の間に2倍以上になり、バイアグラの売り上げは1998年の市場投入から4年でほぼ2倍になり、リタリンの売り上げは1992年から10年で5倍になった(Drug Enforcement Administration,2001;Eli Lilly,2000;Rafalovich,2005;Scrip,1995,1999;Timmerman,2003)。カナダやオーストラリアでも同様の傾向がある(Phillips,2006: 433)。このような成長の説明には、医薬品化のひとつの重要な側面がある。
産業界、技術科学、大衆の言説の中に深く根付いているのは、製薬化の進展は医学の進歩を反映しており、ADHD、うつ病、勃起不全など、以前は診断も治療もされていなかった状態の人々が、必要とする薬を受け取ることができるようになるという生物医学的な見方である(Castellanos 2002;Harding 2001)。たとえば、この考え方によれば、ADHDは、ドーパミン不足による脳の器質的機能障害と診断され、生化学的な介入によって治療可能であると考えられる(Barkley,1996,1997;Couvoisie and Hooper,2003;Diller,1998;Krause et al;Rafalovich,2005;Zametkin et al.,1990)。
しかし、このように医薬品化が進む中、生物医学が宣言した技術的進歩は、科学文献や臨床現場において多くの不確実性を示していた(Rafalovich,2005)。ADHDの脳画像研究は、その状態や薬物効果の生化学的基盤を検出することになっているが、サンプルサイズや対照群と試験群の子どもの年齢のマッチングにおいて再現性や実験の厳密性に欠けていた(DeGrandpre,2000;Thambirajah,1998)。さらに、脳内のドーパミンレベルの直接測定は生きている人間から採取できないため、血液、尿、脳脊髄液中のドーパミン代謝物から推測する必要があった。このような測定の妥当性には疑問があったし、今も疑問がある。ADHDと診断された人々がそこから逸脱するとされる、脳内のドーパミンの「正常」レベルの設定も、同様に問題があったし、今もある(Glenmullen,2000;Yuwiler,1994)。生物医学の支持者はまた、医薬品化の進展は、臨床診断の感度が高まり、薬物治療を必要とする人々の発見が容易になったことを反映していると主張する。しかし、過去40年間、ADHDの診断基準は一貫して拡大し、ADHD患者の同定の増加と医療化の増加を切り離すことは事実上不可能であり、「正常な行動」とADHDの間の閾値が低く設定されすぎているという懸念に繋がっている。ADHDの公式診断基準は、アメリカの学齢期の子どものほぼ20%に適用されている(Goldmanら、1998)。その診断基準は、「正常な」経験や他の精神医学的診断と重複しており、米国では、大規模な疫学調査により、50%近くの子どもがADHDの症状基準を満たし、ADHDと診断された子どもの70%は「行為障害」または「反抗挑戦性障害」とも診断されていることが判明している。(Bird et al.,1990;Sharma,2000)。
ADHDは、医療介入の多くの精神・社会的領域において、技術的にありえないことと、診断基準の拡大が、これまで発見されていなかった病人の発見と同様に、医療化を容易に反映してしまうことから、生物医学のテーゼが説得力を持たない理由を示している。同様に、ここ数十年の抗精神病薬の処方の増加は、医学専門家によって抗精神病薬が「双極性障害」の治療薬としても再定義されたことに起因している。一方、イギリスの「うつ病撲滅キャンペーン」は、1990年代に精神科医と開業医の王立大学を通じて行われた疾患認識キャンペーンで、うつ病の流行が宣言されていることに対抗してSSRIを処方するよう医師をターゲットにしていた(HCHC,2005: 70)。)
これらの点から、医療化は医薬品化の拡大を説明する重要な要因であると思われる。診断の境界線の変更や疾患啓発キャンペーンに関与する専門的な医療エリートが、しばしば製薬業界から資金提供や影響を受けていることを考えると、Conrad(2005b)が主張するように、業界の利害が医療化の推進要因となっているのだろう。私は、この相互に補強しあう双方向の因果関係を「医療化-医薬品化複合体」と呼んでいる。なぜなら、業界が支援する疾病啓発キャンペーンは、SSRI、精神安定剤、バイアグラなどの医薬品の効果を誇張し、その結果、技術的科学的根拠のない方法で処方されているからである(Abraham and Sheppard,1999;HCHC,2005: 69-70;Healy,2004;Medawar,1992;Medawar and Hardon,2004)。例えば、Kirschら(2008)は、1990年代に英国と米国で最も広く処方された4種類のSSRIの科学的臨床試験データから、これらの薬剤が中等度や軽度のうつ病に対して宣伝・処方されているにもかかわらず、臨床的には非常に重症の場合にのみ効果があることが示唆されていることを発見している。
医薬品化は、オンラベルかオフラベルかにかかわらず、確立された病状に対して、業界が医療関係者に個々の医薬品を宣伝・広告することによっても推進されている。統合失調症と双極性障害の治療薬として承認されているジプレキサは、メーカーのマーケティング担当者によって、適応外使用である認知症とアルツハイマー病の治療薬として医師に宣伝され、そのような適応外使用を裏付ける科学的根拠がないにもかかわらず、全世界で48億米ドルの売上に達した(Scrip,2009)。これは、医療化を伴わないため、医療化・医薬品化複合体の外にある。ジプレキサは、多くの例の一つである(Scrip,2009: 7)。このような広告やプロモーションは巨大であり、成長しているが、病気マーケティングの見かけの新しさに目を奪われた社会学者によって無視されてきた。医療の精神・社会的領域やライフスタイルの領域で医薬品化が進むなかで、マーケティングは研究開発(R&D)よりもはるかに速いスピードで成長している。1995年から2005年の間に、英国の製薬産業における研究スタッフの数は 2%減少し、マーケティングスタッフは 59%増加した(HCHC,2005: 58)。米国では、製薬業界のマーケティングへの支出は研究開発への支出の約2倍であり 2000年にはそれぞれ540億米ドル、260億米ドルであった(Angell,2004: 40,120)。なぜなら、もし、医薬品化の主要な推進要因が、プロモーションや医療化ではなく、新たな医療ニーズに対応する科学的発見であれば、マーケティング活動に比して研究開発の成長がより明確に証明され、ジプレキサのようなケースは少なくなると予想されるからだ。
製薬会社のマーケティング戦略に上級医療専門家が組み込まれ、製品開発に資金を提供したり、医学シンポジウムでその医薬品について好意的な発言をすることも、医薬品化に寄与するが、必ずしも病気の医療化あるいはマーケティングにはならない。これは、企業がスポンサーとなっている編集者がいる雑誌の特別付録での出版と組み合わされることもある(HCHC,2005: 56-7)。出版前に、科学者の原稿に編集上の変更が加えられ、著者が意図した以上に薬剤が肯定的に描かれることもあれば、原稿は、出版物の名義となる研究者ではなく、メーカーのために働く医学ライターによって「ゴーストライター」されることもある(Abraham,1995a;Healy,2006b)。製薬会社は広報会社を雇い、自社の医薬品を肯定的に紹介する記事についてはメディアや専門家に好意的に受け止めさせるが、否定的な知見の公表を遅らせたり差し控えたりして、処方する医師が読む医学文献に偏りを持たせることがある(Abraham,1994a,1995b;HCHC,2005: 55-6;Lexchin et al,2003)。自社製品への批判を封じ込めるための企業の戦略もまた、処方率、ひいては医薬品化を維持することになる。これには、批評家の意見を聞く場を提供する機関からの資金提供の取り消し、批評家のデータの公表を阻止しようとする試み、批評家の懸念を弱めるためにメーカーを支持する専門家の動員などがある(Abraham,2002b;Abraham and Sheppard,1999;Healy,2004)。
消費主義
製薬化と並行して、患者や消費者団体の反射的な行動、専門性、活動性を特徴とする消費者主義が台頭してきた(Milewa,2009)。しかし、消費者主義が必ずしも医薬品の普及を促進する要因とはなっていない。欧米社会では、少なくとも2種類の積極的消費者主義を識別する必要がある。すなわち、医薬品産業複合体に対する傷害指向の逆襲と、医薬品産業複合体へのアクセス指向の協働である。前者は、自分(あるいは自分の親族)が特定の医薬品によって被害を受けたと考える市民が、製薬メーカーに対してキャンペーンや訴訟を起こすことである。このような敵対的消費者主義は、米国では他の国よりも大規模で成功している。その理由は、勝ち目のない裁判という消費者に優しい法文化、情報の自由という大きな権利によって弁護士が訴訟を起こす自信があり、比較的資金力のある消費者運動があるからだ(Abraham and Sheppard,1998)。
逆訴訟の規模と意味合いは大きくなった。1980年代後半、関節炎治療薬であるベノキサプロフェン(オラフレックス)による傷害の疑いでイーライリリーに対して賠償を請求した原告は、アメリカの裁判所から同社に対する懲罰的損害賠償として数千万ドルを獲得した(Abraham,1994b)。20年後、米国の原告は、関節炎治療薬であるVioxx、Bextra、Celebrexが原因とされる致命的・重傷について、Merckに対して27,000件、ファイザーに対して8億9400万ドルの訴訟を解決し、48億5000万ドルを受け取った(Scrip 2007,2008d)。
ヨーロッパでは、損害賠償を目的とした敵対的消費者主義はあまり一般的ではなく、成功もしていない。英国の原告がイーライリリー社に対してベノキサプロフェン(オプレン)に関する訴訟を起こしたとき、訴訟は、同社が提示した低コストの非訴訟和解に消散した。同様に、1990年代には、ベンゾジアゼピン系薬剤の製造業者に対して、患者による大規模な法的措置がとられ、BBCテレビのパノラマドキュメンタリーでは、ベンゾジアゼピン系薬剤ハルシオンの安全性問題への対応についてアップジョン社を攻撃したが、この傷害訴訟は崩壊し、多くの患者は補償を受けられないまま、ハルシオンに関してはアップジョン社がBBCに対する名誉毀損訴訟で勝った(Abraham 1994b;Abraham and Sheppard,1999;HCHC,2005: 65-6)。それにもかかわらず、ベノキサプロフェンとバイオックスは、世界的に市場から撤退し、その後、同様のタイプの関節炎治療薬の開発とマーケティングが国際的に著しく減少した(Abraham and Davis,2007a;Brown,2006)。
傷害指向の敵対的消費者主義の成長は、製薬化を進めたわけではない。むしろ、医薬品の安全性に対する疑念を高め、医薬品の処方や使用を減少させたのである(Scrip,2008e)。関節炎治療薬で起こったように、傷害指向の敵対的消費者主義は脱医薬品化をもたらすのに十分な力を発揮することができる。対照的に、アクセス志向の協調的消費者主義は、政府規制当局による承認の迅速化を通じて新薬への迅速なアクセスを求める患者集団が関与するため、医薬品化を促進する。また、安全性よりも治療効果に対する期待に重点が置かれている。アクセス重視の共同消費者主義は、キャンペーンや訴訟も行うが、製薬メーカーと連携し、規制当局に対抗することが多い。アクセス重視の消費者主義は、大西洋の両岸でかなりの成功を収めている。
アメリカのアクセス重視の消費者主義は、1980年代後半のHIV/AIDS患者の活動に端を発している。彼らはFDAに対して、HIV/AIDS治療薬の市場承認を早めるか、開発中の治療薬をより広く入手できるようにすることによって、患者がより早く治療薬を入手できるように働きかけた(Epstein,1996)。何人かの著者は、この「エイズ・アクティヴィズム」が、その後のFDAによる医薬品承認の迅速化の唯一の原因であると誤解している(Carpenter,2004;Da,2004)。(Carpenter,2004;Daemmrich and Krucken,2000;Edgar and Rothman,1990)。むしろ、このような活動は、医薬品市場に対するFDAの規制障壁を減らす方法と考えた製薬会社や、規制緩和の政治的性向がすでにFDAに圧力をかけ、産業に対する規制「負担」を減らしていたレーガン政権やブッシュ上級政権からの支持を得ていた(Scrip,1988)。エイズ・アクティヴィズムによって生み出されたアメリカの消費者主義は、産業界と規制緩和の同盟者である政府との協力の一形態であった。
実際、1980年代後半以降、FDAはあらゆる種類の新薬の規制審査時間を半分以下に短縮している(FDA,2004)。1992年からは、FDAは、重篤な疾患や生命を脅かす疾患の治療を目的とする医薬品について、臨床的有用性に関する極めて限られた科学的証拠に基づいて「早期承認」を認める規則を制定した(連邦規則集,1992)。これらの点から、アメリカのアクセス重視の共同消費者主義は、医薬品をより早く患者に提供し、医薬品化を進めることにほぼ成功しているが、医薬品の安全性や有効性に関する規制当局のチェックが緩いこのような急ぎや「迅速化」が公衆衛生に有益であるかは疑問である(Gale 2001)。2004年には、FDAが迅速な手続きで承認した23の新がん剤のうち、市販後の調査で臨床的有用性が確認されたのはわずか6剤であり、確認試験完了までの予測期間は平均10年であると報告されている(Fleming,2005;Roberts and Chabner,2004)。
英国では、アクセス重視の共同消費主義は、NHSにおける新薬への患者のアクセスに焦点を当てた。特に、NHSで使用される医薬品の費用対効果を評価するNICE(National Institute for Health and Clinical Excellence)の判断に関連して、1990年代後半から大きく発展してきた。例えば 2005年3月、NICEは、アルツハイマー病の治療薬4種について、NHSの費用対効果に見合わないとの勧告を行った。しかし、アルツハイマー病協会などの患者団体が参加したメディアキャンペーンとNICEへの正式なアピールを経て、NICEはガイダンスを改訂し、病気の初期ではなく中程度の段階の人々に対する薬剤のNHS資金提供を認めるようにした。その後、アルツハイマー協会がNICEを相手取って裁判を起こし、NICEはすべての患者に対して薬剤を提供するよう主張した(BBC News 24,2007)。注目すべきは、アルツハイマー病治療薬のメーカーが、この裁判の主な原告であり、控訴にも中心的に関わったことである(BBC News 24,2007)。同様の共同活動は、多発性硬化症協会がNHSでのβインターフェロンへのアクセスを求めるキャンペーンに成功した際にも行われた。一方、市場投入が急がれた乳がん治療薬ハーセプチンのメーカーであるロシュは、NICEによる承認の前にNHSでこの薬の助成を受けるために広報会社を雇って一部の乳がん患者の支援を促したと伝えられている(BBC News 24,2006a,2006b;Crinson,2004)。
私は、製薬会社の論争において、積極的消費主義が目的を達成する力は、それが製薬会社の利益を支持しているか、反しているかに大きく依存することを提案する。特にアメリカ以外の国では、製薬業界の支持を得た方が成功する可能性が高い。その結果、アクセス重視の協調的消費者主義がもたらす医薬品化促進効果は、損害賠償重視の敵対的消費者主義がもたらす非医薬品化促進効果に勝る傾向があるが、どちらも社会における医薬品化の性質を形成する役割を担っている。さらに、多くの患者団体が戦術的に有利な場合には製薬会社と提携するだけでなく、製薬会社から資金提供を受けることも多くなっているため、協調的消費者主義が医薬品を取り巻く環境に恒常的に存在するようになるかもしれない(HCHC 2005: 74-6;Herxheimer,2003;Jones,2008;O’Donovan,2007;Phillips,2006.)。434).
組織的な行動主義に加えて、消費主義にはイデオロギー的な側面がある。すなわち、患者の健康上のニーズを市場における消費者の要求として、言説的に流用することである。このことは、過去10年間におけるDTCAに関する産業界や政府の政策言説における患者の描写から明らかである。Milewa(2009)が主張するように、こうした言説は患者の行動やニーズとは異なるものであり、そこから導き出されたものでない可能性さえある。
欧州では、製薬業界が欧州委員会の「企業総局」の支援を受けて、EUにおけるDTCAの合法化を求めて精力的なキャンペーンを展開したが、今のところ失敗に終わっている5。このキャンペーンでは、「情報に通じた患者」と「専門家患者」という言説が用いられ、その後、英国保健省(2001)が無批判に採用し、患者のセルフケアとセルフメディケーションという消費主義的イデオロギーを推進し、患者は処方薬に関する広告表示を評価する十分な知識があり、医師を治療の開始者からせいぜいゲートキーパーに引き下げると主張した(Medawar and Hardon,2004: 121)。医師が処方薬について患者に十分な情報を提供できないことは問題であるが、「患者の専門知識」を構築するために「情報」の提供を計画している人々、すなわち、医師に誤解を招く情報を与えて製品を宣伝してきた実績を持つ利益追求型産業の利害との関係で、「患者の専門知識」言説を考える必要がある(Britten,2008;Scrip,2006,2009)。米国の経験は、製薬会社が医師の残したギャップを埋めることによって患者の健康ニーズを満たすと仮定することが、かなりの信仰の飛躍であることを示唆している。1997年にFDAが規制を緩和した後、アメリカのDTCA放送は3倍以上に増え、製薬業界のDTCAへの支出は2005年に42億米ドルに達した(Conrad and Leiter,2008)。これは、消費者が自己診断し、広告された医薬品を医師に要求することを奨励し、処方を増加させた(Mintzesら 2003)。そして、その処方の半数は、治療効果を裏付ける証拠のない医薬品である可能性がある(Conrad and Leiter,2008: 21)。
バイオメディカリズム、医薬品のイノベーション、規制国家のイデオロギー私は、いくつかの心理社会的あるいはライフスタイルの領域における医薬品の使用と処方の拡大を支持する技術的科学的根拠が弱いため、バイオメディカリズムよりも医療化および業界のプロモーションとマーケティングがより説得力のある医薬品化の推進要因となることを指摘した。また、臨床的有用性の科学的根拠が不十分なまま医薬品の上市を早めたり、規制当局の評価と矛盾するような適応外使用を奨励するなど、消費者主義のある側面が、生物医学主義が擁護できる境界線を超えて医薬品化を推し進めていることも指摘した。しかし、ある新薬(おそらくハーセプチン)が確立された病状(例えば乳癌)に対して明らかに有効であることが発見された場合、その後の医薬品化は、(非合法の)医療化、業界の宣伝、科学的知識を超えたマーケティング上の主張ではなく、患者が合理的に求めた生物医学主義に大きく起因するものであると考えられる。そこで、医薬品化がバイオメディカル主義によってどの程度説明されるのか、他の要因との関連でさらに理解するために、医薬品のイノベーションを検討する必要がある。
医薬品のイノベーションとは、市場に投入された新しい分子実体(NME)のことである。NMEは、ユニークな分子構造を持つ特許可能な技術的新規性である(Vos,1991)。政府の規制当局は、新薬が上市される前に、プラセボと比較して治療効果を実証することを求めているが、NMEはすでに上市されている医薬品を超える治療効果をもたらす必要はない(Abraham and Davis,2009)。すべてのイノベーションはメーカーにとって商業的に重要であるが、患者の健康にとって最も価値があるのは、治療上の大きな進歩をもたらすものなのである。
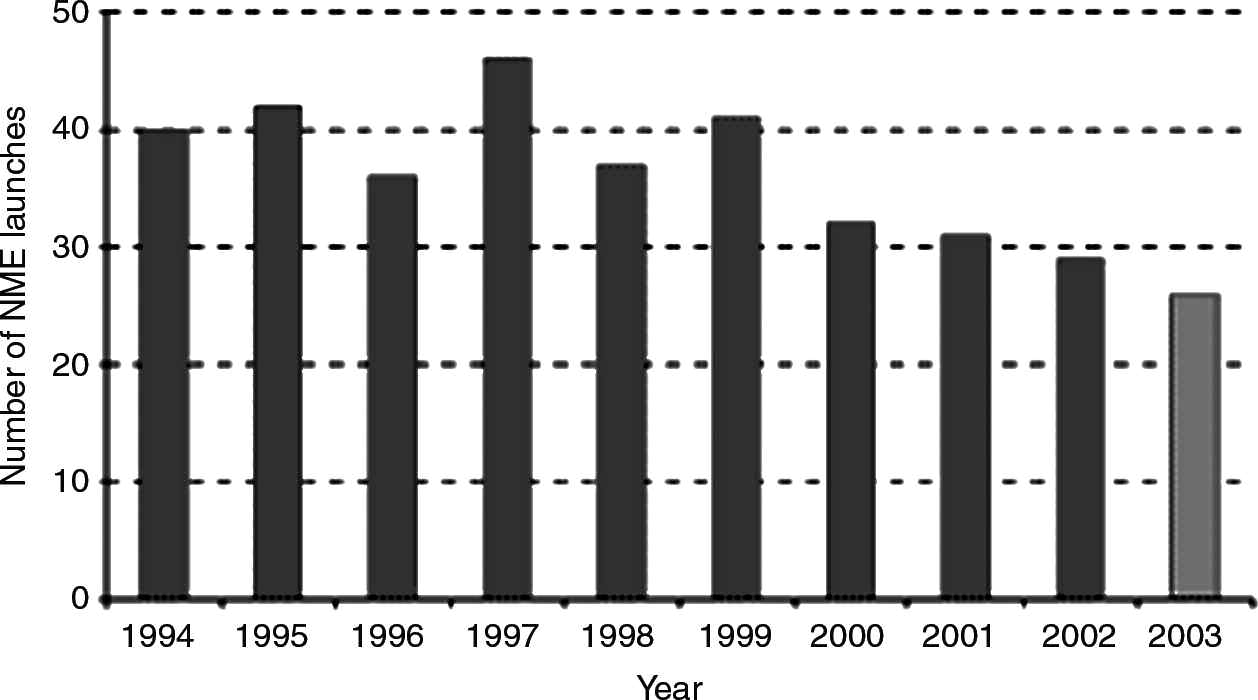
図1世界中で最初に上市されたNMEの数(1994年~2003)
出典:Centre for Medicines Research(2005)、最終欄は2003年の暫定値
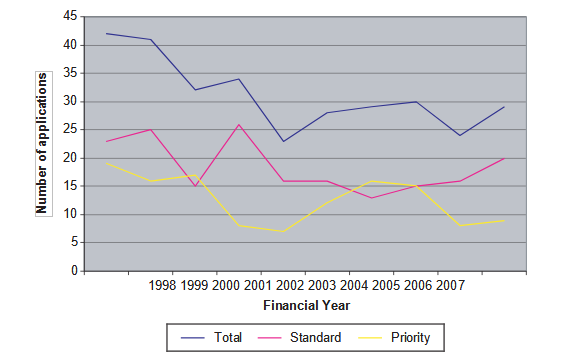
図2 1998-2007年のNMEの申請数
出典出典:FDA PDUFAパフォーマンスレポート(2002年度および2007年度)URL(2009年6月調べ):http://www.fda.gov/AboutFDA/ReportsManualsForms/Reports/UserFeeReports/PerformanceReports/PD UFA/default.htm
多くの精神・社会・生活領域における医薬品化が進んだのと同じ時期に、医薬品のイノベーションは減少した(図1,2)。さらに重要なことは、治療上の大きな進歩をもたらす新薬(FDAの「優先審査」を受けたもの)の数も減少していることである(図2)6。毎年、FDAに提出された新薬の半分以上は、すでに市販されている医薬品(「標準審査」を受けたもの)に対して治療上の優位性をほとんど、あるいは全く示していない。さらに、フランスの医学・薬学専門誌La Revue Prescrire(2005)は、1981年から2004年にかけて、主にフランス、EU、米国で販売された3100の新薬または既存薬の新適応症を検討し、中程度から大きな治療上の進歩をもたらすものは10%に過ぎないと結論づけている。したがって、この分野全体としてみると、治療上重要な進歩をもたらす新薬という形での医薬品化は、この15年間で縮小していることになる。医薬品化の拡大は、健康ニーズに対応した治療上重要な革新的技術の技術的発見の成長では説明できない。
注目すべきは、1990年以降、FDAが優先的医薬品と標準的医薬品の審査・承認に要する時間を大幅に短縮したことである。これは、「過剰規制」が革新を阻害しているという製薬業界と反規制派の「シンクタンク」からの苦情に対応したものである(FDA,2009;Kaitin and DiMasi,2000;Kessler et al,1996)。同様の措置は、欧州の医薬品規制機関でもとられた(Abraham and Davis,2007b;Abraham and Lewis,2000)。しかし、1980年代後半から1990年代にかけてのこの規制緩和の文化は、治療上重要な医薬品の開発を奨励するために、産業界に課せられた規制基準が緩くなったため、技術革新が低下することになった(Abraham and Reed,2002;Schweitzer et al.、1996)。明らかに、規制緩和のイデオロギー(および関連する政策)は、医薬品化を促進する要因となってきた。それは、生物医学のテーゼにあるように、患者や医療関係者が必要とする多くのイノベーションを生み出すことではなく、むしろ、イノベーションが減少する中で、治療の進歩をほとんどもたらさない医薬品の市場を業界が拡大できるようにすることであった。
このことは、抗生物質の場合ほど明らかなことはない。1980年代後半から1990年代初頭までに、既存の抗生物質に対するバクテリアの耐性が重大な健康問題になりつつあることが、生物医学の科学者に知られていた(Blumbergら、1991;O’Neill and McIntosh 1987;Van Klingerenら、1989)。この問題はそれ以来、着実に大きくなっている。世界保健機関(2004)は、薬剤耐性菌による感染症を、最も「医薬品ギャップ」が大きい医療ニーズの分野と位置づけている。この時期は、他のいくつかの分野でも規制緩和政策が行われ、医薬品化が進んだ時期でもある。しかし、1983年から2004年にかけて、抗生物質の開発は着実に減少していった。FDAは1983年から1987年に16種類、1988年から1992年に14種類、1993年から1997年に10種類、1998年から2002年に7種類 2003年から2004年にはわずか3種類を承認した(Infectious Diseases Society of America[IDSA],2004: 15)。2004年以降に承認される可能性のある抗生物質について、Spellbergら(2004)は、主要製薬企業22社の506分子のうち、抗生物質はわずか6分子であることを明らかにしている。IDSAのBradleyら(2007: 68)によれば、「2年後、ほとんど変化がなかった」のは、「抗感染症薬は他の医薬品、特に慢性疾患用の医薬品に比べて収益性が低いため、多くの製薬会社が研究開発の努力を他に集中させている」ためであるという。
考察と結論
医療化-医薬品化複合体の中で医薬品化が進んできたという強い証拠がある。ここで、医薬品化の拡大の規模については、生物医学よりも医療化の方がより説得力のある説明となる。コンラッドが指摘するように、製薬業界はこうした医療化の主要な推進者であった。しかし、製薬業界のプロモーションやマーケティングは、医療化-医薬品化複合体の外でも、医療化を伴わない医薬品化の推進役として機能している。このようなプロモーション主導の薬物化のかなりの部分は、一般的な生物医学的科学的根拠を欠くか、あるいはそれと直接的に矛盾するため、生物医学的な説明では説明できない。しかし、プロモーション主導の医薬品化は、米国におけるDTCAや欧州における「専門家患者」の言説のように、患者のニーズを消費者の要求として、ゲートキーパーである医師を部分的にバイパスするイデオロギーによって増強される。製薬業界、欧米政府の規制緩和派、一部の患者団体は、このようなイデオロギーの流用に協力してきた。
医薬品市場の拡大について生物医学的な説明を最も強く期待できる分野、すなわち治療の進歩をもたらす医薬品の革新において、医薬品化は減少している。ハーセプチンのような重要な治療上の進歩がもたらした医薬品化の説明の大部分は生物医学的なものであるかもしれないが、医薬品市場全体の成長や一部の治療領域における医薬品化の拡大の説明にはなりえない。なぜなら、この15〜20年間、重要な治療上の進歩をもたらす医薬品イノベーションの成長や拡大は起こっていないのである。それどころか、業界の商業的優先順位が生物医学的志向を支配し、マーケティング努力が常に研究開発を上回り、収益性は低いが大きな健康上のニーズを持つ治療領域の医薬品化は停滞または縮小してきたのである。
規制緩和のイデオロギーや国家政策によって、新薬の市場参入に対する技術的・経済的な障壁が低くなり、深刻で生命を脅かす病気のための新薬へのアクセスを求める産業界と消費者の協力が強まったことが、医薬品化の推進力となった。しかし、これらの推進力を合わせても、治療法の進歩をもたらす医薬品イノベーションの数を増加させることはできない。これは、バイオメディカル主義が医薬品化の進展の説明として弱いことを証明している。さらに、特定の医薬品や製薬会社に対するキャンペーンや訴訟といった消費者心理の高まりは、医薬品化の進展を阻害し、一部の治療分野では脱医薬品化をもたらし、その結果、その分野での医薬品開発および医薬品市場シェアが低下しているのである。
医薬品化の進展と薬害事件の規模の拡大を説明する生物医学的手法の弱点は、学術的な興味にとどまらない。医薬品化の進展は、健康ニーズを満たすための医薬品提供の拡大が主因ではないことが明らかになった。むしろ、消費者主義、規制緩和のための国家政策、産業界の商業的優先順位と製品プロモーション、医療化という社会学的要因が、そうした提供の枠を大きく超えた形で、医薬品化を拡大しているのである。ローズ(2007)が指摘するように、マーケティングが必ずしも誤ったニーズを生み出すわけではないが、医薬品がそのニーズを満たす能力について誤った主張と期待を生み出している可能性がある。さらに、患者のニーズを市場における消費者の嗜好としてイデオロギー的に流用することは、抗生物質の開発や薬害からの保護といったマーケティングプロセスにおいて十分に表現されない公衆衛生の要件が、健康を増進するはずの産業によって不適切に無視されることを意味している。
謝辞
本稿の基礎となる研究の一部を助成していただいたESRCおよびMRCに感謝する(助成番号:L218252001)。
ジョン・エイブラハムサセックス大学社会学教授、保健医療研究センター(CRHaM)所長、英国下院議会保健特別委員会の専門アドバイザー。現在、コートニー・デイビス博士とともに「Challenging Pharmaceutical Regulation(医薬品規制への挑戦)」という本を執筆中。現在、コートニー・デイビス博士とともに、「Challenging Pharmaceutical Regulation: Innovation and Health in Europe and the US(Palgrave,forthcoming)」という本を準備中である。
住所サセックス大学法学・政治学・社会学部社会学科、Falmer,Brighton BN1 9SN,UK
投稿日:2009年9月
受理日2009年11月
