Contents
On the effect of vitamin C intake on human health: How to (mis)interprete the clinical evidence
www.ncbi.nlm.nih.gov/pmc/articles/PMC7296342/
オンラインでは2020年5月23日公開。
Jens Lykkesfeldt
概要
何十年もの間、ビタミンCの健康への潜在的な有益性(壊血病の予防という点を除く)については、多くの議論がなされてきた。食事やサプリメントによるビタミンCの摂取量の増加を支持する論文や、ビタミンCの摂取量やサプリメントの摂取量の増加が罹患率や死亡率に影響を与えるという仮説を否定する論文が何百も発表されている。ビタミンCの化学的および薬理学的性質は複雑であり、残念ながら、ビタミンCの健康への影響を検証する臨床研究を計画する際には、ほとんど考慮されていない。しかし、ビタミンCの化学的安定性、用量依存性の吸収・排泄動態、能動輸送による分布、複雑な用量-濃度-反応関係などを無視すると、試験デザインの不備、不適切な組み入れ基準・除外基準、結果の誤認につながる。本レビューでは,ビタミンCの薬物動態が通常の低分子医薬品とは異なることを概説し,試験デザインやデータの解釈に潜む落とし穴に焦点を当て,これらを踏まえてビタミンCの主要な臨床試験を再検討した。
1. はじめに
ビタミンCが壊血病の予防に役立つことが明らかになって以来、数え切れないほどの臨床研究が行われてきた。これらの研究は、大きく分けて、i)ビタミンCの体内動態、ホメオスタシス、および様々な生理学的プロセスにおけるアスコルビン酸の役割を調べるメカニズム研究、ii)ビタミンCの摂取量や状態と罹患率や死亡率との関連性を調べる疫学研究、最後にiii)ビタミンCの補給が疾病の予防、進行、および治療に及ぼす影響を調べる介入研究、に分けられる。このように多くの科学的根拠が得られているにもかかわらず、以下のような非常に基本的な疑問が今日まで解決されていない。「ビタミンCの最適な摂取量はどのくらいか」、「ビタミンCの予防・治療効果はどのくらいか」。
ビタミンCの健康への重要性について議論が続いている主な理由は、入手可能な臨床データの解釈と質にある。無作為化比較試験(RCT)は、一般的に医薬品の有効性と安全性を検証するためのゴールドスタンダードと考えられている。当然のことながら、RCTのパラダイムは微量栄養素の研究にも適用されており、食事によるサプリメントが機能的な健康効果をもたらす可能性の臨床的裏付けを求めている。ビタミンCの場合、このような介入研究は、ごく一部の例外を除いて、罹患率や死亡率に対する効果はわずかか、あるいは全くないという結果に終わっている[1]。しかし、ビタミンCは、典型的な低分子量の医薬品とは多くの点で大きく異なるため、妥当な結論を得るためには、研究デザインや解釈に組み込む必要がある[2]。一方、疫学研究では、選択バイアスや交絡の可能性が指摘されている。さらに、因果関係を立証したり、複数の原因を識別したりする能力に欠けていることから、同定された関連性が、ビタミンCの摂取状況そのものに関連した単なる偶然のものや二次的なものである可能性が示唆されている[3]。
大多数の哺乳類とは異なり、ヒトにはビタミンCを合成する能力がないため、ビタミンCの薬物動態は、取り込み、分布、代謝、クリアランスの評価の基礎として特に注目されている。他の生物種は、必要な時にビタミンCの生合成を増加させる能力を持っている可能性がある。しかし、人間の場合、病気による炎症や酸化ストレスなどでビタミンCの合成量が増えると、摂取量を増やすか、サプリメントで補うしかない。
介入研究における用量選択の重要な点の一つは、治療範囲内でほぼ1次の速度論を仮定することである。ビタミンCについては、何十年も前に、ビタミンCの薬物動態が実際には生理学的範囲内で高い用量依存性を示す説得力のあるデータが発表されている[4,5]。このような重要な発見があったにもかかわらず、ナトリウム依存性ビタミンCトランスポーター(SVCT)が発見されるまで、これらの観察結果の影響やビタミンCのホメオスタシスの真の複雑さは明らかにされなかった。SVCTは現在、ビタミンCのホメオスタシスを全身的に制御する主要な手段と考えられており、かなりの濃度勾配でアスコルビン酸を細胞内に積極的に輸送する能力を持っている[6]。このような薬物動態の用量依存性と非線形性は、試験デザインとデータ解釈の基本を大きく変えるものであるが、残念ながら、ビタミンCの臨床に関する文献では、このような現実はほとんど無視されてきた。
本レビューでは、十分な証拠が得られていないため、上記の非常に適切な質問に答えることはしないが、ビタミンCの薬理学について議論し、誤解を招く可能性のある落とし穴を考慮して、ビタミンCに関する臨床文献の大規模な研究を批判的に再検討することを目的としている。
2. ビタミンCの薬物動態
ビタミンCの薬物動態については、最近、詳細なレビューがなされており[7]、ここでは簡単な概要を示すにとどめる。経口摂取されたビタミンCの腸管吸収は,食品やサプリメントにかかわらず,受動的な拡散ではなく,トランスポータータンパク質を介して行われる[8,9]。数十年前、独立した研究者によって、ビタミンCの経口投与量が200〜400 mg/日を超えると吸収率が低下することが観察され、腸管でのビタミンCの吸収は飽和能を持った輸送であると結論付けられた[4,5]。Levineらはその後、健康な若い男女を対象とした一連の綿密な薬物動態学的研究を行い、血漿中の飽和は70〜80μM程度の濃度で起こることを示した[10,11](図2H)。他の研究でも同じ数値が得られている[12,13]。この現象は、経口投与と非経口投与でビタミンCの薬物動態が大きく異なることの説明にもなっている(詳細は文献[7]を参照のこと)。デヒドロアスコルビン酸(ビタミンCの酸化型)は、拡散が促進されることにより、多くのグルコーストランスポーターを通過する能力があることが知られるようになった[[14], [15], [16], [17]]が、この事実は、経口摂取後の用量依存性を説明するものではなかった。その後、アスコルビン酸(還元型ビタミンC)とデヒドロアスコルビン酸が腸内で別々のメカニズムで取り込まれ、アスコルビン酸の取り込みはナトリウム依存性であることが発見された[18]。これは,塚口らによるナトリウム依存性ビタミンCトランスポーター(SVCT)ファミリーの発見と特徴づけと一致していた[6]。塚口らはその後,腸に低親和性・高容量の活性トランスポーターSVCT1が存在することを発見した[19]。さらに,SVCT1は近位腎尿細管の上皮にも存在し,腎臓でのアスコルビン酸の積極的な再吸収を司っている[19]。SVCT1を欠損させたSlc23a1-/-マウスでは,腎分画排泄量が最大18倍に増加する一方で,腸管吸収量はそれほど低下しないことが示されている[20]。このことから,腎のSVCT1によるアスコルビン酸の再吸収は,全身のビタミンCのホメオスタシスの維持に極めて重要であることが示唆される。活性型トランスポーターには用量依存性があり,その発現はいくつかの組織でビタミンCの状態によって調節されている可能性がある[8,21,22]。
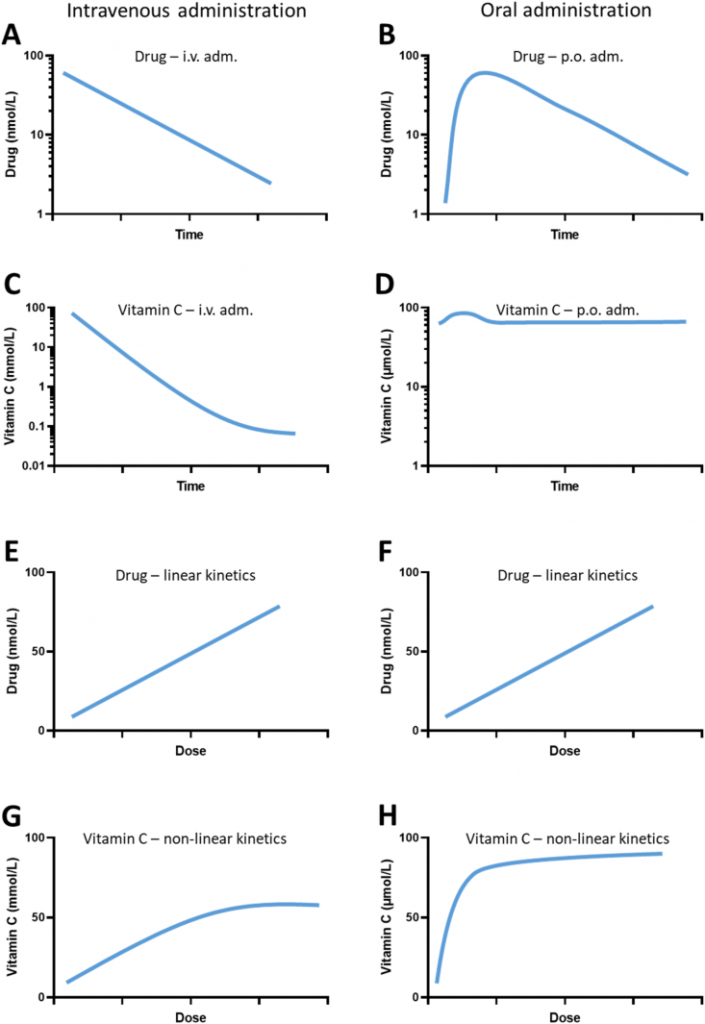
図2 ビタミンCと平均的な低分子医薬品の血漿中濃度の比較
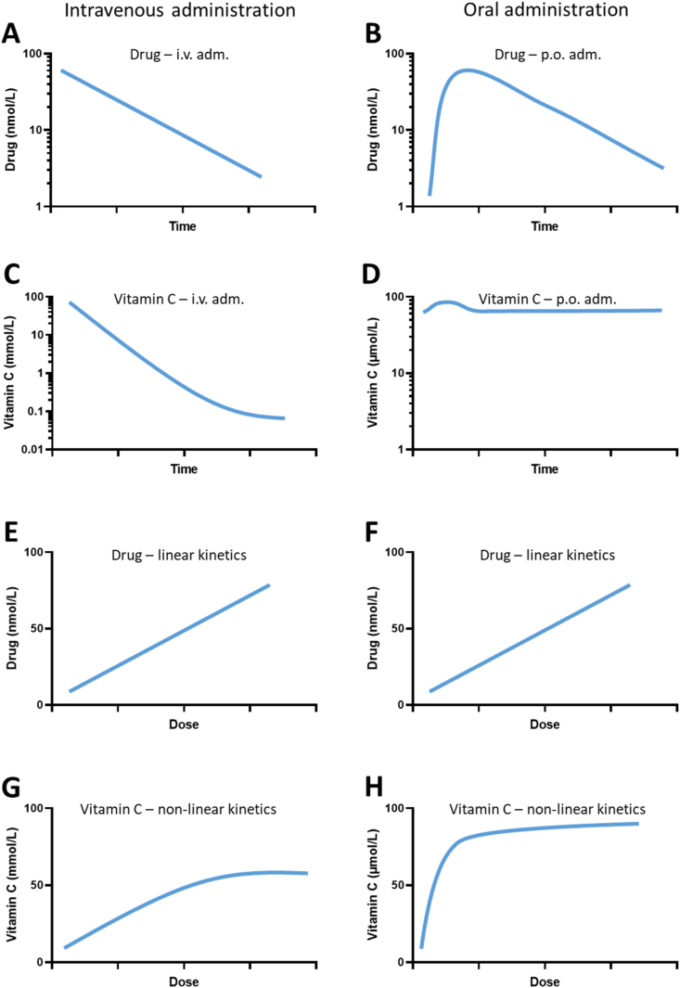
左図は静脈内投与、右図は経口投与を示す。血漿中濃度-ボーラス投与後の時間と最大血漿中濃度-投与量の模式図は、文献[7,10,11,27,48,49,54,[94],[95],[96],[97]のデータから作成した。] プロットは例示のための近似値である。A:平均的な薬物は、i.v.投与後に1次の速度論を示し、排泄半減期は一定である。B:経口投与では、吸収段階の後、i.v.投与と同様の半減期を持つ1次排泄が起こる。C:ビタミンCの静脈内投与では、生理的な濃度範囲に達するまでは1次の速度論となり、排泄量は徐々に減少する。D: ビタミンCを経口投与した場合の血漿中濃度への影響は、個人のビタミンCの状態に大きく依存する。ビタミンCの欠乏は定量的な取り込みを促進し、ビタミンCの充足は血漿濃度プロファイルにほとんど影響を与えずに排泄を促進する。E & F: 平均的な薬物の場合、最大血漿濃度は、投与経路に関係なく、投与量に比例する。G: 最近のi.v.投与のデータをまとめたところ、ビタミンCのi.v.投与後の最大血漿濃度は、約50mmol/L(70g/m2の投与量に相当)までは(点滴)投与量に比例し、その後はそれ以上増加しないことが明らかになった[7]。H:ビタミンCの経口投与による血漿Cmaxは投与量に比例せず、飽和動態を示す[11,98]。
ヒトのSVCT1には、いくつかの一塩基多型(SNP)が同定されている。これらのほとんどは、ホメオスタシスの設定値を低下させることが示唆されているが、個々のSNPsの中には稀にしか存在しないものもあるため、これらの亜集団からビタミンCの動態に関する信頼性の高いデータを得ることは困難であり、これまでのところ、非常に限られたデータしか得られていない。しかし、いくつかの研究では、このようなSNPが疾患リスクの増加と関連している可能性が示唆されている。Zanon-Morenoらは、SLC23A2のrs1279386 SNPと血漿中ビタミンC濃度の低下、および緑内障リスクの上昇との間に有意な関連性を見出している[23]。SLC23A1のSNP rs6596473は、侵襲性歯周炎との関連が示唆されている[24]。Kobyleckiらは、心血管の死亡率と罹患率に関するメンデルスラー無作為化研究において、野生型よりも高いビタミンC濃度を提供するSNP rs33972313を調査した。彼らは、そのデータを「果物や野菜の高摂取による有利な効果が、高いビタミンC濃度によって部分的にもたらされる可能性を排除できない」と結論づけている[25]。言い換えれば、データは決定的ではないものの、SNPが心血管の健康改善と関連している可能性を示していた。興味深いことに、Corpeらは、厳選した既知のSNPについて用量-濃度曲線をモデル化し、同定された最も機能的に劣るSVCT対立遺伝子(A772G、rs35817838)は、生涯にわたるビタミンC欠乏に相当する血漿飽和レベルになることが予想されることを明らかにした[20]。しかし、これらのモデリング研究とその潜在的な表現型の結果は、臨床研究ではまだ確認されていない。
血漿から組織へのビタミンCの分布は、主にSVCT2,すなわち、低容量高親和性バージョンのビタミンCトランスポーターによって支配されている。SVCT2は,ほとんどの細胞型に存在しており,トランスポーターの局所的な濃度やアイソフォームが,個々の臓器・組織の定常状態の濃度を決定すると考えられている[7]。モルモット(ヒトと同様にビタミンCを合成できない)を用いた詳細な研究から、SVCTの発現レベルの違いにより、臓器間のビタミンCの分布が非常に多様になることが知られている(図1参照)[21,22]。例えば、定常状態の濃度が最も高い組織である脳/副腎と定常状態の濃度が最も低い組織である腎臓/心臓/筋肉の間では、定常状態の濃度に最大20倍の差があることが測定されている[[26], [27], [28], [29], [30], [31]]。
図1
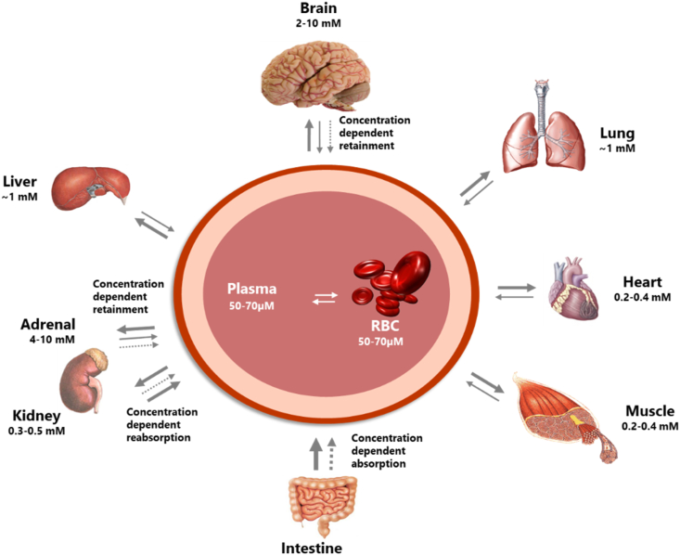
ビタミンCの体内分布は、臓器によって大きく異なる。いくつかの臓器は、濃度に依存したビタミンCの保持機構を持っており、ビタミンCが十分に供給されていない時に、他の臓器を犠牲にして高いレベルを維持している。特に、脳がその役割を担っている。さらに、濃度依存的な吸収と再吸収のメカニズムが、体内のビタミンCのホメオスタシス制御に貢献している。参考文献より転載 [7].
ビタミンCの代謝は、その酸化還元状態と密接に関連している。アスコルビン酸は、フリーラジカルをクエンチする能力と、かなりの数のモノおよびジオキシゲナーゼ酵素に電子を提供する能力を併せ持つ、効率的な連鎖破壊型抗酸化物質である[32]。さらに、酸化されたビタミンCは、さまざまな種類の細胞によって、酸化型から生物学的に活性な還元型のアスコルビン酸へと細胞内でリサイクルされることで、ほぼ定量的に救済されるように、さまざまなメカニズムが進化してきた[[33], [34], [35], [36], [37], [38], [39], [40], [41], [42]]。このように、健康な非喫煙者のビタミンCの1日の回転率はわずか3%と推定されており[43]、十分な量を維持するために摂取する必要のある1日の量は非常に限られている。さらに、試験管内試験および生体内試験の研究では、赤血球は血液中のビタミンCの総量を約3分に1回リサイクルできると推定されている[28,33]。用量依存的な腎再取り込みと、デヒドロアスコルビン酸からアスコルビン酸へのリサイクルは、体内のビタミンCのホメオスタシスの維持に役立っている[7,44]。
ビタミンCの非経口投与は、腸管吸収をバイパスするため、達成可能な血漿濃度を制限する飽和輸送メカニズムを回避する[[45], [46], [47]]。経口投与とは対照的に、5〜70gのビタミンCを静脈内に投与すると、予測可能な血漿濃度が得られ、この用量範囲でのi.v.投与は、約2時間の一定の半減期を持つ1次カイネティクスに従うことが研究で示されている[48,49]。薬理学的用量のビタミンCを静脈内に投与すると、経口投与では達成できないミリモルの血漿濃度が得られる。薬理学的用量のビタミンCは、現在、敗血症と癌治療の両方で評価されている[[50], [51], [52], [53]]。
3. ビタミンCと「通常の」低分子医薬品との比較
ビタミンCの薬物動態特性は、上述したように、その投与量と濃度の関係を、典型的な低分子医薬品のそれとは全く異なるものにしている。図2は、ビタミンCと「平均的な低分子医薬品」との違いを、血漿中濃度対時間、血漿中定常濃度対投与量、および投与経路依存性について示したものである。また、排泄と組織内の定常濃度を図3に示した。一般的に薬物は1次動態を示し、投与量に比例して、投与経路に関係なく、血漿中および組織中の濃度が予測できる(図2A, B, 2E, 2F)。一方、ビタミンCは、経口投与では様々な動態を示し(図2D)静脈内投与ではほぼ生理的レベルに達するまで主に1次の動態を示す(図2C)。経口投与では明らかな用量依存性が見られ(図2H)約70〜80μmol/Lで最大レベルに達する。驚くべきことに,広い範囲で1次カイネティクスを示すものの,70g/m2以上の投与量では静脈内投与でも約50mmol/Lの最大値に達する可能性がある[7]。重要なのは,図2Gの最高濃度を支持するデータは,たった1つの研究から得られたものだということである[48]。表1は、平均的な医薬品の基本的な薬物動態特性(吸収、分布、代謝、排泄、およびモデルオプション)を、ビタミンCのそれと比較してまとめたものである。明らかに、ビタミンCの輸送の用量依存性は、その薬理学に大きな影響を与える。さらに重要なことは、この情報からいくつかの重要なポイントを引き出すことができるということである。第一に、人間に対するビタミンCの介入の潜在的な有効性は、試験開始時の個人のビタミンCの状態と密接に関連している。したがって、ある程度のビタミンCの欠乏や不足がない人は、さらなる補充や摂取によって恩恵を受ける可能性は非常に低いと考えられる。次に、複数の疫学調査によると、世界のほとんどの地域では、人口の大半が食事によって十分な量のビタミンCを摂取していることが分かっている。そのため、ビタミンCの摂取不足を基準としない臨床試験では、測定可能な臨床効果が得られる可能性は極めて低いと考えられる。血漿中の70μmol/L前後の飽和状態のホメオスタシスポイントをオーバーシュートしても、体内のビタミンCは非常に短時間しか増加しないという事実は、臨床文献ではほとんど無視されてきた[54]。実際、死亡率をエンドポイントとしたビタミンCの有効性に関するシステマティックレビューの35の無作為化対照試験を再検討したところ[55]、どの試験もビタミンCの状態を組み入れ基準に入れておらず、介入前のビタミンCの状態がある程度最適でないことを示した試験は1つしかなかった[2]。
図3 ビタミンCと平均的な低分子化合物の組織内濃度の比較
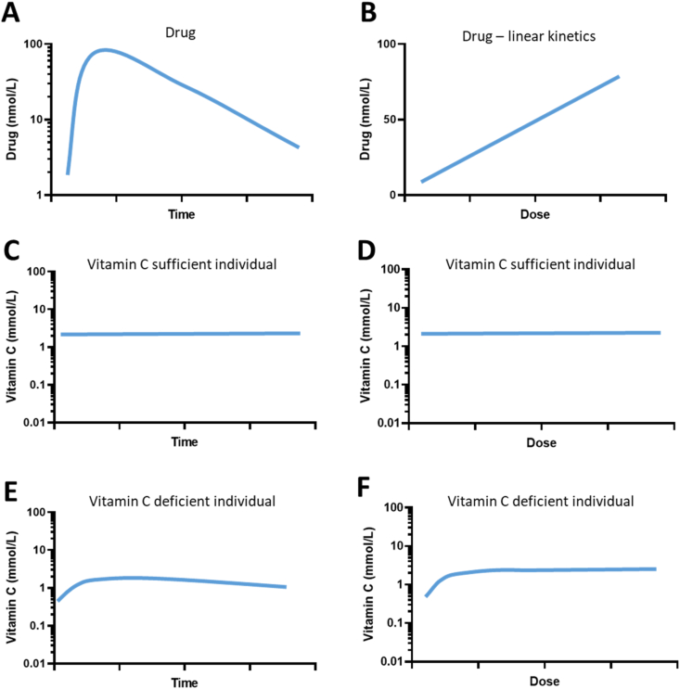
プロットは説明のための概算値。
A:通常の薬物は、投与後、平衡に達するまで受動的拡散により速やかに組織内に分布する。その後、薬物は血漿中の排泄量と同じ半減期で組織から排泄される[97]。
B:最大組織濃度は投与量に比例する。
CとD。ビタミンCを十分に摂取している人では、組織濃度は定常状態にあり、不十分な量を投与しない限り大きな変動はない。個々の組織の最大組織濃度は、SVCTの構成と発現に依存し、投与量の増加とともに飽和動態を示す[7,10,11]。
E: ビタミンC欠乏症の人では、SVCT2の発現と組織の優先順位に応じて、ビタミンCを投与すると組織濃度が速やかに上昇する[7]。ビタミンCの投与を中止すると、組織濃度は徐々に低下するが、血漿コンパートメントからよりもはるかにゆっくりと低下する。脳のようないくつかの組織は、新たな欠乏の結果、増加する濃度勾配に対してビタミンCを保持する顕著な能力を持っている[92,99]。
F: ビタミンCが欠乏している人では、十分なビタミンCが供給されれば、定常状態のレベルに達する。組織の定常状態の濃度は飽和レベルを超えない。
表1 経口投与される医薬品の典型的な薬物動態特性と、食品やサプリメントから摂取されるビタミンCの薬物動態特性(文献[3]より改変)
| 薬物動態特性 | 代表的な経口投与の低分子医薬品 | 食材やサプリメントから得られるビタミンC |
|---|---|---|
| 吸収 | 治療域内での1次吸収動態。受動的な輸送により吸収され、血漿中濃度はナノからマイクロモルの範囲となる。 | SVCT1を介した飽和能動輸送とGLUTトランスポーターを介した促進拡散の混合による非線形吸収動態により、血漿中濃度はマイクロモル、組織中濃度はミリモルとなる。 |
| 分布 | 主に受動的拡散により分布する。直後の分布は主に血流と組織灌流によって決定される。ホメオスタシスは、主に脂溶性、pKa、タンパク質結合などの薬物の物理的・化学的特性に基づいている。 | 主に能動的な輸送により分配される。SVCT2トランスポーターの発現と飽和動態によって支配される組織の優先順位に基づいて即時的に分配される。ホメオスタシスは、適切な投与量と体内のビタミンCの状態に依存する。 |
| 代謝 | 第I相および第II相酵素により非特異的に分解され、水溶性の高い代謝物や抱合体が生成される可能性がある。 | 電子供与体と抗酸化物質によって特異的および非特異的に酸化されるが、多くの細胞タイプによって細胞内で効率的に還元型に再生される。 |
| 排泄 | ほとんどの場合、1次の排泄速度で排泄されるが、pKaに応じて糸球体濾過と受動的再吸収が行われる。尿や胆汁を通して親化合物や代謝物が比較的早く排泄される。 | 非線形の濃度依存性排泄動態により、ビタミンCの利用可能性や体内コンパートメントの飽和度に応じて,0~100%の能動的腎再吸収が行われる。 |
| モデリング | キネティクスは通常、単純なコンパートメントモデルやノンコンパートメントモデルでうまくモデル化できる。 | コンパートメント分析およびノンコンパートメント分析で使用される末端1次カイネティクスの基本的な仮定には準拠していない。 |
4. ビタミンCの臨床試験のデザインと解釈における落とし穴
健康および疾病におけるビタミンCの効果を評価する際には、いくつかの落とし穴やデザイン上の課題がある。いくつかの主な要因を表2にまとめた。疫学研究は、因果関係を確立する能力に欠けており、一般的に臨床エビデンスの階層では高く評価されていない。観察研究には交絡というリスクがつきものであり、ビタミンCのような微量栄養素の研究では、複数の欠乏や未知の欠乏による影響が明らかであり、それを明確に調整することは本質的に不可能である。そのため、ビタミンCの不足と疾患や死亡リスクの増加との関連が確認されても、実際には研究で説明されていない他の要因と因果関係があるかもしれない。しかし、一般的な考え方とは対照的に、同じ臨床テーマを対象としたランダム化比較試験(RCT)と観察研究を詳細に評価したところ、デザインの良い観察研究では、RCTの場合と比較して治療効果の大きさを系統的に過大評価しないことが明らかになった[56]。
表2 健康および疾病におけるビタミンCの臨床研究において、結果を誤って解釈したり、誤った結論を出したりする可能性のある、最も重要なデザイン上の課題のまとめ。
| 研究タイプ | 設計上の課題 | 解釈における潜在的な落とし穴 |
|---|---|---|
| 観察研究 | 交絡 | ビタミンCの欠乏は、他の微量栄養素の欠乏、最適でない生活習慣、その他の残余交絡を伴うのが一般的であり、これらが観察された関連性の一因となる可能性もある。 |
| ビタミンC摂取量をビタミンC状態の代理指標とすること | ビタミンC摂取量の推定は本質的に不正確であり、摂取量と状態の関係は非常に複雑であるため、ビタミンC状態の代理指標としては不十分である。 | |
| ランダム化比較試験 | 被験者は試験開始時にすでにビタミンCを多く摂取していた | 経口投与によるビタミンCの飽和動態のため、個人のビタミンCの状態は、サプリメントの潜在的な効果に大きく影響する。ビタミンCの欠乏は特定の集団に限られることが多いため、この点を考慮しない組み入れ基準では、潜在的な有効性が効果的に希釈されてしまう。 |
| プラセボ群ではサプリメントを継続摂取 | プラセボ群ではサプリメントを継続摂取することで、ビタミンCの補給自体の効果ではなく、2つの用量のビタミンCを互いに比較して検証する。飽和速度論のため、ビタミンCの介入効果を確認する可能性はさらに低くなる。 | |
| 介入群、プラセボ群ともに、生涯にわたってビタミンCを摂取している。 | 人間の食生活では、ビタミンCの補給を考慮しない場合、一般的に1日あたり0〜250mgのビタミンCが含まれており、その範囲は広く、上限はいくつかの大規模介入試験の範囲内、あるいはそれを超える。したがって、試験期間中のサプリメントとプラセボの比較による疾患予防効果の可能性は、試験対象者全員の生涯にわたるビタミンCの状態と比較する必要がある。 | |
| ビタミンCは単一のサプリメントとしてテストされていない | ビタミンCを単一のサプリメントとしてテストしていないため、それ自体の効果を抽出する可能性が限られる。 | |
| すべての研究 | 選択バイアス | 微量栄養素を既に多く含む健康的な食事をしている健康意識の高い自発的な被験者が募集され、背景となる人口よりも疾病率が低くなる可能性がある。そのため、サプリメントの効果を確認することができない可能性がある。 |
| 非絶食時の血液サンプルを用いた場合 | 口腔内でビタミンCを摂取すると、個人のビタミンCの状態に応じて、一過性ではあるが血漿中の濃度が大きく上昇する(例として図2Dを参照)。このため、ばらつきが大きくなり、平均的なビタミンC濃度が人工的に高くなってしまう可能性がある。 | |
| 不適切な試料の取り扱い | 不適切な試料の安定化と取り扱いは、方法の如何にかかわらず、試料採取後の酸化を促進し、事実上低いビタミンC濃度をもたらす。 |
4.1. ビタミンCの摂取量と摂取状態の測定
コホート研究における誤った結論の原因として、ビタミンCの摂取量ではなく、ビタミンCの状態に焦点を当てていることが考えられる。大規模な研究を含む多くのコホート研究では、ビタミンC摂取量と疾病リスクとの相関関係の根拠として、自己申告による食物摂取頻度調査(FFQ)や食物ダイアリーから得られた微量栄養素の摂取量の推定値を用いている(表3)。しかし、上記で指摘したように、ビタミンCの摂取量とステータスの間には直線的な関係はない。さらに重要なことは、ビタミンC摂取量と血漿・組織のホメオスタシスとの関係は、個人のビタミンCの状態に大きく依存しており、それは血漿分析によってのみ評価可能であるということである。さらに、FFQは、人間の想起誤差、食品の保存や調理によるビタミンの損失を考慮できないこと、ビタミンCのホメオスタシスに影響を与える可能性のある多型を考慮していないことなどにより、精度や正確さに欠けるという問題がある[1,[57], [58], [59], [60]。つまり,FFQから得られる情報は,個人の真のビタミンCの状態を確立するには不十分であり,少なくとも変動性が大きく,その結果,タイプ2エラーのリスクが高まることになる。また、ほとんどのコホート研究では、ベースライン時にしか情報を収集していないため、経時的な食生活の変化は考慮されていない。しかし、血漿中のビタミンCの状態は、食品やサプリメントを摂取した直後に大きく変動する可能性がある[54]。したがって、ビタミンCの状態に関する最も信頼性が高く、実際に利用可能な情報は、絶食した人の血液サンプルからしか得られない。この要件は、ほとんどの観察研究では明らかに満たされていない。
表3 主要な観察研究における疾病リスク/死亡率に対するビタミンC摂取の効果。
これらの研究の主な限界は、i)ビタミンC摂取量をビタミンCの状態の代替として推定していること、ii)ほとんどの研究で選択バイアスがかかっていること、iii)ビタミンC摂取量の推定値が1つしか使われていないことである。
| 調査データ | 看護師の健康調査[ 73 ] | EtudeEpidémiologiqueaupre’sdefemmes delaMutuelleGénéraledel’EducationNationale [ 78 ] | 医療専門家の 追跡調査[ 79 ] |
EPICOR研究[ 80 ] | アイオワ女性の健康調査[ 81 ] |
|---|---|---|---|---|---|
| 調査対象母集団 | 30〜45歳の85,118人の健康な米国の女性看護師 | 57,403人のフランスの健康な女性、40〜65歳 | 心血管疾患または糖尿病のない43,738人の米国人男性、40〜75歳 | 41,620人のイタリア人男性および女性(MIまたは脳卒中なし、44〜61歳) | 34,492人の米国の閉経後の女性、55〜69歳 |
| 最高の中央値のvitC摂取量(mg / d) | 704; 上位五分位 | 228 a ; 上位四分位 | 1167; 上位五分位 | 201; トップ三分位 | 679; 上位五分位 |
| 最小の中央値のvitC摂取量(mg / d) | 70; 下の五分位 | 77.5 a ; 下四分位 | 95; 下の五分位 | 83; ボトムタータイル | 82; 下の五分位 |
| 調整 | 年齢、エネルギー摂取量、サプリメントの使用、アルコール、喫煙状況、糖尿病 | 年齢、経口避妊薬、ホルモン療法、アルコール、BMI、身体活動、エネルギー摂取、喫煙、サプリメントの使用、教育、および特定の乳がんのリスク要因 | 年齢、季節、喫煙、エネルギー摂取量、アルコール、高血圧、MIの親の病歴、職業、BMIおよび身体活動。 | 年齢、センター、性別、高血圧、喫煙、教育、エネルギー摂取量、アルコール、胴囲、肥満、および身体活動。 | 年齢、BMI、ウエストヒップ比、高血圧、糖尿病、ERT、教育、婚姻状況、喫煙、身体活動、エネルギー摂取量、コレステロール、アルコール、飽和脂肪、魚、vitE、カロテノイド、繊維、全粒穀物 |
| フォローアップ期間(年) | 16 | 10 | 8 | 7.9 | 11 |
| 終点 | CHD | 閉経後の乳がん | 脳卒中 | 脳卒中 | 脳卒中による死亡 |
| 結果 | ビタミンC摂取量とCHDのリスクとの逆相関。VitCサプリメントはCHDのリスク低下と関連していた | 乳がんのリスクとは関係のないVitCサプリメントの使用。食品からのビタミンC摂取量の上位四分位数は、乳がんのリスクの増加のみを示しました | ビタミンCの摂取もサプリメントも脳卒中のリスク低下とは関連していませんでした | 虚血性脳卒中のリスク低下に関連するVitC | ビタミンC摂取と脳卒中による死亡との間に関連性はありません |
略語の説明 BMI(body mass index)CHD(chronic heart disease)心血管疾患(cardiovascular disease)DBP(diastolic blood pressure)ERT(estrogen replacement therapy)IHD(ischemic heart disease)MI(myocardial infaction)SBP(systolic blood pressure)vitC(vitamin C)vitE(vitamin E) a食品からの平均摂取量のみを報告。
4.2. ビタミンCの不安定性
たとえ空腹時の血液サンプルが得られたとしても、ビタミンCの状態と疾患リスクを関連付けるには大きな課題があると思われる。これは、アスコルビン酸塩が生体外で不安定であることに起因する。アスコルビン酸塩は生体内ですぐに酸化され、その結果生じる酸化生成物はすぐに分解または代謝されるため[13]、分析の回収率が低くなってしまう。さらに複雑なのは、溶液中のビタミンCの酸化は濃度に依存することである[61,62]。そのため、有効なビタミンC濃度を得るためには、サンプルの取り扱いに細心の注意を払う必要がある[[63], [64], [65], [66]]。一般的に、バイオバンクから回収された血液/血漿/血清サンプルは、ビタミンCを分析する目的で特別に安定化して保存されていないため、サンプリング後の酸化を防ぐために適切に取り扱われていない。最後に、ビタミンCの分析は様々な方法論で行われてきたが、その中にはビタミンCとは無関係の多くの検体を検出したり、分解を引き起こす誘導体化手順に基づいたものもある。他の研究者がレビューしているように、アスコルビン酸の堅牢な定量は電気化学的検出を用いた高速液体クロマトグラフィーによって達成されている[67]。
4.3. RCTにおけるデザインの問題
RCTは、医薬品の有効性と安全性を検証するためのゴールドスタンダードと考えられている。しかし、すでに体内にかなりの濃度で存在する微量栄養素の慢性疾患予防における有効性を検証するためには、デザインコンセプトとしてのRCTには多くの課題がある[[68], [69], [70], [71], [72]]。微量栄養素の研究は、ほとんどの場合、二次予防研究よりも統計的検出力の低い一次疾患予防研究として実施される。このような研究では、十分な疾患エンドポイントを蓄積するために、非常に長い介入期間を必要とする場合がある [1]。このような観点から、試験までの間にプラセボ群と介入群の両方で生涯にわたってビタミンCを摂取した場合の蓄積された予防能力と比較することができる。Nurses’ Health研究では、85118人の女性看護師の食事情報を収集し、彼らの食事には61~209mgのビタミンCが含まれていると推定された(最低と最高の五分位における摂取量の中央値) [73]。このことは、介入研究に採用された被験者のかなりの割合が、登録前の何年もの間、試験用サプリメントよりも多くのビタミンCを摂取していた可能性があることを示唆している。残念ながら、この潜在的なバイアスの影響は、利用可能な文献では完全に無視されている。
さらに、RCTにはプラセボ群を含めるべきである。これに加えて、ビタミンCを対象とした最大規模の介入研究のいくつかでは、いわゆる「プラセボ群」が試験期間中、現在のRDAのレベルまでサプリメントを摂取し続けることが認められている([[74]、[75]、[76];表5参照)。ビタミンCの場合、プラセボ群の人たちは、1日あたり約350mgのビタミンCを摂取していても、対照群とみなされる可能性があることを示唆している。ほとんどの場合、プラセボ群の同時摂取の頻度は記録されていないが、Women’s Antioxidant Cardiovascular Studyでは、プラセボ群の27.5%が同時摂取していたと報告されている[74]。また、プラセボ群で報告された血漿濃度から、平均71.5μmol/Lと、プラセボ群がすでに飽和範囲に十分に入っていたことが明らかになっている[74]。前述のように、ビタミンCは用量依存性の動態を示し、70μmol/L付近で飽和状態に達する。これに基づけば、このような介入試験で有意な結果が得られたとしても、それは驚きに値する。事実、ビタミンCを用いた介入研究では、真のプラセボ群は存在せず、多くの場合、あまり変わらない2つの用量のビタミンCの効果を比較しており、対象となるビタミンCの状態から見て、ほとんど重複した集団になる。このため、これらの試験における介入効果の可能性は一般的に非常に低いものとなっている。残念なことに、参加時にビタミンCの状態が悪い人が受ける可能性のある利益は、識別できないほど希釈されているかもしれない。
表5 主要な無作為化比較試験におけるビタミンC補給の効果
提示された研究の主な限界は、ほとんどの場合、i)プラセボ群での同時補充を認めていたこと、ii)ビタミンCが十分な人を対象としていたこと、iii)ビタミンCの量が不十分なマルチビタミンサプリメントを使用していたことである。
| 調査 | 臨県研究[ 88 ] | 予防研究[ 75 ] | 医師の健康調査II [ 76 ] | SU.VI.MAX研究[ 90 ] | 女性の抗酸化心血管研究[ 74 ] |
|---|---|---|---|---|---|
| 人口 | 中国河南省林州県出身の40歳以上の男性と女性29,584人 | CHDまたはその他の閉塞性動脈疾患または糖尿病を患う40歳以上の英国人男性および女性20,536人 | 40歳以上の米国の男性医師14,641人 | 35歳以上のフランス人男性および女性13,017人 | 40歳以上で以前にCVDまたは高リスクの米国女性8171人 |
| 設計 | ½(2×2 x 2×2) | 2×2 | 2×2(×2×2) | 平行 | 2×2×2 |
| エントリー時のVitC濃度(μmol/ L) | 11.4 a | 報告されていない | 報告されていない | 54.5 | 報告されていない |
| プラセボ中のVitC濃度(μmol/ L) | 30.7 | 43.2 | 報告されていない | 58.0 | 71.5 |
| VitCグループ対プラセボ(Δμmol/ L) | 15.3 | +15.7 b | 報告されていない | +11.3 c | +35.2 d |
| 空腹時の血液サンプル(はい/いいえ) | 報告されていない | 番号 | 報告されていない | はい | 報告されていない |
| 被験者はサプリメントを同時に服用することを許可されました(プラセボはサプリメントを服用しています) | 報告されていない | はい、ただし高用量のvitEではありません(報告されていません) | はい、RDAまで(1ヶ月/年以上で4.4%) | 番号 | はい、RDAまで(27.5%) |
| 介入 | ビタミンC(120 mg / d)+ Moを含むさまざまなビタミン/ミネラルの組み合わせ | ビタミンCを含むマルチビタミン(250mg /日) | ビタミンC(500 mg / d)またはその他の抗酸化物質 | ビタミンCを含むマルチビタミン(120mg /日)。 | ビタミンC(500 mg / d)またはその他の抗酸化物質 |
| 研究期間(年) | 5.25 | 5 | 8 | 7.5 | 9.4 |
| 終点 | 死亡率とがんの発生率 | 主要な冠状動脈イベントおよび致命的または非致命的な血管イベント | 心血管イベント、心筋梗塞、脳卒中、またはCVDによる死亡 | 虚血性心血管疾患とすべての原因による死亡率 | 心筋梗塞、脳卒中、冠状動脈血行再建術、またはCVD死 |
| 結果 | ビタミンC + Mo補給の効果なし | ビタミンC補給の効果なし | ビタミンC補給の効果なし | CVDには影響しませんが、男性のすべての原因による死亡率は低くなります | ビタミンC補給の効果なし |
a98名(参加者の約5%)can unselected subsample、d30名の現地参加者で評価した。略語の説明 心血管疾患は心血管疾患、Moはモリブデン。
ビタミンCの臨床試験におけるより一般的な課題として、広告で募集した場合の選択バイアスの可能性がある。微量栄養素研究における「健康な登録者効果」はよく知られており、微量栄養素がすでに豊富に含まれた健康的な食事を食べ、背景の人々よりも運動頻度が高く疾病率が低い、健康意識の高い自発的な被験者を募集する傾向を示している[70,77]。また、ビタミンCは酸化還元活性が高く、不安定な化合物であるため、サンプルの取り扱いは非常に重要であり、特に大規模な多施設試験では特別な注意が必要である[[63], [64], [65], [66]]。試料の安定性の問題に注意を払わないと、作業中の損失によってビタミンCの値が低くなってしまう。一方、非絶食状態の人からサンプルを採取すると、定常状態の値が人工的に上昇することになる(表2)。
5. 臨床的証拠の再検討
以下では、ビタミンCに関する最大の臨床研究を、表1および表2に記載された情報に基づいて再検討する。現実的な理由から、このレビューでは各カテゴリーの最大の5つの研究のみを再検討している。これらの研究は、権威的に最も影響力があると考えられ、網羅的なシステマティックレビューではなく、ビタミンCに関する文献の課題を説明するためのものである。
5.1. ビタミンC摂取量を推定するプロスペクティブコホート研究
ビタミンCと罹患率および死亡率との関係については、数十年にわたってかなりの数の観察研究が行われてきた。ビタミンCと疾病に関する研究の中で最も大規模なものは、ビタミンCの状態そのものを測定するのではなく、FFQや食事日記を用いてビタミンC摂取量と疾病リスク・死亡率との関係を推定するコホート研究である。そのため、推定された摂取量と実際のビタミンCの状態を関連付けることができないという問題がある。これらの研究を表3に示す。
Nurse’ Health Studyでは、慢性心疾患のリスクに対するビタミンCの摂取量と補給量の関連性を調べた [73]。その結果、ビタミンCの摂取量と慢性心疾患との間には有意な逆相関が認められたが、サプリメントの使用にも正の相関が認められた。半定量的なFFQを用いて、追跡期間中に4回、サプリメントを含む微量栄養素の摂取量を評価した。著者らが認めているように、本研究の主な弱点は、サプリメントを利用していない人のビタミンC摂取量の中央値が132mg/日と推定されるなど、対象者が十分に栄養状態にあったことである。これは、研究当時のRDAの2倍以上に相当する量である。したがって、この研究では、ビタミンCの摂取量が少ない人や心血管疾患の危険因子を持つ人に効果があるかどうかはわからない。
フランスのE3N研究では、教師を中心とした健康な女性のコホートにおいて、食品およびサプリメントからの推定ビタミンC摂取量と閉経後の乳がんのリスクとの関連性が評価された [78]。この研究では、ビタミンCのサプリメント摂取と乳がんとの間に全体的な関連性は認められなかったが、驚くべきことに、食品からのビタミンC摂取量の上位4分の1のみが乳がんのリスクの増加を示し、U字型またはJ字型の関係の可能性が示唆された。栄養摂取量の推定には、自分で開発したFFQが用いられ、詳しくは述べられていないが、検証研究では、ビタミンC摂取量の相関係数は、再現性で0.73,妥当性で0.55と、かなり低い値であった。残念ながら、FFQはビタミンCの摂取状態については検証されていないため、この目的には特に適していない。ビタミンCの補給状況は追跡調査で数回評価されたが、食物からの推定ビタミンC摂取量は、ベースラインの1回の時点でしか推定されなかった。そのため、本研究では、FFQに基づくという制限もあり、10年間の追跡期間中の食事の変化を考慮していない。
Health Professionals Follow-up Study [79]では、健康な男性を対象に、推定ビタミンC摂取量と脳卒中のリスクとの関連性が検討された。この研究では、8年後にビタミンCの摂取量またはサプリメントの摂取量と脳卒中のリスクとの間に関連性がないことが報告された。食品およびサプリメントからのビタミンC摂取量は、FFQを用いて2年ごとに評価された。上述の研究と同様に、著者も認めているように、この集団は平均的な集団よりも栄養状態が良かったので、この研究は、ビタミンCの状態が悪い人や脳卒中や心血管疾患の危険因子を持つ人に有効である可能性については、あまり洞察を与えていない。
EPICOR研究は、European Prospective Investigation into Cancer and Nutrition(EPIC)研究コホートのイタリア部分を対象とし、推定ビタミンC摂取量と虚血性脳卒中との相関の可能性を調査したものである[80]。この研究では、ビタミンCが虚血性脳卒中のリスク低下と有意に関連していることがわかった。この研究では、推定総抗酸化力を主要評価項目としていたため、ビタミンC摂取量との相関はサブ解析の結果であった。総抗酸化能は、抗酸化作用を示す無数の多かれ少なかれ重要な分子の非常に粗い尺度であり、この場合は間接的な推定値である。総酸化防止能は、果物摂取の代理指標と考えられるかもしれないが、コーヒーやワインを含む他の多くの成分もかなり寄与していることが示された[80]。この研究の重大な弱点は、脳卒中の総症例数が非常に少なく、調査した328,553人年あたり194例に過ぎないことである。さらに、推定されたビタミンCの摂取量は、ベースライン時に一度しか推定されなかった。そのため、この研究では、約8年間の追跡調査期間中の食事の変化は考慮されていない。
Iowa Women’s Health Studyでは、閉経後の女性における推定ビタミンC摂取量と脳卒中による死亡率との間に相関関係があるかどうかが評価された[81]。ビタミンCの摂取量と脳卒中による死亡率との関連は認められなかった。調査対象者は,運転免許証を持つアイオワ州の女性の無作為抽出標本の一部であった。上述のNurses’ Health研究[73]でも使用されたFFQの妥当性は、44人の女性のサブグループにおいて、5回の24時間の食事記録による平均摂取量と食物頻度調査票による回答を比較することで行われた[82]。そのため,血漿中のビタミンCの状態との相関については評価されなかった。ビタミンCの摂取量に関する2つの食事評価法の比較の相関係数は、食品のみの場合は0.53,食品とサプリメントを合わせた摂取量の場合は0.76であった[81]。ここでも、ベースライン時の推定値は1つしか行われなかった。
以上の研究を総合すると、いずれも非常に大規模で、かなりの追跡期間がある。しかし、これらの研究はすべて、ビタミンCの摂取による影響を調査するという特別な意図を持たない、幅広い目的の人口調査として計画されたものである。これら3つの大規模な研究は、栄養状態の良い人、すなわち医療従事者や教師に明らかな選択の偏りがある。平均以上のビタミンC摂取は全身のビタミンC状態にほとんど影響を及ぼさないため、ビタミンC状態と疾患との関連性を明らかにする上での有用性は著しく低い。また、ほとんどの研究では、ベースラインのビタミンC摂取量の推定値が1つしか含まれていないため、研究期間中の食生活のパターンや変化、さらには疾病リスクに強い影響を与える可能性のある研究までの生涯の食生活についても誤って表現されている可能性がある。最後に、ビタミンCに関する残余交絡の可能性は、ビタミンC摂取量と健康状態との相関が特に高摂取時に低いことから、相対的に高いと予想される。
5.2. ビタミンCの状態を測定する観察研究
FFQや食事日記を用いてビタミンC摂取量を推定するのではなく、血液中のビタミンCの状態を測定した研究に限定することで、少なくとも理論的には科学的な質がかなり向上するはずである。これらの研究は表4にまとめられている。EPIC-Norfolk調査では、ビタミンCに関する2つの研究を含むかなりの数の研究が行われている[83,84]。どちらも約20,000人の男女を対象とした前向きコホート研究である。最初の研究では、4年後の全死因、心血管疾患、虚血性心疾患、およびがんの死亡率との関係の可能性を検討した[84]。この研究では、ビタミンCの状態が、全死亡率だけでなく、心血管疾患および虚血性心疾患による死亡率と有意に逆相関していることが示された。また、このデータは明確な濃度反応関係を示した。血漿中のビタミンC濃度が20μmol/L上昇するごとに、全死亡リスクが20%低下することが確認された(p<0-0001)。また、ビタミンCの状態が上位5分位と下位5分位では、死亡リスクが約半分になった。この結果は、わずか4年間という短い追跡期間を考慮すると、素晴らしいものである。しかし、先に述べた多くの研究と同様に、ビタミンC(この場合は状態)の評価はベースライン時に1回だけ行われた。短期間であるため、食生活が大きく変化する可能性は低くなるが、関連性はある。さらに、この研究では社会階級と身体活動の調整を行っていないが、これは解析時にこれらのデータが入手できなかったためである。2番目のEPIC-Norfolkでは、約10年の追跡期間で、血漿中のビタミンCの状態と脳卒中のリスクとの関係が調査された[83]。この研究では、ビタミンCの状態が上位4分の1の人は下位4分の1の人に比べて、脳卒中のリスクが42%低いことがわかった。この研究では、196,713人年あたり448件の脳卒中発症を対象としており、前述のEPICOR研究に比べて約4倍高い発症率となっている。いずれの研究でも、ビタミンCの定量には、誘導体化後のフルオロメトリック・アッセイが用いられている。これらのアッセイは、高速液体クロマトグラフィーを用いた方法に比べて、精度や正確性が低いことが知られている[67]。しかし、サンプルの取り扱いに細心の注意が払われていれば、サンプルの一般的な過大評価または過小評価が研究結果に影響することはなく、潜在的なばらつきの増加は、観察された差の重要性を弱めるだけであろう。両研究とも、一般的にビタミンCの状態を過大評価する非絶食血液サンプルを使用した。
表4 主要な観察研究における疾患リスク/死亡率に対するビタミンC状態の影響
これらの研究の限界は、i)非絶食の血液サンプルを使用したこと、ii)分析方法が最適ではないこと、iii)複数の欠乏の可能性を考慮していないことである。
| 調査データ | EPIC-ノーフォーク[ 83 ] | EPIC-ノーフォーク[ 84 ] | NHANES II [ 85 ] | NHANES II [ 87 ] | NHANES II [ 86 ] |
|---|---|---|---|---|---|
| 調査対象母集団 | 英国ノーフォーク出身の40〜79歳の男性と女性20,649人 | 英国ノーフォーク出身の45〜79歳の19,496人の男性と女性 | 30〜75歳の8417人の米国の男性と女性 | 30〜75歳の7071人の米国の男性と女性 | 60〜74歳の米国の男性と女性6624 |
| 最高グループのvitC濃度(μmol/ L) | ≥66.0; 上位四分位 | 79.2; 上位五分位 | 79.5(64.7–158.8) | ≥73.8; 上位四分位 | 85.2(64.7–158.8) |
| 最低グループのvitC濃度(μmol/ L) | <41.0; 下四分位 | 25.9; 下の五分位 | 17.0(5.7–22.7) | <28.4; 下四分位 | 17.0(5.7–22.7) |
| 空腹時の血液サンプル(はい/いいえ) | 番号 | 番号 | 番号 | 番号 | 番号 |
| 分析方法 | 蛍光分析 | 蛍光分析 | 比色分析 | 比色分析 | 比色分析 |
| 調整 | 年齢、性別、喫煙、BMI、SBP、コレステロール、身体活動、糖尿病、MI、社会階級、アルコールとサプリメントの使用 | 年齢、収縮期血圧、コレステロール、喫煙、糖尿病、およびサプリメントの使用 | 性別 | 喫煙状況 | 年齢、性別、人種、教育、身体活動、喫煙、アルコール、コレステロール、BMI、糖尿病、高血圧、アスピリン、およびvitEの使用 |
| フォローアップ期間(年) | 9.5 | 4 | ?* | 12〜16 | ?* |
| 終点 | 脳卒中 | すべての原因、CVD、IHDおよび癌による死亡率 | すべての原因、CVDおよび癌による死亡率 | がんとすべての原因による死亡率 | CVD |
| 結果 | 脳卒中のリスクは、上位四分位数と下位四分位数で42%低かった | VitCは、すべての原因、CVDおよびIHDによる死亡に反比例します。死亡のリスクは、上位5分位と下位5分位で約半分でした | 中位および上位のvitCグループでは、下位のvitCグループと比較して、すべての原因による死亡のリスクが25〜29%減少しました。 | 下位四分位数と上位四分位数の男性では、すべての原因による死亡のリスクが57%増加し、癌による死亡のリスクが62%高くなりました。 | CHDと脳卒中に独立して関連する血清ビタミンC; トップグループとボトムグループのリスクが27%低い |
略語は以下の通り。BMI(body mass index)CHD(chronic heart disease)心血管疾患(cardiovascular disease)IHD(ischemic heart disease)MI(myocardial infaction)SBP(systolic blood pressure)vitC(vitamin C)vitE(vitamin E) *追跡調査期間は特に明記されていない。
第2回国民健康・栄養調査(NHANES II)のデータをもとに、以下の3つの研究が行われた。Simonらは、血清アスコルビン酸と原因別死亡率との関係を調べた[85]。彼らは、ビタミンC濃度が低い人に比べて正常または高い人では、心血管疾患のリスクが減少する傾向にあり、全死亡のリスクが25%減少することを報告した。別のNHANES II研究では、血清ビタミンCの状態は、脳卒中および慢性心疾患のリスク低下と独立して関連していると結論づけている[86]。ビタミンC濃度と両疾患のリスクとの間には非線形の濃度反応関係が認められ、ビタミンCの欠乏が特に高い影響を及ぼすことが予想された。Loriaらは同じコホートを調査し、血清ビタミンC濃度の下位4分の1の人は上位4分の1の人に比べて、全死亡リスクが57%、がん死亡リスクが62%増加することを明らかにした[87]。Simonらは、ビタミンCの状態が高い男性ではがんのリスクが有意に低いと報告していたが、予想に反して、ビタミンCのレベルが高い女性ではリスクが高いことを発見した[85]。しかし、同じコホートを用いたLoriaらはこの差を認めなかった[87]。これらの研究ではすべて、非絶食の血液サンプルから血清中のビタミンCを比色法で評価している。
以上の研究は大規模なものであり、追跡期間もまちまちであった。これらの研究は、上述のFFQに基づいた研究よりも選択バイアスが少ないと思われる。興味深いことに、すべての研究で、ビタミンCの高濃度摂取と罹患率や死亡率の低下との間に有意な関係が認められた。したがって、健康な登録者に対する潜在的な選択バイアスがあれば、その効果は弱まったと考えられる。しかし、この5つの研究は、2つの異なる人口調査に基づいており、実質的には2つの異なる研究を表しているに過ぎない。いずれの研究も、分析方法が最適ではなく、サンプル数が非常に多いことや分析時期の問題もあるが、ビタミンCの過大評価または過小評価のリスクが高くなっている。また、相関関係に影響を与える可能性のある複数の微量栄養素の欠乏による交絡の可能性については考慮されていない。
5.3. ビタミンCを介入に用いた無作為化比較試験
5.3.1. Linxian試験
ビタミンCを介入に用いた主なRCTを表5にまとめた。Linxian研究は、抗酸化物質とミネラルの介入の効果を研究した最初の主要なRCTである[88]。中国のLinxianを舞台に選んだのは、食道がんの発生率が高く、住民の一般的な栄養状態が悪いことが理由であった。複雑な1/2(2×2×2×2)デザインで、9種類のビタミンとミネラルの複合効果を検証することを目的とし、参加者全員が4つのグループに分けられたサプリメントの7つの組み合わせのうちの1つ、またはプラセボを5.25年にわたって摂取した。ビタミンCサプリメント(120mg/日)には、モリブデン(30μg/日)を組み合わせました。ビタミンCとモリブデンの死亡率とがん発生率に対する効果は観察されなかった[88]。サプリメントに割り当てられた49人とプラセボに割り当てられた49人において、試験開始の10カ月前にベースラインのビタミンCレベルが評価され、どちらも重度のビタミンC欠乏を示したが、介入群の参加者はプラセボよりも有意に低かった(p<0.03)。介入試験では、介入群とプラセボ群のそれぞれ730〜740人から血液サンプルを採取した。期待通り、ビタミンCの状態は介入群で46μmol/Lとプラセボよりも有意に改善したが(p<0.001)驚くべきことに、プラセボ群のビタミンCの状態もベースラインから30.7μmol/Lと非常に有意に増加しており(p<0.001)この時点では両群とも最適ではない範囲にあり[2]、試験開始時から明らかに増加していることがわかった。プラセボ群が同時にサプリメントを摂取することを許可されていたかどうかは報告されていないが、彼らのサブオプティマルな状態を考慮すると、サプリメントの使用が広く行われていたとは考えにくいであろう。Linxian研究は、ビタミンC欠乏症の被験者を対象としたとされる唯一の主要なRCTであり、興味深いものである。しかし、プラセボ群でビタミンCの状態が有意に上昇したことは、重大な懸念をもたらす。これは、試験開始時に分析された非常に少数のサンプルにおいて、偶然、分析方法の不備、不適切なサンプルの取り扱いなどにより、ベースラインレベルが著しく過小評価されたことを示唆しているか、あるいは、プラセボ群が介入中に食事を変えたり、同時にサプリメントを摂取するなどして、食事を改善したことを示唆している。理由の如何にかかわらず、プラセボ群の変化は、ビタミンCによる介入の効果を評価する研究の能力を著しく制限する。もう一つの大きな懸念は、サプリメントに含まれるビタミンCの量である。この研究の時点では、ビタミンCのRDAは60mg/日であったが、このサプリメントにはその2倍の120mg/日が含まれてた。このような限られた量のビタミンCは、介入群のビタミンC状態を正常化するには明らかに不十分であり、重度のビタミンC欠乏状態が生涯続くと想定される影響と比較して、わずか5年の期間で罹患率や死亡率に変化が生じると期待できるかどうかは、非常に疑問であると考えられる。また、この試験の25年後の追跡調査では、5.25年の補給期間の効果がないことが予想された[89]。
5.3.2. The British Heart Protection Study(英国心臓保護研究)
British Heart Protection Studyでは、冠動脈疾患、その他の閉塞性動脈疾患、または糖尿病を有する高リスク集団の男女を対象に、ビタミンE 600mg、ビタミンC 250mg、β-カロテン20mgを含むマルチビタミンサプリメントとプラセボを5年間比較し、シンバスタチンも含めた2×2デザインで効果を検討した[75]。抗酸化物質による介入では、血管疾患、がん、その他の主要なアウトカムによる5年間の死亡率または発生率の有意な低下は観察されなかった。ビタミンCの状態は試験開始時には測定されなかったが、参加者の約5%に実施された追跡調査時の非絶食血液サンプルによるビタミンCの状態の評価から判断すると、参加者は補充前にはビタミンCが不足していなかった。しかし、介入により、ビタミンCの状態はプラセボに比べて15.7μmol/L増加し、58.9μmol/L対43.2μmol/Lという有意な結果が得られた。ビタミンCの測定方法やサンプルの取り扱いについては報告されていない。高用量ビタミンEを除くすべての被験者は、試験期間中に以前から使用していたサプリメントを継続して使用することができた。非絶食の血液サンプルを使用したことから、研究対象者のビタミンCの状態はやや過大評価されていると思われる。にもかかわらず、使用されたビタミンCサプリメントは、介入に割り当てられた人々を飽和させるには明らかに不十分であり、その結果、集団が一部重複していることに注目すべきである。繰り返しになるが、介入の期間が比較的短く、規模も小さいことから、このような条件下で研究効果を期待することが妥当かどうかを判断するためには、研究対象者のハイリスク状態、および既知または説明されていない生涯の食事およびサプリメントの履歴と比較する必要がある。入手可能な情報に基づくと、これは非常に疑わしいと思われる。
5.3.3. The Physician’s Health Study II
Physician’s Health Study II RCTでは、50歳以上の男性医師14641人を対象に、2×2デザインで、ビタミンC(500mg/日)とビタミンE(400IUを1日おきに摂取)の8年間の補給とプラセボの心血管疾患リスクへの効果が調査された[76]。ビタミンCの補給は,この期間における主要な心血管イベントのリスクを減少させなかった。試験参加者のビタミンCの状態は、エントリー時、介入中、介入後のいずれも評価されなかった。500mg/日のビタミンC補給が個人のビタミンC状態に及ぼす潜在的な効果は、エントリーレベルや食習慣によって非常に有意なものから無視できるものまで様々であるため、このことはデータを再検討して結論を出す可能性を大きく制限している。また、グループ間の潜在的なバイアスも排除できない。さらに、試験参加者は、試験期間中、RDAを上限とするサプリメントの同時摂取を認められた。サプリメントの同時摂取は、年間で1か月以上使用した場合のみ報告された。これらの数値は、プラセボではわずか4.4%であった。
5.3.4. SU.VI.MAX試験
SU.VI.MAX試験は、他の試験よりも若干若い(35歳以上)フランス人男女を対象に実施された [90]。この研究では,一般集団におけるがんおよび虚血性心疾患の発生率を減少させるために,ビタミンC(120 mg),ビタミンE(30 mg),β-カロテン(6 mg),セレン(100 μg)および亜鉛(20 mg)の栄養量を含む1日1回のマルチビタミン・ミネラルサプリメントとプラセボを7.5年間にわたり並行して投与し,その効果を検証した。この研究では、主要アウトカムに対する有意な効果は認められなかったが、サブ解析では、男性のがん罹患率(p<0.008)および全死亡率(p<0.02)に対するサプリメントの有意な正の効果が認められた[90]。著者らはこのジェンダー効果について、男性のビタミンCの状態が一般的に低いことに起因するとしている。介入時のビタミンCの状態は、「選択されていないサブサンプル」の空腹時の血液サンプルで評価され、介入時に参加者は完全には飽和していないものの、十分なビタミンCを摂取していたことが示された。介入により、プラセボと比較して、血漿中のビタミンCの状態はわずかながらも有意に増加し、プラセボ群は同時にサプリメントを摂取することはできなかった。本研究は、先に述べたいくつかの落とし穴を考慮して慎重にデザインされているが、ビタミンCの補給がヒトの疾病リスクに及ぼす可能性を検討するという点では、いくつかの欠点がある。すなわち、ビタミンCの状態が比較的高い栄養状態の人と低用量のサプリメントとの間に重大な選択バイアスがあるため、サプリメントの効果を確認できる可能性は限られている。サプリメントで提供される1日あたり120mgのビタミンCは、おそらく研究参加者の一般的な食事から摂取される量に近いか、それ以下であると考えられる。さらに、ビタミンCは単一のサプリメントとして提供されていないため、男性に観察されたポジティブな効果は、ビタミンCの補給に直接起因するものではない。これらの制限にもかかわらず、SU.VI.MAX研究は、十分なビタミンCを摂取している栄養状態の良い人では、低用量のサプリメントの効果があったとしても限定的であることを十分に示している。しかし、この研究をビタミンC欠乏症の人々に500~1000mg/日のビタミンCサプリメントを用いて実施していたら、非常に興味深いものになっていただろう。
5.3.5. The Women’s Antioxidant Cardiovascular Study(女性の抗酸化心血管研究
ビタミンCを用いた最後の主要な介入研究であるWomen’s Antioxidant Cardiovascular Studyは、心血管疾患のリスクが高い40歳以上の女性医療従事者8171人を対象に、アスコルビン酸(500mg/日)ビタミンE(600IU/日)βカロチン(50mg/日)を2×2×2の要因計画で9.4年間投与し、心筋梗塞、脳卒中、冠動脈血行再建術、心血管疾患死亡の複合転帰に対する効果を調査した[74]。この研究では、心血管イベントに対するビタミンC、ビタミンE、ベータカロチンの全体的な効果は認められなかった。研究集団のビタミンCの状態は、エントリー時に記録されなかった。研究の約半分が終了した時点で「30人の地元の参加者」で評価されたことから判断すると[74]、プラセボ群を含む研究集団は、研究期間中、ビタミンCが飽和状態にあった。論文では報告されていないが、高いビタミンCの状態(特に介入群)から、空腹時の血液サンプルは明らかに得られなかったと思われる。また、試験対象者にはRDAを上限としたサプリメントの同時使用が認められており、プラセボ群の27.5%が試験中にサプリメントの摂取を報告していた。今回の研究では、ビタミンCがサプリメントとして提供されているにもかかわらず、不適切な対象・除外基準が用いられているため、すでに飽和状態にある高リスク者にビタミンCを追加で補給しても、心血管疾患からのさらなる保護は期待できないという結論になった。
以上の研究を総合すると、重大な欠陥があり、特にビタミンCの状態が悪い集団におけるビタミンC補給の潜在的な有益性について、適切な結論を導き出すことができない。1つの研究を除くすべての研究で、プラセボ群は同時にサプリメントを摂取することができ、5つのうち3つの研究では、マルチビタミンカクテルと低用量ビタミンCの併用効果のみが検討されている。プラセボ群の参加者は、ビタミンCを測定した場合、ほとんどが適切なレベルから飽和レベルを示し、栄養状態の悪い集団を対象としたとされるLinxian研究では、研究期間中にプラセボ群のビタミンCレベルが約3倍に上昇した(表5)。
6. おわりに
以上のように、ビタミンCと健康、疾病、死亡率との関係を調べた臨床研究、あるいはサプリメントの効果を調べた臨床研究には、多くの限界があり、人間の健康におけるビタミンCの重要性について結論を出すことができない。疫学研究では、ベースラインでのビタミンCの状態の評価は、個人のライフスタイルを表しており、生涯にわたる暴露の指標となるかもしれないが、食生活の変化が考慮されていないため、これは確実ではない。介入研究では、介入群はライフスタイルの変化を意味し、その影響を介入前の生涯にわたる曝露の影響と比較する必要がある。このような観点からすると、介入期間や投与量は、特にビタミンCが不足していない集団を対象とした場合に、サプリメントの有益性をしっかりと確認するには全く不十分であると考えられる。このように、ビタミンCに関する臨床文献を再検討しても、ほとんど確実性はなく、冒頭で紹介したような多くの疑問が残る。ビタミンCの最適な摂取量はどのくらいなのか、ビタミンCの予防・治療効果はどのくらいなのか。
まとめてみると、ビタミンCの状態が悪いことと、病気や早死にのリスクが高まることとの間には、比較的持続的な関連性があるように思われる。しかし、ビタミンC欠乏による罹患率や死亡率の増加が、ビタミンCそのものの欠乏によるものなのか、複数の共欠乏によるものなのか、あるいはビタミンC以外の物質の欠乏によるものなのかは不明である。介入研究では、すでに飽和状態にある人にビタミンCを補給しても、罹患率や死亡率にはほとんど、あるいは全く影響がないことが示されている。しかし、ビタミンCの状態が悪い人にビタミンCを補給することで、病気の発症や進行を防ぐことができるかどうかは、まだ不明である。この複雑な問題に新たな情報を加えるためには、SVCTに遺伝的に好ましくないSNPsを持つ人を募集することが考えられる。これらの人々は、豊富な共犯者を伴わずに、生涯にわたってビタミンCの状態が悪いと考えられる。その結果、ビタミンC欠乏症に起因する疾患のリスクを調査することが可能となる。しかし、ビタミンCのホメオスタシスを低下させるSNPの負の効果をサプリメントで打ち消すことはおそらく不可能であるため、これらの人々は特に介入研究には適していない。この種の研究の主な課題は、これらのSNPの頻度が非常に低いため、膨大な人口にもかかわらず検出力が比較的低いことである。このように、病気の発症や進行におけるビタミンCの欠乏の役割や、栄養状態の悪い人へのサプリメントの効果を調べるためには、十分にデザインされた研究が必要であると考えられる。
最後に、ビタミンCの作用を示す生物学的シグネチャー、すなわち、ある状態を特異的かつ確実に反映するバイオマーカーやバイオマーカーの組み合わせは、生理学的に十分なビタミンCの状態と不十分なビタミンCの状態の評価や、ビタミンCの状態と特定の疾患との間の潜在的な濃度反応関係を改善するために、切実に必要とされている。これまでのところ、ビタミンCの状態と、生体内でビタミンCが還元等価物を提供する個々の生理的プロセスの機能との関係については、非常に限られた知見しか得られていない。動物実験では、組織や器官の「階層」が存在し、限られた資源しか利用できない場合に、体のどの部分にビタミンCを供給するかを決定することが知られている[26,27,31,[91], [92], [93]]。これらの結果から、例えば、ビタミンCの供給が不十分な時期には、脳が明らかに優先されることがわかる。重要なことは、このような優先順位付けが、ビタミンC欠乏症や最適でないビタミンCの状態の臨床効果に重大な影響を与える可能性があるということである。このように、壊血病を予防するために必要なビタミンCの量は非常に限られており、基礎となる生理学的メカニズムにおいて濃度と反応の関係が非常に良好であることを示唆している。しかし、心血管機能、免疫系、神経系などの健康維持に必要なビタミンC依存性プロセスの間で、どのような優先順位が考えられるかはまだ不明である。このような疾患特異的な濃度-効果関係を解明するには、非常に堅牢な生物学的シグネチャが必要であるが、まだ利用できない。