Nicotinamide Riboside
関連記事
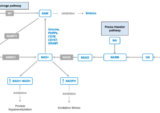
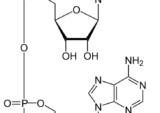
概要
ニコチンアミド・リボシドはニコチンアミドの前駆体
※ニコチンアミドリボシド(ニコチンアミド・リボシド)はニコチンアミド(NAM)に、リボース、ピロリン酸、リボース、アデニンが結合した、ピリジンヌクレオチド
研究
細胞外からのニコチンアミドリボシドの適用は、細胞内NADレベルを増加させる。ニコチンアミドリボシドはPGC-1α発現の活性を介してBACE1を分解促進し、UPSに影響を与えAPPプロセシングに影響を与える。(アミロイドβ形成を抑制し毒性が低下する)
www.ncbi.nlm.nih.gov/pmc/articles/PMC3632303/
ニコチンアミドリボシドは、脳エネルギー代謝を改善、タンパク質、オルガネラの制御、シナプス可塑性と関わる複数の代謝経路を促進することで、ADマウスのタウ変異による有害作用を改善する。アミロイドβ、タウ病理の減少、ミトコンドリアの質の維持、オートファジーの改善と関連。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3596471/
- ニコチンアミドリボシドの投与は、NAD+レベルを効率的に増加
- ニコチンアミドリボシドはSIRT1、SIRT3活性を増大
- ニコチンアミドリボシドは、コレステロールを低下させ高脂肪食の有害作用を防ぐ。
- ニコチンアミドリボシドはミトコンドリア機能と耐久性を向上させる。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3616313/
NAD+補給は、DNA修復欠損症を導入した新しいADマウスモデルにおける主要なアルツハイマー病の特徴とDNA損傷反応を正常化する
www.ncbi.nlm.nih.gov/pmc/articles/PMC5828618/
アルツハイマー病(AD)は最も一般的な認知症であり、治療法はない。アルツハイマー病患者の脳ではDNA修復活性が欠乏しており、特にDNAポリメラーゼβ(Polβ)はDNA塩基切除の鍵となるタンパク質である。
NAD+は、ミトコンドリアの健康と生体形成、幹細胞の自己再生、神経細胞のストレス耐性に重要な細胞内代謝産物である。
今回の研究では、DNA修復欠損が導入された新しいADマウスモデル(3xTgAD/Polβ+/-)でNAD+レベルが低下し、ニコチンアミドリボシドによるNAD+補給は、神経炎症、シナプス伝達、リン酸化タウ、DNA損傷を有意に正常化するとともに、学習や記憶、運動機能も改善したことが示された。このことは、ヒトのADへの介入を示唆している。
機能不全のミトコンドリアは、ADを含む多くの神経変性疾患の特徴であり、その一因はNAD+の枯渇である可能性があり、これはヒトを含むいくつかの生物の老化(主要なADの危険因子)とともに観察される(6)。
NAD+は細胞内代謝物であり、ミトコンドリアの健康と生体形成、幹細胞の自己再生、神経ストレス耐性に重要な役割を果たしている(参考文献7)。この代謝物は、DNA修復タンパク質PARP1、サーチュインファミリーの脱アセチラーゼ、環状ADPリボースヒドロラーゼCD38とCD157の活性に不可欠な補酵素として機能する(8, 9)。
NAD+を消費する酵素は、限られたNAD+のプールをめぐって競い合うため、NAD+のバイオアベイラビリティが低下すると、細胞内での互いの活性を制限することがある(10)。ニューロンは比較的高いエネルギー需要を持っているので、彼らはNAD+の枯渇とATP生産の障害に非常に敏感である(6、11)。
さらに、NAD+は、ミトコンドリアの生合成とマイトファジーの間のバランスの維持を通じて、ニューロンの健康と生存に影響を与える(11、12)。
ニコチンアミドリボシド、ニコチンアミドモノヌクレオチド(NMN)、ニコチンアミド(NAM)などのNAD+前駆体の補給は、神経変性疾患の加齢に伴う病理学的表現型を改善し(13-16)、DNA修復酵素の変異に起因する早老化モデルのマウスにおける病理学的表現型を減衰させる(11, 12, 17)。
また、線虫やマウスでもNAD+補給後の健康改善や寿命延長が観察されている(12, 18)。しかし、ADにおけるNAD+の役割はまだ明らかにされていない。
- 成人の3xTgAD/Polβ+/-マウスおよび3xTgADマウスにおいて、3ヶ月間の慢性的なニコチンアミド・リボシド曝露により、認知障害が大部分回復することが示された。
- ニコチンアミド・リボシドは3xTgAD/Polβ+/-マウスの神経細胞において長期増強(LTP)を特異的に増強するが、3xTgADマウスの神経細胞にはあまり効果がなかった。また、ニコチンアミド・リボシドは神経新生を刺激し、神経炎症や酸化的DNA損傷を減少させることが示唆された。
- AD/Polβマウスでは、歩行速度の低下と歩幅のばらつきの増加傾向が見られたが、ニコチンアミド・リボシド投与後には両パラメータともほぼWTレベルに回復した(図S1 J、K)。
- ニコチンアミド・リボシドはロータロッド、握力、歩行機能試験のパフォーマンスを向上させ、ADマウスとAD/Polβマウスの不安様行動を減少させたが、うつ病様行動は減少させなかった。
- ニコチンアミド・リボシドはAD/Polβマウスにおける海馬シナプス可塑性を回復する。
- ニコチンアミド・リボシドは長期増強を改善する。
- 海馬では、ニコチンアミド・リボシド後のADマウスの免疫経路の変化の方向は、Polβマウスとより類似していたが、AD/Polβマウスでは明らかに異なる反応を示した(図2A)。これらの結果は、ニコチンアミド・リボシドが海馬と大脳皮質の両方で炎症過程を強力に抑制する可能性を示唆している。
- 海馬では、非免疫系のうち、神経伝達物質経路とシナプス機能に関連する経路は、AD/Polβマウスでは特異的に増加していた(図2B)。
- 神経伝達物質経路もまた、ニコチンアミド・リボシド処理後のAD/Polβマウスで有意にアップレギュレートされた。
- 大脳皮質では、海馬で見られたよりも遺伝子型間で統一された応答が得られた(図S3B)。
- P53シグナル伝達は、大脳皮質の全遺伝子型において、ニコチンアミド・リボシド後に普遍的にダウンレギュレートされた。
- インスリンやリボソーム関連のシグナル伝達経路は、ADモデルマウスやPolβマウスでは、WTとは対照的に、ニコチンアミド・リボシド処理後に一様にアップレギュレーションされていた(図S3B)。
- 我々は、ニコチンアミド・リボシド処理したADマウスのスライスでは、対照のADマウスに比べてLTPの大きさが有意に大きいことを示した(図2D)。驚くべきことに、AD/PolβマウスのスライスではLTPは本質的に存在しなかったのに対し、ニコチンアミド・リボシド処理したAD/PolβマウスではLTPは劇的に正常値に回復しており(図2E)、ニコチンアミド・リボシドがシナプス機能を改善することを示している。
- ニコチンアミド・リボシドは神経新生を増加させ、神経炎症を減少させる。成人海馬の神経新生は、歯状回(DG)依存型の学習や記憶において重要な役割を果たしており、ADではその機能が低下していることが報告されている(47)。
- ニコチンアミド・リボシドはNPCsにおける試験管内試験(in vitro)でのEdUの取り込みを増加させ、神経炎症を減少させる。
- AD/Polβマウスにおける脳および全身の炎症をニコチンアミド・リボシド処理が抑制することが示された。
- T細胞およびB細胞(それぞれCD4+、CD8+およびCD19+)、マクロファージ(CD11b+)および樹状細胞(CD11c+)が同定された。
- ニコチンアミド・リボシドは、ADおよびAD/Polβマウスにおけるタウリン酸化を減少させるが、アミロイドβ蓄積を減少させない。
- ニコチンアミド・リボシドはAD/Polβマウスのタウリン酸化を減少させ、ヒトAD線維芽細胞の酸化損傷を減少させる。
- ニコチンアミド・リボシドはヒトAD線維芽細胞におけるミトコンドリアストレスを正常化する。
- 複数の老化、DNA修復、および代謝経路は、NAD+代謝とミトコンドリア機能に収束する(51)。
- ニコチンアミド・リボシドの治療は、SIRT3とSIRT6を介してDNA損傷とアポトーシスを減少させる。

