Neuroprotective immunity by essential nutrient “Choline” for the prevention of SARS CoV2 infections: An in silico study by molecular dynamics approach
www.ncbi.nlm.nih.gov/pmc/articles/PMC7532804/
要旨
出生前のCOVID感染は、COVID-19疾患の中で最も影響を受け、最も研究率の低い側面の一つである。他のコロナウイルスと同様に、CoV2感染は、胎児と胎盤上の母体の炎症反応によって胎児の発育に影響を与えると予想されている。研究では、母親の体内のより高い出生前のコリンレベルは、CoV2感染症の悪影響から胎児の発育中の脳を保護することができることを示した。コリンは一般的にサプリメントとして使用されている。私たちは、バーチャルスクリーニング、分子ドッキング、分子動力学法により、コリンがSARS 3CLproプロテアーゼを強力に阻害する可能性を確立し、出生前COVID-19治療の手がかりとなる可能性を示した。
1. はじめに
コロナウイルスの一種であるSARS-CoV2によって引き起こされたCOVID-19病に端を発したパンデミックの状況が全世界に広がっている。コロナウイルスはここ数十年でよく知られるようになったが、これらのウイルスは特定のエンベロープされたRNAを持っており、これが風邪から重症度の異なる致命的な肺炎まで、様々な呼吸器疾患の原因となることがすでに理解されている[1]。コロナウイルスは、1930年代に家禽から初めて発見され、その後、動物の呼吸器疾患、肝臓疾患、消化器疾患、神経疾患の原因として認識されるようになった[2]。コロナウイルスは7種類が知られているが、そのうち4種類は健康な人には感冒の症状を伴う軽症でしか発症しないとされている。乳幼児や免疫不全患者、高齢者の重篤な下気道感染症や肺炎 [3], [4] は、ごくまれにこれらのウイルスが原因となることがある。残りの3つのカテゴリー SARS-CoV(2003年に同定)[5]、MERS-CoV(2012年に同定)[6]、およびSARS-CoV2(2019年に同定)[7]は、時にヒトにとって致命的になることもある重篤な呼吸器感染症を引き起こす可能性がある。SARS-CoV2の壊滅的で致命的なアウトブレイクは 2019年12月に中国の武漢ですでに観察されている[7], [8]。このウイルスは、出現後数週間で世界的に拡散し、それに起因する呼吸器疾患(急性および重症の両方)の症状を示すことで、世界的な存在感を明らかにすることが観察されている[9]。このウイルスは、通常の呼吸器疾患に加えて、急性呼吸窮迫症候群(ARDS)や死に至る可能性があることが明らかになっていた。COVID-19による死亡および重篤な症状のリスクは、高齢者および肥満、糖尿病、および心臓、肺、腎臓または肝臓疾患を含む他の重篤な医学的問題を有する患者において増加することが観察されている[10]。上記の重症化の転帰は、機械的換気を必要とする呼吸不全、ショック、多臓器不全、および死へと進行し得る[11]、[12]、[13]、[14]。CoV2sは自然界に存在する人獣共通感染性病原体であり、通常は動物が先に出現する。SARS-CoVとコウモリSARS-CoV(SARSr-COV-RaTG13)の完全ゲノム配列認識率が79%と96%の類似性から、コウモリがCoVウイルスの宿主である可能性が示唆されている[15]。同様に、CoV2についても、原宿主、中間宿主、最終宿主が存在する可能性があり、感染した動物からヒトに感染する可能性がある。SARS-CoV2の場合、人から人への感染は、主に呼吸器の飛沫、表面汚染、エアロゾル感染などの感染分泌物を介して容易に起こる可能性がある。これまでに得られた研究結果から、このウイルスは症状のある患者、無症候性の患者、無症候性の患者、および無症候性の患者によって容易に感染するという結論に至っている[16], [17], [18]。最新の報告によると、COVID-19の患者は主に支持療法のみで治療されている[19]。FDAが承認した約200種類の医薬品やワクチンが臨床試験を経て登録されている。いくつかの治験薬のような抗ウイルス薬がある。レムデシビル、ファビピラビル、ヒドロクロロキン、クロロキンなどの治験薬が重篤な症状の患者に使用されている[20], [21]。しかし、これらの薬剤に関連した毒性は、すでにいくつかの重大な致命的な健康問題を生み出している[20]。あるいは、回復期血漿を含む免疫調節療法も使用されているが、現在のところ、COVID-19と戦うための特定の薬剤やワクチンはまだ発見されていないか、あるいはまだ開発中である。この開発の一環として、COVID-19治療の代替としての食事療法、硬性免疫、漢方薬の使用を促進する目的で、インフルエンザ、HIV、他のコロナウイルスなどの様々なウイルスに対する抗ウイルス、免疫調節活性を特異的に有する栄養補助食品や漢方薬が検討されている[22], [23], [24]。一連の研究成果は、栄養食品やハーブがSARS-CoV2に対する潜在的な抗ウイルス能力、ハード免疫力を持っていることをすでに示唆している[23], [24]。
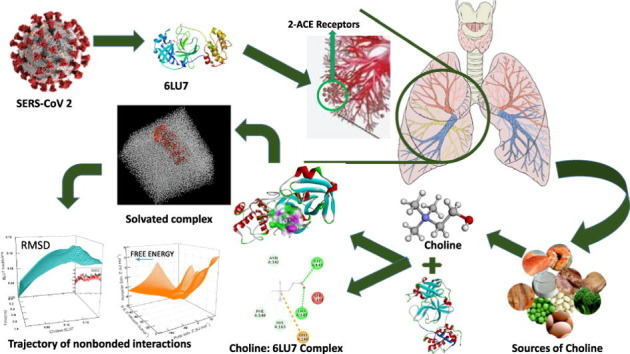
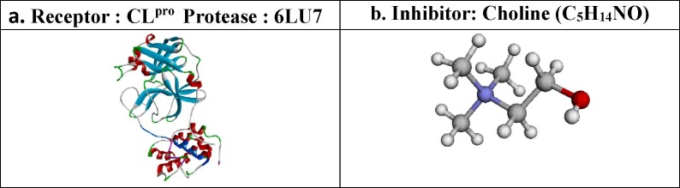
異なるウイルスによる以前のパンデミックは、統合失調症、自閉症スペクトラム障害、注意欠陥障害[25]、[26]のような精神疾患を持つ乳児の数が大幅に増加することにつながった胎児の発達への影響を示している。疾病管理予防センター(CDC)」の報告によると、出生前のCOVID-19感染は、胎児や胎盤に対する母体の炎症反応の影響により、胎児の脳の発達にも影響を及ぼす可能性があるとされている[10], [26], [27]。COVID-19のこの影響に関する裏付けとなるデータは、近い将来に入手可能になると予想される。CDCから報告されているデータは、Infant Behaviour Questionnaire Revised (IBQ-R)規則に基づいており、[27], [28]では、COVID-19に感染した母親の子供は、妊娠16週の間に消化性コリンレベルが高い(7.5μM以上)ことによって、生後3ヶ月以降はウイルス感染の症状は見られないことを示唆している。いくつかの特定の食事や食品サプリメントは、人体へのコリンの供給源となっている。医学的報告では、妊娠中の母親の高いコリンレベルは、母親が脳が形成されている彼らの妊娠段階でCOVID-19感染を得たが、間違いなく乳児の行動発達をサポートする可能性があるCOVID-19から胎児の脳の発達を保護する可能性があることを示唆した[26]、[27]、[28]、[29]。これらの知見から、特定の栄養補助食品の研究に取り組む意欲が湧いてきた。コリン(C5H14NO)は、妊娠中に特に胎児の脳の発達を保護するために使用されることになっている[27]。リガンドとしてのコリンと受容体としてのCoV2の3CLproメインスパイクプロテアーゼのバーチャルスクリーニング、分子ドッキング、分子動力学を用いたin silico研究により、COVID-19による胎児脳への有害な影響から母胎内の胎児の脳を保護するために、コリンを含むサプリメントによって出生前のCOVID-19感染症が無効化されることを確立することができた(図1 a,b)。
図1 (a)受容体タンパク質(6LU7)の構造。(b). コリンの構造
2. 材料と方法
2.1. 潜在的な阻害剤コリン
コリンは、いくつかの栄養補助食品/食品に含まれており、ビタミンBファミリーに属する。コリンは、乾燥ナッツ、全粒粉、種子を含む豆類やアブラナ科の野菜など、多くの植物性製品に自然に含まれている[30]。また、鶏肉、乳製品、肉、卵、魚などの動物性製品にも含まれている。コリンは、チノスポラ・コルディフォリア、ウィタニア・ソムニフェラなどのハーブ植物から抽出された植物成分の一つである[23]。コリンはヒトの肝臓でホスファチジルコリンとして内因性に産生される。しかし、内因性に生産されるコリンの量は、私たちのニーズを満たすのに十分ではない[31]。コリンは、ヒトの遺伝子形成、様々な代謝過程、脂質輸送に非常に重要な役割を果たしている。コリン:尿素(1:2)共晶混合物は、異なる核酸のための深層共晶溶媒(DES)として知られている反応媒体として使用されている[32]。その水を含まない貯蔵容量のために混合物は、異なる生物触媒反応のための反応媒体として、また、高温で長期貯蔵媒体として使用することができる[33]。それは変性からタンパク質の構造を保護するためのナノクラウダーとして機能することができる[34]。また、細胞膜が全身の細胞膜をつなぎ、通信するのを助けます。コリンで構成されたDESは、グリーン化学プロセスを得るために、さまざまな酵素反応に使用することができる[35]。コリンは、子供の胎児の発達が出生初期の段階で依存している母乳の重要なコンポーネントである。医学的研究では、コリンサプリメントの適切な摂取は、母親がダウン症候群、アルツハイマー病[36]のような神経変性疾患から乳児を保護することができることを明らかにした。コリンは、自律神経、認知、運動機能の多くを制御する神経伝達物質である Ach (アセチルコリン) の直接の前駆体です [36]。医学的研究によると、妊娠中に母親がコリンを摂取すると、新生児は十分にCoV2感染症のリスクを軽減することができるようになる[26]。また、出生前のコリン補給は、COVID-19 [26], [27], [28], [37]を含む、欠損障害や統合失調症などの様々なウイルス性呼吸器感染症の影響を減少させることで、胎児の脳の発達を可能にすることが報告されている。他のコロナウイルスと同様に、COVID-19は子供の呼吸器を破壊し、母体の免疫反応を誘発することで脳の発達を阻害する可能性がある。妊娠16ヶ月でフリーマンらより高い母親のコリンレベルが年齢[26]、[27]、[28]の3ヶ月で子供の行動に炎症の影響を減少させることができるように。乳児の発達にCOVID-19感染におけるコリンの効果はまだ不明であるが、まだすべての利用可能な医学的データは、コリンサプリメントは、母親がCoV2感染症[40]、[41]によって影響を受けるが、乳児が健康的な方法で生き残ることができるように、乳児の初期の胎児の脳の発達を保護するために高い出生前コリンレベルを維持するのに役立つかもしれないという事実を検証している。しかし、この仮説を正当化する研究はこれまであまり行われなかった。コリンとSARSのCoV2感染症との関連を探り、コリンが受容体タンパク質CoV2メインプロテアーゼに対する阻害剤として作用するかどうか、また、コリンサプリメントがCOVID-19病患者の利益になるように、薬剤として使用される可能性があるかどうかを決定するためには、まだ厳密な調査が必要である。受容体酵素に対する特定の阻害剤の安定性と活性を理解するためには、異なる実験条件での安定性と活性を理解することが、創薬設計を成功させるためのボトルネックとなることが知られている。コリンのDES混合物としてのカウンターアクション効果は、水溶液中のタンパク質や酵素のネイティブな構造安定性と活性を維持するための効果がすでに証明されている[42], [43]。本研究では、Drugbank(https://www.drugbank.ca/drugs)からコリンの構造をPDB形式でした(図1b)。また、薬物類似性、薬物動態、親油性を評価することにより、適切なバーチャルスクリーニングを行った。主に業界で適用されている薬物類似性のルールには以下のものがある。”Lipinskiの規則」、「MDDRに似た規則」、「Veberの規則」、「Ghoseフィルター」、「Eganの規則」、「Mueggeの規則」など [44], [45], [46], [47]。SWISS-ADMEソフトウェア(https://www.swissadme.ch)は、様々な仮想スクリーニング方法を適用するのに役立っている。分子ドッキング研究のために、リガンドコリンはAuto Dock Tools 1.5.6でpdbqt形式で保存されている[48]。
表 1 生化学的性質、薬物類似性、薬物動態と親油性の性質、コリンの薬効化学
| Properties of Choline (C5H14NO)
|
|||||||||
|---|---|---|---|---|---|---|---|---|---|
| Physicochemical Properties | choline | Lipophilicity | choline | Druglikeness | choline | Pharmacokinetics | choline | Medicinal Chemistry | choline |
| Molecular weight (gm/mol) | 104.1708 | Log Po/w (iLOGP) | −2.41 | Lipinski | yes | GI absorption | Yes | PAINS | 0 alert |
| Num.H-bond acceptors | 1 | Log Po/w (XLOGP3) | −0.40 | Veber | yes | BBB permeant | No | Brenk | 1 alert |
| Num. H-bond donors | 1 | Log Po/w (WLOGP) | −0.32 | Ghose | Partly yes (2 violation) | P-gp substrate | No | Leadlikeness | Partially yes (1 violation) |
| No of rotatable bonds | 2 | Log Po/w (MLOGP) | −3.46 | Egan | yes | Log Kp (skin permeation) | −7.22 cm/s | Mutagenicity | No |
| Molar Refractivity | 29.69 | Log Po/w (SILICOS-IT) | −0.57 | Bioavailability score | 137.87 | Water Solubility | −1.26 | Liver and cardio cytotoxicity | No |
| Topological polar surface area TPSA (Å2) | 20.23 Å2 | Concensus Log Po/w | −1.38 | Synthetic accessibility (SA) | 1.00 | Log S (SILICOS-IT) | |||
2.2. SARS-CoV2の潜在的な標的タンパク質構造
コロナウイルスは多くの構造タンパク質と非構造タンパク質をコードしている。これらのポリプロテインの中には、SARS-CoV酵素の鍵を握るプロテアーゼ3CLproによって切断され、成熟した非構造タンパク質に変換されるものもある[49]。CoVの3CLproは、そのスパイク(S)糖タンパク質によって、機能の複製と転写プロセスを制御する役割を担っている[50]。Sは宿主細胞に入り、ウイルス表面からホモ三量体を形成する。侵入した後、ACE2(アンジオテンシン変換酵素2)受容体と強く相互作用し、いくつかの周期的な過程を経て自己複製を行う [51]。3CLproプロテアーゼを標的とすることは、抗COVID薬の設計に有効なアプローチとなる可能性がある。3CLpro様プロテアーゼの一つの立体構造がX線結晶構造解析データ(PDBID: 6LU7)により報告されている[52](図1a)。本研究では、COVID-19に対するコリンの有効性を見出すために、この天然の3CLpro様プロテアーゼ蛋白質基質の阻害性と結合可能性を確認した。6LU7の構造は、”Protein Data Bank” (www.rcsb.org/)からし、Auto DockVinaソフトウェア[53]のAuto DockとMG Toolsを使用してシミュレーションを行った。内蔵リガンドは、Discovery studio 2020 (Dassault Systèmes BIOVIA) [54]を使用して6LU7から除去し、出力構造をクリーンアップしてPDB形式で保存した。
2.3. 方法:分子ドッキング、分子動力学、結合エネルギー
分子ドッキングは、エネルギーの最小化と結合エネルギーの計算を行い、薬物と標的の相互作用の可能性を予測するために使用される最も応用されているシミュレーションメカニズムの一つである。これにより、リガンドの宿主タンパク質に対する最適な配向や位置を特定することができる。ドッキングアルゴリズムは、いくつかのスコアリング関数の助けを借りて、エネルギーを最小化した状態での適切なリガンドのコンフォメーションを特定するために使用される[55]。分子ドッキングは、リガンド/薬物が受容体タンパク質/DNAとドッキングしているかどうかを予測し、低い結合エネルギーに依存するドッキング化合物のランキングの形で結果を表示することができる。AutoDock Vinaのアルゴリズムは、いくつかの最適な構成パラメータ(結合モード-9,網羅性-8,エネルギー差-3 kcal/mol、標的タンパク質の残基位置の座標x、y、およびzを持つGridbox中心)を使用して、CoV-2のプロテアーゼへの提案された阻害剤のドッキングベースの研究を行うために使用されている[53]。ターゲットタンパク質は Auto Dock Tools [53] で pdbqt 形式で保存され、ドッキングに使用できる状態になっている。シミュレーションの結果、最大の非結合相互作用、最小の結合親和性を持つ双極子モーメント(kcal/mol)乾燥エネルギー、阻害定数を示すポーズを、最適なリガンド:タンパク質複合体構造として選択した。最良のリガンド:タンパク質のポーズを選択するもう一つの基準は、それらの間の結合の種類と数を特定することである。受容体タンパク質との間に最大数の H-結合、静電結合を形成している代謝物ほど、リガンド:タンパク質複合体を形成する能力が高いことがわかった。
MDシミュレーションの結果は、タンパク質とリガンドの相互作用の構造ダイナミクスを調べるのに役立ちました。LINUXベースのプラットフォーム”GROMACS 5. 1 Package” [56]とCHARMM36全原子[57]とGROMOS43A2力場[58]を用いて、提案されたリガンド:タンパク質複合体のポテンシャルエネルギー(Epot)、温度(T)、密度進行(D)、回旋半径(Rg)、背骨の二乗平均偏差(RMSD)、タンパク質Cα背骨の二乗平均揺らぎ(RMSF)、溶媒アクセス可能表面積(SASA)、水素結合、相互作用エネルギーなどの様々な熱力学的パラメータを決定するために使用されている。CHARMM36は、タンパク質、核酸、脂質、炭水化物、薬物様生体分子のパラメータを含む自然界に存在する全ての原子型である。ここでの原子部分電荷は、モデル化合物と水との相互作用の量子化学計算から得られたものである。GROMOS43A2は、主に生体分子システムに適用される、明示的な脂肪族(非極性)水素を含まない単一原子力場である。ここでは、最小の相互作用単位は系の原子群である。コリンは基底集合6.31G(d,p)を用いて密度汎関数理論(DFT)によるガウス9.0で最適化した[59], [60]。TIP3P水モデルと急峻降下アルゴリズムを用いて、時間(1-10ns)を変化させながら50万回の繰り返しの2ステップでシステムのエネルギー最小化を行い、ステリック衝突を低減するために1000 kJmol-1までのカットオフを行った。本研究では、6LU7とコリン:6LU7の両方が10ps以内に安定化することが確認されたため、10nsまでのシミュレーションにこだわることにした。第一段階では、粒子数一定,体積一定,温度一定の境界条件を適用し、第二段階では、圧力1気圧,温度298Kの条件下で粒子数,圧力,温度一定のNPTを適用した。各シミュレーションの最終段階では、得られた軌道と結果をOrigin proを用いて解析した。MDシミュレーション,ドッキング,成分との仮想スクリーニング研究,所要時間,サルベーションボックスの長さなどの詳細な主要情報は、我々の前作[24]と同じであり、その中の参考文献である。
タンパク質:リガンド複合体(ΔGbind)の相互作用自由エネルギーを計算するために、我々はGROMACSとAPBSパッケージから供給される分子力学ポアソン-ボルツマン表面積(Molecular Mechanics Poisson-Boltzmann Surface Area)法(MMPBSA)[61]を使用している。このモデルには、反発成分と魅力的な成分の両方が含まれている[62]。結合エネルギーを予測するために,0から10 nsの間の100 psごとのスナップショットを収集した。水性溶媒中での結合リガンド:受容体複合体の結合自由エネルギーは、以下の式で表すことができる。
原文参照
ここで、ΔEMM、ΔGbind、solv、-TΔSは、それぞれ、気相中の分子力学的エネルギー変化、溶媒和自由エネルギー変化、結合によるコンフォメーションエネルギー変化を表す。ΔEMMは、共有結合エネルギー変化、静電エネルギー変化、ファンデルワールスエネルギー変化の組み合わせである。共有結合エネルギーは結合、角度、ねじれの組み合わせである。ΔGbind,solvはその極性と非極性の寄与に分離される。エントロピー項は、いくつかの選択されたスナップショットを使用して、ノーマルモード法で近似されている。結合自由エネルギーの計算では、MMPBSA法は通常、単一軌道法を用いた複合体のMDシミュレーションの後に開始する[63]。
2.4. 計算設備
MDシミュレーションとg_MM/PBSA計算には、8GBのRAMを搭載したDell Gen 10システム(8 Core i5プロセッサ)を使用している。
3. 結果と考察
3.1. コリンの薬物類似性の解析
プローブ分子コリンの阻害特性は、物理化学的記述子を決定し、ADME(Adsorption, Distribution, Metabolism and Excretion)パラメータを予測するために、SWISS ADMEソフトウェアを用いて研究されてきた。表1に記載されたデータから、我々は、コリンは、分子量が500 g/mol未満、TPSA値が40 Å2未満であるため、Ro5と同様に、最も規定された仮想スクリーニング特性を満たしていたことがわかる。H-結合ドナー≤5,H-結合アクセプター10,それらが容易に合成することができるように5未満の間の合成アクセシビリティカウント。それはまたそれがすべての生物学的利用可能性の条件を満たすことを意味する Veber の規則に続く。その薬物動態は脳の発達のための神経保護の役割を検証する。すべての薬効化学パラメータは、コリンに人間のための点で肝臓細胞毒性効果がないことを示唆するか、または薬剤によって誘発される肝臓損傷、ヌル変異原性は、コリンが癌につながる異常な遺伝的変異を引き起こすことができないことを明らかにする。また、心臓毒性もない。ADMET (vnnadmet.bhsai.org/)のデータによると、最大推奨治療用量は5.2 mg/日である。
3.2. 分子ドッキング結果の解析
受容体タンパク質:6LU7と潜在的阻害剤:コリンについて、ドッキングの結果、コリン:6LU7複合体に適した9つのポーズ構造を、RMSD/ub(上側結合)とRMSD/lb(下側結合)の変化とともに示した。ポーズ 1 については、室温(298 K)での結合エネルギーの負の値が最も高く(-3.7 kcal/mol)複 合体の延伸エネルギーの負の値が最も低く(104.198)阻害定数の負の値が最も低く(ki = 1.92 × 10-3 M)リガンド:受容体複合体のベストフィット構造として得られた(図 2 , 表 2)。ドッキングシミュレーションを数回繰り返し、-3.7 kcal/mol から-3.4 kcal/mol の間でベストフィット構造の結合親和性の変動が得られた。通常、個々のタンパク質とリガンドの脱離エネルギー値は異なるが、それらが複合体を形成した場合、複合体の脱離エネルギーは個々のタンパク質とリガンドの脱離エネルギーよりも小さくなることがわかった。脱離エネルギーが最小の複合体構造が最も好ましい構造に相当する[65]。同様に、ベストポーズ(1)の構造についても、最も低いki値が、コリンの受容体6LU7に対する高い親和性を証明した。計算されたki値は、コリンの毒性用量範囲(表1)よりもはるかに低い値であり、コリンがCoV2感染症の治療薬として提案されていることを立証している。また、ポーズ1の双極子モーメントの最大値(5.374デバイ)は、6LU7残基GLU166とコリンの正に荷電した窒素(N1)との間に強い静電相互作用(魅力的なタイプ)が存在するために生じる、コリンと6LU7との間のより良い錯形成の可能性を検証している。繰り返しになるが、弱い水素結合相互作用はタンパク質:リガンド複合体の安定性を決定する上で重要な役割を果たしている。6LU7(残基:GLY143,LEU141,HIS163,PHE140,ASN142)とコリン(原子:O1,H15,C4,C2,C3)とのドッキング構造のポーズ1では、弱い相互作用(従来の水素結合と炭素水素結合の両方)の数が最も多く観測された(図2a、b、表2)。支持文献1(SD1)では、我々は、最良のポーズ構造としてのポーズ1の選択を正当化する2つのより適切な最近接ドッキングポーズのデータを提示している。したがって、分子ドッキングの結果は、コリンが容易に6LU7タンパク質の好ましいポケット内で阻害することができ、それらの間に強い静電結合と弱い水素結合によって安定なコリン:6LU7複合体を形成することができることを示している。コリンと6LU7の間に強い相互作用が存在することは、次節のMDシミュレーションの結果からも確認されている。
図2
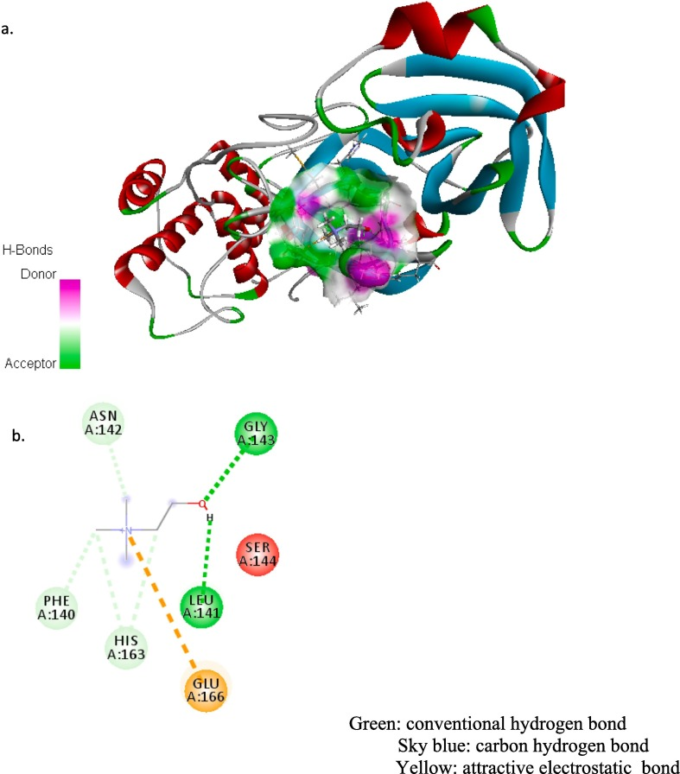
(a) コリン:6LU7の水素結合のドナー:アクセプター面。(b). コリン:6LU7の分子ドッキングから得られたベストポーズ構造で考えられる相互作用の種類。
表2 結合親和性、水素結合相互作用、静電相互作用、双極子モーメント、乾燥エネルギー、阻害定数などの各種パラメータを用いて、コリン:6LU7複合体のベストドッキングポーズ構造を決定した。
| Ligand | Best Binding affinity (kcal/mole) | Hydrogen bonded interaction (donor: acceptor, distance in Å) [Type of bond] | Electrostatic interaction (ligand donor: proton acceptor, distance in Å) [Type of bond] | Dipole moment of ligand (debye) | Drieding energy between protein and ligand | Inhibition constant (M) |
|---|---|---|---|---|---|---|
| choline | −3.7 | (A:GLY143:HN – :PYA0:O1, 2.53816)[Conventional Hydrogen Bond] (:PYA0:H14 – A:LEU141:O, 2.6499)[Conventional Hydrogen Bond] (:PYA0:C4 – A:HIS163:NE2, 3.58031) [Carbon Hydrogen Bond] (:PYA0:C2 – A:PHE140:O, 3.6244) [Carbon Hydrogen Bond] (:PYA0:C2 – A:HIS163:NE2, 3.54655) [Carbon Hydrogen Bond] (:PYA0:C3 – A:ASN142:OD1, 3.243) [Carbon Hydrogen Bond] |
(::PYA0:N1- A:GLU166:OE2, 5.10169)[ Attractive Charge] | 5.374 | 104.198 | 1.92 × 10−3 |
図3

(a) 水環境Na+イオンの存在下でのコリン:6LU7複合体系の溶媒和および中和。(b) コリン:6LU7複合体と裸の6LU7の最適化された形状のポテンシャルエネルギー面。
タンパク質とリガンドの相互作用の強さを定量化するためには、非結合性の静電相互作用が重要な役割を果たす。非結合性の静電相互作用については、主に短距離の静電相互作用に注目している。MDシミュレーションは、10,000 psから100 psまでの時間スケールを変化させて実施している。まず、ホスト構造と複合体構造の安定性を調べた。また、エネルギー最小化処理によりプローブ系を最適化し、両者のポテンシャルエネルギーが最小となるようにした。その結果、エネルギー的に安定な構造では、負のエネルギーの最小値と最大の力の値を持つポテンシャルエネルギーの定常的な収束が得られた(図3b)。6LU7では、Epotで-1.27×106 ± 56.7 (kJ mol-1)、コリン:6LU7では-8.2×105 ± 38.77 (kJ mol-1)であった。CHARM36とGROMOS43A2の両方の力場において、6LU7とコリン:6LU7複合体について同じ順序(エネルギー、エンタルピー、温度、圧力密度、体積、rmsd)の結果が観測され、いずれかの力場(SD2a,b)の適用が可能であることが明らかになった。残りのシミュレーションには、GROMOS43A2を使用した。さらに、NVT及びNPT平衡化アンサンブルの下での構造の安定性を確認するために、100-10,000psの変化する時間軌跡の中で、プローブ系のT,D,P,Vを計算してみた。その結果、各系(受容体、複合体)の温度は非常に早く(100ps以内)安定な値(298K)に達し、CHARM36とGROMOS43A2の両方の力場について、シミュレーションの全過程を通して安定性を維持していることがわかった(図4a参照)。このことは、両力場のMDシミュレーションへの適用性の高さを証明している。また、密度、圧力、体積についても、時間スケールが変化しても同様の安定性が見られた(図4aのインセット)。また、コリン:6LU7複合体の熱力学的パラメータを、裸の6LU7と比較して計算した結果、時間的にどのような構造変化が起こるかを理解することができた。これらのパラメータは、RMSD, RMSF, 非結合相互作用エネルギー, 水素結合, Rg などである(表 3)[67]。(表 3 ) [67]。RMSD は、リガンド結合による宿主タンパク質の安定性を、タンパク質の基準となる背骨構造を基準にして確認するために用いられる。図4bは、コリン:6LU7複合体の6LU7に対する炭素背骨のRMSD値を、1nsまでの時間スケールの軌跡を3Dビューで示したものである(図4b)。より理解を深めるために、より大きな時間的軌跡1〜10nsのための2次元図も図4bの挿入部に提供されている。6LU7 の RMSD が 0.12~0.18 (±0.01) nm であるのに対し、複合体の RMSD は 0.14~0.26 (±0.01) nm の間で変動していることが観察され、コリン結合中に構造が変動する可能性があることが示された。錯体構造の変動が大きくなるのは、主に7.5 nsから10 nsの時間スケールである。また、6LU7(0.16 nm)との複合体の平均RMSD値(0.18 nm)が近いことから、安定なコリン:6LU7ドッキング構造が形成されていることが確認された。3次元等高線プロットの平坦性は、CLproが時間分解シミュレーション中にコリンの存在に大きな変化を示さなかったことを示唆している。また、等高線プロットでは、1nsの時間軌跡の後にRMSDが安定な位相を示すことも明らかになった。RMSFについても同様に、複合体中の6LU7の残基揺らぎは、Cα炭素に関しては非常に小さいことがわかった。このことから、コリン:6LU7ドッキング複合体の構造は、シミュレーション中にほとんど変化しなかったホストタンパク質の構造に影響を与えていないことが示唆された(SD3)。さらにそれを確認するために、我々は、タンパク質のバックボーンの周りの水またはコリンの分布の平均的な画像を与えるコリンと水の放射状分布関数g(r)を解析した。水とコリンのg(r)値はSD4に示されている。図SD4は、水がタンパク質のバックボーンの〜0.44 nmで急激な増加を持っていることを示唆している。この水の横には、半径方向の分布全体で安定した増分を示している。コリンの存在下でピークの高さの突然の増分が観察される一方で。この突然の増分は、水とコリン分子間の反発に間違いなく起因している。この変化は、コリンがタンパク質のバックボーンに向かって水分子をリピートすることにより、タンパク質構造のコンパクトさを維持しようとするという事実に起因する可能性がある。この事実は、コリンとタンパク質のバックボーンとの相互作用の可能性が低いことを正当化している。
図4

(a) CHARM 36およびGROMOS力場における水中環境下での裸の6LU7およびコリン:6LU7複合体の温度および密度(挿入図)の進行データ。(b)裸の状態およびコリンとの複合体中の6LU7の二乗平均偏差(RMSD)バックボーングラフ(3D view upto 1 ns, 2D view upto 10 ns)。
表3 6LU7 のリガンドを含まないベア状態とコリンとの複合体状態における GROMOS43A2 力場を用いた分子動力学シミュレーションによる統計データ。
| Serial no | Parameter | Bare 3CLpro protease (6LU7)
|
6LU7 + choline complex
|
||
|---|---|---|---|---|---|
| Mean | Range | Mean | Range | ||
| 1. | SR Columbic Interaction energy (kJ mol−1) | NA | NA | −50.776 ± 20.12 | −70 to −10 |
| 2. | SR LJ Interaction energy (kJ mol−1) | NA | NA | −95.26 ± 22.10 | −30 to −120 |
| 3. | Average Interaction Energy energy (kJ mol−1) | NA | NA | −160.95 ± 20 | NA |
| 4. | RMSD (nm) | 0.16 ± 0.01 | 0.12–0.18 | 0.18 ± 0.01 | 0.12–0.26 |
| 5. | Inter H-Bonds | NA | NA | 2.5 | 0–6 |
| 6. | Radius of gyration | 2.25 ± 0.01 | 2.25–2.26 | 2.25 ± 0.01 | 2.25–2.26 |
| 7. | SASA (nm2) | 22 | 19–26 | 19 | 16–20 |
| 9. | Potential Energy (kJ mol−1) | −1.27 × 106 ± 56.7 | −7.3 × 105 to −1.3 × 106 | −8.5 × 105 ± 38.77 | −5.4 × 105 to −1.0 × 106 |
| 10. | Binding Energy (ΔG) (kJ mol−1) | NA | NA | –33.497 ± 27.406 | NA |
| 11. | Van der Waal Energy (ΔEvdw) (kJ mol−1) | NA | NA | −34.656 ± 24.958 | NA |
| 12. | Electrostatic Eenergy (ΔEelec), (kJ mol−1) | NA | NA | −7.380 ± 11.506 | NA |
| 13. | Polar solvation Energy (ΔE polar) (kJ mol−1) | NA | NA | 12.790 ± 28.852 | NA |
| 14. | SASA Energy (ΔE apolar kJ mol−1) | NA | NA | −4.251 ± 3.148 | NA |
上記の事実を正当化するために、我々は、タンパク質のバックボーンの周りの水またはコリンのカークウッドG因子(SD 5)を計算した。カークウッドG因子の変化は、タンパク質-水の相互作用と比較して、タンパク質-コリンの相互作用が純減していることを証明している。タンパク質-水のG因子の増加は、明らかにタンパク質の周りの水の密度の増加を示している。同様に、コリン-タンパク質におけるG因子の減少は、タンパク質の周りの水の密度が増加し、コリンがタンパク質のバックボーンから排除されるように、水のダイナミクスに対するコリンの影響を示している。
タンパク質リガンド複合体または塩基性骨格タンパク質の回旋半径(Rg)は、プローブシステムの圧縮された性質のヒントを与えてくれる[68]。全時間の軌跡にわたるRg値の変化は、ホスト6LU7とコリン:6LU7複合体が、シミュレーション期間中、大きな伸縮を欠くことなく、非常に安定で圧縮された構造を示していることを示した。複合体および基底タンパク質構造の両方とも、Rg値は2.25から2.26 nmの間で、平均値は2.25±0.01 nmであることが報告されている(SD6)。現在、主に使用されている抗COVID-19薬は、レムデシビル、ファビピラビル、ヒドロクロロキンである。レムデシビルでは平均Rg値が2.2±0.1nmと報告されている[69]。また、FavipiravirとhydroxychloroquineもRef. [70]. Remdisivirの値は、コリンについて得られた平均Rg値と正確に一致している。これは、提案されたCoV2阻害剤としてのコリンの候補性を正当化する。同様に、SASAは、シミュレーションプロセスの間に溶媒にさらされている受容体の面積を測定する。今回の研究では、6LU7では19~26 nm2,平均値は22 nm2であったのに対し、コリン:6LU7複合体では16~20 nm2,平均値は19 nm2であった(SD7)。裸の6LU7とコリン:6LU7の複合体で観測されたSASA値が近いことから、リガンドの結合は受容体タンパク質の折り畳みにはあまり影響を与えないことが明らかになった。
イオンや共有結合よりは弱いが、分子間水素結合が複合体形成の主な要因であることがわかった。水素結合の数を求めるために、3.5Åのカットオフ条件を用いている。本研究では、水素結合数が0から6の間で変動しており、その平均値は±2.6(SD8)であった。得られた水素結合数は分子ドッキングの結果と完全に一致し、コリン:6LU7錯体の安定性をさらに検証した。短距離非結合相互作用エネルギーは、複合体の成分間の相互作用の強さを定量化するために使用される。今回は、コリン:6LU7複合体の短距離クーロン相互作用エネルギーと短距離レナード-ジョーンズ相互作用エネルギーの時間(0-10,000 ps)に対する変化を3D図5aと表3に示した。エネルギー値は7000psの時間スケールのデータまで安定な性質を示した。計算されたデータからは、クーロン相互作用エネルギー(-50.776±20.12 kJ mol-1)による結合親和性の影響が、レナード-ジョーンズ相互作用エネルギー(-95.26±22.10 kJ mol-1)に比べて少ないことが明らかになった。また、時間分解したエネルギー値の変動は、フルタイムスケール領域の複合体のRMSDと完全に一致していることがわかった。
図5 コリン:6LU7複合体の場合

(a)時間に対するクーロン相互作用エネルギーとレナード・ジョーンズ相互作用エネルギーの変化(特定の色分けをしたカラーコンター表現で添付)(b)真空中のエネルギー、極性溶媒和エネルギー、非極性溶媒和エネルギーの間の関係、(c)。全時間軌道(0-10,000 ps)に対する全自由結合エネルギーの変化。
受容体へのより強いリガンド結合親和性を確立するために、我々は、個々のコンポーネントのエネルギーの包括的なセットの総和として正味の自由結合エネルギー(ΔG)の変化を扱うMM/PBSA法を適用している。分子ドッキングは複合体の結合エネルギーのみを示し、ΔGは複合体形成のための結合領域の非結合相互作用エネルギーを示す。複合体中のコリンの平均MM/PBSA自由結合エネルギー(ΔGbind)は-33.497 kJ/molとして得られたが、これはSARS-CoV2プロテアーゼに対するそのよく結合親和性のために十分である。また、ファンデルワールエネルギー(Ebdw)成分(-34.656 kJ/mol)もまた、コリンの6LU7に対する非常に良好な結合親和性を示したが、静電エネルギー(-7.380 kJ/mol)は複合体化プロセスにおいて重要な役割を示さなかった(Eelectrostatic)。ΔGに必要なすべてのエネルギー(真空中のエネルギー、極性および非極性の溶媒和エネルギー)の変動を図5bに示す。図5cは、全時間軌道における平均的な遊離ΔGbindを示す。本研究で報告され、上記にまとめられたすべてのMDシミュレーション結果は、コリンが、この3CLproプロテアーゼの活性部位に結合した後、SARS-Cov2タンパク質と印象的に安定な複合体を作ることができることを検証している。
4. おわりに
CoV2感染は、胎児と胎盤上の母体の炎症反応を担当することが知られている他の呼吸器ウイルスに似た方法で胎児の発達に影響を与えることが予想される。以前の研究では、母親が妊娠初期の間に呼吸器コロナウイルスに感染しているであろう場合は、母親の体内のより高い出生前のコリンレベルは、CoV2感染症の悪影響から胎児の発達している脳を保護することができることが確立している。コリンの多くの天然資源(例えば、野菜、卵、牛乳、全粒粉、ハーブ植物)がある。我々のADME解析(生理化学的、薬物動態、薬物類似性、薬理化学的)では、SARS-CoV2プロテアーゼ3CLproに対してコリンが強い阻害性を示す可能性があることを発見した。分子ドッキングの結果、強い結合親和性、最小阻害定数、水素結合相互作用の存在により、コリン:6LU7複合体構造の存在の可能性を確立した。分子動力学シミュレーションによって得られた様々な熱力学パラメータ(Epot、T、V、D、Rg、SASAエネルギー、相互作用エネルギー、ΔGbind)は、コリンとCoV2タンパク質(6LU7)との複合体化を検証した。すべてのシミュレーション結果をまとめ、それらの解析結果を解釈することで、コリンがSARS-CoV2の阻害剤として使用される可能性のある有力な候補として確立することができた。今回のin silico研究は、COVID-19の治療のための生前医薬品開発につながるものと確信している。CoV2感染症を効率的にターゲットにするためには、高品質の高濃度コリン抽出物の製造や生体内試験、試験管内試験での検証、臨床試験が必要である。
