Contents
ミトコンドリア機能障害(アルツハイマー病・神経変性疾患)
概要
用語解説
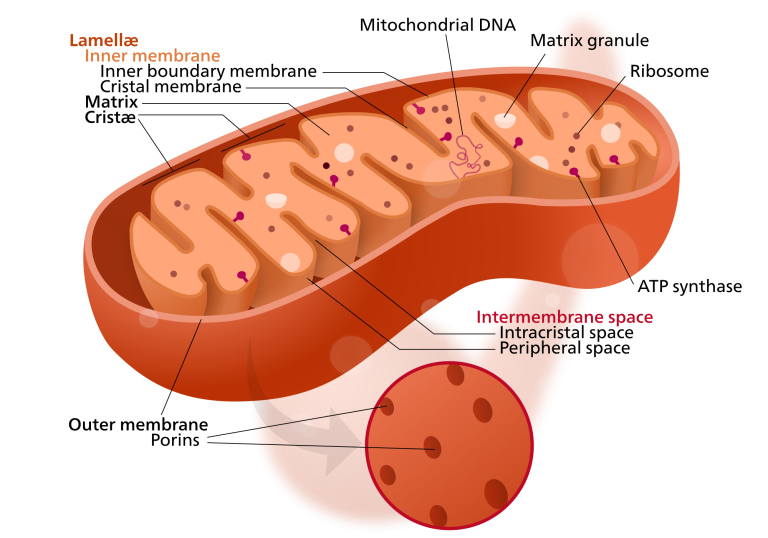
ミトコンドリア
ATP
ATPとは細胞が必要とするエネルギー源であり、生体内ではこのATPにくっついているリン酸分子が離れたり結合したりすることで、エネルギーの出力、貯蔵、あるいは代謝や合成に関わる役目を果たす。
すべての真核生物が直接利用しており、生物のエネルギー代謝の中心を占めることから、ATPは「エネルギー通貨」とも呼ばれる。
神経細胞ミトコンドリア
神経細胞ミトコンドリアの役割
神経細胞のミトコンドリアはATP産生、細胞内Ca2+シグナリング、活性酸素の生成などに加えて、神経伝達、シナプス可塑性、神経幹細胞の調節などといった重要な役割にも関わる。
www.ncbi.nlm.nih.gov/pubmed/17092996
www.ncbi.nlm.nih.gov/pubmed/18759009/
神経細胞におけるミトコンドリアの重要性
脳は体重の2%の重さに過ぎないが、酸素消費は20%を占める。
これは主にニューロンのエネルギー(活動電位の生成に必要なイオン勾配の維持)に用いられる。
そのため脳内の細胞(細胞体、樹上突起、軸索、シナプス末端)は高い代謝速度を有し、酸素とエネルギーの供給が安定的に維持されることを強く必要とする。
ミトコンドリアはそのエネルギー供給に直接的に関わるため、ミトコンドリア機能が変化すると神経細胞の生存と機能に大きな影響を与えうる。
www.ncbi.nlm.nih.gov/pubmed/19853658
神経幹細胞の調節因子
ミトコンドリアは神経幹細胞の調節因子の役割を果たすことが、最近の研究で明らかになってきている。
TCAサイクルの中間体であるαKG(αケトグルタル酸)は、DNAおよびヒストン脱メチル活性を有する酵素の基質である。
幹細胞のミトコンドリアの機能低下は、老化や自己組織再生機能の低下を誘導する可能性がある。
www.ncbi.nlm.nih.gov/pubmed/29654217
www.nature.com/articles/s41583-018-0091-3
神経細胞ミトコンドリアの問題点
中枢神経系が反応種に対して高い感受性をもつ理由
・中枢神経系の高い酸素消費
・中枢神経系は高濃度の多価不飽和脂肪酸が存在し、それらはフリーラジカルの影響を受けやすい
・中枢神経系の不十分な酸化防御(CAT活性の低さ、中程度のSOD、不十分なGPx)
・中枢神経系領域の一部で鉄、アスコルビン酸塩含有量が高い → フェントン反応、ハーバーワイス反応の誘発
活性酸素を産生するミトコンドリア
神経細胞内のミトコンドリアは、エネルギーを得るため酸化的リン酸化(OXPHOS)に高度に依存する。
しかし、OXPHOSはフリーラジカルの主要な供給源であり、過酸化水素(H2O2)、ヒドロキシラジカル(HO)、スーパーオキシドラジカル(O2)により、電子伝達系を阻害しえる。
産生されたフリーラジカルの量がニューロンの中和能力を超えると酸化ストレスが発生し、ミトコンドリア機能不全、ニューロンの損傷が生じる。
これらのフリーラジカルは、ミトコンドリアの成分(脂質、タンパク質、mtDNA)自体へも影響をおよぼす。
加齢によって衰えるミトコンドリア
老化すると、骨格筋量は中年期移行減少し、ミトコンドリアの機能的能力、密度も低下する。
老化そのものによってミトコンドリア機能が低下するのか、老化による活動の低下が結果としてミトコンドリア機能の低下をもたらすのかはわかっていない。
www.ncbi.nlm.nih.gov/pubmed/10878112/
www.ncbi.nlm.nih.gov/pubmed/22212519/
アルツハイマー病
アルツハイマー病ミトコンドリア仮説の歴史
アルツハイマー病にミトコンドリアが関与する可能性のある証拠については、40年以上前から報告されていた。
1980年 FDG-PET研究においてアルツハイマー病患者の脳グルコース利用の低下の判明。クレブスサイクル酵素の欠乏
1990年 アルツハイマー病患者においてシトロクロムオキシダーゼ活性が低下しているという報告。
www.ncbi.nlm.nih.gov/pubmed/2166249/
ミトコンドリアカスケード仮説
2004年 加齢によるアルツハイマー病リスクの増加は、アミロイドカスケード仮説では説明がつきにくことなどの背景のもと、アルツハイマー病の「ミトコンドリアカスケード仮説」が提案された。
www.sciencedirect.com/science/article/pii/S0306987704001252
この仮説によるとミトコンドリア機能は遺伝子をベースラインとし、年齢とともに衰え、環境因子によってその影響が決定される。
最終的にミトコンドリア機能の顕著な低下が、アルツハイマー病に特異的な病理をもたらすというもの。
2010年 ミトコンドリアカスケード仮説 更新
www.ncbi.nlm.nih.gov/pmc/articles/PMC2883665/
アルツハイマー病患者のミトコンドリア異常
ミトコンドリア分裂異常
ミトコンドリアの分裂は、オルガネラの生合成および遺伝に不可欠。
分裂が調整されないまま放置されると、
・不均一なmtDNA分布
・ATP産生能力の変化
・活性酸素種の生成能力の増加
・細胞アポトーシスの感受性増加
をもたらす。
分裂は、老化または損傷したミトコンドリアの除去(マイトファジーを介して)にも必要。
www.ncbi.nlm.nih.gov/pubmed/18806874/
www.ncbi.nlm.nih.gov/pubmed/21035308/
ミトコンドリア融合
ミトコンドリア融合は、均一なオルガネラ集団を維持するために必須であり、mtDNAの相互補完を保証する。
ミトコンドリア融合は、外側および内側の膜が別々の事象によって融合する2段階プロセス。
外膜融合は、2つの大きな膜GTPアーゼタンパク質、ミトフシン1(Mfn1)およびミトフシン2(Mfn2)によって制御されるが、内膜融合は視神経萎縮1(OPA1)によって制御される。
www.ncbi.nlm.nih.gov/pubmed/21035308/
ミトコンドリア密度の低下
ミトコンドリアの分裂、融合のバランス崩壊は、アルツハイマー病ニューロンにおけるミトコンドリア密度の低下を示し、ニューロンの機能不全をもたらす可能性がある。
www.ncbi.nlm.nih.gov/pubmed/19605646/
ミトコンドリアの形態学的変化
ミトコンドリアの形態学的変化は生体エネルギーに影響するが、生体エネルギーの変化もしばしば形態変化をもたらし、その影響は双方向的である。
ミトコンドリアの形状は、核分裂と核融合とのバランスによって大きく決定される。
www.ncbi.nlm.nih.gov/pubmed/21902671/
・健常者
楕円体ミトコンドリア 平均直径650±250nm 平均軸比1.9±0.2
円形ミトコンドリア平均半径 350nm
・アルツハイマー病患者
楕円体ミトコンドリア 平均直径510±250nm 平均軸比1.7±0.2
円形ミトコンドリア平均半径 280nm
www.ncbi.nlm.nih.gov/pubmed/16873959
ミトコンドリアの形態は作業記憶と相関し、エストロゲン投与により改善された。
www.ncbi.nlm.nih.gov/pubmed/24297907/
クリステの数の減少
www.ncbi.nlm.nih.gov/pubmed/10716887/
ミトコンドリア代謝回転速度の低下
アルツハイマー病患者の多くはグルコース代謝が低下している。
複数の研究から、電子伝達系の機能的欠損と、ミトコンドリアの代謝回転効率が密接につながっていることが提案されている。
www.ncbi.nlm.nih.gov/pubmed/20661404/
正常なミトコンドリア機能
ミトコンドリア突然変異
アルツハイマー病患者に対するミトコンドリア突然変異の影響は、再現性にかけており議論の余地がある。
www.ncbi.nlm.nih.gov/pubmed/16920408/
www.ncbi.nlm.nih.gov/pmc/articles/PMC3061980/
ミトコンドリア表面積
www.ncbi.nlm.nih.gov/pubmed/3736776/
酵素マーカー
www.ncbi.nlm.nih.gov/pubmed/6219611/
超微細構造
www.ncbi.nlm.nih.gov/pubmed/6797411/
アルツハイマー病ミトコンドリア仮説
ミトコンドリア機能不全はアルツハイマー病初期の事象
www.sciencedirect.com/science/article/pii/S0925443909002427?via%3Dihub
www.ncbi.nlm.nih.gov/pubmed/20937894/
ミトコンドリア軸索輸送障害
ALS・ADにおけるミトコンドリア軸索輸送障害
ミトコンドリア軸索輸送の変化は、アルツハイマー病、筋萎縮性側索硬化症(ALS)など神経変性疾患と関連する病理学的変化のひとつ。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3971748/
ATP供給のために輸送されるミトコンドリア
大部分のミトコンドリア生合成は核付近の細胞体において行われる。
しかしニューロン伝達の高いATP需要により、細胞体から合成されたミトコンドリアが軸索および樹状突起へ燃料供給のために輸送されることがある。
APP、アミロイドβによるミトコンドリア軸索輸送障害
ニューロン内のアミロイドβ前駆体タンパク質は、ミトコンドリア順行性軸索輸送を減少させる。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3209824/
アミロイドβは、GSK3βを介した作用によりミトコンドリア輸送の阻害を示す。
www.ncbi.nlm.nih.gov/pubmed/17035532/

マイトファジーとミトコンドリア輸送の相互作用
ミトコンドリア軸索輸送とマイトファジーは機能的に相互作用している。
オートファジー-リソソーム経路を介することで遠位軸索から機能不全のミトコンドリアを除去することが可能になる。
アルツハイマー病のマイトファジー障害
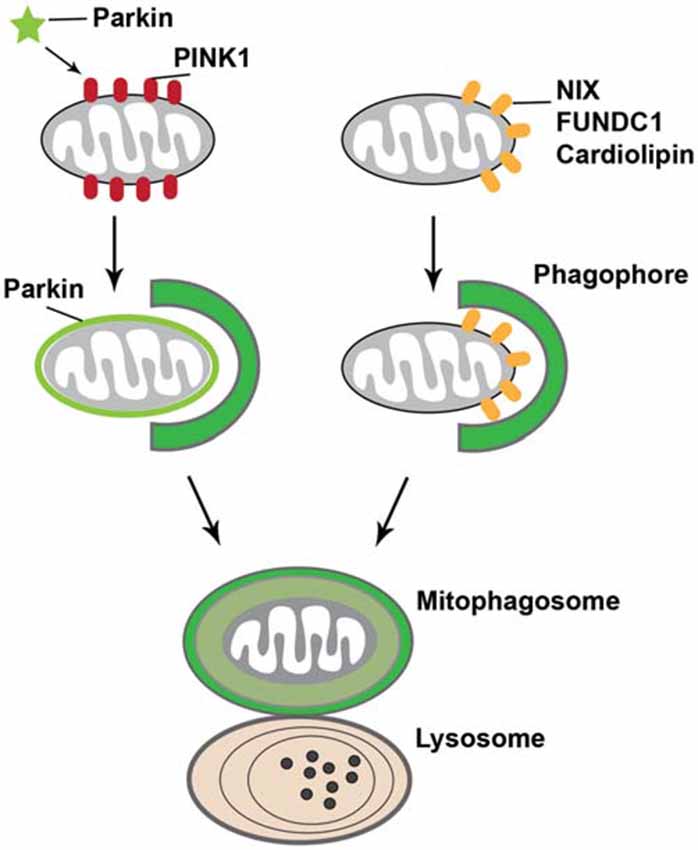
マイトファジー障害
ミトコンドリアは選択的に分解される(マイトファジー)という証拠が蓄積してきている。
どのようにミトコンドリアが選択的にオートファゴソームに隔離させるのか、その方法はまだほとんど未解明であるが、Uth1およびAup1がこのプロセスに関与することが研究によって示されている。
www.jbc.org/content/279/37/39068
www.frontiersin.org/articles/10.3389/fncel.2016.00024/full
リポフスチン蓄積
リポフスチンの蓄積が、オートファジーによるミトコンドリアの代謝回転を妨げ、老化ミトコンドリアの増加を促進させ、ATP産生の欠乏とROS量が増加させる可能性がある。
増加した酸化ストレスは、ミトコンドリアおよびリソソームの両方の損傷をさらに増強し適応能力を低下させ、アポトーシスを促進する経路を誘発し細胞死に至る。
jcb.rupress.org/content/171/1/87
www.tandfonline.com/doi/abs/10.4161/auto.5.4.8096
アルツハイマー病の「カルシウム仮説」
アルツハイマー病におけるカルシウムの調節不全

www.ncbi.nlm.nih.gov/pubmed/20080301/
カルシウムレベルの監視役
ミトコンドリアは、カルシウムイオン(Ca2+)の大容量貯蔵庫としても機能する。
細胞質のCa2+の負荷変化に対して適応し、正常なニューロン機能に必要なCa2+ホメオスタシスの維持をサポートする。
しかし、ミトコンドリアへ過剰にCa2+が取り込まれると、ROS産生が増加し、ATP合成が阻害され、ミトコンドリア透過性移行細孔(PTP)を誘導し、アポトーシスを引き起こすタンパク質を放出する。
これらの機能変化はアルツハイマー病の病因となるメカニズムとして提案されている。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3513836/
www.ncbi.nlm.nih.gov/pubmed/20413848/
Ca 2+ブロッカーおよびミトコンドリア安定剤
メマンチン、ディメボン、
NSAIDS(サリチル酸、スリンダクスルフィド、インドメタシン、イブプロフェン、R-フルルビプロフェンなど)によるミトコンドリアの脱分極(膜電位の減少)は、
ミトコンドリアCa 2+の過負荷、シトクロムcの放出、アミロイドβによって誘導される細胞死を抑制する。
www.ncbi.nlm.nih.gov/pubmed/18648507/
多段階のミトコンドリアカスケード仮説

www.ncbi.nlm.nih.gov/pmc/articles/PMC5869994/
一次ミトコンドリアカスケードは、脳機能を直接的に混乱させる可能性があり、アルツハイマー病の発症原因と関連するかもしれない。
アルツハイマー病が進行すると、アミロイドβなどの上流の病態によりミトコンドリア機能に影響をおよぼし、二次ミトコンドリアカスケードを引き起こす可能性がある。