概要
ミノサイクリンは30年以上にわたって使用されてきた第2世代のテトラサイクリン抗生物質であり、主に尋常性ざ瘡、性感染症などの治療に使用されてきた。現在は慢性関節リウマチなどの炎症疾患の治療目的で使用されている。
近年テトラサイクリンが、抗菌作用以外にも抗炎症活性、抗アポトーシス活性、タンパク質の分解、血管形成、腫瘍転移の阻害などの生物学的作用を発揮することが報告されている。これらの発見は、関節リウマチ、炎症性腸疾患、アテローム性動脈硬化、自己免疫疾患、そして神経変性疾患における神経保護作用を有することが浮上していきている。
この効果はパーキンソン病、ハンチントン病、筋萎縮性側索硬化症、アルツハイマー病、多発性硬化症および脊髄損傷を含むいくつかの神経変性症状の実験モデルにおいて確認されている。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3651660/
神経保護効果
血液脳関門を透過
ミノサイクリンは高い脂質への溶解度をもつことから、血液脳関門を容易に通過し、ミクログリアの活性を阻害し、アミロイドβの原線維形成を阻害し得る。
www.ncbi.nlm.nih.gov/pubmed/16220550/
抗炎症作用
ミノサイクリンは、ミクログリアの阻害よって中枢神経系における炎症を抑制する。
www.ncbi.nlm.nih.gov/pubmed/16336636/
炎症性サイトカインの減少
ミノサイクリンは、リポ多糖類誘発による炎症性サイトカイン分泌を阻害し、高齢マウスのLPS誘発による症状を回復させた。これらは海馬でのIL-1、IL-6、IDOのmRNAレベル低下と関連していた。
www.ncbi.nlm.nih.gov/pubmed/18477398/
ミクログリア活性の低下
ドーパミンニューロン保護
ミノサイクリンはトロンビン誘導性ミクログリア細胞の活性および、NADPHオキシダーゼの阻害を介して、黒漆中のドーパミン作動性ニューロンを保護する。in vivo
www.ncbi.nlm.nih.gov/pubmed/16219027/
www.ncbi.nlm.nih.gov/pubmed/17166727/
脳内の抗炎症作用(MMP9阻害作用による)
www.ncbi.nlm.nih.gov/pubmed/21737808
www.ncbi.nlm.nih.gov/pubmed/20705929
BDNF・NGF増加
www.ncbi.nlm.nih.gov/pubmed/28336494
神経変性疾患
アルツハイマー病
ミノサイクリンはアルツハイマー病様の病状を発症するダウン症候群マウスのコリン作動生喪失を予防する。。
www.ncbi.nlm.nih.gov/pubmed/9861045/
投与タイミングによる異なる影響
しかしアミロイドβ沈着の後にミノサイクリンを投与すると、ミクログリア細胞の活性化は抑制され、アミロイドβの沈着に影響を与えず認知能力を改善しなかった。ミノサイクリンは投与するマウスの年齢によって、アミロイドβの沈着と認知能力の改善への影響が異なる。初期のアルツハイマー病ではミクログリアの活性を抑制し、サイトカイン産生を低下させるが、アミロイドβプラークの形成を増強する可能性がある。
www.ncbi.nlm.nih.gov/pubmed/16534778/
ミノサイクリン投与は、ADアミロイド病理マウスの行動障害を改善し、炎症を低下させアミロイドβ三量体レベルを低下させた。
www.ncbi.nlm.nih.gov/pubmed/20173335/
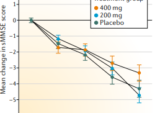
軽度アルツハイマー型認知症に対するミノサイクリン200mgまたは400mgとプラセボの比較:MADEフェーズII、3アームRCT
www.ncbi.nlm.nih.gov/books/NBK556206/
pubmed.ncbi.nlm.nih.gov/31738372/
2014年5月23日から2016年4月14日の間に、554名の参加者が無作為化された。対象となった544名のうち、平均年齢は74.3歳、標準化ミニメンタルステート試験の平均スコアは26.4点であった。
合計252件の重篤な有害事象が報告され、最も多かったカテゴリーは神経精神疾患と心循環系であった。ミノサイクリン400mgでは、200mg[62%(112/181)]またはプラセボ[64%(114/179)]と比較して、治療を完了した被験者が29%(53/184)と有意に少なかった(p<0.0001)。その主な理由は、消化器症状(p=0.0008)、皮膚科的副作用(p=0.02)、めまい(p=0.01)であった。評価率も400mg投与群では低く、24ヵ月後の標準化Mini Mental State Examinationスコアが68%(174例中119例)であったのに対し、200mg投与群では82%(144/176例)、プラセボ投与群では84%(140/167例)であった。
ミノサイクリン併用群における24ヵ月間の標準化ミニメンタルステート検査スコアの低下は、プラセボ群と同様であり(4.1点対4.3点の低下、p=0.9)、400mg投与群と200mg投与群の低下も同様であった(3.3点対4.7点、p=0.08)。
同様に、24ヵ月間のブリストル日常生活動作尺度スコアの悪化も、すべての試験群で同様でした(400mg投与群、200mg投与群、プラセボ投与群でそれぞれ5.7点、6.6点、6.2点、ミノサイクリン対プラセボでp値0.57、ミノサイクリン400mg対200mgでp値0.77)。結果は、異なる患者サブグループおよび欠損データを調整した感度分析でも同様であった。
多発性硬化症
www.ncbi.nlm.nih.gov/pubmed/11835378/
www.ncbi.nlm.nih.gov/pubmed/17395590/
www.ncbi.nlm.nih.gov/pubmed/20110416/
www.ncbi.nlm.nih.gov/pubmed/15122721/
www.ncbi.nlm.nih.gov/pubmed/19776092/
www.ncbi.nlm.nih.gov/pubmed/17463074/
ALS
www.ncbi.nlm.nih.gov/pubmed/12270689/
第三相無作為試験 ミノサイクリンはALS患者に有害な影響をおよぼす。
最大400mg/日 9ヶ月間
www.ncbi.nlm.nih.gov/pubmed/17980667/
ハンチントン病
マウスモデルでは多くの研究で50mg/kg/日が採用され、炎症、行動機能の改善および認知機能障害の軽減に大きな影響が認められる。低用量10mg/kg/日ではミクログリア活性の抑制というわずかな利益しか示さないが、驚くべきことに中等用量ではハンチントン病マウスにおいて行動機能の低下を示したが、5mg/kg/日の低用量ミノサイクリンは、行動機能、抗アポトーシス作用、および疾患死亡率に適度な影響を与えた。
www.ncbi.nlm.nih.gov/pubmed/24077620
その他の疾患
歯周病治療
www.ncbi.nlm.nih.gov/pubmed/17214846/
ミノサイクリンの全身投与により、歯垢指数(PI)、歯肉出血指数(SBI)は、初月に増加したが、プロービング深度(PD)、相対付着レベル(RAL)、マトリックスメタロプロテイナーゼ-8(MMP-8)、プロスタグランジンE2(PGE2)レベルはベースラインからの減少を維持した。
www.ncbi.nlm.nih.gov/pubmed/20663998/
アテローム性動脈硬化症
MMP活性およびサイトカイン誘導性VSMC遊走の阻害による血管平滑筋細胞(VSMC)、新生内膜形成の数を減少に起因して、アテローム性動脈硬化症を予防する可能性。
www.ncbi.nlm.nih.gov/pubmed/14508231/
www.ncbi.nlm.nih.gov/pubmed/15256478/
炎症性腸疾患
ミノサイクリンとプロバイオティクス(ラクトバチルス種)Escherichia coli Nissle 1917 による併用療法による治療は、個々の治療よりも優れた腸への抗炎症作用を発揮し、慢性炎症性腸疾患の再発を減弱させた。
www.ncbi.nlm.nih.gov/pubmed/18240278/