認知症治療薬メマンチン(メマリー)情報
概要
はじめに
メマンチンの基本情報や一般的なメカニズムは、多くの他サイトで解説されているのでここでは省略する。
メマンチンはNMDAグルタミン酸受容体の部分的阻害作用により、神経保護効果をもつと考えられているが、意外にもそのすべての作用機序が解明されているわけではなく、異なるメカニズムによる神経保護効果を含め、多彩に生体への影響をおよぼす可能性がある。
メマンチンの多彩なメカニズム
アミロイドカスケードに対するメマンチンの抑制効果

・神経炎症の低下
・記憶力の改善
・アミロイドレベルの低下
・NMDA受容体の阻害
・BDNFの増加
・酸化ストレスの低下
・BACE-1の低下
www.ncbi.nlm.nih.gov/pmc/articles/PMC5870028/
メマンチンは海馬のCdk5活性化を妨げる
CDK5(サイクリン依存性タンパク質キナーゼ5)は、神経突起および軸索成長を含む神経系における多数の生理学的機能の活性化および維持を行う。
NMDA受容体はアミロイドβの蓄積、酸化ストレスなどの興奮毒性により、カルシウムの増加を介してカルパインの活性化をもたらす。カルパインはCdk5に結合して、タウの過剰リン酸化に影響を与える。
アルツハイマー病ではCdk5上昇することで、タウタンパク質の過剰リン酸化と神経細胞死をもたらすという仮説がある。
www.ncbi.nlm.nih.gov/pmc/articles/PMC2441763/
メマンチンは海馬のCdk5活性化を妨げることがマウスモデルで実証されている。
www.ncbi.nlm.nih.gov/pubmed/26944284/
メマンチンはGSK3βの活性化を抑制する
グリコーゲンシンターゼキナーゼ-3(GSK3)は、アルツハイマー病(AD)の神経病理に関与する。
www.ncbi.nlm.nih.gov/pubmed/16464655/
GSK3β
アルツハイマー病においては、GSK3のアイソフォームGSK3β活性の調節不全が示されている。
GSK-3βの活性は、タウのリン酸化と相関。
GSK-3βは、微小管関連タンパク質(MAP)との相互作用を介して、軸索の安定性を調節する。
GSK-3βは、プロアポトーシスおよび抗アポトーシスの両方の効果を促進する。
GSK-3βの過剰発現は、シナプス密度数と体積の著しい減少を引き起こす。
GSK-3βは、インターロイキン-6(IL-6)、IL-1β、、腫瘍壊死因子などの様々な前炎症性サイトカインの産生を促進する。反対に抗炎症性サイトカインIL-10の産生を減少させる。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4033045/
GSK3の概日リズム変動
GSK3アイソフォーム(αとβ)の慢性活性化は、GSK3の標的BMAL1のリズムを損なう。
GSK3の活性状態は概日クロックによって調節され、GSK3がフィードバックすることで視交叉上核(SCN)の分子時計振幅を調節する。

www.ncbi.nlm.nih.gov/pmc/articles/PMC4586074/
ミクログリア活性の抑制
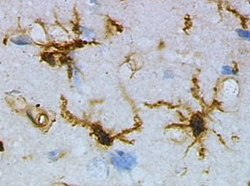
アルツハイマー病におけるミクログリア
アルツハイマー病患者では通常ミクログリア細胞は高度に反応性であり、アミロイドプラークの周辺に位置する。
ミクログリアはアルツハイマー病の初期においては、アミロイドβペプチドを貧食する保護的役割を果たしている。
疾患が進行すると、炎症性サイトカインの誘発と神経毒性をもつ細胞となる。
www.ncbi.nlm.nih.gov/pubmed/8757015
K +(Kir)チャネルの阻害
メマンチンは、K +(Kir)チャネルの阻害によって、ミクログリア細胞への抗炎症作用を有する。
www.ncbi.nlm.nih.gov/pubmed/23817277/
抗炎症作用
メマンチンはグリア細胞NMDA受容体の阻害を通した抗炎症作用を介して神経保護効果を発揮する。
www.ncbi.nlm.nih.gov/pubmed/23109148/
グリア細胞系由来神経栄養因子(GDNF)産生の増加
メマンチンは、ミクログリアの活性を防止することにより、アストログリアからのグリア細胞系由来神経栄養因子(GDNF)産生を増加させる。加えてLPS誘発性のドーパミンニューロン損傷への保護効果も示す。
www.ncbi.nlm.nih.gov/pubmed/19536110/
初期におけるメマンチンの低用量投与
神経炎症疾患の発症早期における低用量メマンチン投与は、ミクログリアの活性抑制を介して、神経保護および認知保護効果をもたらす可能性がある。
www.ncbi.nlm.nih.gov/pubmed/16989956/
メマンチンによるBDNFの増加
NMDA受容体阻害とは異なる機序によるBDNF発現の促進
メマンチンは、NMDA受容体の阻害とは異なる機序によってBDNFタンパク質発現を促進する。
www.ncbi.nlm.nih.gov/pubmed/23891641
BDNF増加による抗うつ作用
うつ病の動物モデルにおいて、メマンチンの投与が海馬のBDNFを増加させ抗うつ作用を示している。
www.ncbi.nlm.nih.gov/pubmed/19954760/
パーキンソン病への記憶と海馬シナプスの効果
メマンチンは、パーキンソン病動物モデルのBDNF低下を防ぎ、記憶および海馬のシナプス可塑性の喪失を防ぐ。
www.ncbi.nlm.nih.gov/pubmed/25560396/
メマンチンの糖尿病への効果
膵臓ベータ細胞のNMDA受容体
膵臓β細胞にNMDA受容体が発現しており、マウスの膵島NMDA受容体の阻害が、グルコース応答性インスリン分泌(GSIS)および膵島細胞の生存を増強することを示した。
NMDA受容体アンタゴニストであるデキストロメトルファンはマウスの耐糖能を増強する。
小規模の臨床試験において、デキストロメトルファン治療により2型闘病病患者の血清インスリン濃度および、グルコース耐性が向上していることが見出された。
www.ncbi.nlm.nih.gov/pubmed/25774850/
ApoE4キャリアへの効果
ApoE4対立遺伝子を保有する中期のアルツハイマー病患者へのメマンチン、リバスチグミンパッチの併用投与は、非ApoE4キャリアよりも日常生活動作のより有益な効果を示した。
www.ncbi.nlm.nih.gov/pubmed/23051684
ブチリルコリンエステラーゼK変異体のApoE4
ブチリルコリンエステラーゼK(BCHE-K)の変異体を有する患者では、リバスチグミンとメマンチンの併用療法に対して乏しい応答を示しており、特にApoE4保有者ではADAS-cogに対する悪い応答を示した。
www.ncbi.nlm.nih.gov/pubmed/25376930/
メマンチンはニコチン受容体を阻害する
www.ncbi.nlm.nih.gov/pubmed/9495824
メマンチンの慢性曝露によるミトコンドリア活性
メマンチンの慢性曝露により、ミトコンドリアの酸素消費量が増加し、NMDA受容体複合体I活性も増加した。
しかし、メマンチンのより高い濃度では、シトクロムオキシダーゼおよびクエン酸シンターゼ活性は減少した。
これらの根本的なメカニズムはわからないが、メマンチンが刺激薬としてミトコンドリアに作用している可能性が高い。
www.ncbi.nlm.nih.gov/pmc/articles/PMC2270256/
メマンチンの臨床効果
痛みの緩和・恐怖の克服
Cdk5は痛みの伝達に必要なキナーゼであることを示唆しており、恐怖学習において海馬の酵素活性が増加する際に持続する。
Cdk5の活性の阻害は、恐怖記憶を忘れて克服するために役立つ可能性がある。
www.ncbi.nlm.nih.gov/pmc/articles/PMC2441763/
www.ncbi.nlm.nih.gov/pubmed/26121895
www.ncbi.nlm.nih.gov/pubmed/28802070
メマンチンは行動症状に用いるべき
無作為化二重盲検プラセボ対照試験
メマンチンは中等度から重度のアルツハイマー病患者の行動症状の治療と予防に有効である。妄想および激越、被害妄想の症状について利益が持続的に観察された。
www.ncbi.nlm.nih.gov/pubmed/18058838/
www.ncbi.nlm.nih.gov/pubmed/19194105/
メマンチンの副作用
メマンチンは耐用性の高い薬である。
転倒
メマンチン投与された患者の約10%で転倒やけがが経験されている。
www.ncbi.nlm.nih.gov/pubmed/17345042/
傾眠
メマンチン療法は、総有害事象、重篤な有害事象、死亡の発生率を有意に増加させなかったが、傾眠のリスクを増加させた。
www.ncbi.nlm.nih.gov/pubmed/25899425
2%以上の有意な副作用
疲労、痛み、高血圧、めまい、頭痛、便秘、嘔吐、背痛、混乱、不眠症、尿路感染症、インフルエンザ様症状、異常歩行、うつ病、上気道感染、不安、末梢浮腫、気分障害、喘息、喘息、吐き気、食欲不振、関節痛
重度の腎障害を有する患者では、1日2回5mgを超えないことが推奨される。
アルツハイマー病以外の疾患への効果
レビー小体型認知症
パーキンソン病
前頭側頭葉変性症
ハンチントン病
www.ncbi.nlm.nih.gov/pubmed/17046312/
www.ncbi.nlm.nih.gov/pubmed/15354397/
筋萎縮性側索硬化症(ALS)
ALSモデルのマウスの疾患進行を有意に遅らせる。
www.ncbi.nlm.nih.gov/pubmed/16262676
うつ病
ランダム化比較試験 アルコール依存症を伴う大うつ病性障害治療
メマンチン投与が選択的セロトニン取り込み阻害剤抗うつ薬であるエスシタロプラムと同様にうつ病および不安レベルを有意に低下させた。
www.ncbi.nlm.nih.gov/pubmed/18348597/
ランダム化比較試験 早期発症の大うつ病性障害患者へのメマンチン投与(20mg/日)の有効性を示した。
www.ncbi.nlm.nih.gov/pubmed/17545748/
難治性偏頭痛
メマンチン10~20mgの投与 3ヶ月後に有意に頭痛頻度が低下
www.ncbi.nlm.nih.gov/pubmed/19031499/
その他
自閉症
www.ncbi.nlm.nih.gov/pubmed/17690064/
www.ncbi.nlm.nih.gov/pubmed/18433015/
www.ncbi.nlm.nih.gov/pubmed/17502791/
統合失調症
www.ncbi.nlm.nih.gov/pubmed/17728110/
www.ncbi.nlm.nih.gov/pubmed/17855055/
注意欠陥障害(ADHD)
www.ncbi.nlm.nih.gov/pubmed/17343551/
オピオイド依存症
www.ncbi.nlm.nih.gov/pubmed/11512037/
過敏性摂食障害
メマンチンは過食、軽度の重症度、障害の軽減に効果があったが、BMIと体重にはほとんど影響しなかった。
www.ncbi.nlm.nih.gov/pubmed/18433015/
強迫性障害
強迫性障害患者へのメマンチン10mg/日投与による有意な改善
www.ncbi.nlm.nih.gov/pmc/articles/PMC4085808/
オープンラベル試験 メマンチンによる強迫性障害および全般性不安障害への有効性
www.ncbi.nlm.nih.gov/pubmed/19204653
併用投与
メマンチンとビタミンDの併用投与
ビタミンD(400~1000IU)とメマンチン(20mg)を6ヶ月間併用投与されたアルツハイマー病患者では、MMSEを4ポイント上昇させたが、メマンチンまたはビタミンDの単独投与では効果を示さなかった。
www.ncbi.nlm.nih.gov/pubmed/22960436
メマンチンとビタミンDの組み合わせは、アミロイドβまたはグルタミン酸塩に曝露された後の皮質軸索の変性をより低下させることで、神経保護効果を発揮する可能性がある。in vitro
www.ncbi.nlm.nih.gov/pubmed/24011542
メマンチン併用投与によるビタミンEの効果の喪失
2000 IU / dのアルファトコフェロール単独投与は、軽度から中等度のアルツハイマー病患者の機能低下を遅らせるのに効果的であり、患者の介護時間を短縮するのにも有効であることを見出した。
メマンチン単独(20mg)またはアルファトコフェロールとメマンチン(20mg)の併用は、軽度から中等度のAD患者では臨床的利益を示さなかった。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4109898/
メマンチンとテヌイゲニン(遠志)、βアサロンの併用投与
ランダム化二重盲検プラセボ対照試験 中等度から重度のアルツハイマー病患者152人
テヌイゲニンとβアサロンとメマンチン(5~20mg)を投与された患者では、メマンチンだけを投与された患者と比べ、MMSEスコア、ADLスコアおよびCDRスコアが有意に高かった。
www.ncbi.nlm.nih.gov/pubmed/29551889

