はじめに
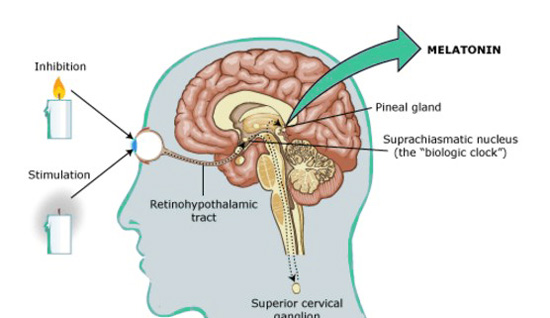
メラトニンは、脳の松果体線から分泌されるホルモンの一種で、睡眠調節(概日リズム調整)、フリーラジカルの除去、免疫の改善、酸化防止に深く関わる。
アルツハイマー病患者はメラトニン濃度が低い
メラトニン分泌量は健康な成人と比べて、健常な80歳以上の高齢者では半分、アルツハイマー病患者では5分の1まで減少する。
メラトニン分泌は10代をピークに(0.5~0.8mg)20歳を過ぎて大きく下がる。より重要な夜間のメラトニン分泌は、40歳から大きく低下し始める。
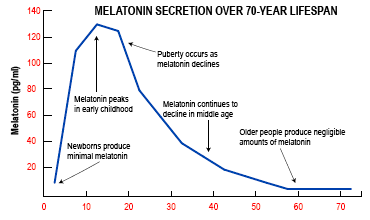
www.askdrray.com/melatonin-more-than-a-sleeping-aid/
アルツハイマー病患者では、メラトニン濃度(血清および脳、脊髄液中)の減少と概日リズムの喪失が観察されている。
www.ncbi.nlm.nih.gov/pubmed/15725334
アルツハイマー病の進行に伴って、脊髄液中のメラトニンは減少する。
www.ncbi.nlm.nih.gov/pubmed/12887656
メラトニン欠乏の原因
原因としては、ノルアドレナリン調節の機能不全、前駆体であるセロトニンの枯渇が考えられている。
またアリセプトなどのコリンエステラーゼ阻害剤によって、メラトニン日内変動が消失している可能性もある。
メラトニンの前駆体であるセロトニンの枯渇が、アルツハイマー病患者のメラトニン低下およびメラトニンリズムの喪失の原因となる。
www.ncbi.nlm.nih.gov/pubmed/17692293/
メラトニンの効果
優れた抗酸化特性
メラトニンは、とても広範囲の種類の酸化物質と、その関連代謝産物を除去するすることができる。
総合的には、たとえばビタミンCやビタミンEなどの抗酸化能力を超える。
メラトニンは、睡眠障害の改善だけではなく強力な抗酸化力や神経変性を改善する効果があることから、アルツハイマー病の治療薬として期待されている。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4257134/
メラトニンの神経保護効果
・脂溶性かつ水溶性であるため細胞膜を自在に通過。
・血液脳関門を通過して脳の神経細胞の酸化障害を防ぐことができる。
・抗アミロイド作用によるアミロイドβ毒性からのニューロン保護作用。
・アミロイドβの誘発によるIL1-β、IL-6、TNF-αを50%減少 in vivo
・アミロイド繊維の形成を阻止。
・レスベラトロールと併用することで、アミロイド班の沈着を相乗的に防ぐ。(AMPKのリン酸化と下流の経路を介して)
・タウたんぱくの過剰リン酸化を阻害。
・コリン作動系への保護作用をもつ。
・グルタチオン産生に必要なγグルタミルシステイン酵素(γ-GCS)を増やす。
・MT1受容体を介したBDNF増加作用
・夜間のメラトニン分泌はグルコガンの分泌を刺激し、脳へのエネルギーを確保
www.ncbi.nlm.nih.gov/pmc/articles/PMC3004402/
www.ncbi.nlm.nih.gov/pmc/articles/PMC3742260/

www.ncbi.nlm.nih.gov/pmc/articles/PMC4665493/
睡眠時無呼吸症候群
睡眠時無呼吸症候群、神経変性疾患を有する高齢者へのメラトニン投与の有効性。
3~12mgのメラトニン用量が、レム睡眠行動障害の症状軽減に有効
メラトニンは筋活動抑制を伴わないREM
www.ncbi.nlm.nih.gov/pmc/articles/PMC4306603/
メラトニン受容体
www.scielo.br/scielo.php?script=sci_arttext&pid=S2359-39972015000500391
MT受容体
概日リズム調整
MT受容体は中枢神経系全体に広く発現しており、視交叉上核(SCN)によるメラトニンにより、ニューロンの発火を抑制し概日リズムの調整を行う。
抗酸化酵素の活性
メラトニンそのものの抗酸化作用だけでなく、メラトニンがMT1、MT2受容体に作用することで、スーパーオキシドディスムターゼ、カタラーゼ、グルタチオンペルオキシダーゼなどの酵素の発現が活性化し増加する。
低濃度である内因性のメラトニンでの発現が認められており、メラトニン用量に依存しない抗酸化作用があることが示されている。
www.ncbi.nlm.nih.gov/pubmed/19710945
MT1・MT2
アルツハイマー病患者の海馬ではMT1の免疫応答が増加し、MT2免疫応答が減少している。
アルツハイマー病患者の脳では、脳の変性組織ではMT1、MT2両方の受容体強度が低下
www.ncbi.nlm.nih.gov/pubmed/17213040
MT1が細胞の活性化に対する抑制作用をもつのに対して、MT2は睡眠のリズム、位相作用に関わる。
血管拡張、PACAPによるCREBのリン酸化にも関わる。
MT1受容体
SCNの神経発火を抑制、
ニューロン発火、血管収縮、レプチン分泌増加
網膜のMT1受容活性化によって眼圧を下げる。
メラトニンはMT1、MT2へ作用する。
ラメルテオンはMT1/MT2へメラトニンよりも長く作用する(MT1への作用がより強い)
MT1受容体は、アルツハイマー病、パーキンソン病、ハンチントン病などの神経変性疾患、精神障害において、発現の変化が多く報告されている。
アルツハイマー病患者の海馬でのMT1受容体の高い発現は、低レベルのメラトニンに対する代償応答かもしれない。
MT1は、睡眠障害、不安、うつ病、アルツハイマー病、疼痛の病態生理学、薬理学に関与する。
www.ncbi.nlm.nih.gov/pubmed/23971978
後期アルツハイマー病患者のわずかなMT1受容体
後期のアルツハイマー病患者では、MT1受容体が極端に減少しており、メラトニンは概日リズム障害に明らかな効果をもたらないさない可能性がある。
www.ncbi.nlm.nih.gov/pubmed/17383938/
薬物乱用治療
MT1は、薬物乱用障害治療の新規標的
www.ncbi.nlm.nih.gov/pubmed/23934259
概日リズム障害
概日リズム障害と関連するうつ病へはMT1受容体を特異的に標的にすべき。
www.ncbi.nlm.nih.gov/pubmed/23357659
MT2受容体
マウスを使った研究では、MT2受容体は軸索形成、シナプスの形成に必須であることが示されている。
www.ncbi.nlm.nih.gov/pubmed/25501601
MT2は催眠性および抗不安特性、精神疾患治療の創薬可能性をもつ標的
www.ncbi.nlm.nih.gov/pubmed/23971978
バルプロ酸によるMT2受容体のアップレギュレーション
MT2アゴニストとバルプロ酸の組み合わせ投与が、アルツハイマー病などの神経変性疾患に有益な治療戦略であることを示唆する。
www.sciencedirect.com/science/article/abs/pii/S030439401400456X
バルプロ酸がラット海馬のMT1、MT2受容体の両方をアップレギュレートする。
MT2受容体がシナプス可塑性および認知機能の調節に関与すると考えられている。
www.ncbi.nlm.nih.gov/pubmed/24909617
MT3受容体
MT3受容体は主に内臓に存在しており、睡眠や覚醒とは関係していないと考えられている。
in vitroで、メラトニンのMT3受容体刺激が、腫瘍細胞の化学療法剤によって誘発された細胞毒性作用およびアポトーシス作用を増強する。
www.ncbi.nlm.nih.gov/pubmed/28956121
GPR50受容体
二量体化によってMT1受容体のメラトニン結合をブロックする。
www.ncbi.nlm.nih.gov/pubmed/16778767/
レプチンのシグナル伝達と相互作用する