Contents
抗炎症・COX阻害
アルツハイマー病患者への抗炎症薬の効果
www.ncbi.nlm.nih.gov/pmc/articles/PMC2912027/
イブプロフェン
www.news-medical.net/news/2008/05/06/25/Japanese.aspx
イブプロフェンは低用量長期投与でアルツハイマー型認知症の予防に効果があるとされ、パーキンソン病の発症率低下に結び付ける研究結果も。
minacolor.com/parts/19/articles/582/
アルツハイマー病の治療に対するイブプロフェンの有益性な証拠はない
www.ncbi.nlm.nih.gov/pubmed/12804498
イブプロフェンは一酸化窒素、グルタミン酸毒性からニューロンを保護し、炎症促進性サイトカインの産生を減少させる。イブプロフェンは、血液脳関門を通過し、アルツハイマー病患者の脳内において神経炎プラーク病理および炎症を抑制する。
イブプロフェンは強力なフリーラジカルスカベンジャーであり、脂質過酸化およびフリーラジカルを減少させることができる。
www.ncbi.nlm.nih.gov/pubmed/15506544
ランダム化二重盲検プラセボ対照試験 軽度、中等度のアルツハイマー病患者へ400mg×2回/日投与イブプロフェンを投与されたApoE4キャリアの患者のグループのみ認知低下を抑制した。
www.ncbi.nlm.nih.gov/pubmed/19448381
インドメタシン
プラセボ二重盲検対照研究 インドメタシン100~150mg/日の投与は、軽度から中等度の障害のあるアルツハイマー病患者の認知機能低下を防ぎ改善を示した。
www.ncbi.nlm.nih.gov/pubmed/8351023
インドメタシンは、軽度から中等度の重篤なアルツハイマー病の治療には推奨できない。
100~150mg/日の用量では、重篤な副作用リスクが存在する。
www.ncbi.nlm.nih.gov/pubmed/12076498
ニモジピン/Nimodipine
ニモジピンは、分類されていないが認知症症状を呈する患者、またはアルツハイマー病、脳血管疾患、混合アルツハイマー病において、いくつかの利点があり得る。副作用が少なく、耐容性に優れている。
www.ncbi.nlm.nih.gov/pubmed/12137606
ニモジピン投与によるアルツハイマー病症状の緩和は、中枢作用性の抗炎症効果による。
www.ncbi.nlm.nih.gov/pubmed/22831460
FTDの主要な遺伝的原因を構成する病原性プログラニューリン変異のキャリアにおいて減少する。
プログラヌニューリンの欠損はTDP-43の蓄積と関連している。
ニモジピンは、脳内のプログラニューリンタンパク質を増加させる可能性がある。
www.alzforum.org/therapeutics/nimodipine
www.nytimes.com/2012/05/06/health/tying-genes-and-proteins-to-dementia.html?_r=4&ref=health&
ミノサイクリン
セレコキシブ
平均58歳の軽度の記憶障害を自己報告するボランティアへ200mgまたは400mgのセレコキシブを投与。プラセボ郡と比べ、前頭前野両側(ブロードマン領域9、10)の代謝が増加を示した。PETデータの統計的パラメトリックマッピングでは6%活性が増加した。
www.ncbi.nlm.nih.gov/pubmed/19038899
COX-2阻害剤、セレコキシブ ランダム化二重盲検対照並列試験 50歳以上の軽度から中等度のアルツハイマー病患者へ52週間、セレコキシブ200mgの投与。アルツハイマー病の進行を遅らせることはなかった。
www.ncbi.nlm.nih.gov/pubmed/17068392
フルリザン/Flurizan
フルリザンは、COX1、COX2阻害剤ではなく、γセクレターゼへの直接作用によりアミロイドβへ選択的に作用する。
flurizanフェーズ3の失敗は、弱い効力と脳への浸透、および標的の調整不良にある。
www.ncbi.nlm.nih.gov/pubmed/20443898
www.alzforum.org/therapeutics/flurizan
タウ凝集阻害
アルツハイマー病の治療のための臨床開発におけるタウ 中心標的と薬物
1. タウリン酸化の阻害
- グリコーゲン合成酵素キナーゼ3β(GSK-3 β)
- サイクリン依存性キナーゼ5(CDK5)
- cAMP依存性プロテインキナーゼ(PKA)
- カルシウム/カルモジュリン依存性キナーゼII(CaMKII)
- PP2A活性化薬剤
2. 微小管安定化の増加
タキソール誘導体TX67/パクリタキセル(イチイの樹皮抽出物)
www.ncbi.nlm.nih.gov/pubmed/17336290/
エポチロンD(ミクソバクテリア族の細菌から発見されたマクロライド化合物)
www.ncbi.nlm.nih.gov/pubmed/22423084/
タキソイドTPI 287
ダブネチド
3. タウクリアランスの増加
4. タウ凝集の阻害
ポリフェノール
ミリセチン
エピガロカテキン
ゴシペチン
4′-ペンタヒドロキシベンゾフェノン
www.ncbi.nlm.nih.gov/pubmed/15611092
オレカンタール(オリーブ油に含まれるフェノール化合物の一種)
www.ncbi.nlm.nih.gov/pubmed/22988908/
ポルフィリン
ヘム(第二鉄デヒドロポルフィリンIX )
チオフラビンS蛍光染色剤
フェノチアジン
メチレンブルー
アズールA、アズールB
www.ncbi.nlm.nih.gov/pmc/articles/PMC38310/
ベンゾチアゾール/シアニン
www.ncbi.nlm.nih.gov/pubmed/27429978
リファンピシン
細胞内アミロイドβオリゴマーの蓄積と毒性に対してもっとも強い活性を示す。
マウスに1mg/日を一ヶ月間経口投与すると、アミロイドβオリゴマーの蓄積、リン酸化タウ、シナプス喪失、ミクログリアの活性が減少し、アミロイドの沈着が減少した。
www.ncbi.nlm.nih.gov/pubmed/27020329
後部帯状皮質のFDG-PETの解析で改善
リファンピシンの予防効果は、投与量と治療期間に依存する。450mg、1年以上
www.ncbi.nlm.nih.gov/pubmed/28690634
www.ncbi.nlm.nih.gov/pmc/articles/PMC5498941/
メチレンブルー
サルサレート/salsalate
非ステロイド系抗炎症薬
アセチル基転移酵素p300がタウのリシン残基にアセチル基を結合する。これらの基を潜在的にはヒストン脱アセチル化酵素6、SIRT1が除去することができる。
抗炎症剤であるサルサレートは、p300、タウアセチルトランスフェラーゼを阻害することで、タウを含む過剰なアセチル化を抑制することができる。

www.alzforum.org/news/research-news/acetylated-tau-mucks-memories
ADマウスにおいて、サルサレートの保護効果は、アルツハイマー病発症後の投与であっても持続されており、治療薬としての可能性をもつ。
FTDトランスジェニックマウスにサルサレートを投与、p300活性を阻害、総タウのタウレベルを低下、記憶障害を改善し海馬萎縮を予防した。
www.ncbi.nlm.nih.gov/pubmed/26390242/
抗凝固剤・血流改善
アスピリン
シロスタゾール(プレタール)/ Cilostazol
血小板または血管平滑筋のホスホジエステラーゼ(PDE3)の活性を選択的に阻害することで、抗血小板作用や血管拡張作用を発揮する薬剤。
脳梗塞やラクナ梗塞後の再発を防ぐために用いられる。
アドオン療法(AChEIとの)を行った場合にはアルツハイマー病患者の認知機能の低下を減少させる可能性がある。50mg×2回/日
www.ncbi.nlm.nih.gov/pmc/articles/PMC5324327/
シロスタゾールの投与は、アミロイドβがすでに蓄積していた場合には、アミロイドβ誘発性の神経病理学的反応を妨げることができなかった。
シロスタゾールの有益な効果は、アミロイドβ蓄積やタウリン酸化の減少、およびアミロイドβ分解を増加させることによるものではなく、ApoE媒介性のアミロイドβ凝集の有意な減少によるものであると説明することができる。
www.ncbi.nlm.nih.gov/pubmed/21530492
シロスタゾールは、アルツハイマー病患者、脳血管疾患の認知低下に対して予防効果をもつ可能性。投与群で右前頭葉ローブにおいてrCBFの増加、対照群(アスピリン100mgまたはクロピドグレル50mg-75mg)は減少。
www.ncbi.nlm.nih.gov/pubmed/22672107
シロスタゾールによって刺激されたCK2結合SIRT1活性化が、P300およびGSK3βの活性化を阻害することによって、タウアセチル化(Acタウ)およびタウリン酸化(Pタウ)を抑制する。
シロスタゾールによるcAMP依存性プロテインキナーゼ関連CK2 / SIRT1発現の増加は、アルツハイマー病脳におけるタウ関連神経変性を抑制する治療戦略となり得る。
www.ncbi.nlm.nih.gov/pubmed/24254769
MMP9活性の阻害による血液脳関門の閉鎖
www.ncbi.nlm.nih.gov/pubmed/11861782
www.ncbi.nlm.nih.gov/pubmed/21151895
www.ncbi.nlm.nih.gov/pubmed/19383431
サアミオン(ニセルゴリン)

ニルパジピン/Nilvadipine
www.ncbi.nlm.nih.gov/pubmed/18033677
83歳の高血圧症を有する初期のアルツハイマー病患者へニルバジピンを投与。
両側前頭皮質、右頭頂皮質、および後部帯状皮質において顕著に局所的な脳血流が増加し、MMSEスコアが23点から27点に増加した。
www.ncbi.nlm.nih.gov/pubmed/18097255
76歳の初期アルツハイマー病の男性に、ニルバジピン、テルミサルタン、ピオグリタゾンを投与。6ヶ月後MMSEに変化はなかったものの、口頭の流暢性が高まり、SPECTのフォローアップ試験では、前頭側および側頭側の領域における脳灌流の改善を示した。
www.ncbi.nlm.nih.gov/pubmed/18753719
カルベジロール/Carvedilol
高血圧、狭心症、心不全治療薬
カルベジロールの長期投与はADマウスの脳内アミロイドβオリゴマーの蓄積を緩和し認知低下を有意に減弱させる。
www.ncbi.nlm.nih.gov/pubmed/20579773
クリニカルトライアル フェーズ4
6ヶ月の無作為プラセボ対照二重盲検治療 1日25mgの目標用量
www.clinicaltrials.gov/ct2/show/study/NCT01354444
www.ncbi.nlm.nih.gov/pubmed/24163077
スタチンおよびβ遮断薬(カルベジロール)の使用は認知機能低下の遅延に関連していた。
β遮断薬カルベジロールは、一過性脳卒中のラットモデルにおいて梗塞サイズおよび神経学的欠損を減少させた。
この神経保護はアポトーシスの減少および炎症誘発性サイトカインTNF- αおよびIL-1- βの脳レベルと関連していた。
活性化ミクログリアにより炎症誘発性サイトカインの放出を介してアルツハイマー病の神経毒性が増加する証拠があり、β遮断薬がアルツハイマー病脳の抗炎症薬として作用する可能性がある。
その他のメカニズム β遮断薬が無症状のうっ血性心不全、冠状動脈疾患の心拍出量を改善する→脳灌流を改善→認知機能の改善
www.ncbi.nlm.nih.gov/pubmed/18978249
カルベジロールの長期経口投与が、ADマウスモデル脳のアミロイドβオリゴマーレベルおよび認知低下を有意に減弱させる。ニューロンの伝達を有意に改善し、ADマウスの脳内の安定性のない「学習」樹状突起スパインの数の維持に関連する。
ビンポセチン
ピラセタム
糖尿病薬
メトホルミン
無作為プラセボ対照クロスオーバー メトホルミンは血液脳関門を通過する。
メトホルミン治療中において、学習、記憶、注意力等、執行機能の改善が認められた
www.ncbi.nlm.nih.gov/pubmed/28538088
長期使用リスク
12年間のフォローアップではメトホルミンの投与グループは、非投与グループよりもパーキンソン病および認知症、アルツハイマー病、血管性認知症の発症リスクを有意に増加させた。
www.ncbi.nlm.nih.gov/pubmed/28583443
60歳以上のメトホルミンの長期使用者は、アルツハイマー病発症リスクがやや高い。
www.ncbi.nlm.nih.gov/pubmed/22458300
認知症予防
メタアナリシス インスリン抵抗性改善薬は認知症予防に役立つ可能性がある。
www.ncbi.nlm.nih.gov/pubmed/27250528
B12欠乏
メトホルミン治療ではビタミンB12欠乏が起こる可能性。
www.ncbi.nlm.nih.gov/pubmed/26900641
アミロイドβ産生を増加
メトホルミンはBACE1転写をアップレギュレーションすることにより、アミロイドβペプチドの生合成を増加させる。
www.ncbi.nlm.nih.gov/pubmed/19237574/
メトホルミンはADマウスモデルにおいて、オートファゴソームの蓄積を引き起こし、γセクレターゼ活性およびアミロイドβ産生を増加させる。
www.ncbi.nlm.nih.gov/pubmed/26967226
メトホルミンは、APP切断およびアミロイドβの細胞内蓄積を増加させ、アミロイドβの凝集を促進する。実験ではメトホルミンが酸化ストレス、ミトコンドリア損傷、ヘキソキナーゼⅡレベルおよびシトクロムC放出の減少をもたらし、アポトーシスを誘導する。
これらはインスリン、フェルラ酸やクルクミンの添加によってメトホルミンはの作用を元に戻すことができた。
www.ncbi.nlm.nih.gov/pubmed/25667085
ピオグリタゾン

ピオグリタゾンは小脳のiNOS発現を抑制し、小胞体の顆粒細胞をリポ多糖類、インターフェロンγ障害からほごすることができる。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3678219/
PPARγアゴニストであるピオグリタゾンまたはNSAIDイブプロフェンの経口治療が、マウスの海馬および皮質のミクログリア細胞活性化および、反応性アストロサイトの数を減少させることが示されている。
www.ncbi.nlm.nih.gov/pubmed/15817521/
ドイツの大規模観察研究 ピオグリタゾンの長期使用は、認知症発症リスクを低下させる。
脳関門の透過性
ロシグリタゾンは血液脳関門をわずかに透過し積極的に脳から排出されていることによって脳におけるインスリン感作効果が限定的なものとなっている可能性がある。
ピオグリタゾンはロシグリタゾンとの構造的類似性があるため、同様に脳内への浸透が制限されていると考えることもできる。ラセミ体ではないピオグリタゾンによる脳透過性の増加
www.nature.com/articles/srep09000
リラグルチド
www.alzdiscovery.org/cognitive-vitality/article/promise-in-off-label-drugs-for-alzheimers
脂質代謝改善
シンバスタチン
脂溶性スタチンは血液脳関門を通過しやすい。
水様性スタチン(プラバスタチン、ロスバスタチン)はリスクを減少させない。
アミロイドβの産生を阻害
テルミサルタン
テルミサルタンは、多面的な効果によって神経炎症および神経毒性を低下させることが期待されている。脳卒中後の高血圧患者のアルツハイマー病予防アプローチ
www.ncbi.nlm.nih.gov/pubmed/24435631
PPARγの部分活性機能をもつテルミサルタンが、ARBにおいてアルツハイマー病の認知障害予防効果をより強く有する。
www.ncbi.nlm.nih.gov/pubmed/18715543
低用量テルミサルタンは、ラットのメタボリックシンドロームを改善し、高用量のテルミサルタンは、メタボリックシンドロームと高血圧を改善することで、アミロイドβ、およびリン酸化タウの蓄積および炎症応答を減少させる。
www.ncbi.nlm.nih.gov/pubmed/25241340
テルミサルタンは、グルコースの代謝産物であるメチルグリオキサールを介したアポトーシスを阻害する。これは糖尿病関連心血管疾患に対しるテルミサルタンの有益な効果となりうる。
www.ncbi.nlm.nih.gov/pubmed/18565324
アンジオテンシン受容体アンタゴニストは、アルツハイマー病リスクの低下と関連している。体内および脳内の血圧を調節するレニン – アンジオテンシン系に作用し、脳血流を制御、脳の微小血管系を保護、脳内のプラーク形成を減少させることによってアルツハイマー病発症リスクを遅らせる。
www.alzforum.org/therapeutics/telmisartan
フィブラート系 Fenofibrate
www.ncbi.nlm.nih.gov/pmc/articles/PMC3743740/
ステロイドホルモン
経皮エストラジオール
塩酸ラロキシフェン
エストロゲン受容体モジュレーター
二重盲検プラセボ対照試験 12ヶ月後のADAS-cogスコアに有意な差はなかった。
www.ncbi.nlm.nih.gov/pubmed/26537053
ラロキシフェン120mg/日の投与は、閉経後の女性の認知障害リスクを33%低下させる。60mg/日の投与では群間の有意差はなかった。
ラロキシフェン3ヶ月と短期間の使用では、群間の有意差がADAS-cogで認められた。
影響をおよぼすには12ヶ月以上かかる可能性がある。
特定の認知機能に対する選択的効果が認められる。
有効性の証拠としては弱いものの、ADAS-cogでは5ポイントに相当し、これは臨床的に有用性として認められる範囲に入る。
www.ncbi.nlm.nih.gov/pubmed/15800139
clinicaltrials.gov/ct2/show/NCT00368459
www.medpagetoday.com/neurology/alzheimersdisease/54511
S-エクオール
www.alzforum.org/therapeutics/s-equol
エクオールはヒト尿中に含まれる。Sエクオールはエストロゲン受容体に対して高い親和性をもつ。Rエクオールは不活性。
www.ncbi.nlm.nih.gov/pubmed/15883431
エストロゲンの神経保護効果は、必ずしも抗炎症特性には依存しない。エストロゲン受容体は神経変性疾患の神経保護として潜在的な標的となりうる。
www.ncbi.nlm.nih.gov/pubmed/17785421
アロプレグラノロン
www.alzforum.org/therapeutics/allopregnanolone
DHEA/デヒドロエピアンドロステロン
DGAVP(合成バソプレッシン類似体)
www.ncbi.nlm.nih.gov/pubmed/3247253
キレート
www.ncbi.nlm.nih.gov/pmc/articles/PMC2836834/
www.alzheimersanddementia.com/article/S1552-5260(16)32412-8/fulltext?code=jalz-site
デフェラシロックス/Deferasirox
www.ncbi.nlm.nih.gov/pubmed/26484920
www.alzheimersanddementia.com/article/S1552-5260(16)32412-8/abstract
academic.oup.com/ndt/article/23/10/3356/1854304
デフェリプロン/Deferiprone
www.ncbi.nlm.nih.gov/pubmed/22406440
デフェロキサミン
www.ncbi.nlm.nih.gov/pubmed/20013176
EDTA
ヒートショックプロテイン/ HSP
テプレノン/Teprenone
Geranylgeranylacetone (GGA)
GGAは脳内の他のストレッサーによって誘導されるHSP70の発現を増強する可能性がある。
APP23マウスに経口投与されたGAAは、脳内のアミロイドβモノマーおよびアミロイドβオリゴマーレベルを低下、アミロイドβプラークの沈着を改善した。
GGAの抗アミロイド効果は、HSP70発現のアップレギュレーションを通じて達成することが示唆される。
GGAによるHSP70発現のアップレギュレーションは、アミロイドβの神経毒性が著しく増加している場合において作用する可能性がある。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3788141/
www.jneurosci.org/content/31/14/5225.long
ミトコンドリア保護
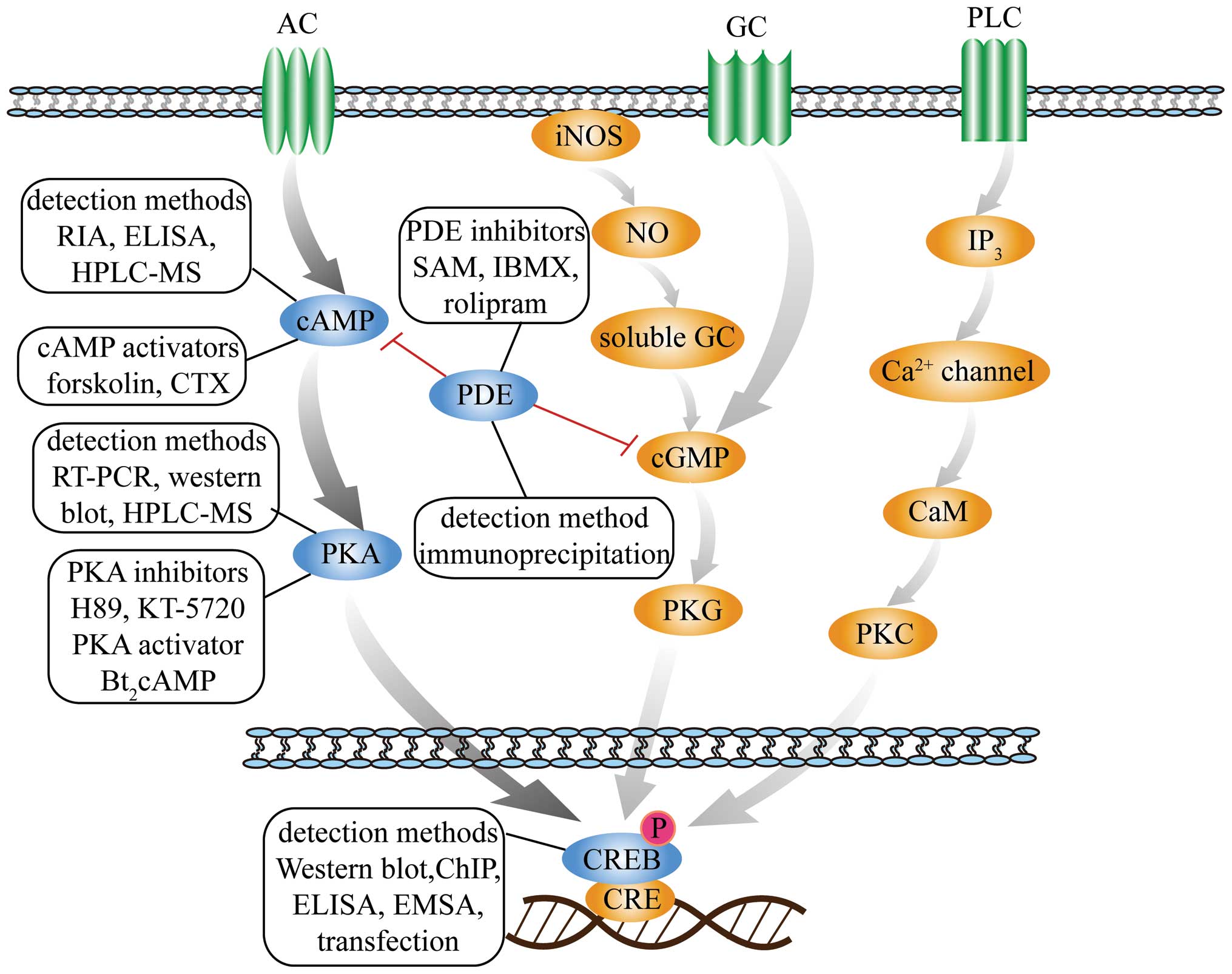
シルデナフィル PDE5阻害剤
PDE5(ホスホジエステラーゼ5)
多彩な薬理作用があり、そのひとつとしてアルツハイマー病疾患への適用も考えられている。イカリインもPDE5阻害作用を有する。
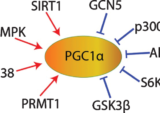
PDE5がcGMP経路の増強を介してCREBのリン酸化を促進、シナプス、学習、記憶障害を改善。アミロイドβの低下とも関連。
www.ncbi.nlm.nih.gov/pubmed/19553447
www.ncbi.nlm.nih.gov/pubmed/23173065
シルデナフィル治療によって、ADマウスの認知障害を完全に逆転させた。
海馬のタウの過剰リン酸化の減少、GSK3βのCDK5活性の抑制が介在。海馬のBDNFレベル、活性調節細胞骨格関連タンパク質(Arc)を増加させた。
www.ncbi.nlm.nih.gov/pubmed/21627640
www.ncbi.nlm.nih.gov/pubmed/23313637
PDE5とHDACの同時阻害は、アルツハイマー病の新しい治療アプローチとして検証されている。
pubs.acs.org/doi/abs/10.1021/acs.jmedchem.6b00908
イデベノン
プラセボ無作為化二重盲検試験 軽度から中等度のアルツハイマー型認知症患者450名へプラセボ、90mg/日、120mg/日に割付12ヶ月間投与。
ADAS総合および二次的変数において、有意な用量依存的改善を示した。
www.ncbi.nlm.nih.gov/pubmed/9850939
プラセボランダム化二重盲検 MMSEスコア12~25点のアルツハイマー病患者500名
イデベノン治療はアルツハイマー病患者の認知低下を遅らせることができない。
www.ncbi.nlm.nih.gov/pubmed/14663031
www.alzforum.org/therapeutics/idebenone
ja.wikipedia.org/wiki/%E3%82%A4%E3%83%87%E3%83%99%E3%83%8E%E3%83%B3
ニコチン性受容体モジュレーター
ニコチン製剤
ドーパミン作動性
セレギリン

メタアナリシス アルツハイマー病患者へのセレギリン投与は、患者にとって臨床的に有意な利益の証拠はない。
日常生活の活動に関して4-6週間統計的な有意差があったが、後の評価で消失した。
www.ncbi.nlm.nih.gov/pubmed/12535396
onlinelibrary.wiley.com/doi/pdf/10.1002/gps.545
メタアナリシスでは、いくつかの認知テストにおいて記憶機能に対する利益を示した。簡易の精神医学的評価尺度および、認知症気分評価尺度の測定では、気分と行動に有益性が認められた。グローバル評価尺度ではセレギリンの効果は認められなかった。
www.selegiline.com/alzheimer.html
ラサギリン
www.ncbi.nlm.nih.gov/pubmed/19110207
アルツハイマー病、Lewy小体型認知症、パーキンソン病の潜在的治療法
www.ncbi.nlm.nih.gov/pmc/articles/PMC3620452/
ラサギリンの主要代謝物であるアミノインダンは神経保護活性をもつことが実証されている。
ラサギリンハPKC-MAPキナーゼ経路を直接活性化することにより神経保護に関与する。
www.ncbi.nlm.nih.gov/pubmed/14732458/
www.ncbi.nlm.nih.gov/pubmed/20919927/
ラサギリンおよびその代謝物アミノインダンによるBcl-2の誘導およびPKCの活性化は、抗アポトーシス作用およびα-セクレターゼの活性化によるAPPのプロセシング能力と密接に関連している可能性が高い。
www.ncbi.nlm.nih.gov/pubmed/12043833/
左半球障害を誘発したマウスへのラサギリン投与は、脳損傷直後の後遺症を軽減させることができる。
www.ncbi.nlm.nih.gov/pubmed/10082192/
ラサギリンのプロパルギル部分のプロパギルアミンがBcl-2、および神経栄養因子グリア細胞系由来神経栄養因子(GDNF)および脳由来神経栄養因子(BDNF)の遺伝子発現レベルを上昇させ、Bax遺伝子発現を低下させることを実証した。APP代謝の調節に関連する神経応答活性示す。
www.ncbi.nlm.nih.gov/pubmed/16148027/
ブレキスピラゾール
ドーパミン受容体D2アゴニスト アリピプラゾールの後継品
www.alzforum.org/therapeutics/brexpiprazole
プラミペキソール
ドーパミンアゴニスト
www.alzforum.org/therapeutics/dexpramipexole
オピオイド
ナルトレキソン
内因性のオピエートは、呼吸抑制することが示されている。そのため、睡眠時無呼吸症候群においてオピエート抑制剤であるナルトレキソンが役割を果たす可能性がある。血液ガスパターンの有意な改善により、総睡眠時間、REM睡眠、の有意な減少を引き起こした。
www.ncbi.nlm.nih.gov/pubmed/10607087
https://alzhacker.com/the-promise-of-low-dose-naltrexone-therapy-4/
GABA作動性
バクロフェン
GABA作動薬
アカンプロサートカルシウム(アルコール依存症治療薬)との組み合わせ療法
www.nature.com/articles/srep07608
ベキサロテン
ミクログリアを増加させてアミロイド班を除去、ニューロン新生の活性、損傷を受けた樹状突起の修復
www.alzforum.org/therapeutics/bexarotene
www.alzforum.org/news/research-news/bexarotene-revisited-improves-mouse-memory-no-effect-plaques
www.uspharmacist.com/article/off-label-use-of-alzheimers-drugs
コリン作動性
アリセプト
軽度認知症障害患者へのドネペジルのオフラベル使用は、特定の遺伝子変異を有する人(ブチリルコリンエステラーゼK遺伝子変異)にとっては認知低下を加速させる可能性がある。
www.sciencedaily.com/releases/2017/02/170225102126.htm
BchE-K変異体 rs1803274(G;G)ノーマル
www.ncbi.nlm.nih.gov/pmc/articles/PMC3196893/
フィゾスチグミン
ムスカリン受容体アゴニスト
NMDA
デキストロメトルファン&キニジン
NMDAの弱いアンタゴニスト&シグマ1受容体のアゴニスト
キニジンはデキストロメトルファンの生体吸収率を上昇させる。
www.alzforum.org/therapeutics/avp-923
リルゾール
グルタミン酸放出および後シナプスグルタミン酸受容体シグナル伝達の両方を阻害
www.alzforum.org/therapeutics/riluzole
SSRI
シタロプラム
シタロプラムはアルツハイマー病の激越症状を治療する。
1日30mgの臨床試験での投与量では、精神バランスの安全性にリスクが伴う。食品医薬品局(FDA)では、高齢患者のシタロプラムの服用は、20mg/日以下を推奨。
www.alzforum.org/news/research-news/citalopram-calms-agitation-alzheimers-carries-risks
シタロプラムの投与は、プラセボグループと比べて、激越症状のあるアルツハイマー病患者の幻覚、夜間行動障害に有益な有意性が認めらた。シタロプラムの総合的な治療効果は、激越、攻撃性の緩和、過敏性、不安、妄想頻度の減少である。
www.ncbi.nlm.nih.gov/pubmed/27032628
www.ncbi.nlm.nih.gov/pubmed/26303700
www.ncbi.nlm.nih.gov/pmc/articles/PMC4086818/
動物モデルではアミロイドβ班を抑制か
dislocon.blog.fc2.com/blog-entry-616.html?sp
フルオキセチン
シグマ受容体への活性を介した認知機能改善効果 ラット
www.ncbi.nlm.nih.gov/pubmed/19114937
アルツハイマー病患者、および重度の強迫観念的症状への治療選択肢としてのフルオキセチン
www.ncbi.nlm.nih.gov/pubmed/14571357
アルツハイマー病患者のうつ病治療におけるフルオキセチン治療は、47%の患者に改善を示したが、プラセボ郡の33%改善と比較して有意には異ならなかった。
www.ncbi.nlm.nih.gov/pubmed/11495397
アリピプラゾール
プラセボ対照無作為化二重盲検試験 合計10mgまたは15mg/日のアリピプラゾールの筋肉内への分割投与は、長期ケアにおけるアルツハイマー病、血管性痴呆、または混合性認知症に伴う激越の治療に対して、安全であり忍容性が良好であった。
www.ncbi.nlm.nih.gov/pubmed/19111849
プラセボ対照無作為化二重盲検 アルツハイマー病および精神病を有する養護老人ホームの滞在者では、アリピプラゾールは精神病症状の治療に特定の利益を与えなかった。
www.ncbi.nlm.nih.gov/pubmed/18591574
プラセボ無作為化二重盲検 アルツハイマー病関連疾患を有する患者への投与2.5mgまたは10mg/日。アリピプラゾール2mgでは有効ではなかったが5mgでは、精神病の症状、激越、全般的な臨床症状の有意な改善を示した。脳血管有害事象の報告
www.ncbi.nlm.nih.gov/pubmed/17974864
www.alzforum.org/therapeutics/aripiprazole
ピマバンセリン
選択的セロトニン(5-HT)2A受容体インバースアゴニスト
www.alzforum.org/therapeutics/pimavanserin
睡眠・メラトニン受容体
ピエロメラチン
マルチに作用する睡眠薬
MT1、MT2、MT3メラトニン受容体、セロトニン5HT1A受容体、5HT1D受容体アゴニスト
www.alzforum.org/therapeutics/piromelatin
サーカディン
メラトニンの徐放剤
www.alzforum.org/therapeutics/circadin
スボレキサント(ベルソムラ)/Suvorexant
ベルソムラはオレキシン受容体阻害薬
(オレキシンAとオレキシンBをオレキシン受容体1とオレキシン受容体2への結合を阻害するデュアルオレキシン受容体アンタゴニスト)
オレキシンは視床下部外側ニューロンによって産生される神経ペプチド。
オレキシンは睡眠と覚醒のサイクルに強く関わっており、オレキシンによって覚醒状態を維持することができる。
中期、後期のアルツハイマー病患者では平均的にオレキシンレベルが高く、夜間の睡眠障害の重篤化に影響を与える。
中等度、後期アルツハイマー病への有効性
睡眠障害を抱えるアルツハイマー病患者への投与 症例研究
平均年齢87歳 女性5人男性1人 投与量15~20mg 週のうち三日間以上で4時間以上眠ることができない患者への投与 4週間後にすべての患者で6時間以上の睡眠を摂ることができた。
www.ncbi.nlm.nih.gov/pubmed/29237271
AD患者への投与試験
アルツハイマー病患者の不眠症治療 臨床試験 2018年10月2日終了予定
clinicaltrials.gov/ct2/show/NCT02750306
用量依存的な副作用
用量依存的に副作用が生じる。高用量(20mg~)では翌日の車の運転などには注意が必要。10mgがより安全な量であるかもしれない。自殺思考リスクの増加と関連
www.cbsnews.com/news/fda-raises-concerns-about-experimental-sleep-aid-suvorexant/
強迫行動・不安への治療効果
オレキシン1受容体は、マウスのエタノール、ニコチン、コカイン、カンナビノイド、モルヒネなどへの探索の繰り返しに関与している。
ストレスによる刺激は、脳辺縁領域でのヒポクレチン/オレキシン分泌を増加させる。
ヒポクレチン/オレキシンの持続的な放出は、高い覚醒と不安の持続ならびにパニック症状の再発へとつながる可能性があることが示唆されている。
ヒポクレチン/オレキシンの不安誘発特性はオレキシン受容体1の関与が示唆されている。
いくつかの研究では、オレキシン1受容体アンタゴニストおよびオレキシン受容体アンタゴニストの両方が、抗不安効果を示さなかった。
齧歯類の実験では、ヒポクレチン/オレキシン受容体アンタゴニストは、基礎不安レベルの変化はさせないが不安レベルが過度に悪化する場合に抗不安特性を示すかもしれない。
www.ncbi.nlm.nih.gov/pubmed/24592206
免疫抑制
シクロスポリンA
seikagaku.jbsoc.or.jp/10.14952/SEIKAGAKU.2015.870517/data/
ラット海馬CA1領域の神経細胞損傷を改善。
www.ncbi.nlm.nih.gov/pubmed/9125440/
www.ncbi.nlm.nih.gov/pubmed/8719269/
www.ncbi.nlm.nih.gov/pubmed/9813336/
プラセボ対照無作為化試験 重度の脳損傷患者へシクロスポリン1.25-5mg/kg/日 6ヶ月経過後シクロスポリン投与群では有意に良好な改善結果が認められた。
www.ncbi.nlm.nih.gov/pubmed/18826358/
外傷性脳損傷後の初期段階でのシクロスポリンA投与(5mg/kg)は、高い細胞外のグルコースとピルビン酸塩に寄与し、平均動脈圧と脳潅流圧の有意な増加と関連。これらは神経保護効果に寄与する可能性がある。
www.ncbi.nlm.nih.gov/pubmed/18781275/
ラパマイシン/シロリムス
タクロリムス
ダプソン
海馬・神経成長因子増強
セレブロリシン
NGF模倣物
その他
アシトレチン/Acitretin
乾癬薬
アルツハイマー病患者の脊髄液内のAPPs-αレベルを増加。
www.ncbi.nlm.nih.gov/pubmed/25344383
ディメボン
アレルギー性鼻炎として使われていた非選択的抗ヒスタミン薬
www.alzforum.org/therapeutics/dimebon
低親和性NMDA受容体アンタゴニスト
14のオープンラベル試験で潜在的有効性が実証される。作用機序は明確ではなくフェーズ3で失敗した理由とされている。ディメボンの臨床効果は、ヒスタミンH1とセロトニン5-HT6受容体の阻害に起因する可能性。
www.ncbi.nlm.nih.gov/pubmed/21031168
ランダム化比較対象試験 軽度から中等度のアルツハイマー病患者155人 ディメボン(20mg×3回/日)を投与された患者ではADAS-cogを有意に改善。ディメボンは耐用性が良好。
www.ncbi.nlm.nih.gov/pubmed/18640457
ミトコンドリアへの作用としては弱い。複数の神経伝達物質受容体へ作用し、プロコリン作動性である可能性。
アルツハイマー病患者のNPIスコアの改善がディメボンの重要な唯一の有用性。
www.ncbi.nlm.nih.gov/pubmed/23948924
クリオキノール/Clioquinol
銅イオンと亜鉛イオンのキレート形成により認知機能低下を抑制
ja.wikipedia.org/wiki/%E3%82%AF%E3%83%AA%E3%82%AA%E3%82%AD%E3%83%8E%E3%83%BC%E3%83%AB
ADマウスへの経口投与で、PBT2は血液脳関門を通過し、可溶性アミロイドβを著しく低下させ、認知能力を改善した。
www.ncbi.nlm.nih.gov/pubmed?Db=pubmed&Cmd=ShowDetailView&TermToSearch=18614028
PBT2(ヒドロキシキノリン)
銅および亜鉛イオンを細胞に移動させることで、細胞外の濃度を低下させることで、金属介在性のアミロイドβ凝集を減少させる。銅-亜鉛イオンのホメオスタシス回復
www.alzforum.org/therapeutics/pbt2
PBT2 250mg投与、心理テストの2つの項目でプラセボ郡と比べ有意な改善が認められたが、期間は12週間であった。
www.ncbi.nlm.nih.gov/pubmed/18672400
メリッサ/ Melissa officinalis
www.ncbi.nlm.nih.gov/pmc/articles/PMC1738567/
www.ncbi.nlm.nih.gov/pubmed/12810768
www.ncbi.nlm.nih.gov/pubmed/21335973
www.ncbi.nlm.nih.gov/pubmed/27840509
www.ncbi.nlm.nih.gov/pubmed/28042540
ベルナクリン/velnacrine
www.ncbi.nlm.nih.gov/pubmed/15106259
レコゾタン/lecozotan
選択的5HT1A受容体のアンタゴニスト
en.wikipedia.org/wiki/Lecozotan
海馬歯状回のグルタミン酸およびアセチルコリンを有意に増強
www.ncbi.nlm.nih.gov/pubmed/15951399
www.ncbi.nlm.nih.gov/pmc/articles/PMC2948028/
イソプロニクリン/ispronicline
ニコリン性アセチルコリン受容体パーシャルアゴニスト
www.alzforum.org/therapeutics/azd3480
アンパカインズ/Ampakines
SunifiramとUnifiramの混合剤
AMPA受容体に強力に作用する神経変性疾患の潜在的治療薬
受容体の刺激により脳の伝達能力を高めシナプス接続を形成する。覚醒系
en.wikipedia.org/wiki/Ampakine
ベシピリジン/besipiridine
コリン作動性 アドレナリン作動性
www.ncbi.nlm.nih.gov/pubmed/8624122
D-サイクロセリン
抗結核性抗生物質
GSK阻害剤
その他の神経保護剤
脳卒中に対する神経保護 現状と今後の展望
グルタミン酸、グルタミン酸受容体活性化刺激毒性、細胞へのCa2+の流入、ミトコンドリアの機能不全、多くの細胞内酵素の活性化、フリーラジカル産生、一酸化窒素産生、アポトーシスなどへの標的とした1000以上の神経保護療法試されたが、残念ながら200回を超える臨床試験で、すべての試みが臨床的には失敗した。
現在臨床試験中の最も有望な神経保護戦略のひとつは、低体温、すなわち脳の温度を低下させる治療方法である。
考えられている作用機序はフリーラジカルの形成防止、細胞の代謝を遅らせる、グルタミン酸放出を減少、プロテインキナーゼCの活性など。
候補
- 低体温(脳の酸素代謝、シナプス抑制因子を減らす)
- 経頭蓋レーザー治療(ミトコンドリア活性)
- PG-2(中国漢方薬、抗酸化と抗炎症)
- THR-18(合成プラスミノーゲン活性化因子の阻害)
- NXY-059(フリーラジカルを補足)
- エプセレン (抗アポトーシス、酸化的損傷への保護)
- エダラボン(ヒドロキシラジカルのスカベンジャー)
- 硫酸マグネシウム(NMDA受容体興奮毒性の阻害)
- スタチン(抗酸化、抗炎症、NO利用による血流改善)
- DP-b99(二価金属イオンキレーター)
- ミノサイクリン(抗炎症と抗アポトーシス)
- アルブミン(抗酸化、血液の希釈剤、血流増強)
- シクロスポリンA(抗炎症、抗興奮毒性)
- デフェロキサミン(鉄キレート剤、酸化防止)
- GM602(抗アポトーシス、抗炎症)
これからの治療アプローチ候補
・脳組織のリモデリングによる神経学的回復促進治療
・異なる作用機序の薬剤の相乗効果を狙った併用療法アプローチ(NMDA受容体アンタゴニストと神経保護剤とrtPAの組み合わせ、フリーラジカルスカベンジャーとマトリックスメタロプロテアーゼ阻害剤の組み合わせなど)
・生理学的な活性酸素種(ROS)と病理学的な活性酸素種を区別した取り組み
・活性酸素種を特定しそれらを遮断するアプローチ。NOX阻害剤
・NMDA受容体関連タンパク質PSD-95の阻害
・低酸素誘導因子(HIF)の活性化と安定化
・虚血性脳卒中後の炎症因子を標的(IL-1受容体アンタゴニストの投与)
www.ncbi.nlm.nih.gov/pmc/articles/PMC3472773/
腎不全患者のための神経保護 過去、現在そして未来
www.ncbi.nlm.nih.gov/pmc/articles/PMC2631228/
2007年 アルツハイマー病の薬理学的治療
www.ncbi.nlm.nih.gov/pmc/articles/PMC2656293/
アルツハイマー病の創薬、われわれは今どこにいるのか、そしてどこへ向かうのか?
www.ncbi.nlm.nih.gov/pmc/articles/PMC2948028/
2016年 アルツハイマー病治療におけるタウ標的と薬物の臨床開発
www.ncbi.nlm.nih.gov/pmc/articles/PMC4939203/