Long COVID symptoms and duration in SARS-CoV-2 positive children — a nationwide cohort study
www.ncbi.nlm.nih.gov/labs/pmc/articles/PMC8742700/
2022 Jan 9 : 1-11.
概要
急性COVID-19は、ほとんどの子供が軽度の経過をたどる。小児のSARS-CoV-2感染症からの長期的な回復を評価した研究は、サンプル数が少なく、主に非対照の研究しかない。本研究の目的は、小児における「Long-COVID」の症状と期間を評価することである。RT-PCR法でSARS-CoV-2感染が確認された0~17歳の小児37,522人(回答率44.9%)と、対照群の小児78,037人(回答率21.3%)を対象とした全国規模のコホート研究。2021年3月24日から5月9日まで、すべての子どもに電子アンケートを送付した。4週間以上続く症状は、SARS-CoV-2感染児童と対照群の両方に共通していた。しかし,6~17歳のSARS-CoV-2感染児童は,対照群よりも頻繁に症状を報告していた(パーセント差0.8%).就学前の子供で最も多く報告された症状は、疲労感 リスク差(RD)0.05(CI 0.04-0.06)嗅覚障害 RD 0.01(CI 0.01-0.01)味覚障害 RD 0.01(CI 0.01-0.02)筋力低下 RD 0.01(CI 0.00-0.01)であった。学童では、嗅覚障害 RD 0.12 (CI 0.12-0.13)、味覚障害 RD 0.10 (CI 0.09-0.10)、疲労感 RD 0.05 (CI 0.05-0.06)、呼吸器障害 RD 0.01 (CI 0.00-0.01)が最も顕著であった。 06)呼吸器系の問題 RD 0.03(CI 0.03-0.04)めまい RD 0.02(CI 0.02-0.03)筋力低下 RD 0.02(CI 0.01-0.02)胸痛 RD 0.01(CI 0.01-0.01)であった。対照群の子供たちは、SARS-CoV-2感染者に比べて、集中力の低下、頭痛、筋肉痛、関節痛、咳、吐き気、下痢、発熱などの症状が有意に多かった。ほとんどの子どもの「Long-COVID」症状は1~5カ月以内に解消した。
結論としては 小児のLong-COVIDはまれで、主に短期間で発症する。
知られていること
- 成人における「Long-COVID」の報告が増えている。
- 子供のCOVID-19からの長期的な回復を評価した研究はわずかであり、すべての研究に共通しているのは、サンプル数が少なく(対象となる子供の数の中央値は330人)ほとんどの研究では対照群を設けていないことである。
新しい情報
- SARS-CoV-2 陽性の小児の 0.8%が、対照群と比較して 4 週間以上続く症状(”Long-COVID”)を報告した。
- 最も多く見られた「Long-COVID」症状は、疲労、嗅覚・味覚の喪失、めまい、筋力低下、胸痛、呼吸器系の問題であった。
- これらの「Long-COVID」症状は、社会的制約による心理的な後遺症とは考えられない。
- また、集中力の低下、頭痛、筋肉痛、関節痛、吐き気などの症状は「Long-COVID」症状ではない。
- ほとんどの場合、「Long-COVID」の症状は1~5ヶ月以内に消失する。
キーワード
SARS-CoV-2,子供、COVID-19,Long-COVID、長期的な回復
概要
成人と比較して、小児は急性COVID-19の経過が軽度である[1, 2]。さらに、SARS-CoV-2の有病率は小児の方が低い。米国、イタリア、デンマークでは、小児患者の割合はそれぞれ11.8%(0~17歳)15.6%(0~18歳)10%(0~19歳)となっている[3-5]。デンマークでは、COVID-19を発症した小児のうち、入院を必要としたのはわずか0.08%であった[6]。世界的に見ても、小児のCOVID-19による死亡は依然として稀で、人口10万人あたり0.17人となっており、平年の全原因による推定死亡率の0.48%を占めている[7]。
SARS-CoV-2感染の累積発生率が増加するにつれ、急性感染後に多臓器症状が持続することへの懸念が高まっている。Long-COVIDは、急性COVID-19の後に継続または発症し、他の診断では説明できない兆候や症状を表すために使用される。現在のところ、この症候群の定義や期間について、明確な合意はない。NICEガイドラインによると、「Long-COVID」には、進行中の症候性COVID-19(急性COVID-19後4~12週間)とPost-COVID-19症候群(急性COVID-19後12週間以上)の両方が含まれる[8]。
成人における「Long-COVID」に関する報告が増えている[2, 9-12]。しかし、小児におけるCOVID-19からの長期的な回復を評価した研究はわずかしかない[13-26]。すべての研究に共通しているのは、サンプル数が少なく(対象となる子どもの数の中央値は330人)ほとんどの研究では対照群がないことである。これらの研究では、不眠、呼吸器症状、鼻づまり、疲労、筋肉や関節の痛み、集中力の低下、嗅覚や味覚の喪失など、COVID-19の急性期後の症状を4~66%の子どもが経験したと報告している[13~26]。対照群を含む大規模な小児科研究が行われていないことから、小児および青年における「Long-COVID」を定量化し、特徴づけるためには、さらなる疫学的データ収集が必要である。
本研究の目的は、SARS-CoV-2に感染した18歳未満の小児の全国規模のコホートにおいて、「Long-COVID」の症状と期間を記録することである。また、SARS-CoV-2感染と症状の関連性を評価するために、SARS-CoV-2の陽性反応が出ていない小児の対照群を加えた。
材料と方法
ポリメラーゼ連鎖反応(RT-PCR)によりSARS-CoV-2感染が確認された0~17歳の小児37,522人と、SARS-CoV-2の陽性反応が確認されていない無作為に選ばれた小児78,037人を対象に、全国規模のコホート研究を実施した。コビッドワクチンの接種を受けた子どもはいなかった。本研究は,デンマーク保健データ局(The Danish Health Data Authority)の承認を受け,中央デンマーク地域で登録された(# 1-16-02-621-20).デンマークの法律では、倫理的な承認は必要なかった。
出生時または移住時に,すべてのデンマーク国民には,デンマーク市民人口登録簿に登録された固有の個人識別番号が割り当てられる [27].この番号は,すべての医療関係者に使用され,デンマーク国内のレジスター間の機密保持が容易になっている。本研究では,Danish Health Data Authorityが,デンマークの全児童の社会保障番号を全国微生物データベースにリンクさせた。この連結により,2020年1月27日から 2021年3月19日までの間のいずれかの時点で,RT-PCR法によりSARS-CoV-2感染が確認された0~17歳のデンマーク人小児の完全なリストが作成された。
2021年3月24日から5月9日まで、SARS-CoV-2感染が確認されたすべての子どもと対照群に、電子アンケート(REDCap)を送付した。この期間中、質問票は7~10日後のリマインダーを含めて2回送付された。両グループの子どもたちの回答期間は4週間だった。
SARS-CoV-2陽性グループは、社会保障番号に連動した安全でプライベートなデジタルポスト(e-boks)に両親が直接アンケートを送った。15歳以上の青少年は、法的権利のため、親のサポートを受けて記入するようアドバイスを受けながら、自らアンケートを受け取った。調査票は,0〜5歳の子ども6.674人と、6〜17歳の子ども30.848人に送付された。
対照群として、デンマークの5つの自治体(Aalborg, Herning, Aarhus, Randers, Frederiksberg)の公立学校またはデイケアに通う0-17歳の子どもの親にアンケートを送付した。保護者は、学校またはデイケアのオンラインコミュニケーションプラットフォームによって、直接アンケートを受け取った。45,240人の学童(6-17歳)と32,797人の保育園児(0-5歳)がアンケートを受け取った。SARS-CoV-2の検査で陽性となった子どもを対照群から除外するため、SARS-CoV-2感染の既往が最初の質問で取り上げられ、確認された場合は残りの質問項目を終了した。
両グループの質問票は、人口統計学的情報、慢性疾患の既往歴、投薬、4週間以上続く症状に関する同じ質問で構成されている(S1)。また,9歳以上の子どもについては,WHO-5の幸福度指標の質問が含まれている[28]。
SARS-CoV-2グループと対照グループを比較するために,子どもたちを就学前の0~5歳と学童の6~17歳の2つの年齢グループに分け,リスクの違いを推定した(RD)。SARS-CoV-2陽性の子どもと対照群の子どもとの比較は、「Long-COVID」の症状と、学校閉鎖や社会的距離といったパンデミックに起因する症状とを区別するために行われた。また、9歳以上の子供の幸福度をWHO-5の幸福度指標の質問で評価し、症状が幸福感の低下を反映しているかどうか、SARS-CoV-2感染の直接的な影響ではないかどうかを分析した。
SARS-CoV-2感染が確認されてからアンケートに回答するまでのフォローアップ期間は、子供によって異なる。継続的に報告された症状の期間については、SARS-CoV-2感染が確認された日とアンケート回答日の差を計算することで対応した。
統計解析
統計解析には,StataMP 17を使用した。
SARS-CoV-2の関数として、それぞれの長い共感症状のリスク差(RD)をパーセンテージポイントと95%信頼区間で推定するために、二項回帰を行った。
2つのグループの平均値の間に有意差があるかどうかを判断するために、不等分散の対のない2サンプルt検定を用いた(α=0.05)。2つのカテゴリー変数が独立しているかどうかの検定には,Pearson Chi-square 検定を用いた。
結果
SARS-CoV-2感染児童37,522人のうち、合計16,836人(44.9%)から回答が得られた(0~5歳44.6%、6~17歳39.1%)。対照群では、合計16,620人(21.3%)がアンケートに回答した(0~5歳21%、6~17歳18.3%)。
0-5歳児の平均年齢は、SARS-CoV-2陽性者が2.7歳、対照群が2.8歳で、平均差は-0.1歳(CI-0.17~-0.02)。6~17歳の子供の平均年齢は、SARS-CoV-2陽性者が12.0歳、対照群が10.5歳で、平均差は1.5歳(CI 1.41~1.59)。
質問票は、症状、年齢、子どもの性別に関するデータが欠落している場合には、解析から除外された。質問票の回答時に、SARS-CoV-2のPCR検査陽性の日から18歳になっていた青年もいたが、これらは分析から除外した。また、PCR検査から4週間以内の回答者も、「Long-COVID」の分析から除外した。調査の対象となったのは、SARS-CoV-2陽性の子ども15.041人と対照群の子ども15.080人である(図1)。
図1 研究参加者のCONSORTフローチャート

年齢にもよるが、アンケートに回答したSARS-CoV-2感染が確認された小児の12~51%が、SARS-CoV-2感染と診断されてから4週間以上後に症状を経験していた(図2)。症状を経験したSARS-CoV-2感染者の数は、年齢が上がるにつれて増加し(図2)就学前の子供439人/2.976人(14.8%)対、学童3.374人/12.065人(28%)p=0.000となった。主な症状は、疲労感、嗅覚・味覚の低下、頭痛、集中力の低下などであった(図3)。
図2 4週間以上続く症状の有病率
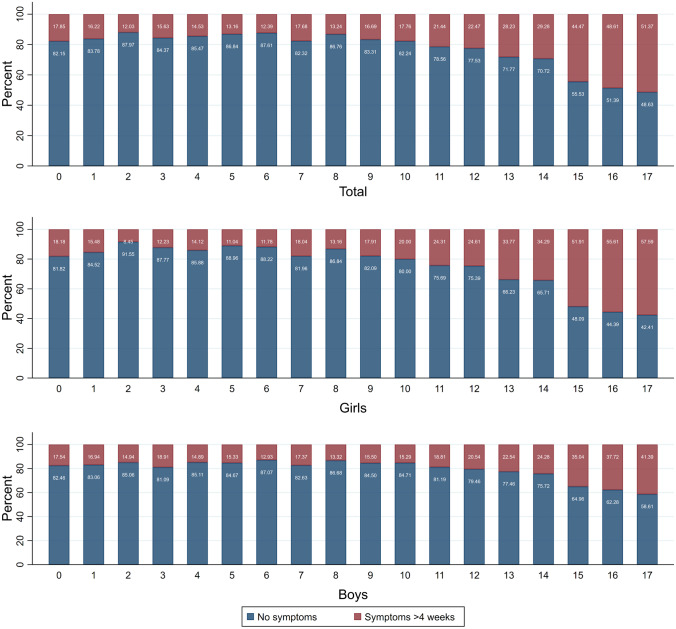
SARS-CoV-2 に感染した小児のうち,少なくとも 1 つの症状が 4 週間以上続いたと報告した者(赤棒)と,症状がなかったと報告した者(青棒)の割合。データは、SARS-CoV-2感染児童の総人口(上段)と男女別(女子、中段、男子、下段)で示した。
図3 SARS-CoV-2感染児童(上段)と対照群(下段)が報告した4週間以上持続する症状を示すヒートマップ
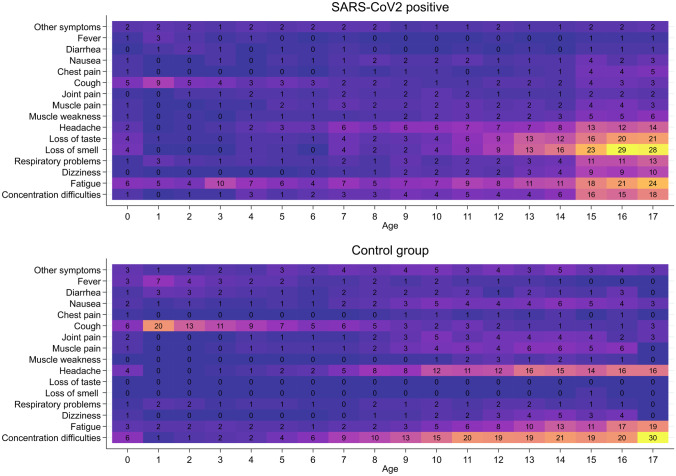
数字は、特定の症状を報告した子供の割合を1歳ごとに示したもの
アンケートに回答した対照群の子どものうち、15~38%(年齢による)が4週間以上続く症状を経験しており、未就学児は6.832人中1.201人(17.6%)学童は8.248人中2.245人(27.2%)であった;p=0.000。対照群では、集中力の低下、咳、頭痛、疲労感などが主な症状として報告された(図3)。
両群とも5%の子どもが、主に呼吸器系の診断を受けた慢性疾患を患っていた(慢性疾患を患っていたSARS-CoV-2感染者の51%が呼吸器系の診断を受けていたと報告されている)。
0~5歳の年齢層では、SARS-CoV-2陽性の子供に比べ、対照群では4週間以上続く症状を訴える子供が多かった(14.8%対17.6%、p=0.001,差-2.8%)。6~17歳の年齢層では、SARS-CoV-2陽性の子どもが4週間以上続く症状を訴えた割合は、対照群の子どもよりも0.8%多かった(28%対27.2%、p=0.020,差は0.8%)。
また、SARS-CoV-2陽性児は、対照群の児に比べて症状の負担が大きかった(p < 0.0001)。考えると、4週間以上続く症状を報告したSARS-CoV-2陽性児3813人のうち、1つの症状を報告したのは1323人(34.7%)2つの症状を報告したのは1095人(28.7%)3つ以上の症状を報告したのは1395人(36.6%)であった。対照群で4週間以上続く症状を報告した3446人のうち、1870人(54.3%)が1つの症状を、794人(23%)が2つの症状を、782人(22.7%)が3つ以上の症状を報告した。
一部の症状はSARS-CoV-2感染児に多く見られたが、他の症状は対照群の子どもたちに多かった。SARS-CoV-2感染の就学前児童では、疲労感RD 0.05(CI 0.04-0.06)嗅覚障害RD 0.01(CI 0.01-0.01)味覚障害RD 0.01(CI 0.01-0.02)筋力低下RD 0.01(CI 0.0-0.01)の頻度が高かった(図4およびS2)。一方、SARS-CoV-2感染の学童では、嗅覚障害RD 0.12(CI 0.12-0.13)味覚障害RD 0.10(CI 0.09-0.10)疲労感RD 0.05(CI 0.05-0.06)が多く見られた。呼吸器系疾患 RD 0.03(CI 0.03-0.04)、めまい RD 0.02(CI 0.02-0.03)、筋力低下 RD 0.02(CI 0.01-0.02)、胸痛 RD 0.01(CI 0.01-0.01)では、リスクの差は小さかったが、依然として有意であった(図4およびS2)。
図4 SARS-CoV-2感染児と対照群における症状の有病率の比較を、リスク差(RD)95%信頼区間、p値で示した
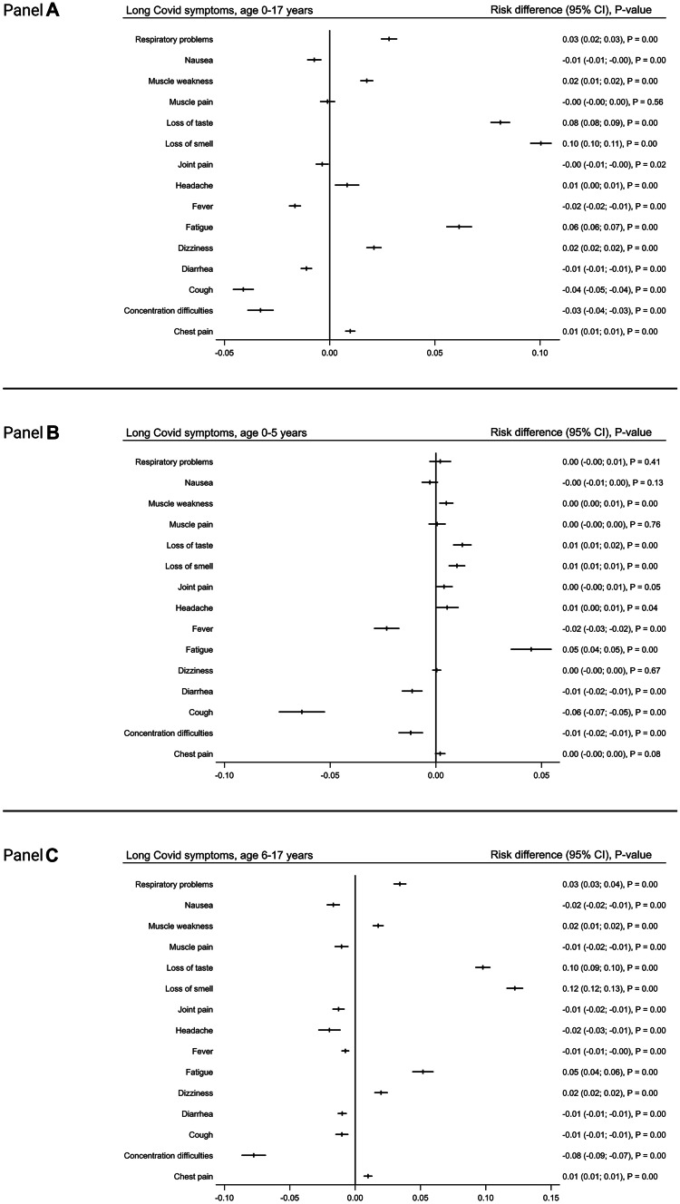
パネルA:0-17歳の子供の比較。パネルB:0-5歳の未就学児のサブグループ比較。パネルC:6-17歳の学童のサブグループの比較
対照群の0-5歳児は、SARS-CoV-2感染群の子どもに比べて、咳、発熱、集中力低下、下痢が有意に多かった。これに対応して、6~17歳の対照群は、SARS-CoV-2陽性群に比べて、集中力低下、頭痛、吐き気、筋肉痛、関節痛、咳、下痢、発熱を起こしやすかった(図4,S2)。
症状が4週間以上続いたと報告したSARS-CoV-2感染児童の7%は、急性感染時には無症状であった。
年齢にもよるが、最低でも54~75%の小児が1~5カ月以内に症状を消失した(図5,パネルA)。SARS-CoV-2感染者の39%は、アンケート回答日時点で症状が継続していると回答した。症状が継続していると回答した子供たちのフォローアップ期間を図5のパネルBに示す。
図5 RT-PCR法によるSARS-CoV-2陽性反応が出た日からアンケート回答日までの症状の持続時間(1歳階級別)
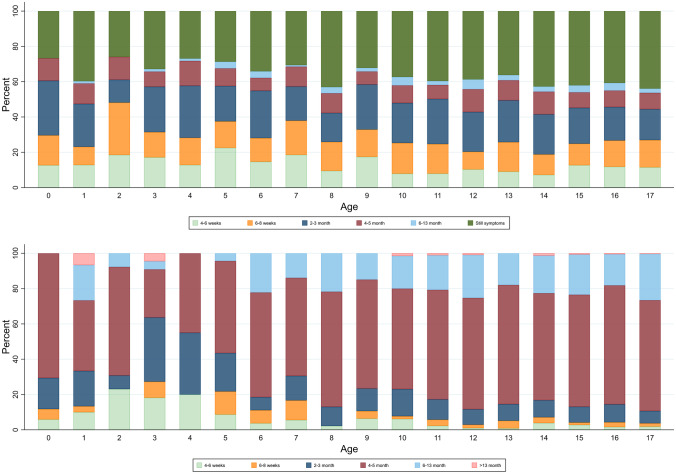
上段の濃い緑色の棒グラフは、アンケート記入時に症状が治まっていないと答えた子供の割合を示している。下の図は、これらの子どもたちの症状が続いている期間を示している。
対照群のアンケート回答者とSARS-CoV-2感染児を比較したところ、SARS-CoV-2感染児は対照群に比べて幸福感が高く、WHOスコアの差は4(CI 3.5-4.8)であった。症状が4週間以上続いた両群の小児は,同じ群で症状がなかったSARS-CoV-2陽性の小児に比べて幸福感が低かった。SARS-CoV-2陽性:WHOスコアの差12(CI 11.1-12.8)対照群。WHOスコア差17.2(CI 16.2-18.3)。
考察
我々の知る限り、本研究は、RT-PCRで検証されたSARS-COV-2感染児と、無作為に選ばれたSARS-CoV-2陽性ではない小児の対照群とを比較した全国規模のコホートで、「Long-COVID」の症状と期間を記録した最大の研究である。
COVID-19パンデミックでは、SARS-CoV-2の感染を減らすために、政府による介入が導入された。検疫体制、手指衛生の強化、学校や保育園の閉鎖、スポーツやレジャー活動の中止、社会的な距離の取り方など、様々な介入が行われている。これらの社会的影響が子どもの精神的健康に及ぼす悪影響について、報告書は懸念を示している[29]。この点を考慮すると、SARS-CoV-2感染経験のある子供たちが報告した「Long-COVID」症状を、背景にいる人々を代表するコホートと比較することは非常に重要だ。対照群を持たない小児集団で「Long-COVID」を記述すると、「Long-COVID」症状が過大評価される可能性があるからである。
今回の研究では、SARS-CoV-2感染群と対照群に含まれる小児は、年齢、性別、既往の慢性疾患に違いはなかった。SARS-CoV-2陽性の子どもと対照群の子どもは、4週間以上続く症状が高い頻度で報告された。これらの症状は、SARS-CoV-2感染やSARS-CoV-2以外の感染に起因する可能性もあれば、パンデミックの心理的・社会的影響を反映した症状である可能性もある。残念ながら、今回の研究では、対象となった子どもたちの他のウイルス感染症に関するデータはない。しかし、SARS-CoV-2以外のウイルス感染症は、2つのグループに均等に分布していると考えられる。我々の分析によると、SARS-CoV-2陽性で4週間以上症状が続く子供は、SARS-CoV-2の検査を受けたことがない4週間以上の症状を持つ子供に比べて、高い幸福感を報告した。このように、SARS-CoV-2陽性群の症状の有病率は、社会的制約による心理的後遺症とは言い切れない。一方、対照群ではWHO-5スコアが低く、症状の有病率が高いことから、社会的制約やパンデミックによる心理的影響を反映しているのではないかと推測される。
SARS-CoV-2陽性群の6~17歳の小児では、4週間以上持続する症状が多く報告されている(28.0%)にもかかわらず、対照群の対応する症状の有病率(27.2%)を差し引くと、0.8%の差しか残っていない。この0.8%という数字は、SARS-CoV-2陽性の子供たちの本当の「Long-COVID」の有病率をより信頼性高く見積もっているのではないかと推測される。しかし、この数学的計算では、両群間で報告された症状の種類や症状の重さの違いが考慮されていないことに留意する必要がある。これまでの小児科研究では、SARS-CoV-2陽性児の8~58%が「Long-COVID」症状を経験していることがわかっている[13, 15-17, 21-26]。しかし、これらの研究には対照群が含まれていなかったため、「Long-COVID」の有病率が過大評価される危険性があった。3つの研究では対照群を含み、「Long-COVID」症状の有病率がはるかに低いことが記録されている[19, 20, 30]。対照群と症例群で4週間以上続く症状は、それぞれ1.7%対4.6%[30],0.9%対4.4%[19]、53.4%対66.5%[20]と報告されている。これらの「Long-COVID」の低い有病率は、今回の結果と同程度のものである。
先行研究[19, 23, 26]と同様に、本研究では症状の年齢分布が異なっており、高学年の学童は低学年や未就学児に比べて罹患率が高いことが示された。
SARS-CoV-2感染者と対照群の回答を比較したところ、統計的に有意な「Long-COVID」症状として最もよく見られたのは、疲労、嗅覚障害、味覚障害であり、さらに筋力低下、胸の痛み、めまい、呼吸器系の問題が見られた。これらの症状は、他の研究でも「Long-COVID」症状としてよく報告されている[31]。特に疲労、嗅覚・味覚の喪失 [32] は、SARS-CoV-2 陽性の子供に頻繁に見られる症状として報告されている。疲労は、罹患期間が4週間を超えるSARS-CoV-2陽性小児の最大85%で報告されている[14-16, 19, 20, 22]。一方、エプスタイン・バー・ウイルス感染後の疲労の持続期間の中央値は15.5日である[33]。
以前、非対照試験において、集中力低下、頭痛、筋肉痛、関節痛、咳、吐き気、下痢、発熱が、小児のSARS-CoV-2感染症の「Long-COVID」症状として報告されている[24, 34]。しかし,これらの症状は対照群のほうが統計的に有意であることがわかった。また,我々の研究では,対照群の子どもはSARS-CoV-2陽性の子どもに比べてWHO-5スコアが低かったことが記録されている。したがって、集中力の低下、頭痛、筋肉痛、関節痛、吐き気などは、パンデミックの社会的影響が子どもの心身の健康に及ぼす悪影響を反映した症状ではないかと考える必要がある。また、無作為に抽出された対照群において、発熱の頻度が高いと報告された理由は、具体的な体温評価の方法や付随する症状に関する質問が含まれていないため、推測するしかない。一般的に、パンデミックの最初の年は、呼吸器合胞体ウイルスやインフルエンザウイルスなどの発症率の高い感染症の発症率が驚くほど低いことが知られている[35, 36]。したがって、発熱の発生率も低いと予想された。
「Long-COVID」症状の持続時間は、子どもと家族にとって意味のある重要な問題である。今回の小児コホートでは、ほとんどの子どもが最長でも1~5ヵ月で回復した。これまでの小児科研究では、回復までの期間は2週間~3か月とされていた[15, 19, 24]。
この観察研究には大きな限界がある。まず,本研究の質問票は,より大規模なパイロット研究で検証されていない.さらに,データは参加者の親や自己の症状を遡って報告したものであり,想起バイアスのリスクがある.しかし,SARS-CoV-2は社会的に注目されている感染症である。しかし、SARS-CoV-2は社会的に注目されている感染症であり、参加者は感染時に症状を強く意識していた可能性があるため、想起バイアスは少ないと考えられる。しかし,対照群やSARS-CoV-2感染群では,症状の軽い子どもや無症状の子どもに比べて,症状を経験した子どもの方がアンケートへの回答意欲が高かったことも推測される。そのため、選択バイアスがかかり、報告された症状が過大評価される可能性がある。また、本研究では、非症候性の対照群が過小評価される非応答バイアスが生じる可能性もある。質問票は配布され、オンラインで回答しなければならなかった。このため、社会経済的背景の高い参加者が選ばれる可能性があり、これらの参加者は疾患後の予後不良のリスクが低いと考えられる。
次に、対照群には、検査を受けずにSARS-CoV-2に感染したことのある子どもが含まれている可能性がある。これは、子どもたちが急性COVID-19の症状を持たない、またはほとんど持たないためのリスクである。以前、SARS-CoV-2陽性の子どもの25~36%が無症状であることが報告されている[24, 37]。さらに、親は、侵襲的で不快な手順のために、子どもに検査を受けさせることに抵抗を感じるかもしれない。対照群の子どもたちは、SARS-CoV-2の検査で陽性になったことはない。それにもかかわらず、血清有病率のデータは、小児人口における対応するPCR結果の2~3倍の感染率を示唆している[38]。2021年3月、無作為に選ばれた12~18歳の子供530人を対象としたデンマーク全国規模の血清有病率調査では、8.1%がSARS-CoV-2 IgG陽性であったことが記録されている(国内未発表データ)。12歳以下の子供も8.1%の血清有病率を占めていることが推測される。対照群にSARS-CoV-2感染歴のある子どもがいる可能性があるため、「Long-COVID」の症状を過小評価することになる。
第三に、質問票に回答した子どもの数は、SARS-CoV-2陽性の子どもの方が対照群よりも多かった(44.9%対21.3%)。SARS-CoV-2感染歴のある子どもたちの回答率が高いのは、これらの子どもたちとその家族が「Long-COVID」の症状に対する認識が高く、SARS-CoV-2の急性期後遺症に関する知識を欲している可能性があるからである。この問題は、「Long-COVID」の過大評価につながる可能性がある。しかし、どちらのグループでも、アンケートに答えた子どもたちの年齢分布は同じであった。
本研究の強みは、主にサンプルサイズが大きいことと、対照群が含まれていることである。さらに,デンマーク保健データ局は全国をカバーしており,デンマーク国民は全員,税金で賄われる国民健康保険に加入している。また,デンマークではSARS-CoV-2のRT-PCR検査が無料で受けられるため,選択バイアスを最小限に抑えることができる。SARS-CoV-2陽性の子どもたちの感染状況は、全国的に検証されたRT-PCRによって確認されており、感染状況の大きな誤分類はない。さらに,SARS-CoV-2検査の結果は,デンマーク市民人口登録簿[27]と国の微生物学データベースに登録された固有の個人識別番号にリンクされており,デンマークでパンデミックが始まってから 2021年3月19日までの,18歳以下のSARS-CoV-2感染児童の完全なコホートとなっている.
対照群は全国規模ではなく、デンマーク国内に広く点在する大都市と農村部を含む5つの自治体から無作為に選ばれた0~17歳の子どもたちで構成されている。そのため、この対照群はデンマークの一般的な子どもたちを代表していると考えられる。以上のように、本研究の結果は一般化しやすいものとなっている。しかし,主観的な回答を含む質問票に基づいた観察研究であり,子どもたちの客観的な検査を行っていないことから,パズルの一片しか得られないことを考慮することが重要だ。小児集団における「Long-COVID」に関する知識を深めるためには、さらなる研究が必要である。
結論として、今回の研究は、SARS-CoV-2陽性の小児における「Long-COVID」の症状と期間に関する研究としては、対照群を含めても最大規模のものである。本研究は、小児における「Long-COVID」の新たな証拠となり、「Long-COVID」は主に年長の学童に見られることが証明された。SARS-CoV-2感染児童において、長期にわたる症状が報告された割合が高い(12~51%)にもかかわらず、「Long-COVID」の真の有病率はもっと低く,0.8%程度であると思われる。最も一般的な「Long-COVID」症状は、疲労感、嗅覚・味覚の喪失、めまい、筋力低下、胸痛、呼吸器系の問題である。これらの症状は、社会的制約による心理的な後遺症とは言えない。また、集中力の低下、頭痛、筋肉痛、関節痛、吐き気などの症状は、SARS-CoV-2感染とは別の要因が考えられる。ほとんどの場合、「Long-COVID」の症状は1〜5ヶ月以内に解消する。
資金調達
1844年に設立された財団です。財団は、研究デザイン、データの収集、データの分析と解釈、報告書の作成、および論文発表の決定には一切関与していません。
宣言文
透明性に関する声明
主著者は、本稿が報告されている研究の誠実かつ正確で透明性のある説明であることを確約する。本研究の重要な側面が省略されていないこと。本研究は当初の計画通りに実施されました。
利害の衝突
著者は競合する利益を宣言しない。
