Long COVID in a prospective cohort of home-isolated patients
公開日:2021年6月23日
Bjørn Blomberg, Kristin Greve-Isodahl Mohn, Karl Albert Brokstad, Fan Zhou, Dagrun Waag Linchausen, Bent-Are Hansen, Sarah Lartey, Therese Bredholt Onyango, Kanika Kuwelker, Marianne Sævik, Hauke Bartsch, Camilla Tøndel, Bård Reiakvam Kittang, Bergen COVID-19 Research Group, Rebecca Jane Cox & Nina Langeland
Nature Medicine (2021)Cite this article
概要
新型コロナウイルス019(COVID-19)感染後の長期合併症は入院患者に多く見られるが、軽症の場合の症状のスペクトラムについてはさらなる検討が必要である。ノルウェーにおける第1次パンデミックの波の中で、ベルゲンで全症例の82%を占める312人の患者-自宅隔離患者247人、入院患者65人-を対象に、前向きコホート研究で長期追跡調査を行った。6ヵ月後の時点で、全患者の61%(189/312)が持続的な症状を呈しており、この症状は、初期症状の重さ、回復期の抗体価の上昇、既存の慢性肺疾患と独立して関連していた。その結果、16~30歳の若年層の52%(32/61)が6ヵ月後に症状を呈しており、味覚や嗅覚の喪失(28%、17/61)疲労感(21%、13/61)呼吸困難(13%、8/61)集中力の低下(13%、8/61)記憶障害(11%、7/61)などの症状が認められた。軽度のCOVID-19を発症した若年層の家庭内隔離者は、呼吸困難や認知症状が長期に渡って続くリスクがあるという今回の結果は、ワクチン接種などの感染対策の重要性を強調している。
主な内容
重症急性呼吸器症候群新型コロナウイルス(SARS-CoV-2)の侵入・感染部位は呼吸器であるが、COVID-19は心血管系、腎系、血液系、消化器系、中枢神経系にも影響を及ぼす複雑な全身疾患である1。線維化に関連した肺機能の障害が優位に持続するという証拠が出てきているため、COVID-19が他の臓器に及ぼす長期的な影響について、より多くのデータが必要とされている2。重度のCOVID-19を克服した患者には多数の症状が持続し(参考文献3,4)Long-コービッド症候群が提唱されている5,6。しかし、症状の重さや期間については、まだほとんど知られていない。慢性疲労は 2003年のSARS感染後に発生し(参考文献7)様々な感染症の後遺症としてよく知られている8,9,10,11,12,13。SARS-CoV-2パンデミック以前は、集中治療室での患者管理は心身の衰えと関連することが多く、このことは重症患者のLong-COVIDを部分的に説明することができる14。しかし、軽症から中等症の患者におけるLong-COVIDの負担については、十分に定義されていない。本研究では、ノルウェーのベルゲンで発生した第1次パンデミックの入院患者と自宅隔離患者の前向きコホートを対象に、初回COVID-19から6カ月後の持続的な症状を評価した。
結果
ベルゲン市の唯一の集中検査施設で診断されたすべての患者と、市内の2つの病院に入院したすべての患者に参加を呼びかけた。Haukeland大学病院とHaraldsplass Deaconess病院の2つの病院に入院している患者も対象とした。最初に診断された自宅隔離患者と最初に入院した患者から募集を開始し、最初のパンデミックの波の中で92%の患者が参加に同意した。目的は、長期的な合併症に関連する因子やバイオマーカーを特定することであった。2020年2月28日から4月4日まで、SARS-CoV-2が陽性の患者357人を連続的に募集した。人口統計学的データと臨床データ、および血液サンプルを収集した。コホートの完全性を確保するため、陽性と判定された患者の家族も対象とし、2か月後にSARS-CoV-2特異的抗体により感染を診断した15。6カ月後の追跡調査では、解析可能な研究集団は312人で、そのうち247人が自宅隔離、65人が入院していた(図1)。
図1:試験集団のフローチャート
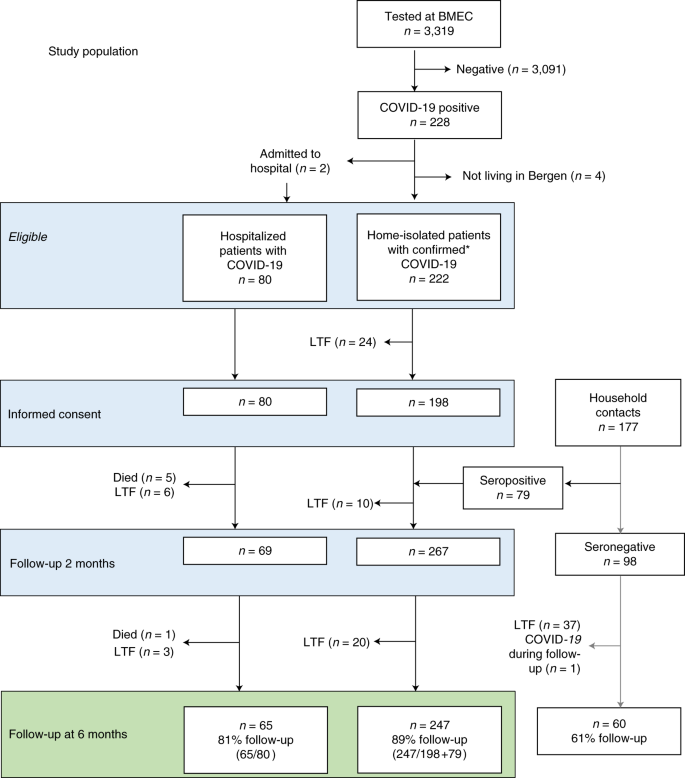
ベースライン、2ヵ月後の採血、6ヵ月後の評価と疲労度評価で対象となった参加者の数。BMEC, Bergen Municipality Emergency Clinic; LTF, lost to follow-up.
調査対象者の年齢中央値は46歳(四分位範囲(IQR)30~58歳)で、51%(160/312)が女性であった。44%が併存疾患を有しており(137/312)最も多かったのは、慢性肺疾患(12%、38/312,喘息を有する34)高血圧(11%、35/312)慢性心疾患(7%、22/312)リウマチ性疾患(6%、20/312)糖尿病(4%、13/312)免疫抑制状態(4%、11/312)であった。急性期に症状を記録した272名の患者では、疲労感(90%、244/272名)咳(71%)頭痛(64%)筋肉痛(58%)呼吸困難(55%)が最も多く、発熱は21%にとどまった。入院患者は自宅隔離患者よりも年齢が高く、BMI(体格指数)が高く、慢性肺疾患、慢性心疾患、高血圧、糖尿病などの併存疾患が多かった(表1)。
表1 6カ月後の追跡調査が可能な研究集団の特徴
原文参照
COVID-19を発症してから6カ月後、全患者の61%(189/312人)に持続的な症状が見られ、最も多かった症状は、疲労感(37%)集中力の低下(26%)嗅覚や味覚の障害(25%)記憶障害(24%)呼吸困難(21%)であった。ほとんどの症状の頻度は年齢とともに増加したが、嗅覚や味覚の障害は46歳以下の人に多く見られた(表2)。調査対象者の39%は、主に小児や若年成人で、6ヵ月後には症状がなかった。自宅隔離された247名の患者でも、55%(136/247)が6ヵ月後に持続的な症状を経験しており、最も多かったのは疲労感(30%)味覚や嗅覚の障害(27%)集中力の低下(19%)記憶喪失(18%)呼吸困難(15%)であった(表2)。
表2 COVID-19を発症した在宅隔離患者247名の6ヵ月後の追跡調査における年齢層別の長期合併症
原文参照
最も若い年齢層(0~15歳)では、症状が持続することはほとんどなかったが(13%、2/16)軽度から中等度の初期疾患で自宅隔離された16~30歳の若年成人では、52%(32/61)が症状が持続しており、最も多かったのは味覚・嗅覚障害(28%)疲労感(21%)呼吸困難(13%)集中力低下(13%)と記憶力低下(11%)であった(表2)。これらの若年層では、対象者数が少なかったものの、症状の持続性(33%対31%、P=1)や疲労感(47%対27%、P=0.2)と併存疾患との有意な関連は認められなかった。
療養中の抗体は感染後約1~2カ月でプラトーに達し、免疫反応の大きさを示す一般的な指標となる16。2カ月後に検出されたSARS-CoV-2スパイクタンパク特異的IgGおよびマイクロ中和抗体の力価は、入院患者の方が自宅隔離患者よりも有意に高かった(P < 0.001;拡張データ図1)。2ヵ月後の抗体価の上昇は、多変量解析において、初診時の重症度、高齢、BMIの高さと関連していた(表3,図2;重症度スコアはBeigel et al 17から引用)。
表3 COVID-19における回復期抗体価の上昇と関連する要因
原文参照
図2:ノルウェー・ベルゲンにおけるCOVID-19患者の6カ月間の追跡調査。
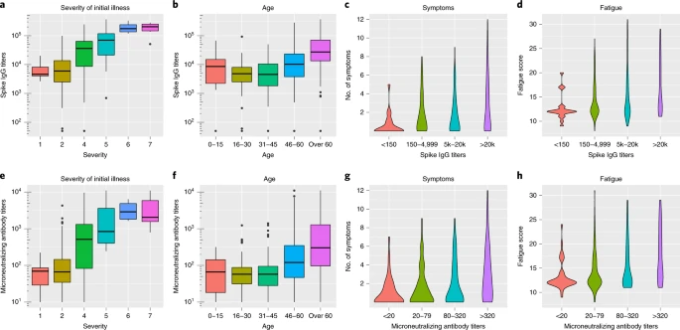
COVID-19の初発の重症度および年齢と、2ヶ月後の抗SARS-CoV-2スパイク抗体価(aおよびb)およびマイクロ中和抗体価(eおよびf)との関係。2ヵ月後の抗体価と、6ヵ月後のフォローアップにおける持続的な症状の数(cおよびg)およびChalderスケールによる総疲労スコア(dおよびh)との関係。使用した13の症状を表2に示す。重症度は以下の通りであった。1-無症状(n=5)2-症状を伴う自宅隔離(n=242)3-医療ニーズのない入院(n=0)4-医療ニーズのある入院(n=31)5-O2を必要とする入院(n=24)6-非侵襲的換気を必要とする入院(n=4)7-人工呼吸器を必要とする入院(n=6)。a,b,e,fはスパイクIgGおよびマイクロ中和抗体価の中央値(水平線),25%および75%の分量線(箱),および95%信頼区間(線)と外れ値(点)を示す。cおよびdは、スパイクIgGの4つのカテゴリー:<150(n=21)150-4999(n=96)5,000-20,000(n=103)>20,000(n=92)に分けた症状の数(最大13)または疲労スコア(値0-33)のバイオリンプロット。gおよびhはマイクロ中和力価の4つのカテゴリーのバイオリンプロットである。<20未満(n=42)、20-79(n=107)、80-320(n=92)、320以上(n=71)。O2,補助酸素。
抗体価の上昇および既存の肺疾患は、多変量解析において、6ヵ月後の持続的な疲労と症状の総数の両方に独立して関連していた(表4および図2c,d,g,h)。最初の病気の重さは、持続的な疲労と関連し、症状の総数とは弱く関連していた(表4)。
表4 COVID-19患者因子は、6ヵ月後の追跡調査での症状数の増加および疲労スコアの上昇と関連する-陰性二項回帰分析
原文参照
ウイルス感染後の疲労は、SARS感染7やその他のウイルス感染11,12,13の後に報告されている。疲労の評価には、成人で有効とされているChalder fatigue scoreを用いた18,19。疲労は、11の質問に対する二峰性スコアの合計が4以上と定義されている。16歳以上の在宅隔離患者の30%(69/231)が6ヵ月目に疲労を抱えていたのに対し、入院患者の63%(39/62)が疲労を抱えていた。6ヵ月後の重度の疲労(bimodal score ≥4 + total ordinal score ≥23と定義)は、在宅隔離患者の7%(17/231)と入院患者の24%(15/62)に見られた(補足表1)。在宅患者では、身体的疲労の症状(質問1~7)として、疲労感(35%、81/231)休息の必要性の増加(30%)気力の欠如(29%)が最も多く、精神的疲労の症状(質問8~11)として、言葉が見つからない(23%)集中できない(19%)記憶障害(18%)が最も多かった(補足表1)。
16歳以上の患者では、二項ロジスティック回帰分析において、急性期の発熱、初発の重症度、女性の性別が6ヵ月後の疲労感と関連していた(補足表2)。多変量解析では、女性の性別に加えて、肺疾患の既往、急性疾患の重症度、回復期の抗体価の上昇が、6ヵ月後の疲労度スコアの上昇と独立して関連していた(表4および図2d,h)。
初期疾患の重症度と2ヵ月後の抗体価には相関関係があったが、多変量解析では両因子ともLong-COVIDの特徴と独立して関連していた(表4および補足表2)。症状が軽度から中等度の242名の在宅隔離患者を対象とした層別解析では、抗体価の上昇は、症状の数(オッズ比(OR)=1.56,信頼区間(CI)=1.23-1.96)および疲労スコア(OR=1.07,CI=1.02-1.12)と依然として関連していたが、二分法変数としての疲労については統計的に有意ではなかった(OR=1.48,CI=0.98-2.31)。
考察
我々の研究は、入院患者だけでなく、若年者や病状の軽い在宅患者においても、Long-COVID症状を評価するという点で新規性がある。強みは、免疫学的にナイーブな集団において、すべての重症度を含む第一次パンデミックウェーブの抗体および逆転写酵素ポリメラーゼ連鎖反応(RT-PCR)陽性患者のほぼ完全な、地理的に定義されたコホートであることである。今回の研究ではサブグループの数が少なかったことが限界であり、今回得られた知見をより大規模なコホートで確認する必要がある。
我々のコホートでは、COVID-19の生存者の大部分が、初発から6カ月後にも症状が持続していることがわかった。重症のCOVID-19で入院した患者は、長期にわたる症状に悩まされることが多いことがこれまでに報告されているが20,21,22,23,我々は、自宅で隔離された軽症から中等症のCOVID-19患者の半数以上が、感染後6カ月経っても症状が残っていることを発見した。入院していない若年層(16-30歳)が、感染から半年後に集中力や記憶力の低下、呼吸困難、疲労感などの重篤な症状を引き起こす可能性があることは憂慮すべきことである。特に学生の場合、このような症状は学習や勉強の進行に支障をきたす可能性がある。
COVID-19患者の持続的な疲労感の高さは顕著であり、インフルエンザ、エプスタインバーウイルス単核症、デング熱などの一般的な感染症の後に観察されるものよりも高いようである11,12,13。ノルウェーのデータによると、一般人口における慢性疲労の有病率(11%)は、今回の家計調査対象者(14%)よりもわずかに低いことが示されている24が、この家計調査対象者は感染者よりも若く、合併症も少なかったが、同時に採取された。しかし、この明らかな違いは、人数が少なかったための偶然かもしれない。女性の方が疲労の有病率が高いという今回の結果は、ノルウェーの一般住民を対象とした以前の研究結果と一致している24。また、重症度と持続的な症状との関連は、COVID-19による入院患者のデータと一致している(参考文献20)。COVID-19の主な標的臓器は呼吸器であることから、基礎疾患である慢性肺疾患(主に喘息)と、疲労感などの持続的な症状との関連性を見出したことは驚くべきことではない。
重度の初期疾患と2ヵ月後の抗体価の上昇との関連は、ウイルス量が多いために免疫系がより深く起動する可能性がある25。また、年齢の上昇に伴って回復期の抗体価が上昇するという知見は、年齢が重度のCOVID-19の強力なリスク要因であることが知られていることから、高齢者の疾患がより重度であることで説明できるかもしれない。しかし、高齢者のインフルエンザ感染後に見られる免疫老化とは対照的に、多変量解析では年齢と重症度が抗体価の上昇と独立して関連していることが示された。これらの結果から,COVID-19の集団予防接種プログラムのサーベイランスを強化する必要があると考えられた。軽度のCOVID-19を発症した16~30歳の自宅隔離患者は、呼吸困難や認知症状が長期にわたって続くリスクがある。現在進行中のパンデミックで何百万人もの若者が感染していることを考えると,今回の知見は包括的な感染制御と集団的な大規模ワクチン接種を強く促すものである.
方法
倫理的配慮
すべての参加者、または16歳未満の子どもの場合はその保護者が、書面によるインフォームド・コンセントを提供した。本研究は、ノルウェー西部の地域倫理委員会の承認を得た(no.118664)。参加者に対しては、診療所までの交通費の払い戻し以外の報酬は提供しなかった。
研究対象者
長期追跡調査を行う前向きコホート研究の一環として、ノルウェーのベルゲンでパンデミックの第一波が発生した2020年2月28日から4月4日の期間にCOVID-19と診断された自宅隔離患者を連続的に登録した。入院患者については、5月6日までの入院の遅れによる長期の組み入れを受け入れた。研究対象者は、ベルゲン市の救急クリニックで診断されたSARS-CoV-2 RT-PCR陽性患者と、隣接する2つの市立病院に入院した患者である。Haukeland大学病院とHaraldsplass Deaconess病院に入院した患者を対象とした。特定された患者の家庭内接触者は、二次感染者(セロコンバーター)または血清陰性の対照者として研究に参加するよう求められた15。登録されているSARS-CoV-2患者全員に参加を呼びかけた。参加時の初期参加率は92%(278/302人)2カ月後の参加率は88%(336/381人、分子と分母にはこの時点で血清陽性の世帯員を含む)6カ月後の参加率は82%(312/381人)であった。抗SARS-CoV-2抗体価を検出するため、感染から 2カ月後に回復期の血清サンプルを採取した。
ベルゲンでのすべての検査は、緊急クリニックと市内の2つの病院に集中して行われ、ベルゲンでCOVID-19と診断されたすべての同意患者を対象とすることができた。この期間中、市の緊急クリニックでは、合計3,319人の患者がRT-PCRで検査された。このうち、228人がRT-PCRで陽性と判定され、6人は住所がベルゲン市外であったり、入院していて入院患者に分類されたりしたために除外された。Municipality Emergency Clinicで受診した疑いのある症例はすべて、臨床的に診察され、医療スタッフによって診断された。中等症の患者は自宅隔離のために帰宅させられ、重症と判断された場合には入院させられた。入院患者のほとんどは、入院時に診断された。実験室での確認のために鼻咽頭ぬぐい液が採取された。患者には、三次病院の基準微生物検査室で行われたRT-PCR検査の結果が電話で伝えられた。自宅で隔離されたことが確認された患者全員に、研究への参加を促す電話連絡が行われた。さらに79名の患者が、RT-PCR陽性患者の家族のセロコンバージョンを調査することで特定された。臨床データと人口統計学的データを収集するために、医療スタッフが電話インタビューを行った。参加者は、2カ月後(6~8週間後)と6カ月後(±1カ月後)に大学病院に通院し、医療スタッフによるフォローアップのための診察を受け、長期的な症状について聞き取り調査を受けた。
臨床データ
同意を得たすべての患者は、ベースライン時、2ヵ月後、6ヵ月後にフォローアップクリニックに通い、医療スタッフによるインタビューを受けた。その際、人口統計学的情報、ベースライン時と6カ月後の症状に関する臨床情報、併存疾患や投薬の有無などの潜在的な危険因子に関する情報を提供した。急性疾患時に記録された具体的な症状は、発熱、咳、呼吸困難、疲労、筋肉痛、頭痛などであった。喘息、慢性閉塞性肺疾患、慢性心疾患、高血圧、慢性肝疾患、腎疾患、神経筋疾患、認知症、リウマチ性疾患、活動中のがん、その他の重篤な慢性疾患、遺伝的免疫不全、HIV、臓器移植、静菌剤などの免疫抑制剤投与などの免疫抑制状態を含む共存症があるかどうかを尋ねました。データは、初期疾患の重症度、すなわち入院の必要性、急性疾患中の症状、非侵襲的な人工呼吸器や呼吸器治療の必要性について収集した17。X線検査は、入院患者のみを対象に実施した。6ヵ月後の追跡調査では、16歳以上の参加者全員に、Chalder疲労尺度18,19に従った11の重要な質問を含む有効な疲労質問票を記入してもらった。疲労は、二分法によるスコアの合計が4以上と定義した。重度の疲労は、疲労に加えてChalderスコアの合計が23以上であると定義した。
検査方法
COVID-19 の診断は、鼻咽頭ぬぐい液のサンプルを用いた RT-PCR と、SARS-CoV-2 抗体が陽性であることを示す血清学的証拠に基づいて行われた26。血清サンプルは、抗SARS-CoV-2抗体価を検出するために感染から 2ヵ月後に採取し、分析するまで-80℃で保存した。検体は56℃で1時間熱活性化した後、受容体結合ドメイン(RBD)に対するSARS-CoV-2特異的IgG抗体(Southern Biotech, cat.no.2040-05)を検出する2段階のELISA(スクリーニング1:100希釈)およびスパイクタンパク質(1:100から5倍希釈で確認)で二重に分析した。エンドポイントの抗体価は、過去のパンデミック前の血清サンプル(n=128)26の平均値よりも3標準偏差の光学密度値を与える血清希釈の逆数として計算した。RBDに対する抗体を持つ血清は,バイオセーフティレベル3の認定を受けた研究所で,現地分離株hCoV-19/Norway/Bergen-01/2020(GISAID accession ID EPI_ISL_541970)を用いたマイクロ中和アッセイで検査した27.簡単に言うと、血清を1:20希釈から始まる倍加希釈で二重に検査し、100TCID50のウイルスと混合した後、SARS-CoV2 NPに対するウサギモノクローナルIgG(Sino Biological, cat. No.40143-R019-100)ビオチン化ヤギ抗ウサギIgG(H+L)(Southern Biotech社、cat.No.4050-08)およびエキストラビジンペルオキシダーゼ(Sigma-Aldrich社、cat.No.E2886)を用いてインキュベートした。マイクロ中和抗体価は、ウイルスの感染を50%阻害する血清希釈率の逆数である。すべての対照者について、6ヵ月後に血清学的に陰性であることが確認された。
統計解析
データはREDCap(Research Electronic Data Capture,Vanderbilt University)の電子症例報告書を用いて入力した。すべての解析は,R バージョン 4.0.3(www.r-project.org)で行い,グラフは R の ggplot および gridExtra パッケージを用いて作成した。質問票に回答した患者を解析対象とし、結果は平均値または中央値と95%CIを含むパーセンテージで示した。単変量解析では、カテゴリー変数をカイ二乗検定と二項ロジスティック回帰を用いて比較し、OR、95%CI、P値で示した。
多変量解析は、二分法の結果変数に対して二項ロジスティック回帰で行った(補足表1および2)。また、RのMASSパッケージを用いた負の二項回帰により、数値化されたアウトカム変数(表4)すなわち、表2に記載された症状に応じて0~13の整数でコード化された「症状の数」と,0~33の値を含むChalderスケールに基づく疲労スコアとの関連因子を分析した。結果変数である回復期抗体価については、ほぼ正規分布になるように対数変換した後、線形回帰を行い、単変量解析では未調整、多変量解析では調整済み幾何平均比として結果を報告した(表3)。また、多変量解析では、単変量解析でP<0.1の有意水準を示した変数に加えて、性別も含めた。スパイクIgGとマイクロ中和抗体の力価には強い共線性があり、またマイクロ中和抗体は総IgGに占める割合が高いため、多変量解析からはマイクロ中和抗体を除外した。
本解析では、暴露変数としての抗体価が、結果変数としての疲労度と症状スコアにそれぞれ影響を及ぼす可能性に着目。単変量解析で有意であった他のすべての曝露因子について、交絡と効果サイズの修正を評価した。
重症度は、既報17のとおり、8カテゴリーの順序尺度を用いて分類した。カテゴリーは以下の通りである。1-入院しておらず、活動に制限がない、2-入院しておらず、活動に制限があり、在宅酸素が必要、またはその両方がある、3-入院しており、補助酸素を必要とせず、継続的な医療を必要としなくなった(感染症対策やその他の医療以外の理由で入院期間が延長された場合に使用)。4-入院中で、補助酸素を必要としないが、(COVID-19またはその他の病状に関連して)継続的な医療を必要としているもの、5-入院中で、補助酸素を必要としているもの、6-入院中で、非侵襲的人工呼吸または高流量酸素装置の使用を必要としているもの、7-入院中で、侵襲的人工呼吸または体外式膜による酸素供給を受けているもの、8-死亡のもの。
報告の概要
研究デザインについての詳細は、本記事にリンクされているNature Research Reporting Summaryを見てほしい。