Contents
はじめに
LED(光線治療)の医学的応用は、元々、創傷治癒、頚部痛、腱鞘炎、手根管症候群などの整形外科的症状における疼痛、炎症の軽減についての研究から始まっている。
これまでサイトで紹介してきたLLLTによる認知機能への治療研究は比較的最近のものが多い。
www.ncbi.nlm.nih.gov/pubmed/22045511
腰痛や膝の痛みなどで、リコード法の運動がむずかしいという認知症患者さん、高齢者の方の話をよく耳にする。
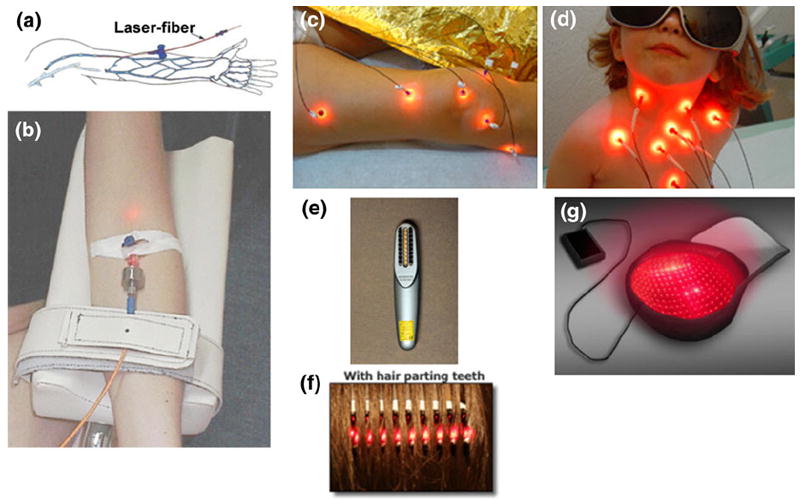
サイトで紹介している認知機能改善目的の赤外線カメラ用の照射型LEDライトが、慢性疼痛への治療器具と理論的にも経験的にも類似する効果を有すると考えられるため紹介しておきたい。

www.ncbi.nlm.nih.gov/pmc/articles/PMC3288797/figure/F5/
疼痛には大きくそのメカニズムによって侵害受容性疼痛、神経因性疼痛、中枢性疼痛の3つが存在する。
低レベルレーザー治療(LLLT)は、侵害受容性、神経因性疼痛の治療が可能であることが多くの小規模研究で実証されている。
中枢性疼痛へのLLLTの効果はまだ証明されていないが、セロトニンの増強、HPA軸への作用もあることから理論的には影響をおよぼしうる。
www.ncbi.nlm.nih.gov/pubmed/25237637/
www.ncbi.nlm.nih.gov/pubmed/25024832/
30日未満続くものを急性疼痛と呼び、6ヶ月以上持続するもの。または予想される治癒期間を超えて広がる疼痛を慢性疼痛と定義される。
疼痛 3つの発症メカニズム
侵害受容性疼痛
打撲、切り傷、骨折、やけどなどによる一般的な痛み。末梢の侵害受容器が,組織への外傷、熱や機械的な刺激などによって活性化されて生じる痛み。
急性痛や炎症による痛みと同じメカニズム。
プロスタグランジンやブラジキニンなどの痛みと関わる物質が末梢神経にある「侵害受容器」を刺激することで痛みを感じる。器質的疾患によるものが多い。
オピオイド、モルヒネなどは侵害受容性の疼痛に対して特に有効で、手術中の痛み、陣痛などによく使われる。
神経障害性疼痛
腫瘍、椎間板の破裂、手根管症候群、手術などによって痛みの感覚を司る神経経路(中枢,脊髄,末梢神経)が損傷し、その神経が支配する領域に異常が生じることで感じる痛み。灼熱痛、チクチク感、触覚や低温に過敏になったりする。
神経障害性疼痛の原因や病態ははっきりと分かっておらず、一般的な鎮痛薬は効かない。
神経系が痛みに敏感な構造に変わってしまい、慢性痛原因となる難治性の痛みとされている。
中枢性疼痛
心理的な原因に由来する痛みなどだが、単純に心の問題というわけではなく、社会生活で受けるストレスや日々の不安など、生物学的,心理的,社会的,行動要因なども複雑に関与する。
多発性硬化症、脳卒中後など脳の損傷や機能障害なども含むが、中枢神経や末梢神経系への影響による痛みは含めない。
LLLTが疼痛を緩和するメカニズム
侵害受容器の一時的遮断
9.6J/cm2(830nm) 適切なLLLTの照射は、感覚ニューロン(DRGニューロン)のミトコンドリア膜電位(MMP)を低下させ、その後ATP産生が一時的に低下する。その結果神経遮断となり侵害受容性が調節され、痛みが軽減する。
この効果は体性感覚誘発電位(SSEP)の伝達、侵害受容器の遮断による即時的な効果であり、数分以内に痛みの軽減が起こる。
www.ncbi.nlm.nih.gov/pubmed/24026991/
サブスタンスP・CGRPの減少
抹消の感作作用の阻害は、神経の活性化閾値を低下させるだけでなく、炎症性神経ペプチド、サブスタンスP、CGRP(カルシトニン遺伝子関連ペプチド)の放出も減少させる。
慢性疼痛障害においては、活性化された侵害受容器への刺激が持続的に減少し、二次ニューロンの長期的な下方制御を引き起こす。
www.ncbi.nlm.nih.gov/pubmed/17374099/
www.ncbi.nlm.nih.gov/pubmed/8003306/
PGE-2・COX-2の阻害
LLLTは、シクロオキシゲナーゼ-2(COX-2)mRNAレベルの減少を介して、PGE2を阻害した。この作用メカニズムは抗炎症薬を模倣しうる。
www.ncbi.nlm.nih.gov/pubmed/10706474/
セロトニン・エンドルフィンの増加
疼痛障害ではセロトニン、エンドルフィンレベルの変調が動物モデルにおいて生じうることが示されている。
LLLTは内因性オピオイドの分泌を増強させ鎮痛効果をラットモデルにおいて増強させる。(830nm)
www.ncbi.nlm.nih.gov/pubmed/18081143/
LLLT治療はオピオイド作動系,セロトニン作動系の活性化により、ラットの疼痛行動を軽減する。
www.ncbi.nlm.nih.gov/pubmed/23291880/
LLLTは9J/cm2の照射量で用量反応鎮痛効果を誘導。オピオイド含有白血球の動員を含む抹消オピオイド状態の活性化が鎮痛効果に少なくとも部分的に関与する。
www.ncbi.nlm.nih.gov/pubmed/23832179/
トリガーポイントへの効果
22人の健康な学生のトリガーポイントへの赤外線(904nm)照射は、プラセボ群と比べ疼痛の閾値(痛みの耐性)を有意に増加させた。
www.ncbi.nlm.nih.gov/pubmed/2568075/
LLLTは、トリガーポイントの低酸素状態にある細胞へ酸素供給を増加させ、老廃物を除去することができる。LLLTの臨床的有効性は急性疼痛で70%以上、慢性疼痛では60%以上であり、成功率は適切なエネルギー量に依存する。
www.ncbi.nlm.nih.gov/pubmed/9456632
リンパ節への効果
乳房切除術後リンパ浮腫(PML)患者への2サイクルのLLLT照射は、3ヶ月後に、患者の33%で罹患した腕の体積、細胞外液、組織の硬さを減少させるのに有効であった。
www.ncbi.nlm.nih.gov/pubmed/12973834/
LLLTの特性
慢性疼痛の効果 用量反応曲線

LLLTの用量反応関係は、一般的な薬物投与によるS字曲線ではなく、ホルミシス応答である逆U字曲線を描く。
長期的効果
LLLT治療の有意差は3回目から見出され、8回目に累積効果が観察された。しかし、鎮痛効果はプラセボグループと類似していたため、優位性を実証することはできなかった。
www.ncbi.nlm.nih.gov/pubmed/19891258/
LLLTの使用
LLLTの照射パラメーター
760~850nm
ビーム出力が500mw/cm2である場合、組織化5cmの深さでは0.5mw/cm2のパワー密度を達成できる。
連続波 vs パルス波
連続波とパルス波の両方が、疼痛レベルを減少させたが、パルス波がより効果的であった。
10Hzおよび8000Hzが60Hzよりも効果的であった。
www.ncbi.nlm.nih.gov/pubmed/17725044
4Hz、60Hz、200Hzの比較 4Hzのパルス波は一過性であったが急速な鎮痛効果を示した。
60Hzはより遅い効果を示したが、長期的な効果を維持できた。
200Hzでは、鎮痛効果はまったく得られなかった。
www.ncbi.nlm.nih.gov/pubmed/2890276
LLLT照射の標的部位
- 炎症を低減し治癒を促進するための外傷、損傷部位
- 浮腫と炎症を鎮めるためのリンパ節
- 痛覚を麻痺させる神経
- トリガーポイントへの照射による筋繊維の弛緩
疾患への臨床研究
慢性腰痛の臨床研究
プラセボ対照二重盲検 慢性腰痛患者への890nmのLED照射試験
照射密度34.7mw/cm2 40分間/週3回
照射グループでは慢性腰痛患者の障害の重症度および恐怖を回避する思い込みの軽減、身体活動の増加と有意に関連していた。
link.springer.com/article/10.1007%2Fs10103-013-1378-2
論文での照射密度 34.7 ÷ LEDライトの照射密度 約70 = 0.5
0.5 × 40分 = 20分
アルツハッカープロトコル
サイト掲載の赤外線LEDライトを腰痛の箇所に照射
最初は5分からスタート/週3回
毎週5分ずつ増加 最終的に一回20分/週3回~
膝の痛みの臨床研究
プラセボ対照二重盲検 膝の痛みを抱える86人の被験者 週3回/全12回の治療
905nm超、875nm(20mw/cm2)、640nm(20mw/cm2)/1000Hzを組み合わせたLEDを痛みのある膝へ投射。両膝が痛い場合は両膝。一つの膝に対して13分
10回目の治療より痛みを有意に減少させ、健康度、機能性、身体活動などの主要項目でプラセボグループよりも有意な改善を示した。
www.ncbi.nlm.nih.gov/pubmed/24844921/
論文によれば、膝の痛みには複数の病因が関与しており、複数の波長を組み合わせることで膝痛治療に効果的に働きかけることが可能とのこと。
アルツハッカープロトコル
痛みがある膝の皿を中心に周囲から4~5箇所に分けて照射 後ろ膝へ一ヶ所照射
膝2分 後ろ膝1分 ももの付け根1分/週3回 最低10回行う。
創傷治療
健康な大学生集団22名 波長:820nm 8 J / cm2 照射時間:2分5秒 64mw? パルス:700 Hz
治療後6日目から照射グループがプラセボグループよりも、有意に小さい創傷であったことが確認できた。
www.ncbi.nlm.nih.gov/pmc/articles/PMC522143/
LLLTによる創傷治療へ期待できるメカニズム
- 抗炎症作用
- 血管新生
- 上皮および線維芽細胞の増殖
- コラーゲンの合成と沈着
- 血管再生、創傷収縮などの生理学的効果の促進
創傷治療に有効な用量は3~6J/cm2の間 10を超えると有害な効果と関連する可能性がある。
三叉神経痛
三叉神経痛へのLLLT照射 文献レビュー
長期的使用6~10J 短期使用3~6J ヘリウムネオンレーザーが最も効果的であり、トリガーポイントへの照射が最も有効。
830nm、60mwのLLLTにもヘリウムネオンレーザーには劣るが効果がある。12回のセッション後に痛みの緩和が見出された。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4091693/