Contents
レビー小体型認知症とパーキンソン病の違い
pubmed.ncbi.nlm.nih.gov/29222591/
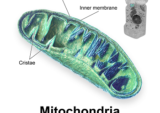
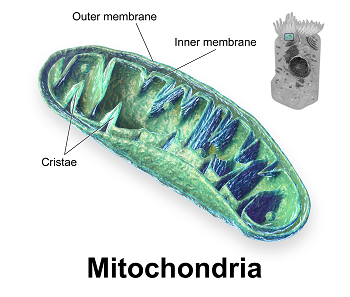
両者とも、皮質および皮質下の広範なα-シヌクレイン/レビー小体に加え、β-アミロイドやタウの病理が形態学的に特徴的である。DLBコンソーシアムの第4次コンセンサスレポートなど、最近の発表に基づき、その概要を説明する。DLBとPDDの臨床的特徴として、認知障害、パーキンソニズム、幻視、注意力の変動が挙げられる。
また、PETや死体解剖の結果、PDDよりもDLBの方が、より顕著な皮質萎縮、皮質および辺縁系レビー病(APOE ε4)の増加、さらにアルツハイマー病がより多く存在することが明らかとなった。これらの変化は、DLBにおける認知機能障害の早期発症と重症化の原因であると考えられるが、マルチトレーサーPET研究ではコリン作動性障害とドーパミン作動性障害に差は認められなかった。
遺伝的、神経化学的、形態学的要因を共有するDLBとPDDは、α-シヌクレイン関連疾患スペクトラム(レビー小体病)の2つのサブタイプであると考えられる。
最も重症な端にある付随性レビー小体病-パーキンソン-非痴呆性-DLB(パーキンソン病なし)-アルツハイマー病付きDLB-ADから始まり、一方、DLBはPD/PDから始まっておらずDLB-ADに必ず進行するとは限らず、これらを同じ疾患と考える人もいる。
DLBとPDDはともに不均一な病態と神経化学的変化を示し、ADや他のプロテインパチーとの重要な共通した分子病態を有していることが示唆されている。認知機能障害は、αシヌクレインによる神経変性だけでなく、複数の領域の病態スコアによって引き起こされる。
基本的な考え方
毒素の解毒
レビー小体型認知症を引き起こす少なくとも要因の一部には毒素、化学薬品、有害金属、生物毒素などの様々な毒素と関連がある可能性が多くの研究で報告されている。リコード法においても、レビー小体型認知症、パーキンソン病患者さんは毒素型である3型に沿って検査・解毒・治療が行われている。

多因子疾患としてのレビー小体型認知症
ここにある治療アプローチは、リコード法で案内されているものではないが、レビー正体型認知症が多因子疾患であることを前提に、いくつかの提唱されている発症リスク因子を元に、それぞれまた研究されているサプリメント、薬剤、治療手段を列記してみた。
それぞれ考えられているメカニズムごとに記載している。検査を行い最適化することとは別に、多因子介入としての相乗効果を(鉄キレートを除き)狙ってできるだけ多く実行することを前提に考えている。
検査について
明確な発症機序はわかっていないものの、蓄積タンパク質はレビー小体型認知症と同様であり上記で書かれてあるように、代謝障害のレベルにおいても多くが重複する。繰り返しになるがパーキンソン病もまた毒素が関連する可能性が高いため(確率的にはアルツハイマー病よりも)、レビー小体型認知症と同様リコード法、CIRSに基づく毒性の検査が望ましい。基本的なプロセスは3型のアルツハイマー病治療と変わらないが、パーキンソン病では農薬などの化学毒素そして有害金属がより関連している可能性が高いことが多くの疫学研究で証明されている。
標準的なパーキンソン病治療研究では、鉄キレートを除いて、農薬などを解毒する直接的な介入研究はほとんど行われていない。(予防研究では取り組まれている。)おそらく検査を行っても彼らには治療手段がないことから、科学毒素、有害金属、検査もまず行われない。これら2つはリコード法で、検査プロトコルが確立されており、どのように対処すべきかのガイドラインも存在する。
必ずしもリコード法を標榜する病院でなくとも、検査自体は栄養療法など、一部のクリニックで行ってくれるところがある。リコード法病院も極めて少ないことから、自ら探して解毒方法を学び個人で実行していくことが多くの人にとってはより現実的だろう。
有機化学毒素の検査

有害金属
有害金属の検査は複数あり、少し複雑なため、「アルツハイマー病真実と終焉」参考に実行してほしい。
病院へ行かずとも簡単にできる有用な有害金属の検査として毛髪ミネラル検査がある。


αシヌクレインの凝集を防ぐ

グルカゴン様ペプチド-1(GLP-1)アナログのexenatide【再利用薬】
GLP-1受容体の活性化によるこの効果については、アポトーシスの抑制、ミクログリア活性化および神経炎症の抑制、酸化ストレスの軽減、神経新生の促進など、いくつかのメカニズムが提案されている。最初の非盲検試験において、エキセナチドはPD患者において安全であることが示され(体重減少の問題を経験した患者もいた)、認知機能と運動機能の改善が認められ、それは投与中止後も持続した。現在、多施設共同第III相試験が設定されており、参加者は週1回のエキセナチドまたはプラセボを投与される。
pubmed.ncbi.nlm.nih.gov/18492290/
ミリセチンを含む食品の摂取(生・新鮮)
キャベツ、パセリ、ブロッコリー、クランベリー
アントシアニン、ケルセチン、エピカテキン
www.ncbi.nlm.nih.gov/labs/pmc/articles/PMC3320056/
ロズマリン酸を含有するハーブ
ペッパーミント、ローズマリーなどの調味料。日本の家庭料理でローズマリーなどのハーブの大量使用は一般的でないことから、サプリメントを利用したほうが良いかもしれない。
一回二錠 朝、昼摂取
テアフラビン(発酵紅茶成分)
アッサムティー、ルイボスティー等 紅茶には約23mgのテアフラビンが含まれる。
経口からの吸収率は非常に低い。保護効果をもつ最低用量は1.6mg/kg(体重60kg換算で96mg)
オートファジー
オートファジー

マイトファジーの活性
αシヌクレインの標的はミトコンドリアであるため、ミトコンドリアのオートファジーであるマイトファジーも重要。

ニロチニブ
慢性骨髄性白血病の治療に用いられるABLチロシンキナーゼ阻害剤。ABL活性は、マイトファジーの開始に重要なパーキンの活性を阻害し、ニロチニブはオートファジー活性を高め、α-シヌクレイン凝集体の蓄積を減少させる可能性が提案されている。
脳脊髄液(CSF)中の総α-シヌクレインに対する病原性オリゴマーα-シヌクレインの比率を減少させるようである。しかし、NILO-PD試験の最近のプレスリリースによると、安全性と忍容性は高いものの、ニロチニブは臨床的な利益をもたらさなかったという。[R]
リソゾーム酵素
散発性PD患者の約5%に見られるGBA1変異を有する。GBA1遺伝子はリソゾーム酵素であるグルコセレブロシダーゼをコードしており、その活性はGBA1変異のないPD患者で低下していることが分かっており、より広いPD患者集団の治療ターゲットとして興味深いものである。これらの変異は、αシヌクレインのクリアランスに重要なリソソームオートファジーシステムの機能障害に関連している。
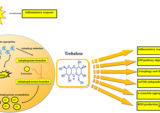
トレハロース

ガストロジン
HSP90
テラゾシン
前立腺肥大症に用いられるα1-アドレナリン拮抗薬であるが、最近、PDの治療薬として期待されてきている。テラゾシンは、phosphoglycerate kinase-1と細胞内ストレス反応に関与するシャペロンタンパク質HSP90を活性化することが見出されている。[R]
テラゾシンは、トランスジェニックマウスおよびLRRK2変異を有するPD患者由来のニューロンにおけるα-シヌクレインレベルを低下させた。[R]
さらに、レトロスペクティブ疫学研究により、テラゾシン服用者はPDの相対リスクが減少することが判明した。[R]
これらの有望な知見により、テラゾシンは、Hoehn and Yahr ステージ 3 の PD 患者 20 名を対象とした無作為化プラセボ対照試験に速やかに移行しましたNCT03905811)。しかし、テラゾシンは血圧を下げるため、起立性低血圧を引き起こす可能性があり、これは進行したPD患者の多くで問題となるため、この疾患への適用が制限される可能性がある。
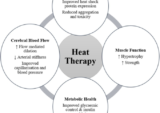
温熱療法
芍薬(ペオニフロリン)
HSPB8
www.ncbi.nlm.nih.gov/pmc/articles/PMC6688727/
ミスフォールドタンパク質の悪影響は、シャペロンタンパク質と分解系からなるタンパク質品質管理システム(PQC)の活性によって打ち消すことができる。
テプレノン
ゲラニルゲラニルアセトン(GGA)、別名テプレノンは、いくつかのHSPの誘導物質であるが、HSPB8の発現を強力にアップレギュレートし、デスミン関連心筋症におけるアミロイドオリゴマーと凝集体の形成を減少させることができることが証明されている。
トレハロース
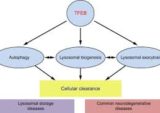
HSPB8の発現を誘導することができる他の小分子は、特徴づけられている。その一つは、オートファジーを誘導する能力でよく知られた無毒の天然化合物であるトレハロースで 、その作用機構は最近解明されている。TFEBは、トレハロースの効果の主なメディエーターである。トレハロース処理は、急速かつ一時的なリソソーム膜の透過と、おそらくリソソームカルシウムの放出によるカルシニューリン/TFEB経路の活性化に相関している。この事象は、オートファジーによる損傷したリソソームの特異的除去(ライソファジーと呼ばれる)と正常なリソソームの恒常性の回復につながるTFEB標的遺伝子の誘導を引き起こす。トレハロースは、細胞および動物モデルの両方において、多くの異なるNDにおいてミスフォールドしたタンパク質の除去に非常に効率的であることが証明されている。
エストロゲン
エストロゲンや選択的エストロゲン受容体モジュレーター(SERM)もHSPB8発現の強力な活性化因子であり、このことは、いくつかの加齢性NDsの発症リスクにおける性差の存在の説明に役立つかもしれない
NF-κBk
HSPB8(とBAG3)の最もよく知られた制御因子の一つがNF-κB転写因子で、これは一般に熱ショック後の回復期に活性化される。この経路の制御はまだ不明瞭であるにせよ、NF-κB経路のモジュレーターが細胞内のHSPB8の発現にも影響を与えることが期待される。
HSF-1
www.ncbi.nlm.nih.gov/pmc/articles/PMC3518299/
HSP90阻害剤
HSP90を薬理学的に阻害すると、HSF1の活性化が促進され、シャペロンタンパク質の発現が増加することになる。
ゲルダナマイシンおよびその誘導体は、アルツハイマー病80-84、パーキンソン病およびハンチントン病などのタンパク質ミスフォールディング病の実験モデルにおいて、HSF1依存性のシャペロンタンパク質の発現を促進し、それによってタンパク質の凝集および細胞毒性を改善する効果があることが証明された。
いくつかのクマリン系抗生物質、特にノボビオシンは、HSP90のC末端領域に結合し、HSP90活性を阻害すると考えられている。
EGCG
(-)-epigallo-catechin-3-gallate, gedunin, AEG3482, ITZ-1などのいくつかの追加化合物もHSP90のC末端ATP結合ポケットに結合してHSP90活性を阻害し94,95HSF1依存のシャペロン蛋白発現活性化を促進した。
ゲラニルゲラニルアセトン(セルベックス)・カルノシン酸亜鉛
ゲラニルゲラニルアセトン(GGA)、カルベノキソロン、亜鉛l-カルノシン、レバミピドなどいくつかの抗潰瘍薬が、シャペロンタンパク質の発現活性化物質として同定されている。
NSAID(アスピリン、イブプロフェン等)
NSAIDsは熱ショックに最適でない温度への曝露と相乗して、HSF1標的遺伝子の発現を促進する。スリンダック、ナブメトン、フェニルブタゾンなどの他のNSAIDsは、より強力なHSF1活性化剤であり、細胞ストレスがない場合でもHSP70の発現を促進するようである。
アリモクロモール
これらの化合物単独ではHSF1依存性のシャペロンタンパク質の発現を促進しないが、その活性はストレスによるHSF1の活性化を長引かせる。
単独ではHSF1活性を誘導できないにもかかわらず、いくつかの神経変性疾患に対する有望な治療薬になる可能性がある。ビモクロモールはシャペロンタンパク質の発現を増幅し、糖尿病、心血管疾患、腎不全の疾患モデルにおいて細胞保護作用を示すことが実験的に示されている。また、ビモクロモールの誘導体であるアリモクロモールは、ALSの治療に有効であるかどうかが検証されている。家族性ALSのモデルであるSOD1G93Aマウスにarimoclomolを投与すると、発症後に投与しても病状が緩和され、寿命が延長した。
急速進行性SOD1型ALSにおけるarimoclomolの無作為化二重盲検プラセボ対照比較試験
www.ncbi.nlm.nih.gov/pmc/articles/PMC5818014/
アリモクロモールは、1日200 mgの用量で安全かつ良好な忍容性を示した。
有害事象の発生頻度は低く、通常は軽度であり、試験薬との関連性は低いかないと判断された。リルゾールとベースラインのALSFRS-Rで調整すると、生存率はアリモクロモルに有利で、ハザード比は0.77(95%信頼区間[CI]0.32-1.80)であった。ALSFRS-R と FEV6 はアリモクロモール群でより緩やかに減少し、治療差はそれぞれ 0.5 ポイント/月(95% CI -0.63~1.63),1.24 percent predicted/月(95% CI -2.77~5.25),CAFS は同様にアリモクロモールが有利であった。
リルゾール
リルゾールは現在、ALSの治療薬として承認されている唯一の薬理学的薬剤ですが、生存期間を3~5ヶ月延長するのみである。最近、リルゾールはまた、HSF1の定常レベルを増加させることにより、シャペロンタンパク質の発現を刺激することが示唆された。
ドーパミン作動性ニューロン
コーヒー・カフェイン

男性へのカフェインの改善効果
疫学的調査では、男性のパーキンソン病患者にのみカフェインでの改善を示した。
www.ncbi.nlm.nih.gov/pubmed/20182023/
ホルモン補充療法とカフェインの併用による高リスク
ホルモン補充療法を受けているカフェイン消費量が女性は、カフェイン消費量が少ない女性よりもパーキンソン病発症リスクが4倍高い。
閉経後ホルモン補充療法を行っていない女性では、カフェインがパーキンソン病発症リスクを低下させることを示唆する。
www.ncbi.nlm.nih.gov/pubmed/12629235/
ナリンゲニン・ナリンギン
神経変性の軽減
グレープフルーツに含むナリンギンはパーキンソン病ラットにおいて、神経変性を減弱させる。
www.ncbi.nlm.nih.gov/pubmed/26878791
黒質・線条体の神経保護
マウスへのナリンゲニンの経口投与は、黒質、線条体のドーパミン作動性神経変性および酸化的損傷に対して有意な保護効果をもたらした。
www.ncbi.nlm.nih.gov/pubmed/23970941/
プエラリン
クズの根に含まれるイソフラボンの一種プエラリンは、パーキンソン病ラットモデルのアポトーシスを阻害し、ドーパミン作動性ニューロンの回復示した。
さらに線条体におけるグリア細胞系由来の神経栄養因子の発現レベルを増加させた。
www.ncbi.nlm.nih.gov/pubmed/20509103
ラサギリン・セレギリン
ラサギリン投与群は、認知症基準を満たさないパーキンソン病患者の言語的流暢性をプラセボ群に比べ有意に改善した。
www.ncbi.nlm.nih.gov/pubmed/21500280/
パーキンソン病の治療薬として病院で処方が可能。または個人輸入
www.takeda.com/ja-jp/announcements/2018/azilect_launch/
www.takeda.com/jp/newsroom/newsreleases/2017/20170921_7840/

脳深部刺激療法(DBS)
脳深部刺激療法(DBS)は、レボドパによる副作用が特に問題となる場合に、ドーパミン依存性の運動症状の治療に有用な、PDのもう一つの確立された治療法である。DBSは、視床下核や内果球を含む皮質下構造を刺激する電極を外科的に埋め込むものである。
DBSは、一部の進行したパーキンソン病患者において、最良の薬物療法と比較して運動症状や変動に著しい改善をもたらすが、振戦以外のドーパミン抵抗性の症状(例:歩行障害や姿勢不安定)は反応性が低い。また、非盲検試験において、DBSは早期パーキンソン病患者において有益であり、振戦スコアの改善とde novo振戦の発生を抑制することが示唆されている。
外科的合併症に加え、DBS戦略は認知および神経精神医学的な副作用、さらに言語機能障害を引き起こす可能性がある。適応型DBS、異なる部位を標的とするDBS、および術中の画像技術の改良を含む新しいDBSアプローチは、臨床適用性の向上と副作用の影響の低減を約束するものである
経頭蓋磁気刺激
電気ショック治療と経頭蓋磁気刺激はレビー小体型認知症で効果的であった。
非ドーパミン性神経伝達系をターゲットとする
PDの運動機能の多くはドーパミンに反応するが、歩行凍結や振戦のような他の機能については、ドーパミンはほとんど役に立たない。現在では、他の神経伝達系における欠陥が、これらの特徴のいくつかに関係していることが理解されている。そのため、ドーパミン抵抗性のPDを治療するために、その機能を調節することに関心が持たれている。
サフィナミド
強力な可逆的モノアミン酸化酵素B阻害剤であり、PDのドーパミン作動性側面の治療に有益である。また、グルタミン酸の伝達を調節し、PDの非運動性の特徴のいくつかに関与している可能性がある。[R]
中等度から進行度のパーキンソン病患者669人を対象とした多施設共同第III相臨床試験において、サフィナミドはUPDRS運動スコアの改善、オフタイムの短縮、うつ病およびコミュニケーションスコアの改善をもたらした。[R]
現在、Safinamideは臨床で広く使われるようになってきているが、その正確な役割はまだ決定されていない。現在のところ、特に問題となるジスキネジアや変動が見られる患者に対して、レボドパベースの治療の補助薬として使用される可能性が高いと思われる。
メチルフェニデート・アトモキセチン
ノルアドレナリン再取り込み阻害剤であるメチルフェニデートとアトモキセチンも、PDのバランスと歩行に対する効果を現在進行中の試験で検討されている。背側皮質核のセロトニン作動性ニューロンは、レボドパによるジスキネジアに関与しているとされ、セロトニン作動薬の使用により、動物モデルでジスキネジアを軽減することが確認されている。しかし、セロトニン作動薬の使用は、いくつかの臨床試験においてPDの他の運動機能の悪化を伴っている68。しかし、レボドパ誘発性ジスキネジアの発症におけるセロトニン系の役割の理解が進んでいるため、治療法としてこの系の調節に関心が持たれている。[R]
アセチルコリンの増強
レビー小体の注意、執行機能、視空間能力障害へは、コリンエステラーゼ阻害剤がよく反応する。レビー小体型認知症患者へのコリンエステラーゼ阻害剤投与は、有害事象が増加するにもかかわらず治療によって死亡率の低下と関連している。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3221408/

リバスチグミン・ドネペジル
さらに、コリンエステラーゼ阻害剤であるリバスチグミンとドネペジルは、PDにおける転倒を減少させる作用について試験され、有望な予備的結果が得られている。[R][R]
ニコチン
translationalneurodegeneration.biomedcentral.com/articles/10.1186/s40035-017-0090-8
男性のみでPDのリスク低下と関連し、女性では関連しないと思われるカフェイン、尿酸塩、およびフラボノイド、とは異なり、喫煙とPDリスクとの強い逆相関が、集団全体の男女で一貫して観察されているのは注目に値する。この関係は、タバコに含まれるニコチンまたは他の化合物が優れた治療薬となり得ることを示唆している。
少量のニコチンが脳内のニコチン受容体のかなりの部分を飽和させるため、食事など他の供給源から摂取したニコチンは、PDに対する予防的治療物質として有望であると考えられる。
食事性ニコチンとPD
www.ncbi.nlm.nih.gov/pmc/articles/PMC5494127/
神経画像研究によって実証されたように、比較的少量のニコチンに暴露されると、ニコチン受容体のかなりの部分が占有されるようになる。この概念は、喫煙-PD関係において喫煙強度よりも長期間の喫煙がより重要であるという観察によってさらに支持されている。タバコの他に、ニコチンは植物相に広く分布しており、生物学的にナイトシェード科に属するいくつかの一般的な野菜に含まれている。それらは、ジャガイモ、トマト、ピーマンなどである。注目すべきは、これらの野菜からの摂取量は、一般にタバコからの摂取量に比べはるかに少ないということだ。
241人のPD症例を含む最近のケースコントロール研究において、食用ナス科野菜を1皿追加するごとに、非喫煙者におけるパーキンソン病リスクが31%低下することが示された(図1)。
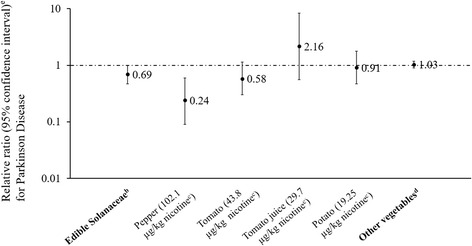
- トマト(平均で1個あたり〜332ngのニコチン)
- ジャガイモ(〜675ng)
- ナス(〜525ng)
www.pmiscience.com/en/smoke-free/nicotine/nicotine-from-plants-to-people/
唐辛子
トウガラシの消費の多さは、女性ではPDのリスクの低下(5回/週以上対3回/月以下の調整済みHR、0.49;95%CI、0.25-0.94)と関連していたが、男性ではそうではなかった(調整済みHR、1.04;95%CI、0.57-1.90)。
www.ncbi.nlm.nih.gov/pmc/articles/PMC7258060/
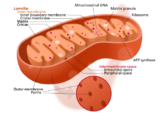
ミトコンドリア機能の改善




ウルソデオキシコール酸(UCDA)
PARKINおよびLRRK2変異を有する患者由来の細胞、ならびにPDの無脊椎動物および齧歯類モデルにおいてミトコンドリア機能を回復することが判明した。[R]
UCDAは最近、無作為化プラセボ対照第II相試験に移行し、現在、早期PD患者30名を募集中である。
抗酸化作用
グルタチオン

N-アセチルシステイン
pubmed.ncbi.nlm.nih.gov/28940353
メラトニン
高用量メラトニン

腸内環境の改善
プレバイオテックと食物繊維の組み合わせ
www.sciencedirect.com/science/article/pii/S0014299917303734#bib106
プレボテラシエ/PREVOTELLACEAE
パーキンソン病患者はPrevotellaceaeファミリー系の細菌がいちじるしく少ない。
www.sciencedaily.com/releases/2014/12/141211081120.htm
プレボテラシエは、動物性脂肪が少なく炭水化物の多い食事をする人々、例えば菜食主義者や非西洋人的な食事をする人々の消化管によく見られる。
shop.ubiome.com/pages/prevotellaceae
ザクロ(ウロリチンA)
ザクロに含まれるエラジタンニンは上部胃腸管で加水分解され、ウロリチンA、B、C、M6、イロソリチンA
www.ncbi.nlm.nih.gov/pubmed/26559394/
ザクロの代謝産物であるウロリチンAは線虫の寿命を45%伸ばし、高齢のマウスに投与すると走る時間が42%延長した。
ウロリチンは損傷したミトコンドリアを除去する。
ザクロに含まれるエラギタンニン → 胃で加水分解されエラグ酸 → 腸内細菌によってウロリチンAの産生
www.kagaku-kentei.jp/news_detail/data/288
230ccのザクロジュースを8週間飲用した軽度の記憶障害を訴える中高年では血漿ウロリチンAの濃度が上昇し、それと相関して言語および視覚記憶が有意に改善した。
www.ncbi.nlm.nih.gov/pubmed/23970941/
メトホルミン
メトホルミンの投与により、酪酸やプロピオン酸などの特定の種類の短鎖脂肪酸を生産する細菌の能力が向上する。
www.sciencedaily.com/releases/2015/12/151202142210.htm
ラクトバチルス・ロイテリ菌
SCFA酪酸生成細菌
onlinelibrary.wiley.com/doi/10.1002/mds.26307/abstract

ビフィズス菌
パーキンソン病の進行は消化不良と関連する。
パーキンソン病患者ではビフィドバクテリウム(ビフィズス菌)が有意に少ない。
L-プランタラム、ブレビス
www.ncbi.nlm.nih.gov/pmc/articles/PMC5665539/
ボーンブロスの摂取

煙草!?
喫煙もまた、パーキンソン病と直感に反して関係がある。50喫煙がリスクを下げる理由はまだ解明されていない。ニコチンが神経細胞を保護することを示唆する研究もあれば、喫煙が環境毒素の分解を促進することを示唆する研究もある51。
喫煙はまた、鼻や腸を経由して保護効果をもたらすかもしれない52。喫煙は、パーキンソン病の原因となる外的要因の侵入をブロックするか、その他の方法で妨害する可能性がある。喫煙の煙はもちろん吸引されるため、鼻腔の被覆や局所的な免疫反応に変化をもたらす53。
喫煙は腸内環境も変化させる。腸内細菌、つまり私たちの腸に住む細菌のコミュニティは、驚くべきものである。100兆個を超える細菌は、体内の人間の細胞の数よりもはるかに多く、私たちの住処となっている54。
例えば、喫煙は腸のバリア機能を高める可能性のある特定のバクテリアの個体数を増加させる56。この腸のバリアは、環境(摂取物)と私たち自身の間の主要な接点であり、有害物質を排除する機能が重要だ。
そのため、喫煙者の腸内細菌数の増加は、バリア機能を高め、パーキンソン病のリスクを高める毒素から喫煙者を守る可能性がある。あるいは、特定の種類の細菌の数が多いため、他の種類の有害な細菌、つまりパーキンソン病の発症要因となり得る細菌を抑えているのかもしれない。2016年の研究では、腸内細菌が病気の発症に寄与していることが示された57。遺伝子改変したマウスに抗生物質を投与して腸内細菌を死滅させると、パーキンソン病の病態が軽減された。
さらに驚くべきことに、この腸内細菌による寄与は伝染する可能性がある。パーキンソン病でない人の糞便(多数の腸内細菌がいる)をマウスに与えたところ、マウスの運動機能は変化しなかったのである。ところが、パーキンソン病の人の糞便をマウスに与えたところ、運動機能が悪化したのである。これらの結果は、腸内細菌が脳に影響を与えている可能性を示唆している。ウンチの移植がパーキンソン病を治療する日が来るかもしれないという超現実的な可能性も含め、新たな病気の腸脳軸を探るため、さらなる研究が必要である58。
喫煙の潜在的な利点が何であるかにかかわらず、誰もパーキンソン病のリスクを減らすために喫煙すべきではないし、喫煙を続けてはならない。この病気との因果関係は証明されていない。また、平均して10年の寿命を失うなど、喫煙の悪影響は、パーキンソン病に関連する潜在的なプラス面をはるかに上回る59。
腸内環境を破壊する因子を避ける
殺虫剤ロテノンが腸管内のαシヌクレインを放出させる。
尿酸値を上げる
尿酸は、フリーラジカルおよび鉄キレート剤として作用することで酸化ストレスを減少させることができる天然抗酸化物質。
運動
運動は尿酸レベルを上昇させる。
パーキンソン病患者の高プリン体ダイエットは疾患の進行を遅らせる可能性がある。
www.ncbi.nlm.nih.gov/pubmed/18618666/
食事
尿酸値を上げる食品(つまり痛風では避けるべき食品リスト)
- 赤肉、魚 サバ、卵、イワシ、パン酵母
- ほうれん草、アスパラガス、レンズ豆、キノコ、エンドウ豆
- ビール、アルコール
イノシン
本研究は経口イノシンの分子標的である尿酸値の上昇を証明した。イノシンは、血清尿酸値を7-8mg/dLまで上昇させ、疾患進行の遅延に関連する濃度を示した。尿酸値を上昇させるイノシン投与は、明らかなベネフィットをもたらさなかった。
イノシン治療のPD進行に対する有益性を示す証拠がないことは、それ以前(診断前)またはそれ以上(数年から数十年)尿酸に曝露したPDにおいて、その有益性を否定するものではない。。尿酸塩ではなく尿酸塩前駆体であるイノシンが投与されたため、尿酸塩上昇の利点を相殺する尿酸塩に依存しない有害な作用が生じた可能性がある。PD患者のごく一部の集団に有効性がある可能性を排除するものではない。INPPK5 については、PD の進行に対する尿酸塩との相互作用を相殺する別の遺伝子変異を持つ集団の可能性が示唆されている。
pubmed.ncbi.nlm.nih.gov/34519802/
ビタミンC

飲尿療法
100mlあたり約1gの尿酸を含む。

細胞内カルシウム恒常性の調整
クレアチン
www.ncbi.nlm.nih.gov/pmc/articles/PMC5457735/
過去に発表された5つの論文のメタアナリシスにおいて、プラセボと比較してクレアチン使用によりSchwab & England Scaleスコアがより改善することが確認された。
ミトコンドリア機能障害を対象とした研究では、クレアチンがうつ病と有意に相関することが明らかになった[31]。この分析に含めたある研究では、クレアチンで治療した患者は精神UPDRSのスコアが有意に良かった(P= 0.046 )ことが判明し 、別の研究では、クレアチンとコエンザイムQ10の併用は、モントリオール認知機能評価法( MoCA )で評価したパーキンソン病患者の認知機能の低下を遅らせることができることが判明した。[R]。したがって、PDの運動症状を緩和するクレアチンの効果に注目するだけでなく、精神症状および認知症状に対する効果も検討する必要がある。
クレアチンのミトコンドリア機能改善効果は以前から証明されていたが、今回の解析ではパーキンソン病患者に対する効果は示されなかった。したがって、ミトコンドリア機能不全はPDの発症に間接的な役割を果たしている可能性があり、他の多くの基礎的な、しかしまだ知られていない要因に影響されやすいという仮説を立てている。したがって、PDの治療に他の神経保護剤を使用することは、まだ研究されるべきである。
ビタミンD

脂質過酸化物の抑制・脂質合成の促進
ベータカロチン
ウリジンとDHAの併用
DHA、ウリジンの継続的な投与はラットの記憶障害を改善する。
www.sciencedirect.com/science/article/pii/S0166432808001186
PPAR
ピオグリタゾン・ロシグリタゾン
pubmed.ncbi.nlm.nih.gov/23469878/
ペルオキシソーム増殖剤活性化受容体γ(PPAR-γ)作動薬、主にチアゾリジン系薬剤、ピオグリタゾンおよびロシグリタゾンは、PD実験モデルにおける神経保護能の検証に成功しているが、細胞標的および基礎となるメカニズムは現在議論のあるところである。
神経保護作用の主なメカニズムとして、抗炎症作用とミクログリア症の抑制が提案されているが、細胞の生体エネルギーと酸化ストレスを制御するミトコンドリアタンパク質など、他の細胞標的が関与している可能性もある。
PPAR-γ作動薬が示す強力な神経保護活性の根底には、複数の機能障害経路を同時に標的とする可能性があることが示唆される。
ミクログリアの過剰活性を抑制
ミノサイクリン(抗生物質)
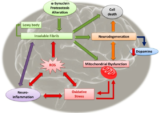
p38 MAPKカスケードを減衰させることでミクログリアの活性化を阻害する。
www.sinobiological.com/P38-MAPK-Signaling-Pathway_image_pp38-mapk-signaling-pathway.html
ミノサイクリンは金属イオンをキレートすることができる。
ミノサイクリンによる強力なドーパミン神経保護効果
ミノサイクリンとクレアチンを組み合わせた神経保護効果
解毒

ニコチン
ニコチンは脳内CYP酵素を誘導する:パーキンソン病との関連性
pubmed.ncbi.nlm.nih.gov/17017527/
シトクロムP450 2B6、2D6および2E1の脳内発現は喫煙者で高く、動物ではニコチンによって誘導される。これらの酵素は、パーキンソン病と関連する多くの神経毒を代謝することができる。喫煙はパーキンソン病に対して予防的であることが知られているので、喫煙者におけるニコチンによる脳内CYPの上昇は、パーキンソン病に対する神経保護に寄与している可能性があると我々は仮定している。このことは、ニコチンがこの病気の進行を遅らせるという治療的利用を支持するものである。
鉄・金属キレート
デフェリプロン
pubmed.ncbi.nlm.nih.gov/28469157/
無作為化二重盲検プラセボ対照試験において、22名の早期発症パーキンソン病患者にdeferiprone(10mg/kg BIDまたはプラセボ)を6ヶ月間投与した。
デフェリプロン治療の忍容性は良好で、プラセボと比較して歯状核と尾状核の鉄分含有量が減少したことに関連した。SNcの鉄量減少は3名のみに認められ、被殻や淡蒼球には変化が認められなかった。30mg/kgのデフェリプロン投与群では、運動機能-UPDRSスコアとQOLに改善傾向がみられたが、有意差には至らなかった。
血清フェリチン値は、デフェリプロンによる鉄キレート療法に最適に反応する患者を特定するための代替マーカーとなるようだ。さらに、血漿フェリチンレベルはIL-6濃度と相関し、PDにおける末梢の炎症と鉄代謝の関連を示唆するものであった。
脳の鉄動員に関しては、試験開始時の血清フェリチン濃度が100ng/ml未満と低いPD被験者において、デフェリプロン治療が最も効果的であることが観察された。このことは、脳の特定部位から鉄を動員する前に、体内の鉄貯蔵量を低下させる必要があることを示唆しているのかもしれない。
結論として、パーキンソン病患者におけるデフェリプロン短期投与は安全であり、脳の特定部位における鉄の減少に関連することが証明された。認知機能および気分は、デフェリプロン治療により悪影響を受けなかった。このようなデータは、PDにおける鉄キレーションの潜在的な利点についてのより広範な臨床試験を支持するものである。
ビタミンE(αトコフェロール)
鉄蓄積を抑制し、ミクログリアの活性化を抑制、酸素ラジカルを補足し、膜脂質のか酸化を防止する。脳内の鉄の蓄積によって引き起こされる酸化ストレスも減少させられると考えられている。
リボフラビン(B2)
フィチン酸 (IP6)
天然鉄キレーター フィチン酸
www.ncbi.nlm.nih.gov/pubmed/18255213/
www.ncbi.nlm.nih.gov/pubmed/9244360/
www.ncbi.nlm.nih.gov/pubmed/21331377/
フィチン酸のヒドロキシラジカル抑制
www.ncbi.nlm.nih.gov/pubmed/12834920/

ロテノンの解毒
無臭の化合物で、フェニルプロパノイドの一種で天然物では植物の根や茎に含まれる。
殺虫剤・殺魚剤・農薬として広く効果を持ち、毒物及び劇物取締法により劇物に指定されている。
ラットに投与するとパーキンソン症候群の原因となる。
www.ncbi.nlm.nih.gov/pubmed/21958946/
ケルセチン
パーキンソン病ロテノンモデルラットでは、ケルセチンを4日間投与すると、線条体におけるドーパミン放出を増強することによって黒質TH陽性ニューロンの喪失を防ぎ、運動機能障害を保護しした。
さらに、ケルセチンは、ミトコンドリア複合体-I活性およびグルタチオン枯渇によるROT誘発性喪失を軽減し、黒質ニューロンにプログラム細胞死を阻止した。
アセチル-L-カルニチン、アルファリポ酸
アセチル-L-カルニチンまたはα-リポ酸による治療は、パーキンソン病ロテノンモデルのラットの運動能力を改善し、脳の脂質過酸化物のレベルを低下させた。
www.ncbi.nlm.nih.gov/pubmed/23357119
クルクミン
www.ncbi.nlm.nih.gov/pubmed/26648392
フェルラ酸
ラットへの4週間のフェルラ酸投与は、黒質領域のドーパミンニューロンおよびロテノンによる損傷を受けた線条体の神経末端を回復させた。フェルラ酸は、脂質過酸化を抑制しながら、抗酸化酵素およびグルタチオンの活性を回復させた。
フェルラ酸による処置後、COX-2および誘導性NOSおよび炎症促進性サイトカインなどの炎症性メディエーターの産生も減少した。フェルラ酸の防御効果は、その抗酸化および抗炎症性の性質を介して発揮される。
www.ncbi.nlm.nih.gov/pubmed/26504373
ナリンゲニン
神経毒MPTPの阻害
N-メチル-4-フェニル-1,2,3,6-テトラヒドロピリジン(MPTP)は、酸化ストレスを介して、ドーパミン作動性変性を誘導する。
www.ncbi.nlm.nih.gov/pubmed/10863545/
MPTPの代謝物は、ドーパミン作動性ニューロンによって選択的に取り込まれ、ミトコンドリアに輸送され、呼吸鎖と干渉し、複合体Iを阻害し、エネルギー枯渇およびROS産生を誘導する。
MPTP誘発神経毒性は、黒質線条体のドーパミン作動性経路に限定され、運動機能障害と関連している。
EGCG
pubmed.ncbi.nlm.nih.gov/35748799/
ECGCは、パーキンソン病(PD)の起源に関係なく、黒質(SN)の神経変性を遅らせるのに有益である可能性がある。
www.ncbi.nlm.nih.gov/pmc/articles/PMC7504552/
緑茶ポリフェノールは、いくつかの遺伝子の発現を調節し、シグナル伝達経路に干渉することによって、PDに対して様々な薬理作用を有することが判明している。
本研究では、食事経路または飲料水とともに投与された緑茶抽出物およびEGCGは、長期間の曝露後でも有害な影響を示さないことが示された。
また、緑茶抽出物を絶食状態で与えたり、濃縮した製剤を使用した場合、肝毒性や消化管への障害が確認されている。さらに、飲料の形態では704 mg EGCG/日、濃縮固体ボーラス投与では338 mg EGCG/日が、成人における摂食条件下での観察された安全レベルと考えられている。
www.ncbi.nlm.nih.gov/pubmed/12387363
www.ncbi.nlm.nih.gov/pubmed/11553681
www.ncbi.nlm.nih.gov/pubmed/28835392
www.ncbi.nlm.nih.gov/pubmed/20541420
www.ncbi.nlm.nih.gov/pubmed/29363729
バイカレイン
www.ncbi.nlm.nih.gov/pubmed/24576689
www.ncbi.nlm.nih.gov/pubmed/24166733
ケンペロール
パーキンソン病モデルマウスへケンペロールを投与することにより、運動協調を改善し、線条体ドーパミンを上昇させ、SODおよびGSH-PX活性を増加させ、MDA含量を低下させることで神経保護効果を示した。
www.ncbi.nlm.nih.gov/pubmed/21804220
ケルセチン処置が、MPTP処置マウスの運動バランスおよび協調を著しく改善する
www.ncbi.nlm.nih.gov/pubmed/22454690
ノビレチン
www.ncbi.nlm.nih.gov/pubmed/25325362
www.ncbi.nlm.nih.gov/pubmed/24316474
ミルクシスル(シリビニン)
www.ncbi.nlm.nih.gov/pubmed/24660866
www.ncbi.nlm.nih.gov/pubmed/25677261
www.ncbi.nlm.nih.gov/pubmed/24345573
ガストロジン
www.ncbi.nlm.nih.gov/pubmed/24345573
サルビア
www.ncbi.nlm.nih.gov/pubmed/25666429
フェルラ酸
www.ncbi.nlm.nih.gov/pubmed/25857436
クルクミン
www.ncbi.nlm.nih.gov/pubmed/18408903
www.ncbi.nlm.nih.gov/pubmed/14680686
ジンセノサイドRg1
www.ncbi.nlm.nih.gov/pubmed/15659115
ルテオリン
www.ncbi.nlm.nih.gov/pubmed/25857436
GDNFを増やす
グリア細胞由来神経栄養因子(GDNF)などの神経栄養因子は、前臨床モデルにおいてドーパミン作動性ニューロンに対して有益な効果を示し、これらを用いた神経保護療法の開発に注目が集まっている。
pubmed.ncbi.nlm.nih.gov/9316852/

Neurturin
GDNFのアナログであるNeurturinもまた、患者で試用され、GDNFで見られたのと同様の結果、すなわち、有望な非盲検試験で、大規模試験での臨床効果に結びつかなかった78-81。しかしながら、最適な患者の決定、投与システムの改善、新しい神経栄養因子アナログの開発により、この方法は依然として注目されており、現在、脳ドパミン神経栄養因子(CDNF、Herantis Pharma)を対象とした新しいEU資金による試験で検討されている。最近、プレスリリースで、この薬剤は大きな副作用なく投与できることが報告されたが、患者にとって治療効果があるかどうかを判断するのは時期尚早である。
グルコセレブ(GBA)の最適化
GCase競合阻害剤
www.ncbi.nlm.nih.gov/pubmed/17187079/
アンブロキソール(去痰薬)
www.ncbi.nlm.nih.gov/pubmed/23158495/
www.sciencedaily.com/releases/2016/02/160222112642.htm
www.ncbi.nlm.nih.gov/pubmed/24574503
イソファゴミン(IFG)
www.ncbi.nlm.nih.gov/pubmed/22167193/
セラストロール
www.ncbi.nlm.nih.gov/pmc/articles/PMC3890874/
LRPK2標的
LRPK2は家族性パーキンソン病の原因遺伝子のうちもっとも高い頻度をもつ。
LRRK2遺伝子変異パーキンソン病患者は、孤発性パーキンソン病患者と類似する臨床症状および病理学的所見が観察される。
一部の患者ではレビー小体陰性の症例報告もあり、LRRK2変異の神経病変には多様性があると考えられている。
HSP90阻害剤
https://alzhacker.com/hsp/
抗酸化剤
抗酸化物質はパーキンソン病に関連するLRRK 2 の神経毒性を抑制する。
- ピセアタンノール
- チモキノン
- エスクレチン
クルクミン、シリマリン、緑茶抽出物(フラバン3オールカテキン)、グレープシード抽出物、
www.ncbi.nlm.nih.gov/pmc/articles/PMC4818746/
ビタミンB12
LRRK2モジュレーター
小胞体ストレスの軽減


その他
精神障害への対応
抗精神病薬
レビー小体型認知症の管理上最も憂慮すべき判断は、抗精神病薬であり、それらの投薬をやめれば、死亡リスクは著しく低くなる。
ピマバンセリン・メラトニン・クロナゼパム
選択的セロトニン5-HT2Aアゴニスト、ピマバンセリンは、シヌクレイン関連の精神障害への代替療法として有望。メラトニン、クロナゼパムが有効。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4448151/
レム睡眠行動障害の改善
メラトニン(徐放剤)
レム睡眠行動障害は低用量のクロナゼパムで治療することができる
www.ncbi.nlm.nih.gov/pubmed/14596656


非薬理学的介入
レビー小体型認知症への非薬理学的介入 システマティックレビュー
www.ncbi.nlm.nih.gov/pmc/articles/PMC6088773/
嚥下障害
最も強力な証拠は、嚥下障害のある参加者における液体の誤嚥を防ぐための介入を評価したランダム化対照試験から得られた。この試験では、132人のパーキンソン病認知症患者において、蜂蜜でとろみをつけた液体、ネクターでとろみをつけた液体、およびあごを引いた姿勢を比較した。その結果、ハチミツ入り飲料の使用は、ビデオ透視検査による液体の誤嚥防止において、他の2つの方法より優れていることがわかった。[R]
電気けいれん療法
つの小規模非対照研究-合計22名の参加-では、電気けいれん療法がレビー小体型認知症のうつ病治療に一定の効果があることがわかった。これらの研究の1つでは、2人の患者が電気けいれん療法直後に混乱を示し、別の研究では、不特定多数が自律神経機能障害の兆候を示したが、持続的な効果はなかった。その他の有害事象は報告されていない。
リポ多糖類の治療
www.ncbi.nlm.nih.gov/pubmed/23821823
ホモシステインの治療
www.ncbi.nlm.nih.gov/pubmed/22418789

オックスフォード大学医学者によるパーキンソン病治療メソッド
- メラトニン(徐放剤)2mg を夜に摂取。
- アルファリポ酸200~400mg /日 、アセチル-L-カルニチン250~500mg /日
- コエンザイムQ10 200mg /日を最大800mg/日の分割投与で、改善するまで増やす。後に200〜400mg /日を維持用量として投与する。
- ビタミンE(コエンザイムQと一緒に1日1回400IU)
- アセチル-L-カルニチン250mgを夜に投与
栄養補助食品
関連記事