Is a COVID-19 vaccine developed by nature already at work?
要旨
COVID-19陽性例は世界中で驚くべき勢いで増加している。その一方で、罹患率や死亡率は時間の経過とともに減少傾向にある。特に興味深いのは、無症候性の重症急性呼吸器症候群コロナウイルス2(SARS-CoV-2)陽性者が増加していることで、免疫が徐々に発達しているのではないかと推測される。これまで、SARS-CoV-2関連分子粒子パターン(SAMPPs)の蓄積については注目されていなかったが、本研究では、SARS-CoV-2関連分子粒子パターン(SAMPPs)の蓄積に着目した。
本論文では、SARS-CoV-2の大きさと呼吸器分泌物中のウイルスの脱離の活発さから、SAMPPsの概念を紹介し、SARS-CoV-2が無生物に存在することは十分に考えられる。SAMPPは粘膜表面やそれに関連した抗原提示樹状細胞と接触することができる。
このことから、SARS-CoV-2感染症に対する免疫の発達にはSAMPPsの存在が関与していると考えられ、その結果、無症状患者の罹患率は増加し、死亡率は減少したと考えられた。今後,SARS-CoV-2感染症に対する自然免疫に関わるSAMPPsの存在を理解するために,SAMPPsに関連する様々な分子粒子に対する血清抗体レベルを調べるために,集団ベースの血清検査を実施することが推奨される。
キーワード SARS-CoV-2,COVID-19,コロナウイルス、ワクチン、免疫
序論
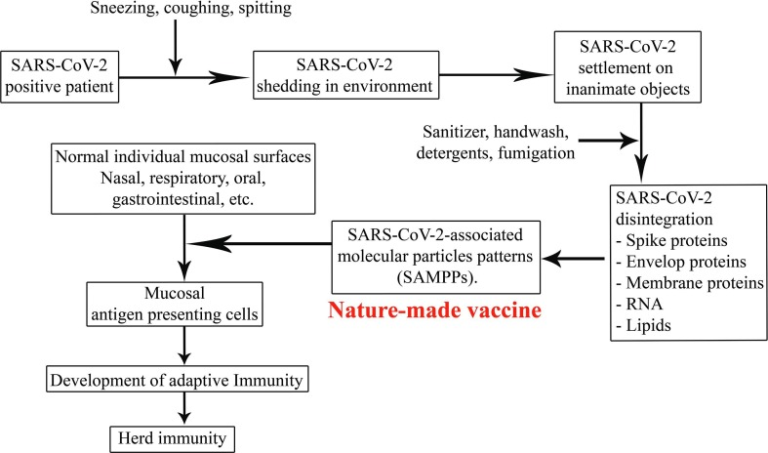
Severe Acute Respiratory Syndrome Corona Virus 2 (SARS-CoV-2)の大パンデミックに伴い、医薬品や非医薬品を含めた介入に関する多くの見解や考え方が出てきている[1]。数多くの薬剤が経験と有用性に応じて経験的に使用されているが、副作用の程度は様々である[2]。医薬品による介入の中でも、ワクチンや薬剤ベースの介入が主な候補となっている。近年、SASR-CoV-2に対するrDNA技術に基づくRNAおよびDNAワクチンについて、有望で興味深いデータが蓄積されている[3]。図1.
図1 天然物ワクチンとしてのSARS-CoV-2関連分子粒子パターンのメカニズムを示すフローチャート
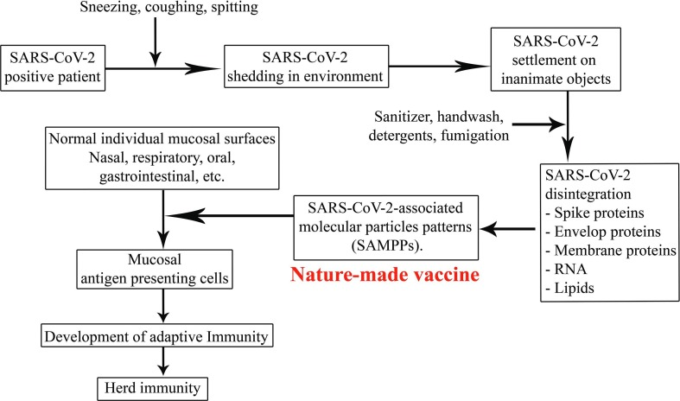
SARS-CoV-2陽性者は、1日平均で約2,55441人(2020年8月5日の7日移動平均値)と驚くべき勢いで増加している[4]。一方、罹患率・死亡率は時間の経過とともに減少傾向にある。初期の症例死亡率(CFR)は15%(41例中6例)であった[5]。その後、時間の経過とともにCFRは4.3%から11%に低下し [6], [7] 、その後3.4%に低下した [8]。2月に中国以外で報告された率はさらに低かった(0.4%;464人中2人)[9]。何よりも興味深いのは、無症候性のSARS-CoV-2陽性者が増加していることであり、徐々に免疫が発達しているのではないかと推測された。COVID-19感染症の病態解明が進んでいるにもかかわらず、死亡率や無症候性症例が減少している理由については、これまでの文献には明確な報告がなかった。
これらの薬剤介入の将来的な役割にもかかわらず、我々は自然界からの寄与として、SARS-CoV-2関連分子粒子パターン(SARS-CoV-2関連分子粒子パターン:SAMPPs)の蓄積を無視してきた。無生物にSAMPPが存在することは、呼吸器分泌物中のウイルスの大量脱落と、ウイルスの大きさによる沈降のしやすさから考えられる。これを裏付けるように,物体表面から採取したサンプルからも空気中のサンプルからもSARS-CoV-2 RNAが検出されている[10], [11], [12].本論文では、SAMPPsの概念と適応免疫の発達におけるメカニズムについて、科学的根拠と正当性をもって紹介した。
仮説
SARS-CoV-2に対する石鹸、洗剤、除菌剤、または他の噴霧化学物質などの要因の作用は、SAMPPsの形成を導く。SAMPPsは無生物上に存在し、コミュニティのCOVID-19感染地域に豊富に存在する。粘膜接触後、SAMPPsは、それらのパターン認識受容体の徳によって抗原提示細胞(主に樹状細胞)によって認識される。さらなる免疫学的事象は、SAMPPsの様々な構成要素の分子単位に対する抗体の開発につながる。抗原提示細胞にSAMPPsを繰り返し曝露することで、SARS-CoV-2に対する免疫力の低下を防ぐことができる。このように、SARS-CoV-2感染症に対する免疫の発達にはSAMPPsが関与していると考えられ、その結果、無症候性症例の罹患率が増加し、死亡率が低下した。また、SARS-CoV-2感染症に対する自然に発達した集団免疫を達成する上で、このメカニズムの意義を提案する。
自然が生み出したCOVID-19ワクチンとしてのSAMPPs
世界レベルでは、石鹸、洗剤、消毒剤、除菌剤、その他の散布剤などの非医薬品による介入は、SARS-CoV-2の感染を食い止めるのに非常に有効である[13]。さらに、再利用可能なフェイスマスクは、WHOによって防護措置として推奨されている。これらの再利用可能なマスクは、石鹸、洗浄剤、消毒剤、その他の噴霧化学物質で処理されており、これが不活化・殺処分されたSARS-CoV-2とその分子粒子の蓄積地点としても機能している可能性がある[14]。この場を借りて、この実体をSAMPPsとして造語する。
咳やくしゃみをすることにより、鼻咽頭分泌物がSAMPPsへの寄与の主な供給源となる。しかし、唾液はSARS-CoV-2を保有していることも報告されており、RT-PCRを用いた診断検査のための媒体として有望視されている[15]。これらの情報から、唾液が飲食などの無生物と接触するすべての活動がSAMPPsの形成に寄与する可能性があることを想定した。
実際には、石鹸、洗剤、除菌剤、および他の噴霧化学物質は、自然界では非常にアルカリ性である。SARS-CoV-2の3つの主要な構成要素は、脂質、RNA遺伝物質、および標的細胞への付着を担うSPIKEタンパク質などの糖タンパク質を含むタンパク質である[16]。原核生物系、真核生物系のゲノムを含むRNA物質の不安定性を示す事実は確立されている。生物学的試料から得られたウイルスRNAゲノムは、アルカリ性条件下で加水分解されるというデータがある[17]。RNA ゲノムを含むインフルエンザウイルスの場合も同様の可能性が期待される。自然由来のワクチンの生成は、数十年のうちに対象となるヒトの免疫が観察されたことに起因しているかもしれない。SARS-CoV-2の最も感染性の高いタンパク質はSPIKEタンパク質であり,糖タンパク質の一種であることに注意が必要である.糖タンパク質は、数種類のウイルスのRNAや脂質などの生体分子と比較して、アルカリ性条件下でも安定性が高いというデータがある[18], [19]。
SARS-CoV-2による罹患率・死亡率の傾向が発症率と相関を示さないことから、自然界で作られたワクチンが免疫の発達に寄与していることを裏付けることができる。我々は、自然界で作られたワクチンが、石鹸、洗剤、消毒剤、その他多くの化学物質の使用を含む非医薬品介入の間にSAMPPsが直接または間接的に曝露された主な原因ではないかと推測している。SAMPPの性質および組成は、動的で不均質なものとなるであろう。しかし、理論的には、ウイルスの様々な成分とそのサブユニットであるエンベロープ(E)スパイク(S)膜(M)ヌクレオカプシド(N)から構成されていると考えられている。
著者らは、抗原性スパイク糖タンパク質を含むSARS-CoV-2成分に基づく非医薬品的介入は、目、口腔、呼吸器、鼻、生殖器、消化管などの様々な経路で宿主体内に侵入する可能性があると指摘している。興味深いことに、抗原性SPIKE糖タンパク質を含むSAMPPのこれらの進入点は、これらの組織系内に存在する抗原提示細胞の潜在的な供給源である可能性があり、曝露された患者の間で体液性および細胞性免疫応答に寄与し得ることに留意すべきである。SAMPPsは常に無生物上に存在するため、繰り返しの曝露はブースター用量として作用し、SARS-CoV-2に対する免疫力の低下を防ぐのに役立つことが予想される。さらに、SAMPPに由来する複数の抗原への曝露は、SARS-CoV-2に対するより包括的な抗体反応を提供する可能性がある。このことは、近年の無症候性症例の増加と死亡率の低下に非常によく表れている。我々はまた、提案されたコンテンションが、SARS-CoV-2に対する自然群免疫の発達にも責任を持つと考えている。
RNA/DNAベースのワクチンの潜在的な限界
近年、rDNA技術は、インフルエンザおよびSARS-CoV-2ウイルスを含む多くのウイルスに対するRNA/DNAベースのワクチンの設計を可能にした[3]。mRNAベースのワクチンに対する免疫応答の生成の可能性に関するデータが蓄積されているにもかかわらず、mRNAまたはDNAベースのワクチンが宿主細胞系によって遺伝的に改変または編集される可能性がある。このようにして、標的集団間の遺伝的不均一性に起因する望ましくない効果および非応答性が予想され得る。そのようなmRNAまたはDNAベースのワクチンのより頻繁な投与が、標的集団の寿命の間に必要とされ得る。バイオアベイラビリティの形での制限は、宿主患者間でのRNA/DNAベースのワクチンの親への投与中にも可能であり、そのような問題は、対象集団間で不均一であるかもしれない。もう一つの限界は、短い時間枠内でワクチン接種を必要とする78億人以上の人口に対して、必要なワクチンの用量を利用できるかどうかである。
もし、SAMPPsを媒介とした免疫が宿主に存在することが適切な実験で証明されれば、高価なRNA/DNAベースのワクチンの必要性を妨害することになるであろう。逆に言えば、SAMPPs媒介免疫の証拠がない患者だけが、どのような形のヒト由来ワクチンであってもワクチン接種の対象となり得るということである。
仮説の検定
この仮説を証明するためには、無生物上にSAMPPが存在することを証明することが最も重要である。これは、包括的な高分解能質量分析装置を用いた綿棒サンプルの分析によって達成される。さらに、生物に付着した様々なSARS-CoV-2粒子のより特異的な同定と確認は、リアルタイム逆転写ポリメラーゼ連鎖反応を用いて行うことができる。すでに文献研究では、大気中だけでなく様々な物体表面にSARS-CoV-2 RNAが存在することが確認されている[10], [11]。COVID-19の指定病院では、触れることのできる表面のほとんどがウイルスで汚染されており[12]、環境がSAMPPの潜在的な存在媒体であることが示唆されている。
SARS-CoV-2に対する自然免疫に関連するSAMPPsの存在を理解するために、SAMPPsに関連する様々な分子粒子に対する血清抗体レベルを調査するために、将来の集団ベースの研究が推奨される。具体的には、スパイク蛋白質、小エンベロープ糖タンパク質、膜糖タンパク質、ヌクレオカプシド蛋白質、およびいくつかの付属タンパク質を含むことができる。さらに研究に深みを持たせるためには、前述の各タンパク質のドメインやサブドメインに対する抗体産生を調べることができる。SARS-CoV-2陰性または無症候性SARS-CoV-2陽性患者にこれらの抗体が存在することは、提案された仮説をより強固なものにするだろう。
最近、様々な集団環境における抗SARS-CoV-2抗体を同定するために、文献の中で抗SARS-CoV-2抗体の血清プレバランス研究が急速に増加している。同様の根拠に基づくシステマティックレビューでは、親密な接触者と高リスクの医療従事者では、それぞれ22.9%(95%CI:11.1-34.7%)14.9%(4.8-25.0%)と高い血清分離率が報告されている。しかし、低リスクの医療従事者では5.5%(4.6-6.4%)一般集団では6.3%(5.5-7.1%)とわずかに低率であった[20]。このデータは提案された仮説を支持するものではあるが、今後の同様の研究により、この仮説をさらに強固なものにしていくことを推奨する。