Genetically modified foods: safety, risks and public concerns—a review
www.ncbi.nlm.nih.gov/pmc/articles/PMC3791249/
要旨
遺伝子組み換えは、動物、植物、または微生物などの生物の遺伝的機械を変更する遺伝子技術の特別なセットである。異なる生物の遺伝子を組み合わせることは組換えDNA技術として知られており、結果として得られる生物は「遺伝子組み換え(GM)」「遺伝子組み換え」「トランスジェニック」と言われている。
畑で商業的に栽培されている主要なトランスジェニック作物は、除草剤および殺虫剤耐性のある大豆、トウモロコシ、綿およびキャノーラである。その他、アフリカの収穫物の大部分を破壊する可能性のあるウイルスに耐性のあるサツマイモ、アジア諸国の慢性的な栄養不良を緩和する可能性のある鉄分とビタミンを増加させたコメ、極端な天候にも耐えられる様々な植物などが商業的に栽培されている。
B型肝炎などの感染症に対する人間用ワクチンを生産するバナナ、より早く成熟する魚、何年も早く収穫できる果樹やナッツの木、ユニークな特性を持つ新しいプラスチックを生産する植物などがある。遺伝子組み換え食品のための技術は、21世紀の最大の課題のいくつかの分野を満たすための劇的な可能性を提供している。
すべての新しい技術と同様に、それらはまた、既知と未知の両方のいくつかのリスクをもたらする。遺伝子組み換え食品や作物を取り巻く論争や世間の関心は、一般的に人間と環境の安全性、ラベリングと消費者の選択、知的財産権、倫理、食糧安全保障、貧困削減と環境保全に焦点を当てている。遺伝子操作に関するこの新しい技術で 「母なる自然を改ざん 」することのリスクは何か?
このレビューでは、遺伝子組み換え食品や組換え技術に関わる安全性、環境・生態系リスク、健康被害に関する主要な懸念事項についても言及する。
キーワード
遺伝子組み換え食品、遺伝子組み換え食品、トランスジェニック食品、食品の安全性、アレルギー性食品、国民の関心事
序論
科学者たちは1946年に、DNAが生物間で転送されることを初めて発見した(Clive 2011)。現在では、DNAの移動にはいくつかのメカニズムがあり、これらが自然界で大規模に発生していることが知られており、例えば、病原性細菌の抗生物質耐性の主要なメカニズムとなっている。1983年には、抗生物質耐性を持つタバコの植物を使って、初めて遺伝子組み換え(GM)植物が生産された。
中国は、ウイルス耐性タバコの導入により、1990年代初頭にトランスジェニック作物を商業化した最初の国であった。1994年、トランスジェニック「フレーバーセーバートマト」は、米国での販売のために食品医薬品局(FDA)によって承認された。この改良により、トマトはピッキング後に熟すのを遅らせることができるようになった。
1995年には、いくつかのトランスジェニック作物が市販承認を受けた。これには、オイル組成を変更したキャノーラ(Calgene)、Bacillus thuringiensis(Bt)コーン/メイズ(Ciba-Geigy)、除草剤ブロモキシニル(Calgene)、Bt綿(Monsanto)などが含まれている。Bt ジャガイモ(モンサント社)、除草剤グリホサートに耐性のある大豆(モンサント社)、ウイルス抵抗性スカッシュ(アスグロウ社)、追加の遅熟トマト(DNAP、ゼネカ/ペト、モンサント社)(Clive 2011)。
1996年までに6カ国とEUで8つの異なる形質を持つ8つの遺伝子組み換え作物とカーネーションの花の作物を商業的に栽培するために、合計35の承認が与えられてた(Clive 1996)。2011年現在、米国は遺伝子組み換え作物の生産で複数の国のリストをリードしている。現在、遺伝子組み換えバージョンが存在する食品種の数がある(ジョンソン2008)。
市場に出回っている食品には、綿花、大豆、キャノーラ、ジャガイモ、ナス、イチゴ、トウモロコシ、トマト、レタス、カンタロープ、ニンジンなどがある。現在開発中の遺伝子組み換え製品には、医薬品やワクチン、食品・食品原料、飼料、繊維などがある。昆虫抵抗性や望ましい栄養素など、重要な形質の遺伝子を見つけることは、このプロセスの中で最も重要なステップの一つである。
遺伝子組み換え作物に由来する食品
現在、食用として使用されている遺伝子組み換え作物はいくつかある。現在のところ、食用として承認されている遺伝子組み換え動物はないが、遺伝子組み換えサケがFDAの承認を目指して提案されている。直接食品として消費されるケースもあるが、ほとんどの場合、遺伝子組み換えを行った作物が商品として販売され、さらに食品原料として加工されている。
果物や野菜
パパイヤは遺伝子操作によりリングスポットウイルスに強い品種が開発され、生産性が向上した。1990年代初頭、ハワイのパパイヤ産業は、致命的なリングスポットウイルスの影響で大惨事に見舞われてた。このウイルスに耐性を持たせた品種を開発したのが、唯一の救世主であった。これがなければ、ハワイのパパイヤ産業は崩壊していたであろう。現在、ハワイのパパイヤの80%は遺伝子組み換え品種で、リングスポット・ウイルスの防除には従来の方法や有機栽培の方法はない。
ニューリーフ™ポテトは、収穫量を奪うコロラド州のポテトビートルから苗を守るために、土壌中に存在する天然のバクテリア(Bacillus thuringiensis (Bt))を使用して開発された遺伝子組み換え食品である。これは1990年代後半にモンサント社がファーストフード市場向けに開発したもので、市場に持ち込まれた。これは、ファーストフードの小売業者がこれを取り上げなかったため、2001年に市場からの撤退を余儀なくされ、その結果、食品加工業者は輸出問題に直面した。報告によると、現在、遺伝子組み換えジャガイモは、人間の消費を目的として販売されていないという。しかし、農業のための植物バイオテクノロジーソリューションの主要なサプライヤーの一つであるBASFは、その’Fortunaジャガイモ’のための食品や飼料としての栽培とマーケティングのための承認を要求した。この遺伝子組み換えジャガイモは、メキシコの野生ジャガイモ「Solanum bulbocastanum」に由来するblb1とblb2の2つの抵抗性遺伝子を追加することで、晩枯病に対する抵抗性を持たせたものである。2005年現在、アメリカで栽培されているズッキーニの約13%が3つのウイルスに抵抗するように遺伝子組み換えされている;このズッキーニはカナダでも栽培されている(Johnson 2008)。
植物油
米国では、元々の遺伝子組み換え作物から抽出された植物油には、タンパク質やDNAが全く残っていないか、または著しく少ないと報告されている。植物油は、食用油、マーガリン、ショートニングなどとして消費者に販売され、惣菜などに使用されている。植物油は、植物や種子から抽出したトリグリセリドを精製した後、さらに水素化処理を経て液体の油を固体にする場合がある。精製工程では、ほぼすべての非トリグリセリド成分が除去される(Crevel er al)。 食用油、マーガリン、ショートニングもまた、いくつかの作物から作られることがある。米国で生産されるカノーラの大部分は遺伝子組み換えであり、主に植物油の生産に使用されている。カノーラ油は世界で3番目に広く消費されている植物油である。遺伝子組み換えは、除草剤であるグリホサートやグルホシネートに対する耐性を付与し、油の組成を改善するために行われている。キャノーラ種子から油分を除去した後、約43%のミールは高品質の飼料として使用されている。キャノーラ油は、多くの食品の主要成分であり、マーガリンまたは食用油として消費者に直接販売されている。カノーラ油は多くの食品以外の用途にも使用されており、口紅などにも使用されている。
トウモロコシは、アメリカではトウモロコシと呼ばれ、トウモロコシを挽いて乾燥させたコーンミールは、世界の多くの地域で主食となっている。アメリカとカナダでは1997年から栽培されており、2010年にはアメリカのトウモロコシ作物の86%が遺伝子組み換え(Hamer and Scuse 2010)、2011年には世界のトウモロコシ作物の32%が遺伝子組み換え(Clive 2011)となっている。収穫されたトウモロコシの大部分は、蒸留機用穀物を含む家畜の飼料に使用されている。残りはエタノールや高果糖コーンシロップの生産、輸出に使用されており、他の甘味料、コーンスターチ、アルコール、人間の食べ物や飲み物にも使用されている。トウモロコシ油は、食用油として直接販売され、ショートニングやマーガリンを作るためのほか、ビタミン担体を作るため、レシチンの供給源として、マヨネーズ、ソース、スープなどの惣菜の材料として、またポテトチップスやフライドポテトを揚げるためにも使用されている。綿実油はサラダ油や食用油として、国内でも工業的にも使用されている。アメリカの綿花の93%近くが遺伝子組み換えである。
砂糖
アメリカは砂糖の10%を他国から輸入しており、残りの90%は国産の甜菜とサトウキビから抽出されている。国産の砂糖のうち、半分が甜菜から、残りの半分がサトウキビから抽出されている。2005年の規制緩和後、米国ではグリホサート耐性のある甜菜が広く採用されるようになった。米国では、テンサイの 95%のエーカーにグリホサート耐性の種子が植えられている(Clive 2011)。除草剤耐性のある甜菜は、オーストラリア、カナダ、コロンビア、EU、日本、韓国、メキシコ、ニュージーランド、フィリピン、ロシア連邦、シンガポール、米国で承認されている。シュガービーツの食品は、精製された砂糖と糖蜜である。精製工程で残ったパルプは、動物の飼料として利用されている。遺伝子組み換え甜菜から作られた砂糖は高度に精製されており、DNAもタンパク質も含まれておらず、非遺伝子組み換え甜菜から作られた砂糖と同じショ糖に過ぎない(Joana er al)。
食品中の遺伝子組み換え生物(GMO)の定量化
食品や飼料中の遺伝子組み換え作物の検査は、DNA マイクロアレイや qPCR のような分子技術を用いて日常的に行われている。これらの検査は、p35S、tNos、pat、bar、またはMon810、Bt11、またはGT73のような公式のGMOのためのイベント固有のマーカーのような遺伝的要素をスクリーニングすることに基づいている。アレイベースの方法は、マルチプレックス PCR とアレイ技術を組み合わせて、スクリーニング要素、植物特異的マーカー、イベント特異的マーカーなどの異なるアプローチを組み合わせて、異なる潜在的な GMO のサンプルをスクリーニングする。qPCR は、スクリーニング要素またはイベント特異的マーカーのための特定のプライマーを使用して、特定の GMO イベントを検出するために使用される。偽陽性または偽陰性の結果を避けるためには、コントロールが必要である。例えば、ウイルスに汚染されたサンプルの場合に偽陽性を回避するために CaMV の検査が使用される。
Joanaら(2010)は、ラウンドアップレディ(RR)大豆の存在をモニタリングするために、完全な工業用大豆油処理チェーンと共にDNAの抽出と検出を報告している。終点ポリメラーゼ連鎖反応(PCR)によるダイズレクチン遺伝子の増幅は、抽出と精製の全工程で達成された。イベント特異的プライマーを用いた PCR アッセイによる RR ダイズの増幅もまた、抽出と精製の全工程で達成された。これは、試料が不安定なためか、中和、洗浄、漂白といった精製の中間段階を除いたものである。特定のプローブを用いたリアルタイム PCR アッセイではすべての結果が確認され、完全に精製された大 豆油中の遺伝子組み換え作物を検出して定量することが可能であることが証明された。
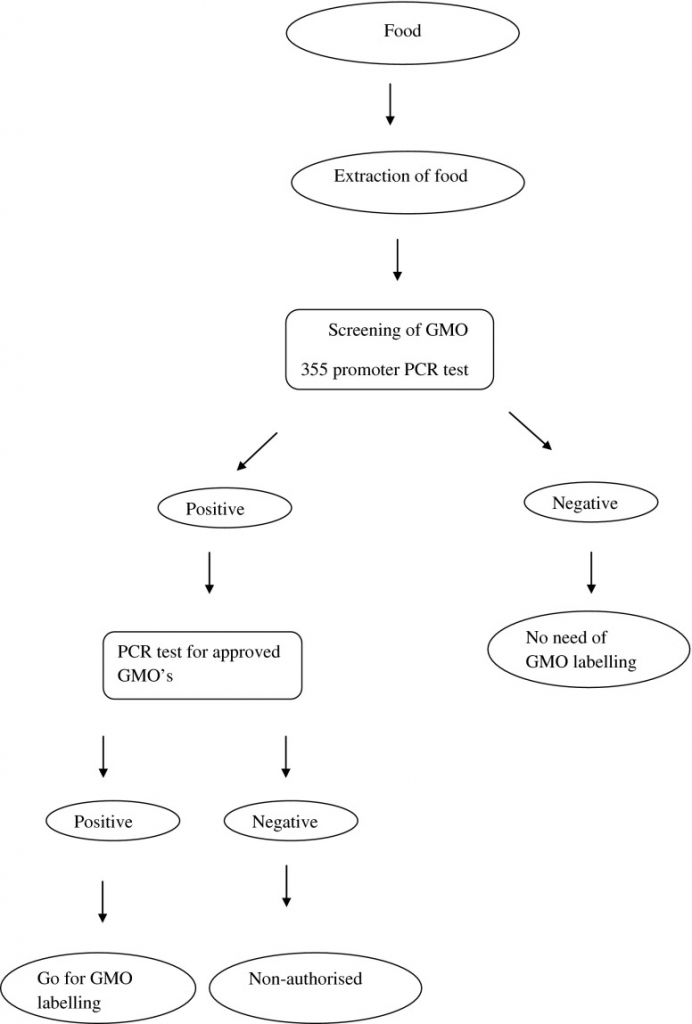
図 1 は、遺伝子組み換え作物の検査の全体的なプロトコルを示したものである。これはカリフラワーモザイクウイルスに由来する 35S プロモーター領域に特異的な PCR 検出システムに基づいている(Deisingh and Badrie 2005)。35S-PCR法は、食品や原材料中のGMO含有量を0.01~0.1%の範囲で検出することが可能である。定量的競合 PCR(QC-PCR)、リアルタイム PCR、ELISA システムなどの定量的検出システムの開発により、ほとんどの製造工程で DNA の生存率が向上した。それ以外のELISAでは、食品加工中にタンパク質の変性がある可能性がある。実験室間の差は、QC-PCR の方が定量 PCR よりも少ないことがわかったが、これはサンプルの均質化が不十分であったためであろう。しかし、主に増幅される可能性のある DNA の量が食品加工技術の影響を受け、最大で 5 倍まで変化するという欠点がある。そのため、植物特異的な QC-PCR システムを用いて結果を正規化する必要がある。さらに、増幅できない DNA は、すべての定量的 PCR 検出システムに影響を与える。
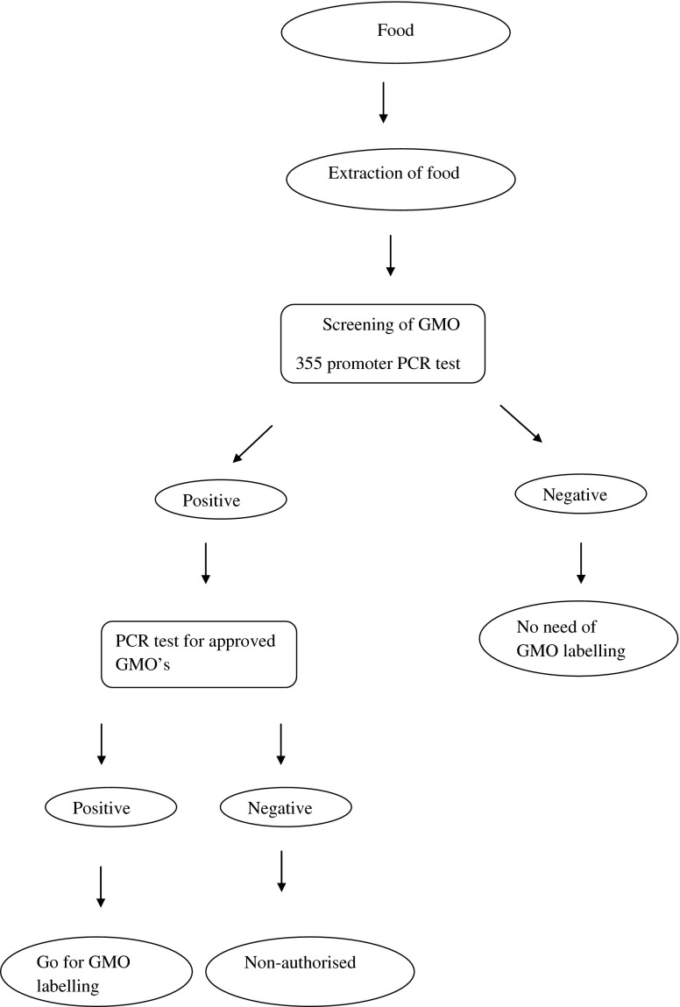
図1 遺伝子組み換え食品の試験のためのプロトコル
最近の研究では、La Mura ら(2011)は、QUIZ(情報ゼロを用いた量子化)を適用して、片方または両方の GM を含む加工食品中の RoundUp Ready™ 大豆と MON810 の含有量を推定した。QUIZを用いることで、認証された標準物質を必要とせずにサンプル中のGMの定量が可能であることを報告している。結果は、導き出された値と既知の遺伝子組み換え原料の入力との間に良好な一致が見られ、定量的リアルタイムPCRと比較しても良好な結果が得られた。ループ媒介等温増幅とラテラルフローディップスティックを組み合わせたラウンドアップレディダイズの検出は、最近報告されている(Xiumin er al)。
遺伝子組み換え食品のメリットとデメリット
遺伝子組み換え食品を持つことを考える前に、安全性に関しては特にメリットとデメリットを知っておくことが非常に重要である。遺伝子組み換え食品とは、DNAに他の種の遺伝子を挿入して作られた食品のことである。この種の遺伝子組み換えは植物でも動物でも行われているが、後者よりも前者の方が一般的である。専門家は、特定の疾患や病気を緩和する能力を持つ食品の開発に取り組んでいる。研究者やメーカーは、これらの食品を消費することの様々な利点があることを確認しているが、人口のかなりの部分が完全にそれらに反対している。
遺伝子組み換え食品は、特定の病気の発生を制御するのに有用である。これらの食品のDNAシステムを変更することにより、アレルギーの原因となる特性が正常に除去される。これらの食品は、伝統的に栽培されている食品よりも早く成長する。おそらくこのために、生産性の向上は、より多くの食品を人口に提供している。また、干ばつの多い場所や、土壌が農業に適していない場所では、これらの食品は恩恵をもたらする。時には、遺伝子操作された食品作物は、あまりにも不利な気候条件を持つ場所で栽培することができる。通常の作物は、特定の季節や好ましい気候条件の下でしか育たない。このような食品のための種子は非常に高価であるが、害虫や昆虫に対する自然の抵抗力のため、生産コストは従来の作物よりも低いと報告されている。これにより、有害な農薬や殺虫剤を使用する必要性が減り、化学物質を使用しない、環境にも優しい食品となっている。遺伝子組み換え食品は栄養価が高く、伝統的に栽培された食品よりも多くのミネラルやビタミンを含んでいることが報告されている。これ以外にも、これらの食品は味が良いことで知られている。遺伝子組み換え食品を選ぶもう一つの理由は、保存可能期間が長くなるため、食品がすぐに腐ってしまう心配が少ないということである。
遺伝子組み換え食品が引き起こす最大の脅威は、人体に有害な影響を及ぼす可能性があるということである。これらの遺伝子組み換え食品の消費は、抗生物質に免疫がない病気の発症を引き起こす可能性があると考えられている。また、これらの食品は新しい発明品であるため、長期的な人体への影響についてはあまり知られていない。健康への影響が不明であるため、多くの人がこれらの食品から離れた方が良いと考えている。製造業者は、食品が遺伝子操作によって開発されたものであることをラベルに記載しないが、これは自分たちのビジネスに影響を与えると考えているからであり、良い習慣ではない。多くの宗教的・文化的なコミュニティは、このような食品を不自然な生産方法と見なしているため、このような食品に反対している。また、動物の遺伝子を植物に移植したり、その逆を行うことにも多くの人が反対している。また、この交雑受粉法は、環境で繁栄する他の生物にダメージを与える可能性がある。専門家はまた、このような食品の増加に伴い、開発途上国は、将来的には食品生産が工業国によってコントロールされる可能性が高いため、より工業国に依存するようになるだろうとの意見を持っている。
市販の遺伝子組み換え作物の安全性試験
遺伝子組み換えトマトは、「アンチセンス」遺伝子組み換え法(IRDC 1998)により、トマトにkanr遺伝子を挿入することにより生産された。その結果、総タンパク質、ビタミン、ミネラル含有量、および有毒グリコアルカロイドに有意な変化は見られなかった(Redenbaugh et al 1992)。したがって、遺伝子組み換えトマトと親トマトは「実質的に同等」と判断された。均質化した遺伝子組み換えトマトを経管栄養した雄雌ラットを用いた急性毒性試験では、毒性はないと報告されている。B. thuringiensisの毒素CRYIA (b)を発現するGMトマトを用いた研究では、ヒトおよびアカゲザルの盲腸/大腸へのBt毒素の試験管内試験(in vitro)結合が免疫細胞化学的に実証されていることが強調されている(Noteborn et al 1995)。
遺伝子組み換えトウモロコシ
ホスフィノトリシンアセチルトランスフェラーゼ遺伝子を発現させた Chardon LL 除草剤耐性 GM トウモロコシの 2 つの系統は、アンサイリングの前後で、非 GM トウモロコシと比較して脂肪および炭水化物含量に有意な差が見られ、したがって、実質的に異なる来歴を持っていた。毒性試験は、遺伝子導入やベクター、遺伝子挿入による予測不可能な影響を実証したり、排除したりすることができなかったにもかかわらず、トウモロコシのみを用いて実施された。これらの実験は、遺伝子組み換えトウモロコシの消化性が悪く、飼料転換効率が低下するため、実験の設計にも欠陥があった。トランスジェニックイベント 176 由来の Bt トウモロコシ(Novartis)を含む飼料を用いたブロイラー鶏の給餌試験が 1 件発表されている(Brake and Vlachos 1998)。しかし、この試験の結果は、学術的な科学的研究よりも商業的な研究に関連している。
遺伝子組み換え大豆
大豆を除草剤耐性にするために、アグロバクテリウム由来の5-エノールピルビルシキメート-3-リン酸合成酵素の遺伝子を用いた。安全性試験では、この遺伝子組み換え品種は従来の大豆と「実質的に同等」であると主張されている(Padgette er al)。 この除草剤を散布したGTS(グリホサート耐性大豆)についても同様のことが主張されていた(Tayller et al 1999)。しかし、GMと対照系統の間にはいくつかの有意差が記録され(Padgette et al 1996)、健康に重要なゲニステイン(イソフラボン)の含有量に統計的に有意な変化が見られ(Lappe et al 1999)、トリプシン阻害剤の含有量が増加していることが示された。
グリホサート耐性大豆(GTS)の2つのGM系統のラット、ブロイラーニワトリ、ナマズ及び乳牛に対する飼料価値(Hammondond et al 1996)及び考えられる毒性(Harrisonn et al 1996)についての研究が行われた。牛の成長、飼料転換効率、ナマズのフィレ組成、ブロイラーの胸筋と脂肪パッドの重量、乳生産、ルーメン発酵、消化率は、GTS と非 GTS の間で類似していることが判明した。これらの研究には以下のような問題点があった。(a) 個々の飼料摂取量、体重、臓器重量は示されておらず、組織学的研究は膵臓の定性顕微鏡検査であったこと、(b) 2 つの GTS ラインの給餌量は、ラット/キャットフィッシュの成長が GTS ラインの一方の方が他方の方よりも有意に優れていたため、どちらも実質的に同等ではなかったこと。(c) ブロイラー鶏を対象とした研究のデザインはあまり説得力がなく、(d)授乳牛の乳量と成績も、遺伝子組み換え飼料を与えた牛とそうでない牛の間で有意な差が見られた。1996)は、経口投与試験では GTS 産物ではなく大腸菌組換え体を使用していたため、無関係であった。別の研究(Teshima er al)。 2000)では、30%トーストしたGTSまたは非GTSを食事に与えたラットとマウスでは、栄養学的パフォーマンス、臓器重量、病理組織学、およびIgEおよびIgG抗体の産生に有意な差がなかったと主張している。
遺伝子組み換えジャガイモ
遺伝子組換えジャガイモのタンパク質含量やアミノ酸プロファイルに改善は見られなかった(Hashimoto er al)。 大豆グリシニン遺伝子を発現する遺伝子組み換えジャガイモの安全性を確立するための短期間の給餌試験では、ラットに 2g の遺伝子組み換えジャガイモまたは対照ジャガイモ/kg 体重を毎日強制給餌した(Hashimoto et al 1999b)。群間の成長、飼料摂取量、血球数、体組成、臓器重量に差は認められなかった。この研究では、動物によるジャガイモの摂取量が低すぎると報告された(Pusztai 2001)。
Bacillus thuringiensis var.kurstaki Cry1 毒素遺伝子またはその毒素自体で形質転換したジャガイモをマウスに給与すると、絨毛上皮細胞の肥大と多核化、小絨毛の破壊、ミトコンドリアの変性、リソソソームとオートファゴ液胞の増加、クリプト・パネス細胞の活性化が引き起こされることが示された(Fares and El-Sayed 1998)。その結果、マウスの腸内で安定なCryI毒素が得られた。生または茹でた非遺伝子組み換えジャガイモとスノードロップ(Galanthus nivalis)球根レクチン(GNA)遺伝子を有する遺伝子組み換えジャガイモを含む等タンパク性および等カロリーバランス飼料で飼育したラットを対にして飼育したところ(Ewen and Pusztai 1999)、遺伝子組み換えジャガイモを与えたラットの胃の粘膜厚および腸のクリプト長の有意な増加が認められた。これらの効果のほとんどは、形質転換に用いたコンストラクトの挿入または遺伝子形質転換そのものによるものであり、過形成性腸成長(Pusztai er al)。 1990)および上皮Tリンパ球浸潤を誘導できない非ミトティックレクチンとして予め選択されていたGNAによるものではなかった。
GM米
大豆グリシニン遺伝子を発現させたもの(40-50 mg グリシニン/g タンパク質)が開発され(Momma er al)。 しかし、タンパク質含有量の増加は、タンパク質の真の増加というよりは、水分の減少によるものであると考えられる。
遺伝子組み換え綿花
主要な鱗翅目害虫からの保護を強化した Bacillus thuringiensis subsp. kurstaki の遺伝子を用いて、いくつかの遺伝子組換え綿花の系統が開発されてきた。これらの系統は、多量栄養素とゴシポールのレベルにおいて親系統(Berberich er al)。 シクロプロペノイド脂肪酸およびアフラトキシンのレベルは、従来の種子よりも低かった。しかし、不適切な統計を使用したため、遺伝子組み換え系統と非遺伝子組み換え系統が同等であるかどうかは疑問視されていた。
遺伝子組み換えエンドウ
豆のα-アミラーゼ阻害剤を発現させた遺伝子組み換えエンドウをラットに 10 日間与えた場合の栄養価は、30%と 65%の 2 種類の用量で、親系統のエンドウと同程度であることが示された(Pusztai er al)。 同時に、ヒトに対する安全性を確立するためには、より厳密なリスク評価が必要である。実験動物を用いた栄養学的/毒性試験は、ヒトボランティアを用いた臨床的な二重盲検プラセボ試験に従うべきである。
アレルゲン性試験
遺伝子がアレルゲン性が知られている作物からのものである場合、遺伝子組み換え食品がアレルゲン性であるかどうかは、元の作物に感作された個体の血清を用いたRASTや免疫ブロッティングなどの試験管内試験(in vitro)試験を用いて容易に立証することができる。これは、ブラジルナッツ2Sタンパク質を発現する遺伝子組み換え大豆(Nordlee et al 1996)や、コッドタンパク質遺伝子を発現する遺伝子組み換えジャガイモ(Noteborn et al 1995)で実証された。また、遺伝子操作が内因性アレルゲンの効力に影響を与えたかどうかを評価することも比較的容易である(Burks and Fuchs 1995)。B. thuringiensis 農薬に曝露された農業従事者は、皮膚感作性とBt胞子抽出物に対するIgE抗体を発現していることが示された。したがって、彼らの血清を用いて、Bt 毒素を発現する遺伝子組み換え作物のアレルゲン性を検査することが可能になるかもしれない(Bernstein er al)。 Bt毒素Cry1Acは強力な経口/鼻腔抗原およびアジュバントであることが示されているので、これは非常に重要である(Vazquez-Padron er al)。
トランスジェニックに発現したタンパク質の大きさや安定性などの要因に基づく間接的なアプローチ(O’Neil et al 1998)はさらに不確実であり、特に腸内タンパク質分解に対する安定性は、生体内試験(in vivo)(ヒト/動物)試験ではなく、試験管内試験(in vitro)(シミュレート)試験(Metscalf et al 1996)によって評価されており、これは根本的に間違っている。ほとんどのアレルゲンが豊富なタンパク質であるという概念は、例えば、タラの主要なアレルゲンであるGad c 1は、優勢なタンパク質ではないので、誤解を招く可能性がある(Vazquez-Padron et al 2000)。しかし、イネのα-アミラーゼ/トリプシン阻害剤/アレルゲンの遺伝子のように、アレルゲン性の原因となる遺伝子がわかっている場合には、クローニングと配列決定により、アンチセンスRNA戦略によりそれらのレベルを低減する道が開かれる(中村・松田 1996)。
遺伝子組み換え食品の健康への悪影響に関する主な懸念事項は、抗生物質耐性の移行、毒性、アレルゲン性であることが知られている。アレルギー性の観点からは2つの問題がある。これらは、ある作物から発生する可能性のある既知のアレルゲンを、アレルゲン性のない対象作物に移行させることと、集団内で自発的な感作が発生する新アレルゲンの生成である。大豆ではなくブラジルナッツにアレルギーのある患者は、遺伝子組み換え大豆に対してIgEを介した反応を示した。Lack (2002)は、IgE結合研究を行い、タンパク質の物理化学的特性を考慮に入れ、既知のアレルゲンデータベースを参照することで、このような発生を防ぐことが可能であると主張している。2番目に考えられるde novo感作のシナリオは、リスク評価を容易に行うことができない。彼は、遺伝子組み換え食品の生産に使用されている技術がアレルギーの脅威をもたらすという証拠は、食品業界で広く受け入れられている他の方法論に比べて非常に不足していると報告している。
リスクと論争
遺伝子組み換え食品をめぐっては、遺伝子組み換え食品で生産された食品が安全かどうか、表示すべきかどうか、表示すべきであればどのようにして表示すべきか、農業バイオテクノロジーとそれが世界の飢餓に対処するために必要かどうか、より具体的には知的財産権と市場力学、遺伝子組み換え作物の環境への影響、工業的農業における遺伝子組み換え作物の役割など、いくつかのレベルで論争が起きている。
「母なる自然に手を加える」ことのリスク、消費者が認識すべき健康上の懸念、組換え技術の利点など、多くの問題が、害虫抵抗性植物や除草剤抵抗性植物にも生じている。スーパーバグやスーパー雑草と呼ばれる抵抗性害虫や雑草の進化も問題である。抵抗性は、選択的圧力が十分に強い場合にはいつでも進化する可能性がある。これらの品種を商業規模で栽培した場合、その生息地では強い選択的圧力がかかり、数年後には抵抗性昆虫の進化を引き起こし、トランスジェニックの効果を無効にしてしまう可能性がある。同様に、新しい栽培品種によって除草剤の散布がより定期的に行われるようになると、周囲の雑草がその作物が耐性を持つ除草剤に対して抵抗性を持つようになる可能性がある。そうなると、除草剤の投与量の増加、または除草剤の変更が生じ、作物の植物にかかる除草剤の量や種類が増加することになる。皮肉なことに、除草剤を販売している化学会社が、この研究の原動力となっている(Steinbrecher 1996)。
もう一つの問題は、これらの作物の害虫抵抗性の特性が雑草の親戚に逃げて、抵抗性のある雑草を増やしてしまうのかどうかという不確実性である(Louda 1999)。また、害虫抵抗性植物がある特定の害虫の死滅を増加させると、競争が減少し、マイナーな害虫を大きな問題に誘引する可能性がある。さらに、害虫の個体群が、かつては脅威にさらされていなかった別の植物の個体群に移ってしまう可能性もある。これらの影響は、はるかに広範囲に及ぶ可能性がある。Bt作物の研究では、「作物の害虫を捕食することからその名がついた有益な昆虫も、有害な量のBtにさらされていた 」ことが示されている。その影響は食物網のさらに上の方にまで及んで、人間が消費する動植物にも影響を及ぼす可能性があると述べられている(Brian 1999)。また、毒性学的な観点から、除草剤や害虫抵抗性植物からの残留物が、バクテリア、真菌、線虫、その他の微生物など、周囲の土壌に存在する主要な生物群に害を及ぼす可能性があるかどうかを判断するためには、さらなる調査が必要である(Allison and Palma 1997)。
耐病性植物に伴う潜在的なリスクは、ほとんどがウイルス抵抗性に関係している。ウイルス抵抗性は、新しいウイルスの形成につながる可能性があり、その結果、新しい病気が発生する可能性がある。天然に存在するウイルスは、トランスジェニック植物を作るために導入されたウイルス断片と再結合し、新しいウイルスを形成することが報告されている。さらに、この新たに形成されたウイルスの多くのバリエーションが存在し得る(Steinbrecher 1996)。
遺伝子組み換え食品に関連する健康リスクは、毒素、アレルゲン、または遺伝的ハザードに関するものである。食品ハザードのメカニズムは、3つの主要なカテゴリーに分類される(Conner and Jacobs 1999)。それは、挿入された遺伝子とその発現産物、遺伝子発現の二次的・多元的効果、遺伝子統合に起因する挿入突然変異誘発である。最初のカテゴリーに関しては、健康リスクをもたらすのは移入された遺伝子そのものではない。考慮すべきは、遺伝子の発現と遺伝子産物の影響である。新しいタンパク質が合成され、予測できないアレルゲン効果をもたらすことがある。例えば、システインおよびメチオニン含量を増加させるように遺伝子操作されたマメ科植物は、トランスジェーンの発現したタンパク質が非常にアレルゲン性が高いことが発見された後に廃棄された(Butler and Reichhardt 1999)。牛乳、卵、ナッツ類、小麦、豆類、魚類、軟体動物、甲殻類など、一般的にアレルギーの原因となる食品の遺伝子を操作した食品には十分な注意が必要である(Maryanski 1997)。しかし、トランスジェニックの製品は、通常、事前に特定されているため、一般消費前にその量や効果を評価することができる。また、潜在的なリスク、免疫学的、アレルゲン性、毒性、または遺伝的に有害なものは、健康上の懸念が生じた場合に認識され、評価され得る。利用可能なアレルゲンのデータベースの詳細を表1に示す。
表1 アレルゲンデータベース (Kleter and Peijnenburg 2002)
名称 ウェブサイト アレルゲンの種類 詳細
- AgMoBiol ambl.lsc.pku.edu.cn 食品、花粉 北京大学蛋白質工学・植物遺伝工学研究所 農業分子生物学研究室
- 中央科学研究所 www.csl.gov.uk/ タンパク質 食品安全・応用栄養のための食品医薬品局センター、サンドハットン、ヨーク、イギリス
- FARRP www.farrp.org Proteins 658 allergens, The Food Allergy Research & Resource Program, University of Nebraska-Lincoln.
- NCFST www.iit.edu/∼sgendel/fa.htm イリノイ工科大学グルテン国立安全技術センター
- PROTALL www.ifr.bbsrc.ac.uk/protall 植物の生化学的・臨床的データ・PROTALLプロジェクト, FAIR・CT98-4356, The Institute of Food Research, UK
- SDAP 129.109.73.75/SDAP/ タンパク質 アレルゲン性タンパク質(Ivanciuc er al)。
- SwissPort us.expasy.org/cgi-bin/lists?llergen.txt Proteins SIB スイスバイオインフォマティクス研究所、ジュネーブ)
- WHO/国際免疫学会連合 www.allergen.org タンパク質命名法 (Chapman 2008)
- アレルゴーム www.allergome.org タンパク質 Mari and Riccioli (2004)
- 食物アレルゲンに関するインターネットシンポジウム-2002 www.food-allergens.de ・食物アレルゲンデータコレクション
より懸念されるのは、二次的効果や多元的効果である。例えば、多くのトランスジェニックは生化学的経路を変化させる酵素をコードしている。これは、特定の生化学物質の増減を引き起こす可能性がある。また、新しい酵素の存在は、酵素基質の枯渇およびそれに続く酵素生成物の蓄積を引き起こす可能性がある。さらに、新たに発現した酵素は、代謝物をある二次代謝経路から別の経路へと分岐させる可能性がある(Conner and Jacobs 1999)。このような代謝の変化は、毒素濃度の上昇につながる可能性がある。毒素の評価は、動物モデルの限界により、より困難な作業である。動物は実験群間でのばらつきが大きく、ヒトと同等の結果が得られるようなトランスジェニック食品の適切な用量を動物に投与することは困難である(Butler and Reichhardt 1999)。その結果、植物における生化学的及び調節経路は十分に理解されていない。
挿入突然変異誘発は、宿主植物における既存の遺伝子の発現を破壊したり、変化させたりすることができる。ランダムな挿入は、内因性遺伝子の不活性化を引き起こし、突然変異植物を生成することができる。さらに、植物のDNAと挿入されたDNAから融合タンパク質を作ることができる。これらの遺伝子の多くは、ナンセンスな産物を作り出すか、または不正確な外観のために作物選択において排除される。しかし、最も懸念されるのは、サイレントまたは低発現遺伝子の活性化またはアップレギュレーションである。これは、「有毒な二次化合物の生産に向けた生化学的経路の酵素をコードする遺伝子」を活性化することが可能であるという事実に起因する(Conner and Jacobs 1999)。これは、新しいタンパク質や毒性化合物が植物の食用部分で発現して、食品が従来の対応物と実質的に同等でなくなる場合に、より大きな問題となる。
遺伝子組み換え食品のリスクに関しては、未知の部分が非常に多い。ある評論家は、「人間の食物連鎖にはなかった外国のタンパク質が、やがて大量に消費されるようになる」と宣言した。DDTがエストロゲン活性を持ち、人間に影響を与える可能性があることに気づくまでには何年もかかったが、「しかし今では、まだ死体を見ていないから、遺伝子組み換え食品でも問題ないと信じるように求められている」(Butler and Reichhardt, 1999)。遺伝子組み換え食品に対する国民の関心が高まった結果、各国政府は遺伝子組み換え食品の生産と取引を規制するために動いている。
報道によると、遺伝子組み換え作物は29カ国で1億6000万ヘクタール以上で栽培されており、それを栽培していない国(ヨーロッパのものを含む)から輸入されているという。ほぼ3億人のアメリカ人、1350万人の中国人、2億8000万人のブラジル人と数百万人が他の場所で定期的に直接および間接的に、遺伝子組み換え食品を食べている。ヨーロッパ人は、遺伝子組み換え食品についての大きな懸念を表明しているが、彼らは遺伝子組み換えトウモロコシの栽培を許可している。それは、動物飼料としてGM大豆ミールとトウモロコシを輸入している。何百万人ものヨーロッパ人がアメリカや南米を訪れ、遺伝子組み換え食品を食べている。
約300万人のインド人がアメリカ市民になり、さらに数百万人が観光やビジネスのためにアメリカに行き、アメリカでGM食品を食べることになる。インドの活動家は、遺伝子組み換え食品は本質的に危険であり、インドで栽培してはならないと主張している。活動家たちは、インドでのBtコットンの栽培に強く反対し、この作物は畑で失敗したと主張するレポートを発表した。同時に、農家はすぐにBt綿が非常に収益性が高いことを経験から知り、3,000万人の農家が急いでBt綿を採用した。その結果、インドの綿花生産量は倍増し、輸出量も急増した。パンジャブ州の農家は、1エーカーあたり3万ルピーの土地を借りてBtコットンを栽培している。
公共の関心事-世界のシナリオ
1980年代後半には、遺伝子組み換え食品が市場に出回っていなくても、遺伝子組み換え食品に関連した大きな論争があった。しかし、遺伝子技術の産業応用は、生産・販売状態にまで発展した。言葉の後、欧州委員会は欧州全域の国内規制を調和させた。特に遺伝子組み換え作物の認可については、1990 年代以降、コミュニティ側からの懸念が出てきており、マーケティング面での規制のフレームワークが洗練されてきている。遺伝子組み換え作物の人間の消費への使用に関する問題は、1997年に「新規食品成分に関する規則」(1997年1月27日付258/97/EC)に導入された。この規則は、遺伝子組み換え作物から作られた食品を含む新規食品の認可と表示に関する規則を扱っており、情報に基づいた選択をするためのツールとして消費者が情報を得て表示する権利を初めて認めた。この規則に該当しない遺伝子組み換えトウモロコシ品種と遺伝子組み換え大豆品種の表示は、規則(EC 1139/98)の対象となっている。その他にも、遺伝子組み換え作物のトレーサビリティーと表示、食品・飼料中の遺伝子組み換え作物の認可などの法律上の取り組みがある。
最初の欧州指令の実施の結果は、遺伝子応用に関連する技術をめぐる対立が収束したかに見えたが、1996年までには、第二次国際レベルの論争が起こった。1996年までに、遺伝子技術をめぐる第二の国際レベルの論争が出てきて、ヨーロッパの港(Lassen et al 2002)でGM大豆の到着を誘発した。除草剤に抵抗するためのモンサント社による遺伝子組み換え大豆は、ヨーロッパでの遺伝子組み換え食品の最初の大規模なマーケティングを表している。そのような遺伝子組み換えトウモロコシや他の遺伝子組み換え商品の商業化などのイベントは、動物や人間のクローニングなどの他の遺伝子技術のアプリケーションを行ったように、新興のバイオサイエンスに国民の注目を集めた。遺伝子組み換え食品に関連する問題についての公的な議論は、明確な関心を持つ多くの非政府組織の形成につながった。同時に、購入決定や消費者のボイコットを通じて遺伝子組み換え製品の受け入れや拒否を表明する規制や科学的戦略に関する問題への国民の参加が強く求められている(Frewer and Salter 2002)。
ほとんどの研究努力は、技術としての遺伝子組み換え食品に対する人々の態度を評価することに費やされてきた。数多くの「世論調査」タイプの調査が国レベルおよび国をまたいだレベルで実施されている(Hamstra 1998)。倫理的な懸念も重要であり、特定の技術が何らかの形で 「自然をいじっている」、または意図しない影響が予測不可能であり、したがって、科学にとって未知のものであることを、倫理的な懸念も重要である
(マイルズとフリーワー2001)。
遺伝子組み換え食品に対する消費者の態度
消費者の受容は、消費者がほとんど理解していない技術で加工された食品を消費習慣に導入することで、消費者が感じるリスクによって条件付けられている。スペインで行われた研究では、遺伝子組み換え食品をアグロフード市場に導入する際には、消費者の安全性を保証するための適切な政策が必要であるというのが主な結論であった。これらの行動は、具体的に健康に関連した情報を提供することで、消費者が感じるリスクを低減させることを可能にするだろう。なぜなら、これらの食品から消費者が認識するリスクに最も影響を与える要因は、健康への懸念であるからである(Martinez-Poveda er al)。
Tsourgiannisら(2011)は、ヨーロッパの地域で、より正確にはドラマ-カヴァラ-キサンティ県で、GMOフリー(GMフリー)の食品に対する消費者の購買行動に影響を与える要因を特定することを目的とした研究を実施した。2009年にドラマ、カヴァラ、ザンティの都市で337人の消費者からなる無作為に選ばれたサンプルで実施されたフィールドインタビュー。主成分分析(PCA)を実施し、GMフリー製品の消費を好む人々に影響を与える要因を明らかにした。調査地域の人々が GM フリー製品を購入することに影響を与える要因は以下の通りである。
- (a)GMフリーやオーガニック製品としての認証、
- (b)環境保護や栄養価への関心、
- (c)マーケティングの問題、
- (d)価格や品質である。
さらに、クラスター分析と判別分析により、消費者は以下の2つのグループに分類された。
- (a) 製品の価格、品質、マーケティング面に影響を受ける人と、
- (b) 製品の認証や環境保護に関心を持つ人である(Tsourgiannis er al)。
Snell ら(2012)は、遺伝子組み換えトウモロコシ、ジャガイモ、大豆、米、ライコムギを含む飼料が動物の健康に及ぼす影響について、12 の長期研究(期間は 90 日以上、最長 2 )と 12 の多世代研究(2 世代から 5 世代)を検討した。これらの研究では、GM 飼料に関する 90 日間の研究のうち、長期または多世代の研究データが利用可能なものを参照している。生化学分析、特定臓器の組織学的検査、血液学的検査、トランスジェニック DNA の検出を用いて、多くのパラメータが検討されている。
24の研究の結果はすべて健康被害を示唆するものではなく、一般的に、観察されたパラメータ内に統計的に有意な差は見られなかった。これらの研究ではいくつかの小さな差が観察されたが、これらは考慮されたパラメータの正常変動範囲内に収まっており、生物学的または毒性学的に有意な差はなかった。レビューされた研究は、遺伝子組み換え植物が非遺伝子組み換え植物と栄養的に同等であり、食品や飼料に安全に使用できることを示す証拠を提示している。
遺伝子組み換え食品:インドに関する問題
農作物における遺伝子組み換え技術の推進派にとっては大きな後退となり、2012年の農業議会委員会はインド政府に対し、すべての圃場試験の中止を求め、Bt. brinjalなどの遺伝子組み換え食用作物の禁止を求めた。同委員会は、農作物における遺伝子組み換え技術の「倫理的側面」や、長期的な環境や慢性毒性の影響に関する研究を提起し、農家にとって大きな社会経済的利益はないと指摘した。
インドのような国は、安全保障上の懸念が大きいと同時に、小規模で限界のある農家に特有の問題を抱えている。インドでは、限界地で栽培され、非常に貧しい人々に消費されているLathyrus sativusの毒素のない品種を使用することができる。遺伝子組み換えマスタードは、好ましくない影響を及ぼす可能性のある不安定な遺伝子コンストラクトであるバルナーゼ-バルスター-バル遺伝子複合体を使用した品種であり、ハイブリッドマスタードの品種を作るために使用される雄性不稔系統を実現するために使用される。インドでは、ハイブリッド生産のための雄性不稔系統を作るために、非遺伝子組み換えの良い代替品種があるので、プロアグロの品種はほとんど使用されていない。食用作物であることから、遺伝子組み換えマスタードは非常に慎重に検討されなければならない。仮にメリットがあったとしても、人間の健康や環境へのリスクを考慮しなければならない。これとは別に、マスタードは交配受粉作物であり、その外来遺伝子を持つ花粉は、遺伝子組み換えでないマスタードや野生の親戚にも届く可能性がある。これがどのような影響を及ぼすかはわからない。もしインドで遺伝子組み換え技術を使用するのであれば、マメ科植物、油糧種子、飼料のような作物や、干ばつ耐性や塩分耐性のような形質について、インドの農家の真のニーズに向けられるべきである。
バスマティ米とダージリン茶は、おそらく食品の分野ではインドで最もわかりやすい高級品である。バスマティは非常に珍重されているお米で、その市場は拡大しており、国際市場では高級品で高価な製品となっている。シャンパンワインやフランスのトリュフのように、国際的な消費者はバスマティを特別な高級食品として扱っている。米は栄養的に貧弱な穀物なので、遺伝子組み換えで鉄分やビタミンAを加えれば栄養価が上がると考えられている。では、Btコットンのような遺伝子組み換えバスマティを育種することに意味があるのであろうか?しかし、プレミアムワインメーカーは、二日酔いをカットするために設計され、「より健康的」であるはずの遺伝子組み換えワインの概念を完全に拒否している。特別なワイン、トリュフ、バスマティ米のようなプレミアム製品は、特別なプレミアムな方法で扱われる必要がある(Sahai 2003)。
食品生産チェーンにおける遺伝子組み換え作物のトレーサビリティー
トレーサビリティシステムは、製品の歴史を文書化し、マーケティングと健康保護の両方の目的を果たす可能性がある。この枠組みでは、分離とアイデンティティの保全システムは、「農場からフォークまで 」からGMと非GM製品の分離を可能にする。これらのシステムの実装は、食品加工チェーンの各特定のステップのための特定の技術的要件が付属している。さらに、トレーサビリティシステムの実現可能性は、各遺伝子組み換え製品に固有の識別子、検出方法、許容される汚染レベル、および財政的コストを含む多くの要因に依存する。遺伝子組み換え製品のサンプリング、検出、トレーサビリティの分野では進歩が見られるが、解決しなければならない課題もある。成功のためには、法律によって設定された不定形汚染のしきい値レベルに大きく依存することになる(Miraglia er al)。
遺伝子組み換え作物の検出とトレーサビリティに関する問題は、世界的な普及とそれに関連した社会経済的な意味合いから、世界的に関心が高まっている。また、トレーサビリティの観点からの科学コミュニティの関心も同時に高まっている。サンプリングと検出方法における重要な要因は、関与する遺伝子組み換え作物の数とトレーサビリティに関する国際的な合意である。信頼性の高いトレーサビリティ戦略の利用可能性は非常に重要であり、これは遺伝子組み換え作物に関連する問題の透明性に対する国民の信頼を高める可能性がある。
オートクレーブやマイクロ波加熱のような加熱処理方法は、DNAにダメージを与え、検出可能なDNAレベルまで低下させる可能性がある。遺伝子組み換え大豆やトウモロコシに含まれるこのような DNA を検出するための PCR 法が標準化されている(Vijayakumar er al)。 マルチプレックス法やリアルタイム PCR 法などの分子法が開発され、遺伝子組換え EE-1 ブリンジャルでは 20 pg のゲノム DNA を検出することができるようになった(Ballari er al)。
比較的新しい診断法の分野である遺伝子組み換え作物の検出・同定には、DNAやタンパク質に基づく方法が採用されている。また、マイクロアレイをベースとした新しい診断法も開発されており、世界市場で増加している遺伝子組み換え作物を単一のサンプルから同時に同定することができる。これらの技術のいくつかは、Celliniら(2004)によって、遺伝子組み換えの意図しない影響を検出するために議論されている。適切なトレーサビリティシステムの実施には、技術的なツールだけでは不十分であり、ラベリングの制約と厳密にリンクしている。ラベリング要件が厳しくなればなるほど、関連するトレーサビリティ戦略は、これらの要件を満たすために、より高価で困難なものとなる。
遺伝子組み換え作物のラベリングとトレーサビリティの両方が、貿易と規制において検討されている現在の問題である。現在、検出可能な遺伝子組み換え物質を含む遺伝子組み換え食品の表示は、EU の法律で義務付けられている。提案されている一連の法律案は、この表示を遺伝子組換え物質の痕跡のない食品にまで拡大するものである。これらの新しい法律はまた、食品および飼料製造システム全体の文書化に基づくトレーサビリティシステムと表示を課すことになる。リスク分析と表示に関する規制上の問題は、現在コーデックス委員会によって整合化されている。この規制の実施と維持には、食品や飼料サンプル内の遺伝子組み換え生物の含有量を正確に判定できるようなサンプリングプロトコルと分析方法論が必要となる。遺伝子組み換え生物の分析のための現在の方法論は、遺伝子組み換え製品に挿入された遺伝子組み換えDNAまたは発現した新規タンパク質の2つのターゲットのいずれかに焦点を当てている。DNA を用いた検出法の多くはポリメラーゼ連鎖反応を用いている。DNA ベースの検出法を使用する際に考慮すべき事項としては、特異性、感度、マトリックス効果、内部参照 DNA、外部参照物質の利用可能性、ヘミ接合性とホモ接合性、余分な染色体 DNA、国際的な調和などがある。
ほとんどのタンパク質ベースの方法では、新規タンパク質を結合した抗体を用いた酵素結合免疫吸着法が用いられる。抗体に結合する抗原の選択、精度、バリデーション、マトリックス効果を考慮する必要がある。現在、遺伝子組み換え作物の分析のための検出法のバリデーションが行われている。マイクロアレイ、質量分析、表面プラズモン共鳴の利用に加えて、新しい方法論が開発されている。GMO検出の課題には、染色体数の異なる材料中のトランスジェニック物質の検出が含まれる。遺伝子組み換え製品のトレーサビリティに関する既存および提案されているEUの規制要件は、一般的に食品のトレーサビリティ、そして商業的には互いに識別可能な製品のトレーサビリティに向けた幅広い傾向の中に収まっている。
ヒトボランティアを対象とした遺伝子導入研究
2009年1月の時点で、遺伝子組み換え食品の影響について実施されたヒトの摂食研究は1件しかなかった。この研究には、以前に医学的な理由で大腸を摘出した7人のボランティアが参加していた。これらのボランティアは、遺伝子組み換え大豆のDNAが人間の腸内に自然に住んでいる細菌に転送されたかどうかを確認するために食べるために遺伝子組み換え大豆を提供された。研究者らは、7人のボランティアのうち3人が、給餌実験開始前に遺伝子組み換え大豆の遺伝子が腸内細菌に移行していたことを確認した。遺伝子組み換え大豆を摂取しても、この低頻度の遺伝子移入は増加しなかったことから、実験中に遺伝子移入が起こったのではないと結論づけた。完全な消化管を持つボランティアでは、トランスジェーンは無傷の消化管を通過しても生き残らなかった(Netherwood 2004)。他の研究では、摂取した動物の血液及び組織中にM13ウイルス、GFP、さらにはリビュロース-1,5-ビスフォスフェートカルボキシラーゼ(Rubisco)遺伝子からのDNAが見出されている(Guertler et al 2009;Brigulla及びWackernagel 2010)。
遺伝子組み換え飼料を動物に与えた場合に考えられる影響に関する2つの研究では、遺伝子組み換え植物由来の材料を含む飼料の安全性と栄養価に有意な差はないことがわかった(Gerhard er al)。2005; Beagle er al)。2006)。具体的には、この研究では、遺伝子組み換え植物を与えた動物から得られた臓器や組織のサンプルからは、組換えDNAや新規タンパク質の残基は発見されていないことが指摘されている(Nordlee 1996; Streit 2001)。
今後の展開
遺伝子組み換え食品は、世界の飢餓や栄養不良の問題の多くを解決し、収量を増やし、合成農薬や除草剤への依存度を下げることで環境を保護・保全する可能性を秘めている。今後の課題は、安全性試験、規制、政策、食品表示など多くの分野にある。多くの人々は、遺伝子工学が将来の必然的な波であり、このような莫大な潜在的利益を持つ技術を無視するわけにはいかないと感じている。
未来はまた、遺伝子組み換え作物の応用は多様であり、食品への医薬品、B型肝炎(Kumar er al)。 2005)などの感染症に対する人間用ワクチンを生産するバナナ、より早く成熟する代謝的に操作された魚、数年早く収穫する果物やナッツの木、一般的な不耐性に関連する特性をもはや含まない食品、ユニークな特性を持つ新しい生分解性プラスチックを生産する植物(van Beilen and Yves 2008)などが含まれることを想定している。商業生産における実用性や有効性はまだ十分に検証されていないが、研究者が個々のプロジェクトの範囲を超えて生物に適用可能なゲノムリソースへのアクセスを増加させることで、今後10年間で遺伝子組み換え製品の開発が飛躍的に増加する可能性がある。
遺伝子組み換え食用作物の潜在的な健康リスクに関するデータが少ないことについては、導入前にテストされ、排除されているはずなのに、多くの意見があることに同意しなければならない(Domingo 2000)。遺伝子組み換え作物と非遺伝子組み換え作物の間の小さな違いは生物学的にはほとんど意味がないと主張されているが、ほとんどの遺伝子組み換え作物と親系統の作物は実質的な同等性の定義を満たしていないと指摘されている。いずれにしても、この技術を適切な科学的基盤の上に置き、一般の人々の不安を和らげるためには、遺伝子組み換え作物と従来の作物の間の組成、栄養、毒性、代謝の違いを探り、遺伝子組み換え作物の開発に使用された遺伝子技術の安全性を調べるための新しい方法と概念が必要である。この遺伝子技術に対する人々の態度を理解するためには、相当な努力が必要である。同時に、遺伝子組み換え作物に関する機関や制度の活動に対する信頼の欠如にも注意しなければならないし、国民は、機関がリスク管理活動の一環として国民の実際の懸念を考慮に入れていないと感じている。