Exploring the Association between Alzheimer’s Disease, Oral Health, Microbial Endocrinology and Nutrition
www.ncbi.nlm.nih.gov/pmc/articles/PMC5717030/
アリス・ハーディング、1 ウルリケ・ゴンダー、2 サリタ J. ロビンソン、3 セントジョン・クリーン、1 シム K. シングラオ1、 *。
要旨
患者の縦断的なモニタリングにより、慢性歯周炎とアルツハイマー病の発症との因果関係が示唆されている。しかし、歯周炎がどのようにして認知症につながるのかについての説明は不明のままである。
作業仮説は、アルツハイマー病の二次的な原因として外因性炎症をリンクしている。この仮説は、口腔衛生が損なわれていると、ポルフィロモナス・ジンジバリス(Porphyromonas gingivalis)という歯周病原体が、その伴侶種と一緒に、宿主の免疫を逆手に取ってしまうことで、口腔内マイクロバイオームが dysbiotic になることを示唆している。
すでに傷ついた軟部組織に支えられた歯を磨いたり、噛んだりすることは、バクテリウム症につながる。その結果、歯周病原体に対して持続的な全身性の炎症反応が起こる。病原体、および宿主の炎症反応は、その後、アルツハイマー病を含む複数の代謝性および炎症性の併存疾患の開始および進行につながる。
必須微量栄養素の不十分なレベルでは、そのような低ヘミンのバイオアベイラビリティの下でジンジバリスのために実証されたような歯周病原体の成長を介して微生物のバイオシスにつながる可能性がある。
また、個人の食生活は、口腔内および消化管(GI)マイクロバイオームに常駐する微生物群集の共同事業を定義する。それらの不均衡は、行動の変化につながる可能性がある。例えば、細菌の乳酸菌属で濃縮されたプロバイオティクスは、摂取したときに、両方の局所的に、そして脳に戻って感覚信号を介して、共通の宿主/細菌の神経化学物質を介して、いくつかの抗炎症作用を発揮する。
早期の人生の食事行動は、人生の後半に健康な消化管マイクロバイオームとは相容れない食事摂取を通じて、宿主/微生物内分泌学の不均衡を引き起こす可能性がある。宿主/微生物内分泌学のこの不均衡は、精神衛生に永続的な影響を与える可能性がある。
この観察は、不安、認知と睡眠パターンに、以前に検出された食事、口腔/GI微生物群集の間の関係の根底にあるかもしれないメカニズムを探求する機会を開く。このレビューでは、健康的な食生活をベースとした介入が、生活習慣や行動様式の改善とともに、アルツハイマー病の発症を減少させたり、遅らせたりする可能性があることを示唆している。
キーワード
アルツハイマー病、併存疾患、食事、内分泌マイクロバイオーム、歯周炎
序論
アルツハイマー病は認知症の中で最も一般的な疾患であり、全症例の60~80%を占めている。認知症患者数の増加と適切な治療法の不足により、今後の管理はアルツハイマー病発症・進行の潜在的な危険因子の同定と修正に重点が置かれている。
アルツハイマー病
アルツハイマー病には、遺伝的要因が知られている「遺伝型」と、原因不明の「散発型」の2種類がある。散発型は、アルツハイマー病症例の大部分がこのカテゴリーに該当するため、本稿では散発型に焦点を当てている。
どのようなタイプのアルツハイマー病であっても、全体的な症状としては、臨床的にはうつ病と認知機能の低下を呈し、死後の剖検では2つの神経病理学的特徴的な病変が認められる。これらの病変は、アミロイドβ(アミロイドβ)と高リン酸化タウタンパク質で被覆された神経原線維のもつれで構成される老人斑として表されるタンパク質である。本人にとっては、病状の経過は容赦なく、家族は精神的な負担を強いられている。
臨床的にはアルツハイマー病は「不可逆的な記憶喪失」と表現されているが、早期介入MEND™プロトコルの最近の臨床研究では、アルツハイマー病の前兆症例で機能喪失が逆転することが実証された(Bredesen et al 2016年)。
この研究では、MEND™プロトコルで示唆されたように危険因子を回避することで記憶を取り戻した患者の少数コホートだった(Bredesen et al 2016)。MEND™プロトコルは、アルツハイマー病における修正可能なリスクについての概念の証明であり、アルツハイマー病を遅らせる/遅らせるためのリスク因子の特定と修正の概念を支持するものである。
これまでの研究では、社会経済的地位(学歴)が低い人や教育レベルが低い人、女性(Brayne and Calloway、 1990; Chen and Miller、 2013; Russら、 2013)は、晩年の認知機能が低下していることが示唆されている(Mardenら、 2017)。このグループは、アルツハイマー病発症のリスクが最も高いように思われる。
最近、FINGER試験(Rosenberg et al 2017)では、低学歴と限られた教育のために認知症を発症するリスクがある高齢者を対象に、マルチドメインの生活習慣介入を行った後の認知機能の改善が実証された。Rosenbergら(2017)の研究では、介入は健康的な食事、運動、認知トレーニング、血管リスク因子の管理を確保するための変化をサポートした。
全体的な転帰は心強いものであった(Rosenberg et al 2017);しかしながら、口腔内の健康状態は彼らのマルチドメインリスク因子分析からは省略されていた。低学歴と早期死亡率との間の経路の1つは、喫煙や飲酒などの不健康な行動の採用である(Krueger and Chang、 2008; Singhら、 2013)。
これらの生活様式の行動は、歯周病の発現を増加させ(Borrell et al 2006; Persson、2008; Bonfim et al 2013)、アルツハイマー病と共存する疾患に影響を与える(図(図11))。
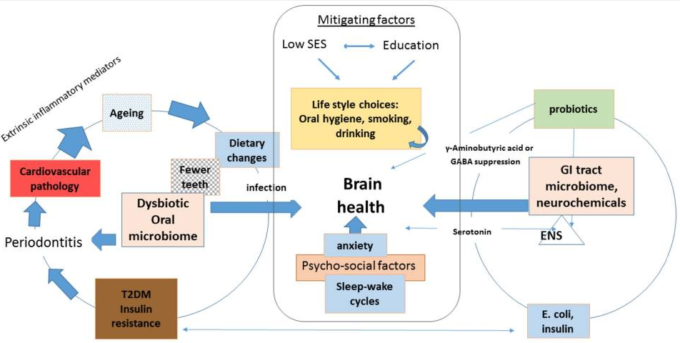
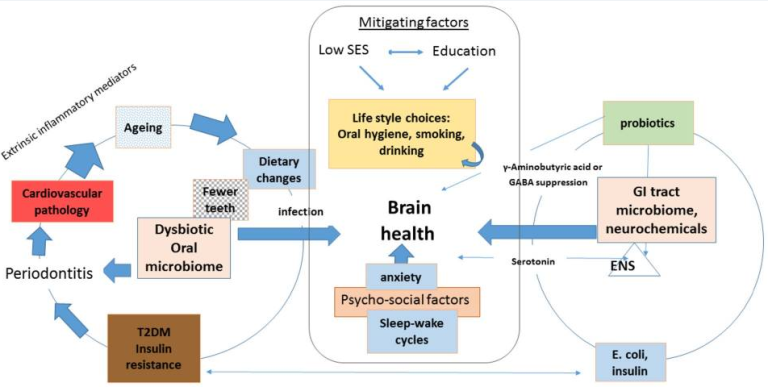
図1
2型糖尿病(2型糖尿病M)のような代謝性疾患を背景に、歯周炎のような口腔内の状態が、歯周病、心血管、アルツハイマー病の順に併存状態の発生に及ぼすノックオン効果を示す模式図。これらの状態は精神的な健康を乱す。教育プログラムとより良い口腔衛生、喫煙の中止、栄養介入、特にGI-トラクト-脳軸からの神経化学物質のバランスを提供するプレバイオティクスを含む改善されたライフスタイルを介して緩和。歯科治療、食事療法、生活習慣の変化と合わせて、潜在的に認知力の向上が期待されている。消化管マイクロバイオームは微生物の変化を通じて脳の健康に影響を与え、それによりγ-アミノ酪酸(GABA)の欠乏は行動に影響を与える。略語。ENS、腸管神経系、学歴、社会経済的地位、GI、消化管。
健康な人における食事の選択は、主にその人の歯列の状態(咀嚼能力)だけでなく、特定の種類の食品に対する食欲や渇望にも左右される。宿主と胃腸(GI)管の微生物内分泌シグナル伝達もまた、食欲に関連した意思決定に影響を与えることが提案されている(Lyte,2013,2014)。
したがって、腸内菌共生バランスを失調したGI管マイクロバイオームを介した行動変化の重要性を支持する別の経路は、γ-アミノ酪酸(GABA)発現細菌の欠乏からである(Foster et al 2016;図1参照)。健康な脳にはGABA作動性ニューロンが豊富に存在し、宿主の神経伝達物質は、個人の行動を調節する上で多様な役割を果たすことが知られており(Brown et al 2008)、ある程度ホリスティックなウェルビーイングである。
微生物内分泌学とヒトGABAとの間で共有されているもう一つの行動形質は、睡眠である(Brown et al 2008;Galland、2014、睡眠の項参照)。今回の論文の全体的な目的は、歯周病病原体とGI路微生物内分泌神経媒介行動の両方から同定された危険因子の背後にある根本的なメカニズムを探ることである。一緒に彼らは、健康的な食事、より良い口腔内の健康と共生GIマイクロバイオームが再開された場合、認知のさらなる改善の可能性を示す可能性がある。
歯周病
歯周病とは、宿主の免疫異常に起因する歯を支持する組織に影響を及ぼす多菌性の病因を有する口腔内(侵攻性および慢性)疾患群を指す(Olsen et al 2017)。歯周病発症の可能性には遺伝的影響が存在することは明らかであるが(Genco and Borgnakke、 2013)、その進行には心理社会的・環境的要因がより重要であるように思われる。
さらに、心理社会的要因は疾患の発症と進行に影響を及ぼす可能性があり、不安のレベルが高いと報告されている人は歯周病にかかりやすくなる(Cekici er al)。、 2014)。また、不安は内因性炎症にも寄与し(Kim and Jeon、 2017)、歯周病の炎症や酸化ストレスレベルを低下させることで(Waddingtonら、 2000)、アルツハイマー病をガードする可能性がある(図(図11))。
アルツハイマー病と歯周炎との関連メカニズム
口腔内の危険因子は、脳にアクセスする歯周病原体とリンクしている(Riviere et al 2002年;Poole et al 2013)。これらの環境因子が高齢者の認知症発症に寄与している可能性がある。いくつかの研究では、ライフスタイルの選択、具体的には口腔保健の実践に従うこととアルツハイマー病の発達との間のリンクが支持されている(Kondo et al 1994; Stein et al 2007; Paganini-Hill et al 2012; Luo et al 2015; Ide et al 2016)。
さらに最近では、台湾の研究で、慢性歯周病(10年前後の暴露)とアルツハイマー病との間に強い関連性があることが明らかになった(Chen er al)。 このレトロスペクティブ研究(Chen et al 2017)は、2つの口腔内細菌に対する循環抗体が10年後の認知欠損にリンクしていた以前のプロスペクティブ研究(Sparks Stein et al 2012)と相関している。
学歴(口腔内の健康状態が悪い、喫煙、不健康な食生活)要因は、脳の感染症を考える上で非常に重要である。文献によると、歯周病は全身性の炎症マーカーに寄与している(Loos、 2005)。研究は、全身性炎症性マーカーがアルツハイマー病の発症を媒介することを示している(Schmidt et al 2002年;Holmes et al 2003年;Engelhart et al 2004年;Kamer et al 2009年;Sparks Stein et al 2012)。
この発見は、歯周病と心血管疾患の病因(Libby et al 2002)およびインスリン抵抗性(Craft、2005)の両方との関連を説明する重要なリンクである。驚くべきことに、大腸菌K12は、哺乳類の機能性タンパク質に類似したインスリンを保有している(LeRoith et al 1981)。
アルツハイマー病脳における大腸菌リポ多糖(LPS)がアミロイドβホールマークタンパク質と共局在化するという事実(Zhan et al 2016;Zhao et al 2017)は、インスリンの外因性供給源が、過剰なインスリンおよび/またはその抵抗性発達に寄与する可能性を示唆している。微生物内分泌学がアルツハイマー病脳における糖尿病の発症に役割を果たしていることを示唆することはもっともらしいかもしれない。
アルツハイマー病と歯周炎の共通の危険因子
エイジング
歯周病は人生の早い時期に始まり、40~50歳の年齢層で慢性歯周炎に進行することがある(Schätzel et al 2009)。研究では、高齢者集団において疾患の重症度が高いことが示されており(Tawse-Smith、 2007; Chen er al)。、 2017)、その説明は、食生活の変化により、歯周病原体が容易に「ラジカル化」されるか、またはdysbiotic(Harding er al)。、 2017)になることと関連している可能性がある。
例えば、P. gingivalisは、異なる環境条件(微量栄養素のバイオアベイラビリティの不足)に応答して、そのLPSマクロモレキュラー内のその脂質Aリン酸塩組成物を変更することができる。これは、異なるToll様受容体4(TLR 4; Al-Qutub et al 2006)を活性化することができる脂質A構造を生成することができ、腸内菌共生バランス失調による同種の選択のための好戦的な環境を作成し、微生物の競争を制御する。アルツハイマー病の発症率は、65~74歳の3%から85歳以上では50%近くまで、年齢とともに指数関数的に上昇している。
ダイエット
歯の喪失は食物の選択に影響を与えるため、栄養不足と関連している可能性がある(Ship er al)。、 1996)。歯を失う年齢に関わらず、食事から新鮮な野菜や果物を省くことは、噛んだり噛んだりすることが困難なためであると考えられる。
したがって、歯を失うと、心血管疾患や脳卒中のリスクを高める炭水化物や脂肪を多く含む快適な食事に頼るようになる可能性がある。認知症の病因には血管系の危険因子が重要であり、歯の喪失は脳卒中(Joshipura et al 2003)、冠動脈性心疾患(Loesche et al 1998)、高血圧(田口 et al 2004)、後期の記憶喪失(近藤 et al 1994)のリスクの増加と関連している。
遺伝的素因
アルツハイマー病には遺伝的な早期発症型がある(O’Brien and Wong、 2011):後期発症型もまた高い遺伝率を持っているが、多くの病原体と関連しており、その多くは実験室モデルでアルツハイマー病の主要な特徴を促進することができる。
興味深いことに、ゲノムワイドアソシエーション研究からのアルツハイマー病関連遺伝子は、P. gingivalisを含むいくつかの病原体によって採用された宿主遺伝子と重複しており、感受性遺伝子と病原体がお互いの疾患促進効果を調節する可能性があることを示唆している(Carter、 2017)。
感染症
歯周病は、ポリ微生物の病因が知られており、最終的に散発性アルツハイマー病に罹患する患者は、認知症の臨床診断を受ける前に感染を繰り返す傾向がある(Dunn et al 2005)。これは、死後のアルツハイマー病脳における微生物の発見によって支持されている(Riviere et al 2002年;Miklossy、2011年、2015年;Emery et al 2017)。
炎症性シグナリング
口腔内細菌が病原性を示し、P. gingivalisの影響下で歯周病の発症と進行をサポートするためには、好気性の環境が非常に望ましい。P. gingivalisのLPSは脂質A領域に不均一性を示し、LPS1435/1449およびLPS1690という2つのアイソフォームを生み出している(Herath et al 2013)。
これらのアイソフォームは、異なる系統の細胞を差異なく活性化する特異的な免疫シグナル伝達経路(NF-κB;p38 MAPKおよび/またはERK1/2)に関与している(Darveau et al 1998;Reife et al 2006;Ding et al 2013;Herath et al 2013)。しかしながら、P. gingivalis LPSが遠隔臓器特異的炎症性病理の開始のための差動免疫シグナル伝達をオーケストレーションするという理論の信憑性は、サイトカイン分泌との関係でこのエンドトキシンにもある(Darveau et al 1998)。
海洋由来のオメガ3脂肪酸(DHA、EPA)、ポリフェノール、その他魚、野菜、ナッツ、果物の非栄養性化合物を消費することは、抗炎症剤として作用する(Calder et al 2009)。
社会経済的地位と低教育
歯周病、低学歴 と アルツハイマー病 の間の関連が確立されている(Brayne and Calloway、 1990; Borrell ら、 2006; Persson、 2008; Bonfim ら、 2013)。
正確にどのように、そしてなぜ学歴がアルツハイマー病の危険因子であるのかは不明であるが、学歴は喫煙やアルコール習慣などの環境因子に影響を与えるという前提がある(Brayne and Calloway、 1990; Russ er al)。 しかし、Rosenbergら(2017)のマルチドメインライフスタイル介入研究では、性別、年齢、学歴(学歴が低い)と認知能力の低下を結びつけることはできなかった。
Rosenbergら(2017)が学歴の危険因子とアルツハイマー病との関連を見いだせなかった潜在的な理由の1つは、彼らが介入に口腔の健康を含まなかったことかもしれない。学歴が低いと、病原性の高い口腔内細菌の割合が高くなることで歯周病の症状との関連性が示されるため、口腔の健康は含めることが有用であったであろう。
さらに、過度の喫煙やアルコールの消費は低学歴と関連しており、これらの健康に悪影響を及ぼす行動の両方が口腔衛生に悪影響を及ぼす可能性がある(Singh et al 2013)。学歴が低い人は、教育の不足が原因ではなく、歯科治療を受けたり、口腔衛生対策を購入したりするための収入が不足している可能性もある。
研究では、年齢、性別、学歴を調整した場合でも、教育の達成度が低いと歯周病のレベルが高くなることがわかっている(Borrell et al 2006)。このことは、個人の学歴の背景とは無関係に、低学歴であることが危険因子である可能性を示唆している。教育レベルと重度の歯周炎との関連性の一つの潜在的な理由として、教育レベルが低い人は、口腔内の健康を維持する方法に関する情報や教育をあまり受けていない可能性が考えられる(Park er al)。
運動
慢性炎症および酸化ストレスは、老化過程において本質的に見られる主要な生物学的変化である(Cannizzo et al 2011)。定期的な運動は抗炎症作用と抗酸化作用を有することが示唆されている(Taafe er al)。、 2000)。定期的な運動と栄養は、より良い歯周病の健康と関連しているようである(Bawadi er al)。
サイコマイクロバイオミクス
消化管微生物-脳軸は、微生物の内分泌寄与がヒトや実験動物の情動行動に影響を与えると概念化している(Bravo et al 2011)。微生物は、人間の宿主と似たような働きをする神経ホルモン/神経伝達物質を持っているようである。
無菌マウスは、ストレスおよびストレス関連ホルモンに関連したGI微生物内分泌学を理解するための良いモデルである(Sudo et al 2004)。無菌マウスを一連の心理学的テスト手順のバッテリーに服従させた後、彼らは減少した不安のような行動を示した。菌株をマッチさせた微生物を移植すると、より早い年齢で無菌マウスのこの表現型が逆転した(Diaz Heijtz et al 2011; Clarke et al 2013)。
このことは、宿主とそのマイクロバイオームとの共生関係の重要性を示している。これらのマイクロバイオームのバランスを維持することは重要であり、神経伝達物質/神経ホルモンをサポートする食事の摂取によって達成可能であり、それによって局所的な活動のバランスを整え、宿主の健康を維持する。
媒介因子 消化管マイクロバイオーム
口腔は、健康的な存在に必要な多くの栄養機能にとって重要であり、それゆえにGI管とリンクしている。前述のように、GI管マイクロバイオームは、歯周病とは無関係にアルツハイマー病に影響を与える可能性がある。しかし、GI路微生物の課題はまた、腸管粘膜バリアが透過性になることへのdysbioticマイクロバイオームの概念を介して興味深いアナロジーを提起する(Daulatzai、2014)。
視床下部-下垂体-副腎(HPA)軸は、歯周病ポリ微生物感染症に応答する。中枢神経系からの関連入力は、消化管からの入力は、脳への感覚経路を介して症状処理を変調する一方で、消化管からの入力は、GI管の機能を変更する可能性がある。アルツハイマー病の発症は臨床発現までの進行が遅いため、Brandscheidら(2017)は、家族性(5xFアルツハイマー病)マウスモデルのGI管内の細菌の変化と無症状の神経病理学が相関しているかどうかを調べた。
興味深いことに、この研究ではタンパク質の分解が減少し、これはトリプシンの分泌不良と関連していることがわかった。トリプシンのレベルが低いと、年齢に依存した方法で変化する糞便微生物組成物によって示されるように、このニッチに影響を与えた(Brandscheid et al 2017)。変化する腸内マイクロバイオームの結果として、特定の細菌種が粘膜バリアを破壊する可能性を獲得する可能性がある。
媒介因子 インスリン抵抗性と炎症
アルツハイマー病と歯周病の両方のリスクを高める最も重要な基礎となる代謝障害は、インスリン抵抗性と慢性炎症状態である。アルツハイマー病症例の炎症性成分の変動性に基づいて、この疾患の3つの主要なサブタイプが記述されており、代謝プロファイリングによって区別される。
そのうち、「炎症性」タイプと「非炎症性」タイプの2つが記述されている(Bredesen、 2015)。炎症性」タイプは、多くの場合、C反応性蛋白(CRP)やIL-6レベル、インスリン抵抗性、高ホモシステイン血症などの全身および脳の炎症のマーカーを示すApoE4対立遺伝子キャリアを包含している。全身性炎症の指標が存在しない間、「非炎症性」タイプのアルツハイマー病インスリン抵抗性、低ビタミンD、高ホモシステイン血症と減少したホルモンが支配している。
しかし、これは脳内炎症の存在を排除するものではない。炎症性サブタイプと非炎症性サブタイプはインスリン抵抗性であり、しばしばFDG-PETスキャンではグルコース利用における側頭頂部の減少が示される(Cunnane et al 2011;Bredesen、2015)ので、栄養支持による管理はもっともらしい。
混合病理を支援するための食事療法に基づく介入
良質な栄養は健康に重要な役割を果たしている。死亡率の5つの主要な世界的リスクは、高血圧、タバコの使用、高血糖、運動不足、肥満であると考えられている。栄養は、これら5つのグローバルリスクのうち3つにうまく対処することができる。
例えば、個人が植物由来の食品を低量摂取すると、2型糖尿病M、メタボリックシンドローム、一部のがん、アルツハイマー病の発症リスクが高まる(Salas-Salvadó et al 2016)。栄養とアルツハイマー病発症の関係は提案されているが、貧栄養がどのようにアルツハイマー病につながるかを説明するメカニズムは不完全である。
ここでは、栄養不良が口腔内の健康不良の危険因子として作用するだけでなく、歯周病とアルツハイマー病発症の関係を媒介するメカニズムにも影響を及ぼす可能性があることを探る。さらに、良好な栄養状態をサポートすることができる介入を探る。
危険因子 西洋式食生活
MEND™プロトコルは食事療法をベースにしており、アルツハイマー病の前兆症例では機能低下の逆転を示している(Bredesen et al 2016)。この研究は、MEND™プロトコルで示唆されたように危険因子を回避することで記憶を取り戻すことができた患者のコホート(N = 10)に言及している(Bredesen et al 2016)。
しかし、欧米の食事に含まれるすべての食品が脳機能を直接阻害するのか、あるいは脳の健康に悪影響を及ぼすのは単一の栄養素なのか、あるいは異なる食事要素の組み合わせなのかは不明である。例えば、飽和脂肪を避けるための強い議論はない(Ravnskov et al 2014; Harcombe et al 2016)が、しかしながら、高血糖の炭水化物と組み合わせた場合、飽和脂肪は健康に悪影響を及ぼす(Varela-López et al 2016)。
しかし、5大陸18カ国を対象としたプロスペクティブPUREコホート研究では、総脂肪摂取量と個々の種類の脂肪酸が総死亡リスクの低下と関連しており、飽和脂肪摂取量はアルツハイマー病の危険因子として確立されている脳卒中のリスクと逆相関していることがわかった(Dehghan et al 2017)。
食事はまた、アルツハイマー病の確立された危険因子である歯周病にも影響を与える(Kamer et al 2015年;Chen et al 2017年;Harding et al 2017)。したがって、良好な口腔内の健康をサポートする健康的な食生活を促進することは、アルツハイマー病の重要な予防策である。
日本人集団を対象とした最近の疫学研究では、脂肪摂取量が少ない人ほど歯周病が進行していることが示された(Hamasaki er al)。 著者らは、脂肪が少なく炭水化物が多い食生活が歯周病の有病率の高さと関連している可能性があると結論づけた。一方、野菜、果物、β-カロテン、ビタミンC、β-トコフェロール、EPA、DHAの摂取は、患者の歯周病のレベルを低下させるのに役立った(Dodington et al 2015)。
インスリン抵抗性と炎症の予防のためには、一価不飽和脂肪酸(オリーブオイル、アボカド、マカダミ、鶏脂など)と海洋由来のオメガ3多価不飽和脂肪酸を多く含む食事、例えば地中海式の食事が推奨されている(Schwingshackl and Hoffmann、 2014)。
疫学研究および介入研究では、タンパク質および脂肪をより多く含む低炭水化物食で、体重減少(Hession et al 2009)、体重維持(Larsen et al 2010)、インスリン抵抗性、トリグリセリド低下およびHDLコレステロール上昇(Shai et al 2008年;Bazzano et al 2014)、およびCRPの低下(Bazzano et al 2014)において、優れた転帰が繰り返し示されている。
定義上低脂肪ではない地中海型の食事を採用した場合も同様である(Schwingshackl and Hoffmann、 2014)。心血管リスクが高い人を対象としたPREDIMED介入試験では、オリーブオイルやナッツ類を補った地中海型の食事パターンと低脂肪食を比較した。その結果、ナッツやオリーブオイルを補った食事を食べた人では、心血管イベントの数が有意に少なく(Estruch et al 2013)、認知機能の低下が遅く(Estruch et al 2013年;Martínez-Lapiscina et al 2013)、心血管イベントの数が有意に少なくなることが示された。
さらに、オメガ3脂肪酸、ビタミンC、D、E、B12、B6、亜鉛、鉄、ヨウ素、マグネシウム、カリウム、マグネシウム、食物繊維などの重要な微量栄養素を多く含む食品は、脳の健康をサポートすることができる(Cunnane、 2006)。
インスリン抵抗性や炎症への悪影響のほかに、単純な炭水化物を多く含む食事はBBBの完全性を損なう可能性がある(Hsu and Kanoski、 2014)。歯周炎の影響を受けやすい個人の改悪されたBBB機能は、脳に微生物を入力することができる、そして、これはアルツハイマー病を開発する可能性を高める可能性がある。
健康的な地中海式の食事を採用したり(Schwingshackl and Hoffmann、 2014)、抗酸化物質が豊富で抗炎症作用を持つ魚、野菜、ナッツ、ココア、様々なベリー類を食べること(Poulose er al)。 そのため、炎症やインスリン抵抗性を低下させる食事は、口腔や脳の健康維持に役立つため、アルツハイマー病のリスクを低下させる可能性がある(Singh et al 2014)。
危険因子 ビタミン類
ビタミンはバランスのとれた食事の重要な要素であり、ビタミン不足は歯周病と認知能力の両方に重要な影響を及ぼす可能性がある。疫学研究は、25-ヒドロキシビタミンD(25OHD)の血清レベルの低さが、う蝕や歯周病のリスクの増加と関連していることを示している(他にも、心血管疾患、2型糖尿病M、うつ病などの他の危険因子と関連している)。したがって、アルツハイマー病のリスクがある高齢者などの集団におけるビタミンDレベルのモニタリングが重要である。
一部の個人は、彼らの食事の選択のためにビタミンD欠乏症に大きなリスクがあるかもしれない。たとえば、菜食主義者は、脂肪の多い魚や放し飼いの卵などのビタミン D を豊富に含む食品を避けるため、摂取量が低い可能性がある、または太陽 (UV-B 放射) への露出が年間を通して不足している気候に住んでいる個人。
さらに重要なことは、成熟したビタミンDは、太陽からのUV-B放射によって開始されたプロホルモン合成の結果であり、その能力は老化の間に低下する。適切にターゲットを絞った栄養、注意深い日光浴、およびサプリメントは、25OHD≥75 nmol/lの健康をサポートする値を達成するのに役立つことができる。
ビタミンBはまた、アルツハイマー病の発症と進行から保護するために重要であるようである。ビタミンB群(葉酸、B12、B6)の不十分なレベルは、高齢者の認知障害と認知症の発生率に関連している(Morris、2012)、おそらくこれらの微量栄養素の低レベルが血漿ホモシステイン(HCys)を上昇させるため。HCysは神経および血管障害性代謝物であり、中枢神経系の機能に不可欠なS-アデノシルメチオニン依存性メチル化反応の障害を引き起こす可能性がある(Selhub et al 2010;Köbe et al 2016)。
ビタミンB12の臨床的に明らかに欠乏なしであっても、低い正常範囲内のレベルは、より低いメモリ性能と海馬、脳領域の減少した微細構造の整合性に関連付けられていた、典型的には、アルツハイマー病(Köbe et al 2016)で最初に影響を受けた。
肉、卵、魚のような食品は、体内にビタミンB12の十分な量を提供している(Cunnane、2006)。B12が不足している植物性食品の厳格な菜食主義者は、B12の食事を補うことを検討する必要がある。
しかし、単一または少数の栄養補助食品を用いた介入研究では、混合した結果が得られており(Eussen et al 2006;Cunnane et al 2009;Quinn et al 2010;Yurko-Mauro et al 2010)、この不一致の一つの説明として、高齢者ではメチル化反応がより効果的ではないということが考えられる。そのため、高齢者にメチル化葉酸とコバラミンを提供してビタミンB12を上昇させたり、ホモシステイン血中濃度を低下させることを推奨する研究者もいる(Bredesen、 2014; 原ら、 2016)。
最近の前向きケースコントロール研究では、原ら(2016)は、L-メチル葉酸、メチルコバラミン、N-アセチルシステインを含むサプリメントを摂取したアルツハイマー病または関連疾患の患者が顕著な利益を示したことを発見した。著者らは、高ホモシステイン血症に対抗するために、メチル化されたビタミンが完全に還元され、生理活性のある機能的な形態になっていることを示唆している(原 et al 2016)。
ビタミンに加えて、N-アセチルシステインおよびS-アデノシルメチオニンを含む硫黄を含む別の栄養製剤もまた、進行性アルツハイマー病症例で見られる認知機能の低下を遅らせることにいくつかの有望性を示した(Remington et al 2015)。
要約すると、ビタミンDとビタミンBのレベルを注意深くモニタリングし、必要に応じて食事介入を行うことは、アルツハイマー病の発症と進行を予防するのに役立つ可能性がある。口腔内の健康をサポートし、認知機能を維持することができる他のビタミンや栄養素を特定するためには、さらなる研究が必要である。
危険因子 消化管の健康不良。プレ/プロバイオティクス
最近注目されているのは、腸-脳軸とプロバイオティクスの身体的、精神的健康の維持における役割である。果物と野菜が豊富で肉が少ない食生活は、異なる消化酵素の遺伝子を発現するバクテロイデス種よりもむしろプレボテラ種の有病率が高いことと関連している(Greiner er al)。、 2014)。
ベジタリアン食は、腸内炎症を減少させ、常在菌を増加させ、病原菌を減少させることが示されている(Kim er al)。、 2013)。これは、炎症やインスリン抵抗性の発達に関連するアディポカインである腸内リポカリン-2を減少させる(Zhang et al 2008; Kim et al 2013)。
プロバイオティクスの補給は口腔の健康維持に有用であると考えられている(Krasse et al 2006);プロバイオティクスミルク飲料を毎日摂取することでプラーク誘発性歯肉炎症を減少させる(Slawik et al 2011)。さらに、Ricciaら(2007)は、慢性歯周炎患者に抗炎症効果を持つプロバイオティクス乳酸菌ブレビスを示している。
しかしながら、最近の系統的レビューでは、歯周病のための現在のプロバイオティクスに基づく治療は短期的な利益しかもたらさないと結論づけられている(Jayaram et al 2016;Bakarcic et al 2017)。したがって、プロバイオティクスの長期的な予防的使用が口腔の健康をサポートするのに有用であるか、または活動性歯周病を治療するためのプロバイオティクスの使用が望ましいかについてのさらなる研究が望まれる。
また、プロバイオティクスは、グルタミン酸シグナル伝達を介して中枢神経系の抑制性神経伝達物質であるGABAの産生を刺激することで、アルツハイマー病の発症を減少させる可能性がある(Bhattacharjee and Lukiw、 2013)。死後の脳組織で行われた研究は、アルツハイマー病 患者の GABA 濃度の低下を示しているので、これは重要である。
さらに、最近の無作為化二重盲検対照臨床試験では、12週間にわたるプロバイオティクスの混合物の消費がアルツハイマー病患者の認知機能にプラスの効果をもたらしたことが示された(Pistollato et al 2016)。プロバイオティクスは、高齢者でアップレギュレーションされているプロ炎症性サイトカインIL-1β、IL-5、IL-6、IL-8、TNF-αのレベルを低下させ、活性化リンパ球、ナチュラルキラー細胞、貪食細胞の数を増加させる(Rincon et al 2014年;Wang et al 2015)。
これらのすべての要因は、炎症の減少とともに、適応免疫応答の改善を示している。全体的に見ると、プロバイオティクスは認知機能の低下や口腔内の健康に有益な効果を提供する可能性を秘めていると思われる。プロバイオティクスが抗炎症効果を示すという事実は、確立されたGI管-脳軸とともに、この有益な効果に対する可能性のある説明を提供し、アルツハイマー病の発症を減少させる可能性のあるメカニズムを示唆しているだろう(Pistollato et al 2016)。
危険因子 高血糖
2型糖尿病Mおよび他のインスリン抵抗性の状態の患者は、歯周炎の高いリスクを示すだけでなく、アルツハイマー病の高いリスクも示す(Ahmed er al)。、 2017; Górska er al)。、 2017)。さらに、高血糖は両疾患の危険因子として浮上する(Crane et al 2013;Miranda et al 2017)。Craneら(2013)は、認知症のない高齢者の大規模コホートを6.8年間にわたって調査した研究を報告している。
潜在的な交絡変数を調整した後、過去数年間の血糖値が高かった参加者は、認知症のリスクが有意に増加していた(Crane et al 2013)。高グルコース値の負の影響は、記憶性能、海馬体積および微細構造に対するグルコースおよびHbA1c値が高い非糖尿病性高齢者に意味を持つ(Kerti et al 2013)。
したがって、糖尿病患者だけでなく、血糖値が正常範囲内にある個人においても、血糖値を下げることを目的とした戦略は、高齢者集団の認知および口腔の健康に有益な影響を与える可能性がある。最適な血糖値を達成する最善の方法は、高度に加工された炭水化物を多く含む食品、高血糖の炭水化物の摂取量を減らし、食物繊維、脂肪およびタンパク質を増加させることである(Volek et al 2009)。
危険因子-低血糖利用
脳内インスリンの欠如またはインスリンシグナル伝達カスケードの無傷の機能は、アミロイドβクリアリング、学習および記憶、満腹感および摂食行動の調節の問題につながる。さらに、障害されたグルコース利用は、正常な加齢過程の一部として見られる(Yao er al)。 幸いなことに、軽度の認知障害および軽度のアルツハイマー病の形態を有するものを含む高齢者は、インスリン非依存性モノカルボン酸トランスポーターを介して、β-ヒドロキシ酪酸(BHB)およびアセトアセテートのようなケトン体を取り込むことができる(Cunnane et al 2016)。ケトン体は、ニューロンおよび他の脳細胞のための代替的かつ効率的な燃料として機能するとともに、酸化的損傷からニューロンを保護する。さらに、ケトン体BHBは、海馬における新しいニューロンの成長に重要な脳由来神経栄養因子(BDNF)のレベルを上昇させることができる(Cunnane et al 2016; Kullmann et al 2016)。
ケトン体は、脂肪酸の酸化による代謝物である。ケトン体を産生する主な末梢臓器は肝臓であるが、脳のアストロサイトも中鎖脂肪酸からケトン体を作ることができる(Nonaka er al)。、 2016; Thevenet er al)。、 2016)。健康な個体を対象とした研究では、少量の中鎖トリグリセリド(MCTs、20〜30g C10/d)が、老化した個体に典型的に見られるエネルギーギャップを閉じ(Courchesne-Loyer et al 2013)、アルツハイマー病症状の発症を遅らせることができることが示されている(Reger et al 2004)。ケトン体(約 0、5 mmol/l)の達成度は、脳のエネルギー代謝の 9 % まで貢献すると推定された。より高いケトン体のレベルでは、より多くのMCTを食べることが必要になるだろう、厳格な食事療法(非常に低炭水化物のケトジェニックダイエット)を採用するか、または高速に。
そのようなバージンココナッツオイルに見られるようなMCTsは、通常の食事の存在下でも、軽度にケトン体のレベルを上げることができるように、彼らは妥協したグルコースの利用とニューロンのための代替燃料の供給を達成するための簡単な方法を提供する。事例研究では、Newportら(2015)が、ココナッツオイル、MCT、ケトン体サプリメントを使用した早期発症アルツハイマー病患者の改善を報告している。健康な老化脳であっても、代償的なケトゲン経路(ヤオ et al 2011)に向かってグルコース主導の生体エネルギーからシフトするように、それはエネルギー不足とインスリン抵抗性の結果として認知機能低下のリスクを軽減するためにケトゲン食品(高品質の、天然の脂肪食品や脂肪)を使用することは賢明であると思われる。ココナッツオイルは肝性ケトン体レベルを軽度に上昇させるが、アストロサイトがケトン体を合成し、隣接するニューロンに届けることは有益であり、潜在的に有用であるように見える。培養アストロサイトを用いた研究では、ココナッツオイルの主要な中鎖飽和脂肪酸構成成分であるラウリン酸(C12)がBBBを横断し、アストロサイトにおけるケトン体合成を活性化することができることが実証された(Nonaka er al)。 あるいは、ココナッツオイルを用いたオイルプリング(これにより、油を口の中に保持する)は、唾液中のS. mutansの個体数を減少させることができ、これは口腔内の健康維持を助ける手段である可能性がある(Kaushik et al 2016)。Peedikayilら(2015)の速報では、抗炎症性・抗菌性化合物であるラウリン酸を多く含むココナッツオイルを用いたオイルプリングの効果が記載されている。アフリカの青年を対象とした塗布30日後のプラーク形成の減少と歯肉指標の改善につながった。
ライフスタイルの選択
危険因子 喫煙
タバコの喫煙は、歯周病が進行する重症度を高める。例えば、ニコチンの使用は、P. gingivalis、Treponema denticolaおよびTannerella forsythiaを含む歯周病原体を選択することが示されており、この口腔疾患の進行を促進する(Zambon et al 1996)。
喫煙は、急速にコロニー化する口腔内細菌のより高い割合を保有することにつながるだけでなく、喫煙しない場合よりも、T. forsythia株およびP. gingivalis株のようなより病原性の高い赤色複合病原体の種のコロニー化を促進するので、歯周指数は劇的に変化する(Kamma et al 1999)。
より多くの数のT. forsythiaおよびP. gingivalisの高病原性形態は、重度の炎症を維持することができ、それらの侵襲性は、歯周病の病理学を悪化させ続けている(Kamma et al 1999; Bergström、2004)。骨調節因子からの二次的メディエーター(Takahashi、 2005; Olsenら、 2016)および喫煙者における自然免疫応答とともに、不衛生に起因する微生物に起因する炎症は、最終的に歯槽骨浸食のより高い率に屈する(Grossiら、 1995)。
したがって、喫煙による炎症性負荷(Kamma et al 1999)は、歯周病原体の影響を受ける遠隔臓器の健康への影響と並んで、歯周炎の発症慢性化を損なう可能性がある。
危険因子 飲酒
飲酒は、歯周病のリスクを適度に増加させる可能性がある(Tezal et al 2004; Genco and Borgnakke、2013)。飲酒量が多いと、自然免疫系に悪影響を及ぼす;慢性的な飲酒は、炎症性マーカーの高レベル化を予測する(McDade et al 2006; Barr et al 2016)。
逆に、適度にアルコールを飲むことは、自然免疫系にプラスの効果によって、歯周病を減らすと考えられているので、血管疾患、アルツハイマー病のリスクを減らすことができる。また、適度な量のワイン(Evers et al 2009)は、有益な抗炎症作用を持つため、歯周炎やアルツハイマー病などの慢性疾患を発症するリスクを低減させる可能性がある。
危険因子 睡眠不足
Sprecherら(2017)による最近の研究では、睡眠不足とアルツハイマー病発症との関連性が強調されている。この研究では、日中の傾眠のレベルが高いなど、いくつかの睡眠不良の尺度を報告している人の脳脊髄液サンプルにおいて、前臨床的なアルツハイマー病バイオマーカーの高いレベルが検出された。
したがって、良好な睡眠衛生に留意することは、アルツハイマー病発症に対する重要な予防策である(Harding et al 2017)。具体的には、高齢化が進む中での十分な睡眠は、記憶を保持するために重要であり、脳の浄化を媒介するグリンパティック系の効果的な機能のために重要である(Iliff et al 2013)。
HPA軸は、睡眠/覚醒パターンの維持に役割を果たすことが示されている。GII管マイクロバイオームを含む異生物学的マイクロバイオームからの感染は、神経化学物質および炎症性メディエーターの変化を介してHPAを変調する(Galland,2014)。例えば、プロ炎症性サイトカインは、非遅発性眼球運動(nREM)睡眠の強力な誘発因子である(Galland、 2014)。
高齢者における睡眠/覚醒サイクルを制御するサーカディアンシステムの悪化は、アルツハイマー病脳における異常なタンパク質の過剰蓄積およびグリンパティックレンジングシステムの障害に寄与する可能性がある(Yesavage et al 2003)。
活動的な歯周病や睡眠期間の制限によるグリンパティック系機能の低下は、P. gingivalisなどの微生物を浄化する脳の能力を損なう可能性もある(Harding et al 2017)。さらに、慢性歯周炎の要となる病原体であるP. gingivalisが実験マウスの脳にアクセスし(Poole et al 2015; Singhrao et al 2017)、ミクログリア細胞の昼夜活動を乱す可能性があることを示唆するいくつかの証拠がある(Takayama et al 2016)。このことは、慢性歯周炎を介したP. gingivalis感染が睡眠の質の低下をさらに助長することを示唆している。
ヒトは日周性哺乳類であるため、代謝活動の多くは日中は活動と貯蔵、夜間は休息、修復、貯蔵された栄養素の利用のために進化してきた。これは、主に光によって調節され、スマートフォン、タブレット、テレビ画面、電子書籍リーダーなどの青色波長発光デバイスによって大きく乱されるメラトニンリズムのようなホルモンリズムによって支えられている(Heo er al 2017)。
毎日のリズムは、夕方や夜の間に私たちをより多くのインスリン抵抗性にする(Carrasco-Benso et al 2016; Morris et al 2016)ので、大きな夕食、特に炭水化物の負荷が重いものは、体が断食し、蓄積された脂肪を使用することを意味している夕方に避けるべきである。
さらに、重い夕食は睡眠を妨げ、睡眠の質を損なう可能性がある。したがって、就寝前に少なくとも3時間の断食を行い、炭水化物の含有量、特に夕食の炭水化物の含有量を減らすことが推奨されている(Bredesen、 2014)。
睡眠を促進するために発見された他の食事介入には、カフェインを含む飲食物や飲み物を避けることが含まれているが、耐性がない場合は就寝前に避け、アルコールは眠気を増加させるが、深い睡眠相サイクルを乱す可能性がある(Ebrahim er al 2013; Clark and Landolt、 2017)。
あるいは、さくらんぼやキウイフルーツを食べることは、それらの自然に高いレベルのメラトニンを介して睡眠を促進することができる(Pigeon er al 2010; Lin er al)。、 2011)。
また、寝る前に牛乳を飲むと、トリプトファンやビタミンB群が多く含まれているため、眠気が増す可能性がある(Peuhkuri er al 2012)。最後に、日中の運動は、特に屋外で自然光の中で行う場合には、睡眠に良い影響を与える可能性がある(Reid er al)。
今後の展望
環境要因が高齢者のメンタルヘルス転帰に与える影響を認識することは重要である。具体的には、見落とされがちな栄養とそれに続く口腔保健への影響を優先すべきであると主張する。
口腔内の健康は、老年期に関連する他の状態の管理に比べて優先順位が低いかもしれないが、口腔内の健康不良が2型糖尿病Mなどの他の状態を引き起こしたり、悪化させたりする可能性があることは明らかであり、その結果、アルツハイマー病発症の危険因子となる可能性がある。
口腔内の健康を維持することの重要性を考えると、地域に根ざした老人医療文化を向上させるサービスの増加が必要である。将来の医療専門家は、初期の研修期間中に老人ホームを訪問し、入居者との交流を深め、高齢者との関係を改善すべきである。
高齢者とそのケアチームの両方に教育と支援を提供することで、高齢者の長寿と生活の質の向上、罹患率と死亡率が大幅に向上する可能性のある、一見優先度が低いと思われるグループとして高齢者を特定し、口腔保健の促進とスクリーニングプログラムのために高齢者に優先順位をつけるための資金と資源の改善を検討すべきである。
介護施設では、地域に根ざした口腔保健ケアが義務化されるべきである。口腔の健康を改善する高齢者のためのより健康的な食生活を支援するために、栄養士からのインプットを検討すべきである。
おわりに
口腔内およびGI管のマイクロバイオームを健全に維持することは、宿主にとって大きな利益をもたらす。口腔内の異生物性バイオフィルムは、局所的にも、またGI管から離れた遠隔の臓器部位でも、疾患の発病を開始させる要因に寄与しているように思われる。
口腔内病原体が破壊を引き起こすメカニズムは、免疫応答のサブバージョンを介して、および差動炎症性シグナル伝達経路の活性化によるものである。GI管異生物性微生物は、行動に関連した特徴を表示するように見える。架橋は、GABA、セロトニン、ストレスホルモンなどの内分泌経路タンパク質を様々な他のものと共に関与している。
これは、GI管微生物細菌が神経化学物質に富み、脳との感覚迷走神経シグナル伝達経路を介した局所的なアップキープに関与しているからである。一つの説明としては、マイクロバイオーム共同事業の変化による神経化学物質の損失は、進行中の炎症の制御を維持するために脳に情報をフィードバックすることができないということが考えられる。これらのバランスは、生活様式、特に加齢の進行に関連した生活様式が日常生活に導入した可能性のある栄養不足を克服することによって維持する必要がある。
現在の記事では、カロリー的に適切な、低炭水化物、十分なタンパク質と脂肪を含む食事を採用することの利点を含む栄養因子を議論しているおよび/または歯周病とアルツハイマー病の両方の進行を防ぐための最良の方法であるように見える。
バージンココナッツオイルとMCTsのサプリメントは、脳をサポートすることができるケトン体を提供し、口腔内のマイクロバイオータを改善するのに役立つ。現在の記事はまた、それらの共存状態の開発に関連して、歯周炎とアルツハイマー病の複数の共有危険因子を議論している。少なくとも 10 年前に強調されたが、ほとんど注目されていない 1 つの重要な歯科の側面は、歯の数が少ない人々 の食習慣と彼らの食事の選択を変更する方法は、口腔、代謝、消化管、脳の健康に影響を与える。
多因子介入(MEND™プログラム)の文脈では、バージンココナッツオイルやMCT-オイル、魚やオメガ3脂肪酸、選択された栄養素や植物化学物質を補った低炭水化物食、口腔衛生や睡眠の改善など、口腔内の健康を改善するために必要なことがあった。これらは、軽度の認知機能低下およびアルツハイマー病の症状を遅らせ、さらには逆転させることで、すでに有望なことが示されている(Bredesen、 2014; Bredesenら、 2016)。
結論として、口腔の健康をサポートするための食事に基づく介入の有効性を評価し、アルツハイマー病の発症と進行に対する栄養の潜在的な影響を評価するために、さらなる研究が必要である。