www.ncbi.nlm.nih.gov/pmc/articles/PMC5775590/

背景
一価不飽和脂肪酸やその他の食事要因が認知機能低下の予防にどのような役割を果たしているかについては、これまで多くの研究が行われてきたが、高齢者の認知機能に低用量のエキストラバージンオリーブオイルが短期的にどのような効果をもたらすかについては、まだ研究が行われていない。私たちの目的は、イタリアの高齢者を対象に、地中海ダイエットのコンテストで、植物油を少量のエキストラバージンオリーブオイルに置き換えることで、認知機能が向上するかどうかを調査することであった。
方法
180名の高齢者をこれらの治療群に1年間無作為に割り付けた。
(1) MedDiet + extravirgin OO, 20-30 g/日;
(2) control MedDiet.
12ヵ月間の認知機能低下の進行を検出するためにADAScaleの認知サブテストを使用した。
結果
群間で異なる食物群で調整した1年後のADAS-cogスコアの変動は、MedDiet群で-1.6±0.4,MedDiet+extravirgin OO群で-3.0±0.4であった(p=0.024)。
エキストラバージンOOの摂取量は、MedDiet群とMedDiet+エキストラバージンOO群でそれぞれ30g±12, 26g±6であった(p=0.044)。
結論
MedDiet単独よりもMedDiet+低用量のエクストラバージンオリーブオイルを摂取した人の方が、認知機能スコアの短期的な改善度が高いことを示した。エクストラバージンオリーブオイルは最高品質のオイルであり、神経保護効果がある可能性がある。
キーワード
認知機能, 高齢者, 地中海ダイエット, エキストラバージンオリーブオイル
背景
認知障害や認知症の患者は、年齢とともに指数関数的に増加し、世界的にも数十年後には悪化する傾向にある[1]。これらの臨床状態は、全体的に高い費用がかかり、社会に深刻な負担を与えている。したがって、非薬理学的な対策も重要である。いくつかの観察研究と無作為化比較試験は、認知機能の低下に対して、アルツハイマー病を開発するリスクを減少させる地中海ダイエット(MeDiet)の保護の役割を示している[2-7]。
MeDietは、高齢者の認知パフォーマンスを向上させることができる[2]と有益な効果は、その高い一価不飽和脂肪酸(MUFA)の含有量に起因している[6]に関係なく、MedDietは、その高脂肪含有量の健康的な食事パターンになる[8]。しかし、高齢者の主な関心事は、特にある程度認知機能が低下している人では、健康的な食生活の変化、食物摂取量への関心の低下、カロリーカウントの低下である[9]。
ある研究では、健康状態を達成し維持するためには、量ではなく質の良い食事が重要な決定要因であることが示唆されている[10]。さらに、MUFAの摂取量を増やすこと自体が認知機能の改善に有効であるという考え方には不確実性がある[11]。本研究では、植物油の質を変化させることで、量よりも高齢者の認知機能を向上させることができると仮定した。しかし、エキストラバージンオリーブオイル(OO)の消費と認知機能との間の具体的な関連性については、特に低用量で短期的にはまだ正式には検討されていない。
そこで、私たちの目的は、高齢者の集団において、すべての植物油を少量のエキストラバージンオリーブオイルに置き換えることで、短期的には対照的な食事よりも認知機能が改善されるかどうかを調査することであった。
方法
この研究では 2013年2月から 2016年8月までの間に実施された “高齢者の認知機能に対するMedDietの効果 “と題した研究に募集された参加者が含まれており、イタリア保健省の資金提供を受け、そのプロトコルは、カタンザーロ、イタリア(プロジェクトコード2011.48)の “マテルドミニ “大学病院で地元の倫理委員会によって承認された。
参加者は地中海地域(南イタリアのカラブリア地方)から来ており、新聞広告によって研究への参加を招待された。被験者はすべて白人で、65歳以上の地域居住者で、MMSEスコアが20以上であった [12]。参加者は識字率が高く、病歴、身体検査、神経学的検査、検査室検査で確認されたように、衰弱性疾患(ステージ2~5の慢性腎臓病、末期肝不全、癌、うっ血性心不全など)に罹患していなかった。また、心血管疾患(心血管疾患)や甲状腺機能障害の既往歴や過度の飲酒歴はなく、栄養補助食品や向精神薬を服用していなかった。すべての参加者は、専門の神経内科医による医学的評価と以下の神経心理学的検査を用いた神経心理学的評価を受けた:Mini Mental State Examination(MMSE)[13-16]およびAlzheimer’s Disease Assessment Scale-Cognitive sub-scale(ADAS-cog)[17-19]。
その後、180名の参加者を2つの食事療法群のいずれかに1年間無作為に割り付けた(割り付け比1:2)。
(1)すべての植物油(オリーブ油、高オレイン酸サフラワー油、高オレイン酸ヒマワリ油、キャノーラ油、水添植物油を含む)を1日20-30gの用量でエクストラバージンOOで置換したMedDiet、
(2)コントロールMedDietのみの群(図1)。
図1 CONSORT研究のフローチャート
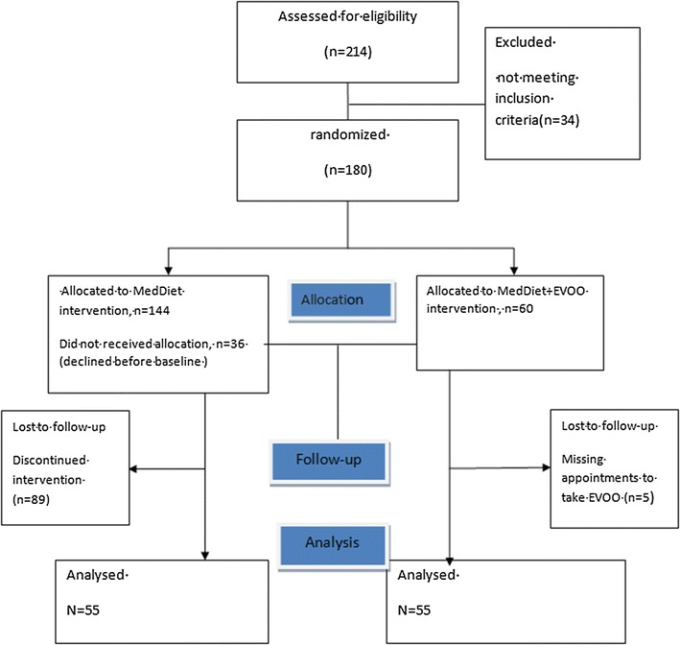
アドヒアランスを向上させるために、MedDiet + extravirgin OOグループでは、参加者に無料でextravirgin OOが与えられ、地元のオイル生産者から3ヶ月ごとに提供された(Opipari and Torchia Companies, Calabria社による3ヶ月分の5Lのextravirgin OO;extravirgin OOの主な特徴:酸度0.8%未満、ポリフェノール含有量280ppm)。
参加者は、MedDietのアドヒアランスを高め、あらゆる種類の脂肪を減らすための集中的な口頭および書面による推奨を受けたが、どの介入群においてもエネルギー制限は推奨されなかった。ADAS-Cogを主要アウトカムとした12ヵ月間の縦断的評価を実施した [18]。
この調査はヘルシンキ宣言[20]に概説されている原則に準拠している。参加者から書面によるインフォームドコンセントを得た。
神経心理学的評価
神経心理学的評価は、診察とMMSEおよびADAS-cogの使用と並行して実施された。MMSEは、方向性、注意力、計算、言語および想起の構成要素を持つ認知機能のグローバルテストである [13]。20点以下のスコアは認知障害を示している。検証済みのイタリア語版が使用された [16]。ADAS-cogは心理測定尺度であり、記憶障害、言語、プレーキシー、注意力およびその他の認知能力を測定する [17]。スコアの範囲は0から70までで、ADAS-cogの尺度は逆になっており,0はエラーがなく、70はすべての項目でエラーがあることを表している[18, 19]。
さらに、行動的および心理的症状、および認知機能の低下を頻繁に伴う可能性のある最終的な日常機能能力の低下を評価するために、検証済みの尺度を使用した。例えば、Beck Depression Inventory-II(BDI-II)Verbal Fluency(VF)Activities of Daily Living(日常生活動作)Instrumental Activities of Daily Living(手段的日常生活動作(I日常生活動作))スケール[21-27]。
その後の訪問時の練習の影響の可能性を減らすために、神経心理学的検査では異なる単語リストを使用した。さらに、認知検査を実施した研究者は、患者の臨床データとランダム化を盲検化した。
体格測定と心血管リスク因子の評価
体重は、12 時間の一晩断食後の朝食前に軽装で測定し、衣服の重量を差し引いた。体重は,0.1 kgの精度で校正されたデジタルスケール(モデル:タニタ BC-418MA)で測定し、立ち姿勢は壁に取り付けられたスタディオメーターで測定した [28]。BMIは次の式で計算した:体重(kg)/身長(m)2。肥満は、ボディマス指数(BMI)≧30kg/m2の存在によって定義された。腰囲および股囲(WCおよびHC)は、過去に記載されたように、衣を着ていない腹部の上では肋骨縁と腸骨クレストの間の最も狭い点で、薄手の衣服の上では臀部の周囲の最も広い直径のレベルで、それぞれ伸縮性のないテープを使用して測定した[28]。
高脂血症、高血圧、糖尿病、喫煙などの古典的な心血管(CV)危険因子の存在を、カルテと患者インタビューから評価した[12,28]。血圧は2回の受診時に測定した。
食事摂取量と心血管リスク因子の評価
食事摂取データは、24時間リコールおよび7日間の食事記録[12,29]によって評価され、栄養ソフトウェアMetaDieta 3.0.1(Metedasrl、San Benedetto del Tronto、イタリア)を使用して計算された。正確には、24時間リコールは、包括的な食品リストに関連付けられた画像を使用した管理栄養士との対面インタビューを介して実行された。リコールは、各参加者のために完了するために15〜20分を必要とした。
患者はまた、7日間の食品日記に任意の成分、食品および食品廃棄物を報告するように求められた。各患者は、研究を開始する前に、熟練した管理栄養士によって訓練を受けた。管理栄養士は、様々な食品がどのように記録されるべきかを示した。使用されたポーションサイズは、典型的なまたは自然に消費されるポーション(例えば、パン1切れ、卵1個)に基づいていた。典型的なポーションサイズが明らかでない場合は、一般的に使用されているポーションサイズを選択した(例えば、カップ1杯)。
栄養素摂取量の計算に使用した栄養データベースは、主にINRAN(National Institute of Food Research)2000およびIEO(European Institute of Oncology)2008 [12, 29]から得たものである。このデータベースには5000以上の食品およびブランド品が含まれており、毎年更新されている。簡単に言えば、食事摂取データは、ソフトウェアMetaDietaに直接入力された。このソフトウェアは、食品やブランド品を名前で検索する。食品とその可変成分のコード化は、データの入力と同時に行われ、同時に栄養素が即座に計算される。栄養素値とその他の食品成分は、食品グループの割り当てとともにデータベースから生成された。
MedDietへのアドヒアランスは、Mediterranean Diet Score (MDS) [4]を用いて登録時に評価した。スコアの合計は0(最低アドヒアランス)から55(最高アドヒアランス)までの範囲である。25~55のスコアは、MedDietへの中程度の高いアドヒアランスを示している。さらに、登録時と1年後にMediterranean Adequacy Index(MAI)を評価した[30]。アドヒアランスのレベルは、低スコア≦2,高スコア≧4,中間スコア≦2≦MAI≦4の3段階とした。
生化学的評価
血清グルコース、総コレステロール、高密度リポタンパク質(HDL)コレステロール、トリグリセリド、クレアチニンを酵素比色法で測定した。低密度リポ蛋白(LDL)コレステロール値はFriedewald式[31]により算出した。品質管理は、すべての測定について毎日評価した。
データ解析
データは平均±SDとして報告されている。ADAS-Cog変化の効果量(ES=平均ADAS-Cog差/ベースラインSD)0.8は臨床的に関連性のある大きな変化と考えられている[32]ので、両側有意水準で80%の力を持つことから、各群25人以上の被験者が必要とされている。
群間の有病率の差を分析するためにカイ二乗検定を行い、ベースライン時と1年後の2群の平均を比較するために独立不対標本のt検定を用いた。ベースラインからフォローアップまでのMMSEおよびADAS cogスコアの変化(群内変動)は、対をなすStudentのt検定(二尾)を用いて比較した。ベースライン時と1年後のグループ間で有意に異なるすべての変数について、ADAS-cog変動を調整するために一般線形モデル(GLM)を使用した。
有意差はp < 0.05(両側検定)で存在すると仮定した。すべての比較は、SPSS 17.0 for Windows(IBM Corporation, New York, NY, United States)を用いて行った。
結果
総勢110名が本研究を終了した(55名/群、図1)。無作為化に応じた研究集団のベースライン特性を表1に示す。両群は、年齢、性別、BMI、摂取カロリーについては同等であった。平均年齢は70±4歳、MMSEスコアは両群で24±1(それぞれp=0.63,0.72)ADAS-cogスコアはMedDiet群で14±4,MedDiet+extravirgin OO群で15±5(それぞれp=0.14)であった。さらに、他のすべてのベースライン特性は群間で有意差はなかった。
表1 ベースラインの参加者の無作為化に従った人口統計学的、体格測定学的、臨床的特徴
| 変数 | MeDiet(N = 55) | MeDietとEVOO(N = 55) | p値 |
|---|---|---|---|
| 年齢(年) | 70(4) | 70(4) | 0.63 |
| 重量(Kg) | 71(11) | 72(14) | 0.68 |
| BMI(Kg / m 2) | 28.0(5) | 28.8(4) | 0.35 |
| WC(cm) | 97(11) | 96(13) | 0.97 |
| SBP(mmHg) | 128(15) | 132(11) | 0.16 |
| DBP(mmHg) | 78(8) | 80(9) | 0.27 |
| グルコース(mg / dL) | 104(34) | 101(21) | 0.60 |
| クレアチニン(mg / dL) | 0.86(0.2) | 0.81(0.2) | 0.21 |
| 総コレステロール(mg / dL) | 200(44) | 194(40) | 0.46 |
| HDLコレステロール(mg / dL) | 54(15) | 59(15) | 0.14 |
| LDLコレステロール(mg / dL) | 128(41) | 124(34) | 0.53 |
| トリグリセリド(mg / dL) | 123(61) | 108(55) | 0.18 |
| 神経心理学的評価 | |||
| 教育レベル(年) | 11(5) | 11(5) | 0.56 |
| MMSE | 24.6(1.3) | 24.5(1.5) | 0.72 |
| ADAS-コグ | 14.0(4.5) | 15.3(5.2) | 0.14 |
| 日常生活動作 | 6.0(0.1) | 6.0(0.1) | 0.43 |
| 手段的日常生活動作(I日常生活動作) | 8.0(0.1) | 8.0(0.2) | 0.15 |
| VF | 25(6) | 23(7) | 0.15 |
| BDI-III | 11(7) | 13(8) | 0.30 |
| 有病率 | |||
| 喫煙者(%) | 52 | 36 | 0.36 |
| 高脂血症(%) | 48 | 55 | 0.56 |
| 脂質低下剤(%) | 45 | 50 | 0.50 |
| 高血圧(%) | 52 | 51 | 0.90 |
| 降圧剤(%) | 50 | 49 | 0.60 |
| 糖尿病/炭水化物不耐性(%) | 54 | 41 | 0.34 |
| 経口血糖降下薬(%) | 51 | 40 | 0.40 |
EVOOエクストラバージンオリーブオイル、BMI体重指数、WCウエスト周囲、SBP収縮期血圧、DBP拡張期血圧、HDL高密度リポタンパク質、LDL低密度リポタンパク質、MMSEミニメンタルステート検査、ADAS-Cogアルツハイマー病評価尺度-認知サブスケール、日常生活動作の日常生活動作活動、日常生活動作の手段的日常生活動作(I日常生活動作)機器活動、VF言語の流暢さ、BDI-IIIベックうつ病目録
表2 エクストラバージンオリーブオイルの摂取量に応じた栄養素と食品群の評価(ベースライン)
| 栄養素摂取量 | EVOOなし(N = 55) | EVOOあり(N = 55) | p値 |
|---|---|---|---|
| カロリー(Kcal) | 1880(452) | 1814(376) | 0.40 |
| MAI | 2.92(1) | 2.83(1) | 0.67 |
| MDS | 33(3) | 33(3) | 0.15 |
| 炭水化物(%) | 46(6) | 47(7) | 0.49 |
| タンパク質(%) | 17(2) | 17(3) | 0.54 |
| 脂肪(%) | 37(6) | 37(7) | 0.70 |
| 炭水化物(g) | 209(59) | 207(49) | 0.81 |
| タンパク質(g) | 78(20) | 75(23) | 0.55 |
| 脂肪(g) | 75(20) | 73(23) | 0.63 |
| 一価不飽和脂肪酸(g) | 38(9) | 37(12) | 0.64 |
| アルコール(g) | 9(12) | 5(8) | 0.037 |
| 食品グループの摂取量 | |||
| じゃがいも(g) | 16(19) | 20(25) | 0.30 |
| シリアル(g) | 205(88) | 200(82) | 0.77 |
| マメ科植物(g) | 15(13) | 25(31) | 0.051 |
| 野菜(g) | 250(133) | 290(136) | 0.11 |
| 果物(g) | 333(162) | 345(206) | 0.73 |
| 魚(g) | 61(45) | 73(64) | 0.27 |
| 肉(g) | 79(44) | 75(48) | 0.66 |
| 卵(g) | 11(10) | 15(28) | 0.30 |
| 牛乳(g) | 139(112) | 122(108) | 0.43 |
| チーズ(g) | 48(39) | 66(50) | 0.038 |
| 動物性脂肪/マーガリン(g) | 0.69(2) | 1.5(5) | 0.29 |
| クッキー(g) | 7.7(16) | 9.6(16) | 0.53 |
| ケーキ/パイ(g) | 28(24) | 38(30) | 0.059 |
| シュガードリンク(g) | 27(89) | 10(30) | 0.18 |
| ワイン(g) | 90(127) | 70(117) | 0.40 |
| EVOO(g) | 33(10) | 36(12) | 0.20 |
EVOOエクストラバージンオリーブオイル、MDS地中海ダイエットスコア、MAI地中海妥当性指数
試験集団の特徴と1年後の神経心理学的スコア
1年後の臨床的特徴と食事摂取量は、エキストラバージンOO(MedDiet群とMedDiet+エキストラバージンOO群でそれぞれ30g±12,26g±6,p=0.044) 炭水化物、果物、牛乳の摂取量を除いて、群間で有意差はなかった(表3)。
表3エクストラバージンオリーブオイルの摂取量に応じた、1年後の参加者の人口統計学的、体格測定学的、臨床的特徴
| 人口統計学的、人体測定学的および臨床的特徴 | MeDiet(N = 55) | MeDietとEVOO(N = 55) | p値 |
|---|---|---|---|
| 重量(Kg) | 71(11) | 71(14) | 0.99 |
| BMI(Kg / m 2) | 27.9(4) | 28.7(4) | 0.29 |
| WC(cm) | 96(11) | 95(12) | 0.80 |
| SBP(mmHg) | 128(12) | 131(15) | 0.40 |
| DBP(mmHg) | 80(8) | 78(10) | 0.34 |
| グルコース(mg / dL) | 103(23) | 103(20) | 0.92 |
| クレアチニン(mg / dL) | 0.86(0.2) | 0.85(0.2) | 0.81 |
| 総コレステロール(mg / dL) | 192(38) | 191(36) | 0.81 |
| HDLコレステロール(mg / dL) | 54(14) | 60(17) | 0.05 |
| LDLコレステロール(mg / dL) | 119(37) | 117(33) | 0.74 |
| トリグリセリド(mg / dL) | 121(57) | 104(38) | 0.08 |
| 栄養素摂取量 | |||
| カロリー(Kcal) | 1545(386) | 1560(292) | 0.81 |
| MAI | 3.09(1) | 3.22(1) | 0.60 |
| ΔMAI | 0.02(1) | 0.18(1) | 0.51 |
| 炭水化物(%) | 47(5) | 51(6) | 0.002 |
| タンパク質(%) | 16(3) | 17(3) | 0.48 |
| 脂肪(%) | 36(6) | 33(5) | <0.001 |
| 炭水化物(g) | 177(48) | 193(42) | 0.053 |
| タンパク質(g) | 61(18) | 63(16) | 0.43 |
| 脂肪(g) | 60(17) | 55(12) | 0.07 |
| アルコール(g) | 8(11) | 6(8) | 0.21 |
| 一価不飽和脂肪酸(g) | 31(10) | 28(5) | 0.025 |
| オレイン酸(g) | 30(9) | 27(5) | 0.027 |
| 食品グループの摂取量 | |||
| じゃがいも(g) | 25(24) | 26(32) | 0.73 |
| シリアル(g) | 164(70) | 171(55) | 0.56 |
| マメ科植物(g) | 19(19) | 26(25) | 0.14 |
| 野菜(g) | 203(295) | 229(128) | 0.55 |
| 果物(g) | 269(149) | 336(188) | 0.041 |
| 魚(g) | 42(32) | 47(40) | 0.48 |
| 肉(g) | 72(42) | 68(45) | 0.64 |
| 卵(g) | 10(11) | 9(11) | 0.87 |
| 牛乳(g) | 104(98) | 145(114) | 0.043 |
| チーズ(g) | 35(29) | 35(26) | 0.98 |
| 動物性脂肪/マーガリン(g) | 0.8(3) | 0.7(3) | 0.78 |
| クッキー(g) | 8(16) | 12(17) | 0.28 |
| ケーキ/パイ(g) | 25(18) | 20(20) | 0.19 |
| シュガードリンク(g) | 4.0(12) | 16(53) | 0.11 |
| ワイン(g) | 74(109) | 51(78) | 0.20 |
| EVOO(g) | 30(12) | 26(6) | 0.044 |
EVOOエクストラバージンオリーブオイル、BMI体格指数、WCウエスト周り、SBP収縮期血圧、DBP拡張期血圧、HDL高密度リポ蛋白質、LDL低密度リポ蛋白質
エキストラバージンOOを摂取した参加者では、MedDiet群と同様に2回目の時点でADAS-cogスコアが改善した(表4)が、ADAS-cog変化は群間で有意差があった(MedDiet群とMedDiet+エキストラバージンOO群では、それぞれ-1.6±2,-3.0±3のADAS-cog変化、p=0.018;表5)。特に、アルコールとチーズ(ベースライン摂取量)炭水化物、果物、牛乳(1年後の摂取量)で調整したADAS-cogスコアの変動は、MedDiet群とMedDietプラスextravirgin OO群でそれぞれ-1.6±0.4,-3.0±0.4,p=0.024,表5)であった。他のすべての神経心理学的スコアは、1年後には群間で有意差は認められなかった。
表4 エクストラバージンオリーブオイルの摂取量に応じた1年後の参加者の神経心理学的特性(グループ内変動あり
| 変数 | EVOOなし | EVOOで | ||||||
|---|---|---|---|---|---|---|---|---|
| 基礎 | ファローアップ | Δ | p値* | 基礎 | ファローアップ | Δ | p値* | |
| MMSE | 24.6(1.3) | 25.6(1.8) | 0.96(1.1) | <0.001 | 24.5(1.5) | 25.9(1.3) | 1.3(1.1) | <0.001 |
| ADAS-コグ | 14.0(4.5) | 12.5(3.6) | − 1.6(2.4) | <0.001 | 15.3(5.2) | 12.4(4.6) | − 3.0(3.3) | <0.001 |
| EVOO(g) | 33(10) | 30(12) | − 3.3(13) | 0.069 | 36(12) | 26(6) | − 10(14) | <0.001 |
MMSEミニメンタルステート検査、ADAS-Cogアルツハイマー病評価スケール-認知サブスケール、EVOOエクストラバージンオリーブオイル、Δ差
*対応のあるT検定
表5 エクストラバージンオリーブオイル摂取量に応じた参加者の1年後の神経心理学的特性
| MeDiet(N = 55) | MeDietとEVOO(N = 55) | p値 | |
|---|---|---|---|
| MMSE | 25.6(1.8) | 25.9(1.3) | 0.24 |
| ΔMMSE | 0.96(1.1) | 1.3(1.1) | 0.08 |
| ADAS-コグ | 12.5(3.6) | 12.4(4.6) | 0.84 |
| ΔADAS-コグ | − 1.6(2.4) | − 3.0(3.3) | 0.018 |
| ΔADAS-COG(調整A) | − 1.6(0.4) | − 3.0(0.4) | 0.024 |
| 日常生活動作 | 6.0(0.1) | 6.0(0.1) | 0.50 |
| 手段的日常生活動作(I日常生活動作) | 8.0(0.1) | 8.0(0.1) | 0.32 |
| VF | 25(7) | 25(6) | 0.78 |
| BDI-III | 11(6) | 12(6) | 0.56 |
EVOOエクストラバージンオリーブオイル、MMSEミニメンタルステート検査、ADAS-コグアルツハイマー病評価スケール-認知サブスケール、日常生活動作の日常生活動作活動、日常生活動作の手段的日常生活動作(I日常生活動作)機器活動、VF言語流暢さ、BDI-IIIベックうつ病目録、Δ差
アルコールやチーズ(ベースラインの摂取量)および炭水化物、果物や牛乳(1年後の摂取)のために調整平均値と標準偏差
議論
本研究で得られた知見は、MedDiet+低用量エキストラバージンOO群の高齢者では、MedDiet単独の場合よりも1年後のADAS-cogスコアの低下(テスト改善)が高かったことを示している(-3.0±0.4 対 -1.6±0.4,表4)。この結果は、短期間で低用量であるにもかかわらず、エキストラバージンOOがADAS-cogスコアの改善に関与している可能性を示唆しており、一方、MedDiet単独では認知機能がわずかに維持されることを示唆している。
この研究では、2つのグループは、アルコールとチーズ(ベースライン時)と炭水化物、果物、牛乳の摂取量(1年後)を除いて、ベースライン時と第2の時点で同様のカロリーと食品群の摂取量を持っていた(表1,2,2,2,3)3)。これらの食物群についてADAS-cogスコアの変動を調整した後、再び、MedDiet+低用量のエキストラバージンOOの参加者では、MedDiet単独の参加者よりも高いADAS-cogスコアの改善が観察された。
認知機能に対するMedDietの有益な効果は、MUFAの含有量が多いことに起因している[6]。しかし、いくつかのエビデンスから、この関連性についての不確実性が指摘されている。60歳以上の成人を対象としたEPIC-Greekコホートでは、MUFAはMMSEスコアと関連していなかった[11]。
横断的研究からの所見では、エキストラバージンOOの消費量の増加は、独立してより良い認知機能に関連していたことが報告されている[33]。しかし、エキストラバージンOOの摂取と短期的、低用量での認知機能や認知症との間の具体的な関連はまだ検討されていない。
いくつかの介入研究では、長期的な脳機能に対する OO や extravirgin OO の保護的役割が示唆されている。これに関して、血管リスクの高い地域住民を対象に実施されたある研究では、EVOO(1L/週)を補充した食事療法は、対照の低脂肪食と比較して、6.5年の追跡調査後にグローバルな認知能力の向上と関連していることが示されている[2]。この研究では、平均MMSEと時計描画テスト(CDT)のスコアは、エクストラバージンOOを補充したMedDiet群に割り付けられた参加者の方が対照群に比べて有意に高かった。しかし、ADAS-cogスコアは評価されなかった。EPIC-Greekの研究では、オリーブオイルの摂取はMMSEスコアと弱く正の相関があることが明らかにされているが、エキストラバージンオイルと認知力との関連性は検証されなかった[11]。
このように、私たちの研究は、研究期間、オリーブオイルの質(エクストラバージンのみ)用量の観点から、独創的なものである。ベースラインと比較して、健常者では、男女ともに、10mg の OO のみを含む地中海式昼食を摂取した場合、血中グルコース、LDL-コレステロール、ox-LDL の上昇が有意に少なく、血中インスリンの上昇が顕著に認められた [34]。糖尿病、脂質異常症、高血圧などの心血管危険因子やインスリン抵抗性などの状態が認知障害の発症と関連していることは十分に認められている[35, 36]。
このことから、低用量であっても、エキストラバージンOOが認知機能にポジティブな影響を与える可能性があると仮定した。さらに 2004年11月、米国連邦医薬品局(FDA)は、オリーブオイルのラベルに、「オリーブオイルに含まれるMUFAにより、1日に約23gのオリーブオイルを食べると、冠動脈性心臓病のリスクに効果がある」と記載することを許可した[37]。
私たちの研究では、脂質に有意な効果が見られた(データは示されていない)。それにもかかわらず、ox-LDLとインスリンは評価されなかったので、これらの生物学的効果を除外することはできない。さらに、心血管リスク因子の減少に関連した認知機能の改善を確認するには、1年では十分ではないかもしれない。
我々は、エクストラバージンOOのサプリメントは低用量でも認知機能検査に急速に影響を与えるという仮説を立てた[2, 34-36]一方で、MedDietは長期間にわたって認知機能の低下を防ぎ、認知症の長い前駆期に有益な効果をもたらす可能性がある[38]。
EVOOは、熟したオリーブを機械的に圧搾して作られる最高品質のオイルで、親油性成分(α-トコフェロール、β-カロテン、フェノール性フラボノイド化合物を含む)のほとんどを保持しており、強力な抗酸化作用を持っている[39]。
対照的に、一般的なオリーブオイルは、バージンオイルと精製されたオイルの混合物であり、抗酸化物質と抗炎症性化合物が少ない[38]。植物からの油の工業的な溶媒抽出には、植物油の大部分が含まれている。したがって、多くの植物油はMUFAsを含む可能性があるが、これらの油の工業化された処理は、健康のためにそれらをより望ましくない選択にする。
これらの理由から、いくつかの実験研究によっても示唆されているように、エキストラバージンOOの低用量(〜26g)は、他の植物油とは異なる中枢神経系への効果を有する可能性があることはもっともらしい。バージンOOと比較して、精製されたOOは、脂質の酸化的損傷、フリーラジカルの生成および炎症活性に対する保護効果が低い[40, 41]。オレウロペインは、一般的にオリーブの品種で最も顕著なフェノール化合物であるため、神経保護効果は、オレウロペインによって媒介されている可能性がある[42]。
もちろん、我々の研究は、オレイン酸のどの成分(オレイン酸やフェノール類)が認知機能との関連性の根底にあるのかを調査することを目的としたものではない。食品の質が健康状態を維持するための重要な決定因子であることが実証されているので[10]、我々の研究は、低用量であっても、外来のオレイン酸を含む食事パターンが認知機能を保護する作用を持つことを示唆している。いくつかの研究では、脳神経伝達物質の食事誘発性変化の証拠が提供されている[43, 44]。したがって、我々の研究は、食事中の植物油の質を変えることによって認知機能の低下を防ぐための新たなアプローチを明らかにする可能性がある。
この研究では、予想通り、両群ともに改善が見られた。我々のコントロールであるMedDiet食は、以前の疫学研究や介入研究[8]と一致して認知機能を改善し、おそらく脳内の酸化ストレスや炎症に対する効果を通して[32, 39]、認知機能を改善した。しかし、MedDiet + extravirgin OOグループの参加者では、MedDiet単独で観察されたものよりも高いADAS-cogスコアの低下が認められた(表5)。
私たちの集団では、カロリー制限についての指示はなかった。しかし、エネルギー摂取量は1年間で約300kcal減少した。我々は、エネルギー摂取量の加齢に伴う減少は、主に健康的な加齢による生理的影響であると仮説を立てている[9]。さらに、歯並びの悪さや加齢に伴う味覚や嗅覚の変化などの身体的要因が、高齢者の食事の種類や量を制限している可能性がある[9]。
この調査では、いくつかの弱点と長所を指摘しなければならない。臨床的に関連する変化があると判断された人の平均ADAS-Cog変化は、臨床的に関連する変化が最小の人では効果量(ES = 平均ADAS-Cog差/ベースラインSD)が0.5以上で3ポイント以上であり、臨床的に有意な変化を受けていない人の値はより小さい(0.2-0.4)[32]であることが示唆されている。したがって、我々の研究では、両群とも臨床的に関連性のある変化であると思われる。しかしながら、現在のところ、臨床的反応に関して患者を正確に分類するADAS cog上のカットオフポイントは、特に食事介入では、普遍的には受け入れられていない。したがって、ADAS-cogスコアの変化に基づいて我々の結果を解釈する際には注意が必要である。
我々の集団グループの食品摂取量がどのように近いかを評価するには、我々は典型的な地中海の食品群からの総エネルギーの割合の合計を非典型的な地中海の食品群からの総エネルギーの割合の合計で割ることによって、MAIを使用した地中海の食事パターンからだった [30]。1年後のMAIに有意な変化が見られなかったのは、地中海ダイエットのアドヒアランスが時間の経過とともに変化しなかったとしても、いくつかの食品の消費は、より健康的な食品パターンに向かって変化することができることが実証されているので、驚きではなかった[45]。また、我々の知見は、高齢者でFidanzaらによって示されたものと一致している[30]。
心血管疾患の影響を受ける高齢者を除外したことで、これらの結果は、コミュニティに住む高齢者集団には一般化できないが、これらの観察結果は、同様の特徴を持つ集団にのみ適用可能である。しかし、介入と研究結果との関連性を変化させる可能性のある中間イベントの数を減らすために、我々は心血管疾患を発症していない人に限定し、1年間の追跡調査を行った。心血管疾患を有する高齢者の追跡期間が長いと、より多くの中間イベントと関連している可能性があり、結果の解釈に偏りが生じる可能性がある [46]。この点では、フォローアップ期間中の脱落率はMedDiet群で62%であった。栄養学的無作為化比較試験(RCT)やコホート研究において、許容できるフォローアップ率の普遍的に合意された基準はない。しかし、一般的に薬物を研究しているRCTでは、エビデンスに基づいた医学(EBM)の「エビデンスレベル」で80%というカットオフ値が用いられており、「高品質」と「低品質」の無作為化試験を区別している[47, 48]。
これらは、これらの知見の信頼性を解釈する上で言及すべき重要なポイントである。プロトコルの逸脱は介入研究では非常に一般的である。この研究では、全体的な脱落率は53%であり、これは研究所見の妥当性と一般化可能性に影響を与える可能性がある。もちろん、データの扱い方によって結論が異なる可能性があり、本研究では因果関係が完全に確立できない可能性がある。しかし、研究を終了した人と退会した人の特徴の違いを調べたところ(追加ファイル 1:表 S1)有意な差は認められず、中途退会率が最終的な結果に影響を与えていないことが示唆された。我々は、プロトコルに違反した参加者(予約の欠席、介入の中止)を分析から除外した結果の頑健性を評価するために、一般的なタイプの感度分析を行った。さらに、全体の脱落率は53%であったが、各群25人の参加者が必要であったため、検出力には影響しなかった。
最後に、OOをMedDietの他の成分から切り離すことは困難であり、プロトコルへのアドヒアランスを向上させることを目的としているため、私たちはこの無作為化試験をデザインしたが、MedDiet+エキストラバージンOO群では、エキストラバージンOOが地元のオイル生産者から参加者に無料で提供された。これがこの研究の強みであると考えている。低用量のエクストラバージンOOを補った地中海式ダイエットが認知症を予防できるかどうかについては、さらなる研究が必要である。結論
本研究では、MedDiet単独よりもMedDiet+低用量(~26g)のエクストラバージンOOを摂取した人の方が、短期的に認知機能スコアの改善が高いことを実証した。高齢者では、植物油の質の変化が量よりも認知機能を改善すると考えられる。この結果を確認するためには、追加の研究が必要である。
