Contents
小児の臨床症状
COVID-19を有する小児の臨床症状:システマティックレビュー
onlinelibrary.wiley.com/doi/abs/10.1002/ppul.24885
合計38件(1,124例)の研究が含まれている。全症例の中から1,117例を重症度分類した。
重症度は、無症状が14.2%、軽症が36.3%、中等症が46.0%、重症が2.1%、重症が1.2%であった。最も多かった症状は発熱(47.5%)で、次いで咳(41.5%)、鼻症状(11.2%)、下痢(8.1%)、吐き気・嘔吐(7.1%)であった。
肺炎と診断された小児は145例(36.9%)で、上気道感染症は43例(10.9%)であった。リンパ球数の減少は12.9%であった.コンピュータ断層撮影での異常は63.0%に報告された。
報告された最も一般的な異常は、グランドガラスの不透明性、パッチ状の影、および固まりであった。死亡例は1例のみであった。
COVID-19を有する小児の臨床症状は成人の症例とは大きく異なる。発熱および呼吸器症状は、小児におけるCOVID-19の特徴と考えるべきではない。
子供の免疫システム
子どもの免疫システム:SARS-CoV-2の感受性を理解する鍵?
pubmed.ncbi.nlm.nih.gov/32458804/
人類は、既知の病原体や新規病原体の伝染病に繰り返し直面し、免疫系は生き延びるために適応してくる。重症急性呼吸器症候群コロナウイルス2(SARS-CoV-2)は新しい人獣共通感染性病原体であるため、既存の免疫が存在せず、人類全体が感染してCOVID-19病を発症する可能性がある。
大人は無症状、軽症、中等症から重症化、死亡と様々な転帰で感染する可能性がある。小児もSARS-CoV-2に感染する可能性があるが、検査室で確認されたSARS-CoV-2感染の小児症例のほとんどは軽症であり、重症のCOVID-19病はまれである1。
これまでのところ、SARS-CoV-2受容体(すなわちACE2)の発現や機能の程度が大人に比べて低いことを示す証拠はあらない。このように、子どもの自然免疫システムを研究することが、SARS-CoV-2に対する防御や感受性を理解する鍵となるかもしれない。
水の衛生管理や衛生習慣によって流行は減少し、致死性疾患を予防するためのワクチンも開発されてきたが4 、すべての微生物は子どもにとって初めてのものである。 生後1年目に頻繁に起こる感染症は、一般的に遭遇する病原体による再感染や病気の発症を防ぐための記憶T細胞やB細胞のプールを構築するのに役立つ5 。
このようにして、小児の免疫システムは、成人では機能が低下し、70歳以上の高齢者では効果がないかもしれない新規性に対応できるように準備されている。 感染症に対する防御には、自然免疫とT細胞が重要な役割を果たしているが、抗体も重要な役割を果たしている。
SARS、エボラ、H1N1の流行では、ウイルス感染から回復した患者の抗体を含む回復期血漿が早期治療に用いられた。 6 ほとんどの場合、ウイルス負荷は感染後1週間でピークを迎え、患者は10日目から14日目までに一次免疫反応を起こし、その後、高親和性抗体やT細胞の作用によるウイルスクリアランスが行われる。
新しい感染症やワクチンに対するナイーブなB細胞の反応は胚中心反応を介して起こり、2週間かかる。これはワクチンへの反応には妥当な期間だが、感染症への反応には長すぎる。胚中心では、免疫グロブリン可変重鎖遺伝子の抗原結合部位に体細胞変異が導入されることで、B細胞は抗体を修飾する。
高親和性の抗体を発現する修飾B細胞のみが選択され、メモリーB細胞(MBC)や血漿細胞になる。 SARS-CoV-2を含む新規病原体に対する子供の免疫準備は、いくつかの要因に基づいているかもしれない。まず、感染の初期段階では、自然抗体8 が最も重要な役割を果たしている。
自然抗体は、ほとんどが IgM アイソタイプで、以前の抗原との遭遇とは無関係に生成され、幅広い反応性と可変の親和性を持っている。彼らは、ウイルスをクリアし、再感染を防ぐ高親和性抗体とMBC9の生産に必要な2週間の間に感染を含んでいる。
高親和性抗体は、スイッチされたMBCによって発現される。ヒトでは、自然抗体は、生得的またはIgM MBCsによって産生され、胚中心から独立して産生されるMBCの集団であり、小児に最も多く存在する10,5
鳥インフルエンザウイルスにさらされたことのない若年成人の血液から選別されたこのB細胞の集団から、抗原的に多様なH1、H2、H5、H6、H8、H9インフルエンザのサブタイプを中和することができるヒト抗体をクローン化した11 。
第二に、子どもたちは、一般的な環境病原体に対する反応によって、まだ選択されて形作られていない幅広い反応性を持つ天然抗体を迅速に産生する能力を持っている。感染後、2種類のMBC、CD27dullおよびCD27bright MBC12が協力している。
この2つの集団は関連しているが、異なる分子シグネチャーと機能を持っている。 CD27ブライトMBCは、抗原によって形作られた高度に変異したVH遺伝子を発現する。刺激を受けると、CD27ブライトMBCは急速に形質細胞に分化し、主にスイッチしたアイソタイプの抗原特異的な抗体を分泌する。
対照的に、CD27dull MBCは変異が少なく、形質細胞をほとんど生成せず、IgM抗体を分泌する。イネイトまたはIgM MBCはCD27dullである。CD27bright MBCが形質細胞を産生し、抗体量を増加させると、CD27dull MBCが増殖し、迅速にMBC数を再構成する12。 第三に、新しい病原体が免疫系に挑戦するとき、CD27dull MBCは、ナイーブなB細胞よりも迅速な反応が可能であるという重要な役割を果たしている可能性がある。
MBCは直ちに抗体を分泌し、同時に胚中心反応に入り、より多くの体細胞変異を獲得し、親和性に基づいてBCRを選択することができる。乳児や小児では、ほとんどのMBCはCD27dullであり、したがって新しい抗原への適応性が高い。
対照的に、高齢者では、ほとんどのMBCはCD27brightだ。CD27ブライトMBCは高度に変異した特異的な細胞であり、標的を認識しますが、新しい抗原への適応はできないようだ。 我々は、上記の仮説を検証することを目的とした前向き研究を開始したところである。
小児における我々の予備的な結果は、ポリクローナルB細胞 Kateryna Kon/Science Photo Library Comment 416 www.thelancet.com/child-adolescent Vol 4 June 2020
多くはIgMアイソタイプのかなりの数のプラスマブラストの産生を伴う初期の反応を示唆している。この反応は、重症の成人(B細胞コンパートメントが枯渇している)では観察されない。小児と成人の抗体の特異性の違いを示すための更なる研究が進行中である。
B細胞は抗体産生のほかに、サイトカインを分泌する機能も持っている。強力な抗炎症性サイトカインであるIL-10は、新生児B細胞、活性化B細胞13、IgAプラスマブラストから産生される。このように、子供の免疫応答は、保護作用と免疫介在性の組織損傷(特に肺)を軽減するという二重の機能を持っている可能性がある。
進化は、既知および未知の病原体と戦うために、子供に生存の優位性を与えている。 成人はまた、高および低特異性を持つ細胞のバランスによってよく保護されている。加齢、栄養失調、免疫抑制、併存疾患などにより、私たちの免疫システムは新規性に適応する能力を失っている。
ワクチンが先決だが、COVID-19パンデミックのような緊急事態では、自然が子どもたちに与えた免疫ツールを調査し、利用することで、管理成績が向上するかもしれない。
子供のCOVID-19 充実したレビュー
COVID-19 in Children: An Ample Review
www.ncbi.nlm.nih.gov/pmc/articles/PMC7334563/
要旨
本レビューの目的は、小児におけるコロナウイルス疾患2019(重症急性呼吸器症候群コロナウイルス2[SARS-CoV-2]感染によるCOVID-19)に関する現在の知見を、疾患経過、治療、予後に関する知見を含め、疫学的、臨床的、検査学的な観点から記述することであった。
大規模な文献検索を行い、2020年1月1日か et al 2020年4月1日までに発表された小児におけるCOVID-19(SARS-CoV-2感染症)に関する論文を特定した。小児におけるCOVID-19に関する関連論文は44編あった。その結果、COVID-19は小児の0.39~12.3%に発生していることがわかった。
臨床徴候や症状は成人と同程度だが、小児ではよりマイルドな型と無症状の保因者の割合が高い。炎症性マーカーの上昇は合併症と関連しており、さまざまな感染症と関連している。
小児の胸部CT(Computed Tomography)スキャンでは、成人と同様の構造変化が認められ、ハローに囲まれた集積はCOVID-19の小児にはやや特異的であった。推奨される治療法は対症療法であり、小児では特に薬物療法は推奨されていない。
予後は成人に比べて小児の方がはるかに良好である。このレビューでは、小児のCOVID-19は成人の疾患と類似しているが、臨床症状、検査結果、胸部画像、治療法には特殊性があることが強調されている。
小児の予後は成人に比べてはるかに良好であるが,パンデミックの進行に伴い,小児の症例は将来的に変化する可能性がある。
序論
最近宣言されたコロナウイルスのパンデミックは、プロトコルやガイドラインに使用される社会における「ダモクレスの剣」を表している。それは2019年末に始まり、致命的なことが多い新形態の肺炎を持つ多くの成人患者が中国の病院に入院したとき、この病気は重症急性呼吸器症候群コロナウイルス2(SARS-CoV-2)によって引き起こされた1。
エビデンスに基づいた医療が主流の現代医学において、必要なエビデンスが不足しており、成人では大規模な研究があるものの、小児ではエビデンスが極めて限られているという困難な状況に直面している。
新しいコロナウイルスは当初、2019-nCoVと命名されたが、後に重症急性呼吸器症候群コロナウイルス2(SARS-CoV-2)と改名された2。中東呼吸器症候群コロナウイルス(MERS-CoV)や重症急性呼吸器症候群コロナウイルス(SARS-CoV)に関連している3 国際的にはコロナウイルス病2019(COVID-19)として知られており、かなりの割合で人に感染するが、特に初期の研究では陽性例の0.9%しか15歳未満の子どもに感染していないことが報告されている4。
現在の感染はヒトからヒトへの感染であり、最初はコウモリからの感染であり、動物を中間宿主としていると考えられているが、家族内および地域内への伝播が見られる5 。10 子ども(特に幼児)の衛生管理が非常に難しい(年齢にもよるが)ため、保菌者が感染しやすいと考えられている。
子どもへの感染性が高いこと、保菌者の健康状態が良好であること(感染の可能性が高いこと)、知識が不足していることなどが大きな問題となっている。母子感染についてはあまり知られていないが、陽性の母親から陽性の新生児が生まれたという研究がある。これらのケースでは、感染が経皮的に起こったのか、周産期に起こったのか(プルーゲ液やミルクなどの分泌物を介して)は明らかではなく、明確な感染経路は確立されていない。
本研究では、小児におけるSARS-CoV-2感染症について、病態、治療、予後などのデータを含め、疫学的、臨床的、検査学的な観点から、現在のデータをレビューすることを目的とした。
疫学
SARS-CoV-2 は多くの疾病を引き起こしており、(2020 年 4 月 1 日現在)世界保健機関(WHO)は 1,133,758 人の確定症例と 62,784 人の死亡を報告している14 。
最初に発表された研究では、この病気が診断されたのは小児の0.39%にすぎないであった15 。その後、全年齢の患者72,314人を対象とした中国の研究では、小児の1%にウイルスが存在したと報告されている16。
17 より広範な検査が開始された後、Luらは中国で最近実施した研究で、COVID-19が確認された小児の発症率は12.3%(評価された1391人のうち171人)に上昇し、平均平均年齢は6.7歳であったと報告している18。
Dongらは、中国の大規模な研究でCOVID-19の小児2143例を調査した(臨床検査で確認された症例は34.1%、臨床診断では65.9%)。これらの小児の平均年齢は6.7歳であった。
男性(56%)と女性の割合に有意な差はなかったが、他の研究では成人男性の有病率がわずかに高いことが示されている17。
17,19 子どもは、どの家族から感染したのか、家族全員が同時に感染したのか、子どもの潜伏期間は明らかにされなかった。Xiaらは、20人のCOVID-19感染児を対象とした小規模な研究を行い、65%が家族との明確な接触があったと報告しているが、残りの子どもたちは接触が不明確であったと報告している21。
臨床像
小児の症状は、疾患の病期、既往の健康状態、併存疾患の有無やその他の個々の特徴に応じて変化する。小児の臨床像には、発熱、咳、呼吸困難、倦怠感が含まれており、これは成人で頻繁に報告されている症状の四徴である20 。
しかし、Dongらの報告によると、小児の4.4%は完全に無症状で、55.3%は鼻咽頭炎などの軽症であったとされている。
22 心筋炎に特有の心臓症状も小児に見られ、副鼻腔頻拍や軽度右枝ブロック(RBBB)がみられたが、有病率は一般的な小児集団と有意差はなかった21 。
COVID-19の身体的徴候には、肺炎に伴う鼻漏、咽頭うっ血、21および肺うっ血25がある。ポリプネア、呼吸困難、胸部拘縮、その他の呼吸不全の代償徴候が観察されている26が、COVID-19の特異的徴候は強調されていない。
これまでのところ、小児では成人と異なり喀血や無臭症の症例は確認されていない27 が、これは小児では臭気がないことを表現するのが難しいためではないかと考えられる。
小児では死亡例も登録されているが、小児では軽症であることが多いため予後は良好であることが多い。
最近、小児における多系統炎症性症候群の発生が報告されている28 。
当初は「Kawasaki-like-disease」と命名され、小児多系統炎症性症候群(pediatric multisystem inflammatory syndrome: PIMS)と改名されたが、成人のCOVID-19の血管性多系統炎症性病変に類似している。
発症は通常、消化器症状が先行し、その後、発疹、口蓋紅斑、結膜炎、口腔粘膜炎、後頚部リンパ節腫脹を伴う長期の無反応発熱を伴う全身性血管炎が続き、時に心筋炎および/または重度の冠動脈炎を合併することがある。
PIMSは英国、フランス、イタリア、米国で報告されているが、幸いなことに川崎血管炎に対する治療法は有効であることが証明されている28。
しかし、Dongらの報告によると、4.4%の子どもは完全に無症状で、55.3%の子どもは鼻咽頭炎などの軽症であったとされている19。
さらに、中国でCOVID-19の子ども2143人を対象とした最近の研究では、94%の子どもが軽症または中等症であったことが明らかになった19 Fangらは、疾患の重症度(臨床像に基づく)に応じて、以下のCOVID-19分類システムを発表している29。
- 無症候性感染症:臨床徴候や症状がなく、胸部画像は正常で、SARS-CoV-2核酸検査が陽性である。
- 軽症:発熱、咳嗽、嚥下、鼻漏、くしゃみ、倦怠感、筋肉痛などの急性上気道感染症の症状。身体所見では、聴診異常を伴わない咽頭の離散的なうっ血のみが認められる。発熱がなく、吐き気、嘔吐、腹痛、下痢などの消化器症状のみを呈する小児もいる1,29。
- 中等症:発熱、優勢な産生性咳嗽および/または喘鳴などの典型的な肺炎の徴候および症状があるが、低酸素血症、呼吸困難、またはその他の呼吸不全の徴候はない。中には、臨床的徴候や症状がなく、CT(コンピュータ断層撮影)所見のみが認められる症例もある29。
- 29 重症の場合:発熱、咳、呼吸困難(中心チアノーゼおよび酸素飽和度92%未満を伴う)、頻呼吸、または重度の下痢。疾患は通常7~10日で進行する。呼吸困難の徴候として、喘鳴、胸部拘縮、徐脈、まれに無呼吸などがみられる。小児では成人と異なり、代償的な徴候を伴わない無症候性低酸素症の症例は報告されていない。30
- 重症:急性呼吸窮迫症候群(ARDS)または呼吸不全へと進行し、血管内播種性凝固、ショック、脳症、心筋炎、心不全、急性腎疾患などの合併症を伴う。
小児におけるウイルスの臨床症状は成人に比べて軽度で重度ではなく、年齢や発育と関連している1,4,5,8,9。小児の臨床症状は成人に比べて不明瞭で重症度も低いのであるが、この年齢層には特徴があり、特に早期診断が疾患の予後に影響するため、特別な注意を払う必要がある。
小児の死亡率と罹患率の危険因子
ほとんどの研究では、糖尿病、慢性肺疾患、心臓病などの併存疾患を含む成人と同じ危険因子が小児にも当てはまることが示唆されており、高血圧、糖尿病、腎臓病、免疫抑制(薬剤による免疫抑制、HIV)、慢性閉塞性肺疾患(喘息を含む)などの併存疾患を持つ成人では、好ましくない転帰がより頻繁に起こることが示唆されている30。
重症のCOVID-19を有する小児で最も頻繁に観察された合併症は、敗血症性ショック、中毒性脳症、多臓器不全症候群、播種性血管内凝固、および状態てんかんであった。
幸いなことに、2173人の小児を対象とした研究では、死亡したのは1人(14歳)だけであったが、重症化・重症化した症例の割合は、感染した乳児では10.6%で、16~18歳では3.0%と年齢の上昇とともに減少した19。より重症化した症例は、16~18歳の感染児(3%)に比べて3歳未満の子ども(10.6%)で多く見られたが、16~18歳の感染児(3%)では重症化のリスクが高いことが示唆されている。
別の研究では、腸閉塞を伴う生後10ヶ月の乳児の死亡が報告されている18。この研究では、重症症例に関連した併存疾患は、白血病(化学療法を受けている)、腸閉塞、および水腎症であった18。
2020年3月31日現在、COVID-19による小児の死亡例は4件、国際的なメディアで報告されている。フランスで16歳児が死亡し、その後ベルギーで12歳児が死亡、英国で13歳児が死亡している(https://www.euronews.com/2020/03/31/)。
診断方法
関連する疫学的背景(例えば、パンデミック地域)において臨床徴候および症状が存在することは、COVID-19の疑いのある症例を示し、特にCOVID-19が確認された症例との接触が知られている場合には、COVID-19の疑いがあることを示している。診断は、ウイルス検出のための臨床検査で確認することができる。発症の時期については、潜伏期間2~14日9、平均3~7日を基準に確認することが重要である。
- 発熱、特定の呼吸器症状、消化器症状、または倦怠感
- 示唆される生物学的所見:正常な白血球レベル、白血球減少、およびC反応性蛋白(CRP)およびプロカルシトニン(PCT)レベルの上昇
- 特定の画像所見(胸部X線[CXR]およびCTスキャンに基づく)
臨床家の中には、臨床徴候や症状が存在し、COVID-19症例との接触があれば診断が可能であると主張する人もいるが、疑いのある症例では、検査室での確認が必要である23 。
鼻咽頭分泌物を用いた検査は、咽頭スワブを用いた検査(30%)に比べて感度が高く(65%)、32 このことが、米国疾病対策予防センター(CDC)が鼻咽頭分泌物または鼻咽頭吸引液を用いたスクリーニングを推奨している理由です33。
サンプル採取のタイミング34 は非常に重要です:スクリーニング検査では、ウイルス負荷は肺疾患の発症とともに上気道では減少し、下気道では増加するため、理想的には疾患の初期(鼻咽頭炎の兆候があるとき)に採取された鼻咽頭分泌物を含むべきです35;したがって、肺疾患の発症後には、喀痰サンプルの採取が推奨されている。
鼻咽頭分泌物を使用すると、気管支分泌物を使用するよりも低い感度につながるが、喀痰排泄物なしで小児のために必要な気管支肺胞洗浄は侵襲的である35と医療従事者36の間で感染のリスクを高める可能性があるので、表示されていない。
血清中の特異的免疫グロブリンM、A、G(IgM、IgA、IgG)の検出によるスクリーニング検査が開発されているが、IgM、IgAはCOVID-19発症から5日目から陽性となるため、診断は遡及的に行われ、早期診断には利用できない36,37。
残念ながら、パンデミックが蔓延しているため、スクリーニング検査の数は国際的に限られており、正確な診断を確立したり、ウイルスの保菌者となる健康な保菌者を特定したりすることは非常に困難である。
検査所見
生物学的調査は、ウイルス性疾患で予想されるように、特異的なものではない。他のウイルス感染症と同様に、COVID-19ではいくつかの血液学的障害が報告されている。いくつかの研究では、リンパ球減少と好中球減少を伴う白血球減少症が成人および小児に認められたことが報告されている36,39。
21,25,26 COVID-19の一部の小児では、CRP、赤血球沈降率1、PCTなどの炎症性マーカーの増加が認められており、細菌の共存感染とそれに伴う合併症を示唆している1,21,25,26。
成人を対象とした研究では、PCTと白血球減少が死亡率上昇の危険因子であることが明らかになったが、小児ではこの関連性は確認されなかった。
成人の心筋炎ではトロポニンの増加が認められ、成人ではCOVIDに関連した筋損傷によりミオグロビン(ミオヘモグロビンとしても知られる)と筋酵素が増加した1,40,41が、小児ではこれらの所見は報告されていない。
CRPとフェリチンの高値は、成人ではDダイマーや血小板減少症の増加と同様に予後不良と関連していた42。
その他の生物学的所見としては、特発性代謝性アシドーシス、インターロイキン(IL)-6などのプロ炎症性サイトカインの血清レベルの上昇が挙げられる。
胸部イメージング
呼吸器疾患の評価やモニタリングには、胸部X線(CXR)、CT、肺超音波検査(LUS)などの胸部画像検査がよく用いられている45 。Aiらは成人を対象とした研究を発表しており、CTは肺の変化を検出するための感度が良いことからCOVID-19診断のためにCTスキャンを検討すべきであると結論付けている47。
ある包括的な報告では、軽度の上気道呼吸器症状を有する小児COVID-19患者の35~50%では胸部CTスキャンは正常であると述べられているが、これは胸部CTスキャンが使用された場合、怪我をしていない小児の割合が不当に高く、CT放射線にさらされることを示唆している。
スクリーニングに使用するためには、胸部CTスキャンは症状のある症例だけでなく、無症状の小児でも肺の変化を検出する必要があるが、COVID-19が確認された小児のCT感度の中央値60%は、無症状の小児を有害な放射線にさらすのに十分ではない。
ウイルス性非合併性肺炎の症例でCTスキャンを行うことは珍しいため、現在のところ、無症候性SARS-CoV-2感染症の小児集団におけるスクリーニングツールとしてCTスキャンを使用することに対する有効な論拠はない。
CTスキャンはCOVID-19に対する特異性を欠いているため、専門家パネルは、特に患者の搬送を必要とする場合の画像選択には注意が必要であると推奨している48。
CXR
肺炎のほとんどの症例では、CXRは重要な診断ツールであるが、COVID-19の診断には限界がある。
4,27,49 しかし、重度のCOVID-19症例では、単発性または両側性のパッチ性またはびまん性の非対称性空域の狭窄、間質の変化、結節性が検出されることがある50 。
胸部CTスキャン
CTはCOVID-19を含むすべての肺病変の検出において高感度である。
しかし、多くの研究では、非特異的であり、他の肺pathologies.49-51にいくつかの類似性を負担するCTスキャン上のCOVID-19病変を説明したグラウンドガラスの不透明度は、主に胸膜下52と主に下葉に記載されていたが、細かいメッシュの影は、疾患の初期段階で発生した21,49,51,52 中等度のCOVID-19の小児では、びまん性のグラウンドグラス、クレイジーパヴィングパターン、圧密を伴う両側性の多小葉状分布が認められた21,47,53。
Xiaらは、重度または中等度のCOVID-19肺疾患を有する小児の半数にハローに囲まれた圧密が認められたことを報告しており、小児におけるこれらの病変にはある程度の特異性があることを示唆している。
非造影胸部CTスキャンはRT-PCR54に比べて早期診断ツールとして使用できることを示す研究があるにもかかわらず(パンデミック時には症例の負担が大きいため、CTはしばしば遅延する)、CTは小児の第一選択診断法として推奨されていない。
その理由は、照射リスク、特異的な病変がないこと、患者搬送時の汚染リスクが高まる可能性があることなどが挙げられる。
Fangらによる研究の結果は、特にRT-PCR検査の結果が陰性の場合、COVID-19に適合する臨床的および疫学的特徴を持つ患者のスクリーニングに胸部CTスキャンを使用することを支持している。
肺超音波検査
様々な研究で、LUSはCOVID-19で起こりうる変化を同定するための貴重なツールであることが実証されている56,57 。
しかし、LUSはCOVID-19に特異的ではない肺のアーチファクトを検出することができ、肺炎で起こる気管支との圧密、肺炎や気管支炎で起こる胸膜下圧密、気管支炎で起こる胸膜線の不整脈59などがある。
肺線維症、胸膜悪性腫瘍、COPD、60-62、気管支炎やウイルス性間質性肺炎の症例にみられる間質性肺胞炎にみられるB線、および線維症、61 嚢胞性線維症、62、気管支拡張症などの慢性肺疾患にみられる間質性肺胞炎にみられるB線がある。60
しかし、他の調査方法とは異なり、LUSはベッドサイドで簡単に利用でき57 、消毒が容易な携帯用プローブを使用することができ、医療スタッフの感染が少なくて済む。
治療法
現在のところ、COVID-19の病因治療や予防法はない。
66 軽症例の治療は現在の症状に対応し、ヒトからヒトへの感染を防ぐための隔離が最も重要な予防治療である。
19,20,26 非侵襲的人工呼吸(NIV)および高流量酸素療法(HFOT)は、ウイルスのエアロゾル化のリスクが高く、マスクの漏れを介してウイルスが拡散する可能性があるため、NIVおよびHFOTは、特定の症例で、マスクが最適な位置に正確に配置されている場合にのみ使用することができる。
COVID-19に関するレトロスペクティブ研究では、一度合併症が発生すると治療効率が悪くなるため、疾患の進化がまだ変化しうる初期の治療ウィンドウで抗ウイルス薬の投与を開始することが示唆されている67 。
これまでのところ、ヒトにおけるCOVID-19の治療に有効な抗ウイルス剤は示されていないが、複数の無作為化臨床試験が進行中である。
一部の抗レトロウイルス薬(ロピナビル/リトナビル、ダルナビル/コビシスタット、ファビピラビル、レムデシビル、リバビリン、オセルタミビル、トシリズマブ、ユミフェノビル、およびアンジオテンシン変換酵素[ACE]阻害薬など)は成人に適応がある1,67。
しかし、COVID-19の小児におけるいかなる抗ウイルス剤の有用性を示す研究はないため、この種の薬剤の使用は推奨されないであろう。
クロロキンおよびその誘導体(ヒドロキシクロロキンおよびクロロキンリン酸塩を含む)は、SARS-CoVおよびエボラに対して成功裏に使用されており、SARS-CoV-2の小児にも有効であることが示されている。小児に対する治療レジメンのほとんどは、クロロキン(またはその誘導体)とロピナビル/リトナビルであり、これらは小児にも許容できる程度の効率性と安全性プロファイルを示すことが報告されている。
小児のCOVID-19の治療にはインターフェロン-αの吸入が使用されているが、その効率性と安全性はまだ決定されていない1,65 。成人の重症例の治療には免疫グロブリンやインターフェロンの静脈内投与などの非特異的な免疫増強療法が使用されているが、小児に使用する前にはさらなる検討が必要である1,9,65。
コルチコステロイドは、ARDS、敗血症性ショック、脳症、出血障害などのCOVID-19の合併症の治療に推奨されており、その他の特定の病態ではステロイドが必要である。
多施設共同のCITRIS-ALI試験では、高用量のアスコルビン酸が他の原因によるARDSの治療に有効であり、死亡率を低下させることが実証されている70 。
COVID-19に関連した二次的な胸部感染症には抗生物質の使用が推奨される。1,4 小児におけるマイコプラズマ感染症の頻度9,21 とアジスロマイシンの抗炎症特性がよく知られていることを考えると、COVID-19 と細菌性重感染症の小児には抗生物質が選択される可能性がある。
最良の治療法の選択肢についてのエビデンスを収集するために、さらなる研究が行われるべきである。地域社会での感染を減らすことを目的とした予防は、さらなる発見がなされるまでは、COVID-19と闘うための唯一の証明された効率的な選択肢であり続けている。
小児における転帰と予後
いくつかの研究によると、COVID-19の臨床経過は成人に比べて軽度で、回復が早く、予後も良好であるとされている1,9,15 。しかしながら、最近の研究では、小児でも同様に重度のCOVID-19が良好な予後を示したと報告されている40 。
一部の研究者は、小児の肺上皮細胞ではACE2タンパク質の発現が少ないか、あるいは異なる形をしたACE2タンパク質が発現し、罹患率の低下につながるのではないかと仮説を立てているが、小児におけるCOVID-19の多様な症状のメカニズムを理解するためには、さらなる研究が必要である。
小児の急性下気道感染症を引き起こす最も一般的なウイルスであるインフルエンザウイルス、パラインフルエンザウイルス、呼吸器同期ウイルス(RSV)、ライノウイルス、またはアデノウイルスがコロナウイルスと交差反応する可能性があることが示されている72 。
ヒトからヒトへの感染を考慮すると、すべての年齢の小児がCOVID-19に罹患しやすいが、大多数はCOVID-19の軽症型であり、良好な経過をたどっている。小児の予後は成人に比べてはるかに良好であるが、小児では無症候性キャリア感染の方が多いと推定されている。
結論
このレビューは、COVID-19が小児ではまれであるとしても、無症候性SARS-CoV-2感染は成人よりも頻度が高いことを浮き彫りにしている。小児の COVID-19 を理解し、最も効率的な症例管理戦略を決定するためには、さらなる質の高いエビデンスの収集が不可欠である。
感染した小児の隔離を通じた感染予防は、適切なモニタリング、疾病合併症の早期発見、および適時の治療の機会と二次感染拡大の抑制を含めて不可欠である。「ダモクレスの剣」とSARS-CoV-2タンパク質の「王冠」が絡むパンデミックに巻き込まれている今、子どもたちはその戦いの鍵を握っているかもしれない。
小児におけるCOVID-19:臨床経過に異常がない理由
www.e-cep.org/journal/view.php?doi=10.3345/cep.2020.00801
キーメッセージ
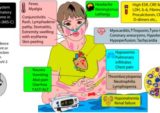
コロナウイルス疾患2019(COVID-19)感染は、新生児および小児の間で報告されている;しかしながら、この集団は成人に比べてはるかに少ない二次合併症を有している。これは、小児ではアンジオテンシン変換酵素2の発現が高く、免疫系がプライミングされ、サイトカインストームが減少していることに起因する可能性がある。さらに、幼児における再発ウイルス感染は、交差反応性免疫状態、微生物相互作用、および競争を介して、COVID-19に対するある程度の保護を提供する可能性がある。
重症急性呼吸器症候群コロナウイルス2(SARS-CoV-2)は、現在パンデミックとなっているコロナウイルス病2019(COVID-19)を引き起こす。原因は判明しているが、肺炎などの発症機序や小児の症状が軽い理由は不明のままである。臨床、疫学、生理学、免疫学的な概念から現在の仮説に基づいて説明されている。
疫学的には、小児のCOVID-19の報告と検査の頻度が少ないため、過少サンプリングと過少報告の問題がある。小児における疾病の重症度の低下と全体的な疾患の回復力は、小児をキャリアとすることでCOVID-19の感染を促進する[1]。
アンジオテンシン変換酵素(ACE)2がCOVID-19肺損傷の病態に関与しているという証拠があるにもかかわらず、小児の肺や他の組織におけるACE2発現の増加または未熟なACE2構造は、肺や他の臓器を有害な臨床経過や合併症から保護する可能性がある。小児の腸内でのACE2発現は、小児が成人よりも長いウイルス脱落期間を持つ理由を説明している[1]。
小児の免疫系は成人よりも活発であり、SARS-CoV-2感染の初期段階ではウイルスの複製を制御することで防御作用を発揮する [2]。さらに、小児におけるワクチン接種と頻繁なウイルス感染は、免疫系の活性化を高め [3]、ほとんどの症例で見られる異常のない臨床経過に寄与している可能性がある。
小児および若年成人のコロナウイルス感染症は、いくつかの国では主に冬の間に発生している。高齢の小児や成人は過去に感染経験があるため、新たに感染することはまれである。そのため、コロナウイルスに対する集団免疫を開発する機会がある。
COVID-19の小児における重篤な症状が稀であることは、高齢者に比べて小児および若年成人群では若年時の感染による交差反応性免疫状態が持続していることに起因すると考えられる。したがって、我々は、微生物の相互作用と競争が、小児におけるCOVID-19疾患の重症度を低下させる可能性があるという仮説を立てた。
自然免疫細胞は、病原体に関連した分子パターンを認識し、プロ炎症性およびインターフェロン(IFNs)カスケードを開始する能力を持っている。IFNは細胞傷害性T細胞およびナチュラルキラー(NK)細胞の活性を高める。
NK細胞は感染部位に移動し、IFN-γを産生し、これはウイルスに感染した細胞を死滅させ、適応免疫応答を高めることに関与している。さらに、インターフェロンはヤヌスキナーゼシグナル伝達経路を活性化し、ウイルスを殺すインターフェロン制御遺伝子のアップレギュレーションにつながる[4]。
Tヘルパー細胞を介した適応免疫応答もまた、COVID-19の重症度において重要な役割を果たしている。小児における比較的未熟な適応免疫系が、軽度の臨床症状の原因となっている可能性がある;しかしながら、これはまだ明らかにされていない。
興味深いことに、他の感染症(A型肝炎、マイコプラズマ肺炎)および免疫学的疾患(川崎病、急性後溶連菌性糸球体腎炎、ヘノッホ-ソンレン紫斑病)もまた、年長の子供や成人よりも年少の子供の方が臨床症状は軽度である[5]。
Chenら[2]は、CD4ヘルパーT細胞がBリンパ球を刺激して、マウスのSARS-CoV-2に対する抗体応答を作り出すことを実証した。このように、産生期のBALB/cマウスにおけるSARS-CoV-2感染に対する細胞性免疫系応答(CD4+ T細胞)は、感染の制御において重要である[2,6]。
小児におけるTヘルパー細胞の産生および効率の向上は、COVID-19に対する追加的な保護を提供する可能性がある。
COVID-19の原因物質はSARS-CoV-2単独ではなく、川崎病[5]やその他多くの症例に見られるように、ウイルスに感染した細胞やヒト微生物叢の他の病原体[7]から排泄される物質である可能性もある。生理学的には、小児の総リンパ球数が高いほど、COVID-19に対する免疫防御力が高くなる可能性がある。
さらに、小児は肺繊毛の拍動頻度が高く [8]、これがウイルスの肺気球への侵入を妨げている可能性がある。併存疾患がなく、環境汚染物質や有害物質への曝露が少ないことも、肺や気道の保護に寄与する他の生理的要因である。
さらに、子どもの十分な栄養状態および身体的および精神的ストレスが相対的に少ないことも、保護に寄与していると考えられる。
COVID-19の急性呼吸窮迫症候群(ARDS)は、肺血管系におけるフィブリン-血小板微小血栓とともに、空隙および肺実質にフィブリンが沈着し、呼吸機能障害が進行することによって開始される[9]。
小児はトロンビン生成能が低く、フィブリン形成速度が低下しているため、COVID-19関連ARDSのリスクが低い[10]。
COVID-19の肺損傷や多臓器不全も、小児の免疫系がマウンティングする能力が低い炎症反応であるサイトカインストームによるものである[11]。
結論として、小児はACE2の発現が高く、免疫系が感作されており、サイトカインストームの頻度が低下しており、健康な生理機能を有しており、これがCOVID-19の合併症率の低さを説明している。
パンデミックしているSARS-CoV-2ウイルスは、新生児や乳児の死亡例や経代感染による死亡例をいくつか引き起こしている。
したがって、本質的に病原性が低いヒト種に適応した一種の微生物と考えることができる。症例の過少報告、不顕性症候群、子供のウイルス脱落期間の長さなどが、ウイルス感染の隠れた一因となっていると考えられる。
関連記事