Contents
COVID-19 can affect the heart
science.sciencemag.org/content/early/2020/09/23/science.abe2813.full
要旨
COVID-19は多様なメカニズムを持つ潜在的な心臓症状のスペクトルを持っている。
7 種類の既知のヒトコロナウイルスは、心臓ではなく呼吸器に影響を与えることで知られている。しかし、最新のコロナウイルスである重症急性呼吸器症候群コロナウイルス2(SARS-CoV-2)は、心臓に対する顕著なトロピズムを有しており、心筋炎(心臓の炎症その細胞の壊死、心臓発作の模倣、不整脈、急性または長期化した心不全(筋機能障害)を引き起こす可能性がある。時にコロナウイルス感染症2019(COVID-19)の臨床症状の唯一の特徴であるこれらの合併症は、軽度の症状を呈した症例や、症状を呈していない人でも発生している。突然死を含む若い運動選手の心臓病変の最近の所見は、現在の知識の限界と、COVID-19の心臓症状の潜在的に高いリスクとオカルト有病率についての懸念を提起している。
4種類の「感冒」ヒトコロナウイルスHCoV-229E、HCoV-NL63,HCoV-OC43,およびHCoV-HKU1は、心臓異常とは関連していない。中東呼吸器症候群(MERS;MERS-CoVが原因)の患者で心筋炎を発症した単独の報告があり、SARS(SARS-CoVが原因)の患者で心疾患を発症した症例シリーズは限られている(1)。したがって、SARS-CoV-2の特徴は、心臓病変がより広範囲に及ぶことであり、これもまた、パンデミックと数千万人の人々がウイルスにさらされた結果であると考えられる。
SARS-CoV-2とSARSを構造的に区別しているように見えるのは、フーリン多塩基部位であり、この部位が切断されると、ウイルスが感染できる細胞の種類(トロピズム)が広がる(2)。ウイルスは全身のアンジオテンシン変換酵素2(ACE2)受容体を標的としており、細胞内のセリンプロテアーゼ膜貫通プロテアーゼセリン2(TMPRSS2ヘパラン硫酸、および他のプロテアーゼの協力を得て、そのスパイク蛋白質を介して細胞の侵入を促進する(3)。心臓はACE2の発現量が多い臓器の一つである。さらに、SARS-CoV-2のACE2に対する親和性は、SARSよりも有意に高い(4)。肺以外の他の臓器へのトロピズムが剖検標本から研究されている。SARS-CoV-2のゲノムRNAは肺で最も多かったが、心臓、腎臓、肝臓でもかなりの量が検出され、死亡した22人の患者のうち16人から心臓でウイルスのコピーが検出された(5)。COVID-19で死亡した39人の患者の剖検シリーズでは、38%の患者で心筋でウイルスが検出されなかったが、31%の患者では心臓で1000コピーを超える高ウイルス量が検出された(6)。
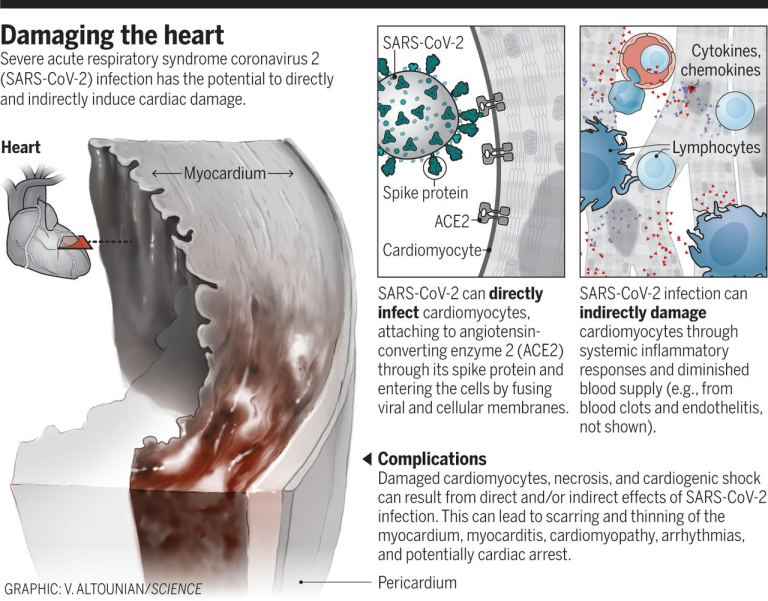
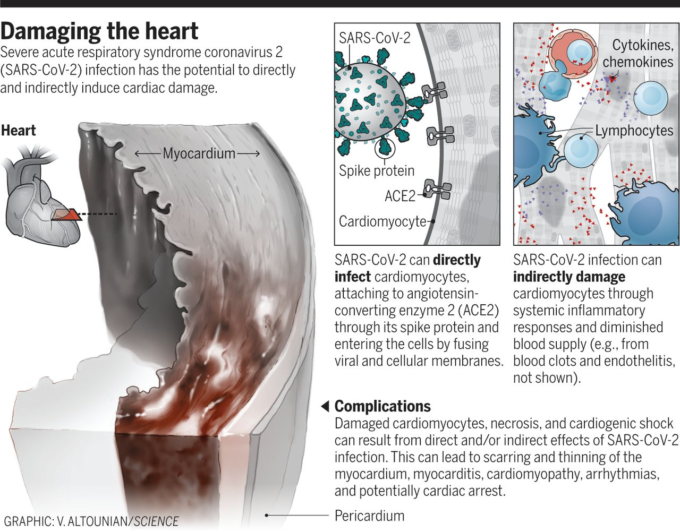
したがって、SARS-CoV-2の感染は、直接的にも間接的にも心臓にダメージを与える可能性がある(図参照)。SARS-CoV-2は、試験管内試験で人工多能性幹細胞(iPSCs)由来の心筋細胞に顕著な感染能力を示し、心筋細胞の断片化という特徴的なパターンをもたらし、「収縮機構の完全な溶解」をもたらした(7)。これらの所見のいくつかは、患者の剖検標本から検証された。別のiPSC研究では、SARS-CoV-2の感染は、曝露後72時間以内にアポトーシスと拍動停止をもたらした(8)。心筋細胞への直接感染のほかに、心臓への血管と複数の血管床に並ぶ内皮細胞へのウイルスの侵入が記録されている。感染した心臓および内皮細胞に対する二次的な免疫反応(内皮炎)は、多くの潜在的な間接的影響の一次元にすぎない。これらには、血圧を調節するレニン-アンジオテンシン-アルドステロン系の調節障害、血小板、好中球、マクロファージ、リンパ球を含む原炎症反応の活性化、サイトカインの放出および原血栓状態が含まれる。微小血管と大血管の両方での凝固傾向は、複数の剖検シリーズおよび若年の脳卒中患者COVID-19で報告されている。
心血管系の症状には多様なスペクトルがあり、心臓細胞の限定的な壊死(傷害の原因となる)から心筋炎、心原性ショック(十分な血液を送り出すことができないことがしばしば致命的である)に至るまで、多岐にわたる。心筋障害は、血中トロポニン(心筋特異的酵素)濃度に反映され、COVID-19では一般的であり、入院患者さんの少なくとも5人に1人と、既往症のある患者さんの半数以上に発生している。このような心筋損傷は院内死亡の危険因子であり、トロポニン濃度は死亡リスクと相関する。さらに、トロポニン量が高い患者では、炎症[C反応性蛋白、インターロイキン-6(IL-6フェリチン、乳酸脱水素酵素(LDH高好中球数を含む]および心機能障害(アミノ末端プロB型ナトリウム利尿ペプチド)のマーカーが増加している(9)。
限定的な損傷のパターンよりもさらに心配なのは、心筋炎である。心臓のびまん性炎症であり、通常、損傷と損傷に対する炎症反応が人の心臓の3層の心膜(心臓を取り囲んでいる)にまで及ぶ可能性があり、損傷の多様な混合物を表している。リンパ球浸潤を示さなかったSARS関連心筋炎とは異なり、この免疫および炎症反応はSARS-CoV-2感染後の剖検で典型的な所見である。電気伝導を調整する心筋細胞が関与すると、伝導ブロックや悪性心室性不整脈を引き起こし、いずれも車内での心停止につながる可能性がある。
このような院内不整脈とともに、COVID-19の普及率が高い複数の地域で院外心停止や突然死が増加したという報告があり、例えばイタリアのロンバルディア州では前年比77%増となっている(10)。16歳の少年のような若い患者でも、胸痛症状の集積、心電図異常、血液中の心臓特異的酵素の増加により、心臓発作を模擬した心筋炎が多数報告されている。広範囲でびまん性の心筋損傷がある場合は、心不全、急性心肺炎(右心不全、肺塞栓の可能性あり心原性ショックを起こすことがある。
COVID-19に関連する心機能障害は、たこつぼ症候群(ストレス性心筋症とも呼ばれる内皮炎および関連する血栓を伴う動脈硬化性プラーク破裂による虚血、小児の多系統炎症性症候群(MIS-C)を含む他の経路にも起因し得る。ストレス性心筋症の根本的なメカニズムは十分に理解されていないが、パンデミックの間に著しく増加した。MIS-Cは免疫介在性と考えられており、血管炎、冠動脈瘤、心原性ショックなど、様々な心血管系の特徴を示する。この症候群は小児に限ったものではなく、45歳の男性の症例など、成人でも同様の臨床的特徴が報告されている(11)。
最近のCOVID-19患者の一連のシリーズでは、心臓の磁気共鳴画像(MRI)または心臓超音波検査を受けたことで、心臓病変に関するいくつかの新しい知見が得られている(12-14)。COVID-19から回復した100人の患者のコホートでは、78人に心臓異常が認められ、そのうち18人中12人は症状のない患者であり、60人には心筋炎と一致する心筋炎症が継続していた(12)。COVID-19を用いた大規模プロスペクティブコホートでは、1200人以上の患者の大多数が心エコー異常を有していた(13)。このことは、特にSARS-CoV-2感染症の少なくとも30~40%は症状を伴わずに発症していることから、予想されていたよりもはるかに多くの心臓病変が存在するのではないかという懸念を生じさせている。このような患者には心臓病変が潜んでいる可能性がある。
これまでに、COVID-19と一致する肺の異常があるかどうかを判断するために胸部コンピュータ断層撮影(CT)スキャンを受けた無症候性の善意の感染者の小規模なシリーズが4例報告されている。実際、無症候性の人の半数には、症状のある患者に見られる肺CTの特徴が見られた。しかし、これまでのところ、SARS-CoV-2で陽性と判定された人や、血清陽性だが症状がない人の心臓画像検査はほとんど行われていない。さらに、SARS-CoV-2感染後の臓器異常の消失や持続の時間経過についても報告されていない。内臓障害を併発しているにもかかわらず、無症候性感染の割合が高いことは、私たちの知識ベースに根本的な大きな穴があることを示している。
症状のない人とは対照的に、long-COVIDと呼ばれる長期にわたる、しばしば衰弱性の病気に苦しむ人がかなりの割合で存在する。典型的な症状としては、疲労感、呼吸困難、胸痛、心臓のリズム異常などがある。免疫学的根拠が考えられるが、まだ確定されていない。このような患者は、心筋炎や線維化などの心臓異常の可能性があるかどうか、系統的な心血管系の評価を受けておらず、それが持続する症状の原因となっている可能性もある。将来、病因不明の心筋症を呈し、SARS-CoV-2抗体陽性の患者が出てきても不思議ではない。しかし、このような心筋症をウイルスによるものとすることは、感染の有病率が高いことを考えると困難であり、因果関係を支持するためにウイルス粒子を同定するために、最終的には生検が必要になるかもしれない。
スポーツ選手の心筋症は、その懸念をさらに高めている。COVID-19から回復した27歳のプロバスケットボール選手は、トレーニング中に突然死を経験した。オハイオ州立大学からの前向きな研究(15)で26人中4人(15%)が心筋炎を患っていることが判明しており、メジャーリーグ野球のトップ投手の1人と一緒に数人の大学のアスリートがいます(14)。これらの若くて健康な患者は軽度のCOVID-19を有していたが、その後、疑われない心臓病変を有していたことが判明した。このような若くて健康な集団は、SARS-CoV-2感染後に症状が出ないことが最も一般的であり、どのくらいのアスリートが潜伏性心疾患を持っているのだろうかという疑問が生じる。症状の有無にかかわらずSARS-CoV-2陽性と診断されたアスリートを、何らかの形の心臓画像検査や不整脈スクリーニングによって適切な対照者と体系的に評価することは、より多くのことが理解されるまでは賢明なことであると思われる。
最も興味をそそられるのは、なぜ特定の患者ではSARS-CoV-2感染後に心臓病変を起こしやすいのかという疑問である。パンデミックが発生して数ヶ月が経過した時点では、心臓病変は主に重症のCOVID-19患者に発生するだろうと予想されていた。明らかに予想よりも一般的であるが、真の発生率は不明である。何がこの病因を駆動しているのかを決定することが重要である。それが個人の炎症反応なのか、自己免疫現象なのか、あるいはその他の説明を明らかにする必要がある。SARS-CoV-2感染を予防することに加えて、心血管系への感染を回避することが最も重要である。COVID-19の顕著な異質性は、症状の欠如から致死性に至るまで、十分に理解されていない。新たに出現したウイルスであり、ヒトの集団全体に広く分布しており、病気の症状は多岐にわたっており、そのすべてがあまりにもオカルトなものであることが多いため、これを解明することは特に困難なことである。