Contents
Broccoli or Sulforaphane: Is It the Source or Dose That Matters?
www.ncbi.nlm.nih.gov/pmc/articles/PMC6804255/
要旨
ブロッコリーの摂取による健康への有益な効果については、疫学的な証拠があるが、その多くは明らかにイソチオシアネートのスルフォラファンによって媒介されている。スルフォラファンはその前駆体であるグルコラファニンとして植物中に存在し、植物組織や哺乳類のマイクロバイオームに存在するβ-チオグルコシダーゼであるミロシナーゼの作用によって形成される。ブロッコリーから初めて単離され、1990年代初頭にラットで癌の化学的保護作用を示すことが確認されて以来、これまでに3,000件以上の論文が発表され、齧歯類疾患モデルでの有効性、作用機序、薬物動態、薬理作用、疾患緩和作用を検討した50件以上の臨床試験が行われてきた。本レビューでは、製剤(例えば、植物、スプラウト、飲料、サプリメントバイオアベイラビリティと有効性、および前臨床試験および臨床試験で使用されているグルコラファニンおよび/またはスルフォラファンの用量との関係について、現在の知見を評価している。動物モデル試験と臨床試験をより良く統合するための課題、特に投与量や投与経路の選択については、特に注意を払っている。根本的な作用機序を解明し、ヒトにおける薬力学的作用のバイオマーカーを開発し、検証するためには、さらなる努力が必要である。痛切な教訓は、世界の人口のすべてのスペクトルに利益を分配するための公衆衛生のパラダイムを実施するためには、アプローチの変更が必要であるということである。
キーワード:ブロッコリー、スルフォラファン、グルコラファンニン、ミロシナーゼ、化学的保護、アロメトリックスケーリング、臨床試験、Nrf2,毒性
1. はじめに
1.1. ブロッコリーの疫学と健康
ブロッコリーの健康への有益な効果についての集団的なレトロスペクティブ(観察的プロスペクティブ、介入的な証拠は堅牢である。前者の2つのカテゴリを簡単にここに要約し、後者はこのレビューの大部分を構成する。ブロッコリーは1500年代に家畜化され、1700年代初頭にイギリスに持ち込まれ、1700年代後半に後のアメリカに持ち込まれたと考えられていたが、アメリカでは1920年代までほとんど知られていなかった[1]。このように、比較的新しい作物であるため、比較的広く消費されていたのは約1世紀程度と考えられる。健康へのブロッコリーの影響の疫学は、その世紀の正確に半分をカバーし、グラハムの初期の仕事では、大腸癌にブロッコリーと他のアブラナ科の野菜の消費との間の用量反応関係を示したことから始まる[2]。それ以来、アブラナ科の野菜および/または膀胱癌[3]と前立腺癌[4]のためのブロッコリーに関連付けられているリスク低減の印象的な実証があっただけでいくつかの名前を付ける。我々や他の研究者は最近、アブラナ科野菜全般、特にブロッコリー、スルフォラファンが神経学的、腫瘍学的、皮膚学的、その他の状態(例えば、[5,6,7,8,9])に関連していることを示唆する疫学的、機械論的研究の増加をレビューしている。世界がん研究基金(World Cancer Research Fund)および米国がん研究所(American Institute for Cancer Research)を含む組織は、がん予防に強い特徴を持つものとして、ライフスタイル(地中海式食生活)および食品群(非スターキー性の野菜または果物)を強調することを選択しており、がんリスクに関して特定の果物または野菜を推奨することから遠ざかっている [10]。しかし、すべての証拠は、ブロッコリー、特にブロッコリー由来のスルフォラファン、およびその生物学的前駆体であるグルコラファニンが、さまざまな慢性疾患、さらには感染症(ヘリコバクター・ピロリなど)の状態から保護されていることを示している[11]。
1.2. 生理活性イソチオシアネートとしてのスルフォラファンの発見
スルフォラファンは前世紀半ばに抗生物質として記述され、レッドキャベツやアメリカ西部の牧草地の雑草ホアリークレスから単離された[12]。その後、さまざまなグループがそれを合成してきたが、TalalayとZhangは、ブロッコリーからそれを分離し[13]、その癌保護特性を実証した最初のグループであった[14]。その後、その前駆体であるグルコラファニンがブロッコリーの新芽に豊富に含まれていることが判明し、スルフォラファンが動物の発がんモデルで活性を示すことが確認された[15]。また、Posner らによって作成された 100 以上の合成アナログの構造活性評価では、スルフォラファンよりも強力な細胞保護酵素誘導剤は見出されなかった[16]。我々をはじめとする多くの研究者は、この分子が哺乳類の細胞、組織、そしてヒトの体内に存在することで、複数の経路や代謝的な結果を明らかにしていた[8,18,19]。ここでは、あまりにも数が多すぎてレビューしきれないが、このような多様な影響については、他の研究者[20,21,22]でも十分にレビューされていることに留意したい。私たちの初期の研究では、損傷を受けていない植物には遊離スルフォラファンはほとんど存在せず、そのすべてが生物学的に不活性な前駆体であるグルコラファニンの形で存在していることが示された[15]。このように、植物におけるグルコラファニンの生合成を制御している要因を考えることは重要である。
1.3. ブロッコリーにおけるグルコラファニンの生合成と機能
グルコシノール酸グルコラファニンはアミノ酸メチオニンに由来する。自然界でのグルコラファニン形成に至る生合成経路は精巧であり、3つの独立した段階(スキーム1)を含んでいる(スキーム1)[23,24]。第一段階では、メチオニンの側鎖が2つのメチレン基によって伸長する。第二段階では、コアとなるグルコシノレート構造を形成する。第三段階は、グルコシノレート側鎖の二次修飾を構成する。
第1段階(スキーム1a)の間に、細胞質分岐鎖アミノ酸アミノトランスフェラーゼ(BCAT)がメチオニンのトランスアミノ化を触媒して2-オキソ-4-メチルチオブタン酸を与える。次に、このα-ケト酸は、葉緑体で起こる3つの連続的な変換の2つのラウンドを含む周期的なメカニズムで、2つのメチレン基によって伸長される。(i)メチルチオアルキルリンゴ酸合成酵素(MAM)によって触媒されるアセチル-CoAとの縮合、(ii)アコニターゼ(AC)によって触媒される異性化、(iii)イソプロピルリンゴ酸脱水素酵素(IPMDH)によって触媒される酸化的脱カルボキシル化。これらの変換の最終生成物である2-オキソ-6-メチルチオヘキサン酸は、BCATによって触媒されるトランスアミノ化反応でジホモメチオニンに変換される。
第二段階(Scheme 1b)では、ジホモメチオニンはチトクロームP450(CYP)を介したアルドキシムへの変換を受け、これはさらに酸化ニトリルに酸化され、その後、グルタチオン(GSH)のような硫黄供与体と共役する。この共役化反応は、非酵素的に行われてもよいし、グルタチオンS-トランスフェラーゼによって触媒されてもよい。結果として生じるS-アルキルチオヒドロキシメートは、C-SリアーゼSUR1によって触媒される反応でチオヒドロキシメートに変換される。
この酵素は基質内の遊離アミノ基を必要とするため、中間工程が必要となる。グルタチオンと活性化されたアルドキシムの間のコンジュゲート内のγ-グルタミル残基の加水分解除去である。第二段階の最後のステップは、グルコシルトランスフェラーゼが媒介するS-グルコシル化であり、その結果、スルホトランスフェラーゼ(ST)によって触媒されるスルホ化により、デスルホグルコシノレートが形成される。このようにして、親グルコシノレートである4-メチルチオブチルグルコシノレート(グルコエルシン)が生成される。
最終段階(スキーム1c)では、グルコシノレート側鎖の二次修飾が起こる。これは、フラビンモノオキシゲナーゼ(FMO)によって触媒されるS-オキシゲナーゼ反応によって達成される。これらの精巧なバイオトランスフォームには13種類の酵素が関与し、グルコラファニンの合成が行われている。注目すべきことに、シロイヌナズナではグルコシノレートの生合成は光によって制御されており(暗闇の期間が長くなると制御が低下し、光に曝されると大幅に増加する一般的な硫黄代謝と協調した日内変動を示している[25]。
グルコラファニンは化学的に安定で生物学的には不活性である。しかし、かじったり噛んだりするような植物組織の損傷に続いて、グルコラファニンは酵素ミロシナーゼ(ß-thioglucosidase)と接触し、そのままの植物ではその基質から物理的に分離される。ミロシナーゼはグルコラファニンの加水分解を触媒してグルコースを遊離させ、不安定なアグルコン(Scheme 1d)を形成する。重要なことに、哺乳類の細胞はミロシナーゼを産生しないが、グルコラファニンからスルフォラファンへの変換は哺乳類ではまだ行われている。この変換は消化管の細菌性微生物叢によって行われ、抗生物質による治療や機械的な腸管洗浄によって大幅に減少させることができる[26]。注目すべきことに、この微生物が介在するグルコラファニンの変換は、最近の研究で、マウスの大腸内で局所的に高濃度のスルフォラファンを生成するために利用されている[27]。
植物では、グルコシノレートの主な機能は病原体や草食動物に対する防御であると考えられており、これは主にイソチオシアネートの加水分解産物に起因すると考えられている。病原体に対する抵抗性は、植物のグルコシノレート含有量と正の相関があり[28]、これは土壌中の真菌類組成にも影響を与える[29]。さらに、植物のグルコシノレートプロファイルの変化と、光合成や成長などの基本的な生理学的プロセスの間には、干ばつ、極端な温度、光、塩分、栄養不足などの生物学的ストレスの間に発生する相関関係がある[30]。これらの相関関係を総合すると、グルコシノレートは、様々な環境的課題から植物を保護するために機能していることが示唆される。したがって、Brassica oleraceaの家畜化された系統は野生種に比べてグルコシノレートのレベルが低いことは驚くべきことではない [31]。逆に、特定の野生のBrassica種(B. villosa)のグルコラファニン含量は高く、この種はグルコラファニンの濃度を高めたブロッコリーの交配種を作るために使用されている [32]。また、興味深いことに、グルタチオン生合成を欠損した変異体は、野生型に比べて成長抑制効果のあるスルフォラファンに感受性が高く、植物と哺乳類のスルフォラファン代謝に類似性があることが示唆されている[33]。
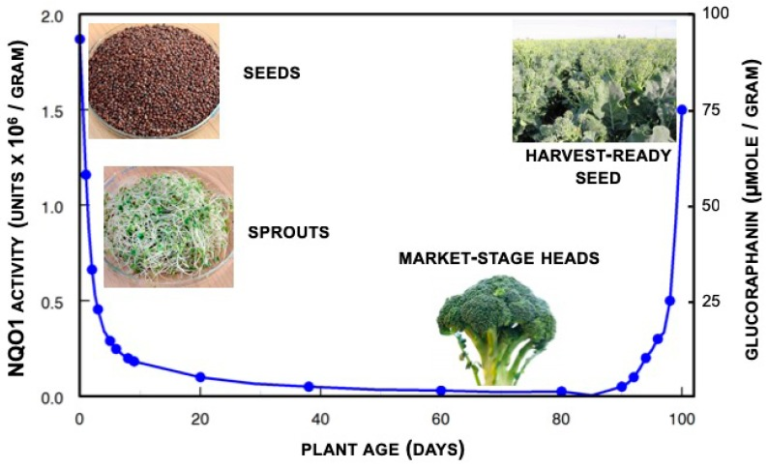
1.4. ブロッコリーのグルコラファニン濃度
グルコラファニンはブロッコリー植物のすべての組織に存在するが、空中部に最も豊富に存在し、花芽(花芽最終的には種子に最も豊富に含まれている(図1)。他の食用アブラナ科(アブラナ科)の2~3種にはかなりの量のグルコラファニンが含まれているが、一般的な文化で言われているほど普及しているとは言えない。異なるボルチモア地域のスーパーマーケットで購入した31の新鮮で調理されていないブロッコリー(Brassica oleracea var. italica)の頭の1つのサンプリングでは、新鮮な重量1グラムあたり平均0.38μmolのグルコラファニンが検出されたが,0.005未満から1.13μmol/グラムの範囲であった[34]。75 種類以上の異なる遺伝子型の畑で栽培されたハイブリッドブロッコリーで試験した場合のグルコラファニンのレベルは、2 年連続で同じ畑で栽培した場合、1 グラム新鮮重量あたり平均 0.88 と 1.10 μmol のグルコラファニンであった [35]。畑と温室で 3 年間栽培した 32 種類の遺伝子型を用いてさらに研究を進めたところ、同様の値が得られ、ブロッコリーの頭部の平均グルコラファニン含量は 1 グラム新鮮重量あたり 0.36 μmol であった [36]。ブロッコリーの種子中のグルコラファニン量は遺伝子型によって大きく決定されるが、植物の生育環境(場所、年、干ばつ、汚染、病害圧など)も明らかに重要な役割を果たしていると判断された [37]。
図1
重量ベースでは、グルコラファニン(右軸)がブロッコリーの種子に最も多く含まれている。酵素的にスルフォラファンに変換された後、これらの植物の抽出物が哺乳類細胞のNQO1などの第2相酵素を誘導またはアップレギュレートする能力は、正確に同じ曲線(左軸)をたどっている。
2. げっ歯類におけるブロッコリーベースの介入
2.1. 剤形・投与経路・用量
我々は、スルフォラファンをマウスやラットモデルの疾患予防薬として評価した膨大な文献を調査した。いくつかの研究では、ブロッコリー(通常は凍結乾燥)を齧歯類の飼料に添加して動物に与えたことが報告されているが、大多数の研究では、スルフォラファンを市販の研究用化学物質として単体で摂取した場合の有効性(分子的、生化学的、生物学的、病理学的なエンドポイントでの評価)が検討されている。注目すべきは、R-スルフォラファンは天然に存在するが、歴史的に入手可能性と相対的なコストの問題から、合成由来のR,S-スルフォラファンがほとんどの動物実験で使用されてきたことである。ほとんどの出版物では、スルフォラファンの形態を直接説明していない。R-スルフォラファンはラセミ体であるR,Sと比較して、様々なモデルにおいて有効性が高いことが示唆されている。本レビューではスルフォラファンを用いた動物実験に焦点を当てているが、ブロッコリー由来の製剤を用いた食事研究では、生理活性量を正確に決定することはほとんど試みられていない。
スルフォラファンの投与経路は、主に経口、腹腔内、外用の 3 種類が用いられている。図2は、マウスへの経口投与と腹腔内投与の用量分布を示したものである。経口投与は NCI が化学予防薬の開発において一般的に使用しているルートである[39]。しかし、図2に示されているように、やや逆説的ではあるが、スルフォラファンを用いた研究では腹腔内投与が最も一般的に用いられている。おそらく、この選択は、動物への投与が比較的容易であることを反映しているのではないであろうか。
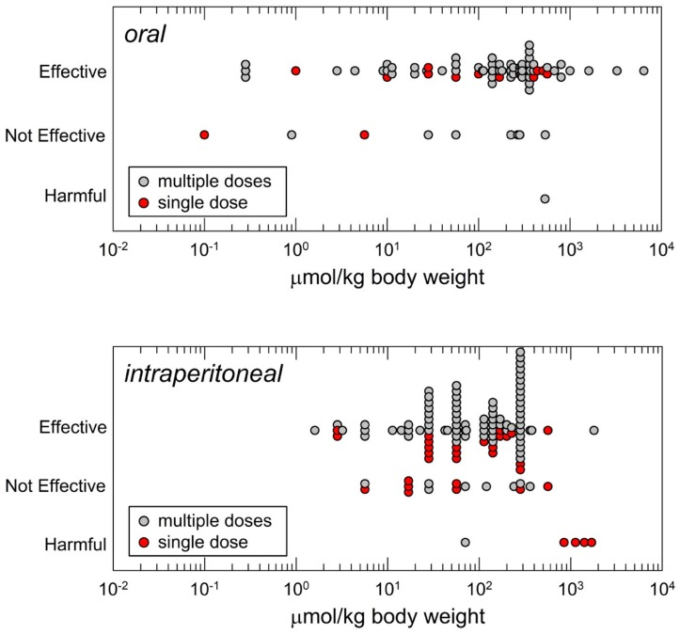
図2
文献で報告されているスルフォラファンのマウスへの1日投与量を投与経路と有効性の結果に基づいて分布した。上段は経口投与(経口投与または食事中投与下段は腹腔内投与。必要に応じて、体重25g、食事摂取量4g/日と仮定して用量を外挿している[38]。
腹腔内投与では、スルフォラファンの優れたバイオアベイラビリティーを反映して、経口投与とほぼ同等の薬理効果が得られると考えられる。経口投与では4対数以上、腹腔内投与では3対数以上の範囲で選択されている。スルフォラファンの有効量の中央値は、経口投与で175μmol/kg、腹腔内投与で113μmol/kgである。投与経路にかかわらず、ほとんどの研究で有効性が肯定的に報告されているのは、論文のバイアスを反映していると思われる。それにもかかわらず、数ははるかに少ないにもかかわらず、いくつかのモデルにおいて有効性の欠如が報告されている研究があるという観察も有益である。例えば、腫瘍の異種移植片や化学発がん、細菌感染、気道の炎症、脳虚血などである。リストアップされた「有効ではない」反応のほとんどについては、用量反応評価の一環として、高用量での試験エンドポイントについて有意な反応が報告されている。有害な結果を報告している研究は非常に少ないが、後述するように注目すべきものである。スルフォラファンの局所適用は、皮膚の紅斑、炎症、または光発がんの緩和に効果的に使用されてきたが、その効果は限定的であった。
スルフォラファンのマウスへの経口投与(表 S1腹腔内投与(表 S2外用投与(表 S3ラットへの経口投与(表 S4)を用いた研究の文献を列挙し、注釈を付した。
2.2. 有効性評価項目。メカニズムと用量、リスクとベネフィット
スルフォラファンの生体内での作用機序を厳密に検討した研究は比較的少ない(図 3)。この実験的な不足は、細胞培養系で確認された作用機序を報告している多くの研究とは対照的である[40,41]。最近の書誌学的レビューでは、スルフォラファンが Nrf2 シグナル伝達の活性化剤として最も多く引用されていることが示されている [42]。実際、いくつかの研究では、野生型マウスとNrf2ノックアウトマウスの転帰を比較することにより、スルフォラファンのNrf2シグナル伝達および疾患予防に対する作用を比較している。いくつかのケースでは、Nrf2依存性の作用が抗炎症作用にリンクしている。いずれの場合も(いくつかの重複する研究を含む広範囲の用量が採用されており、少なくとも有効性の下限(3-10μmol/kg)が示されている。生体内試験でのアポトーシス誘導を検討した研究では、主に異種移植片を用いた抗腫瘍実験では高用量(60μmol/kg以上)が用いられている。同様に高用量への依存度は、ヒストン脱アセチル化酵素(HDAC)活性の阻害に関する研究にも反映されている(>100μmol/kg)。これらの場合のデータがないことは、低用量での効果がないことと区別されるべきである。さらなる実験が必要である。今のところ、生体内での用量反応試験は比較的少ないので、スルフォラファンの用量に対する反応の関係をプロットしたものが “S “や”∩”の形をしているのか、あるいは他の形をしているのかを評価することはできない。最大有効量は確立されていないが、エンドポイントによって異なる可能性がある。
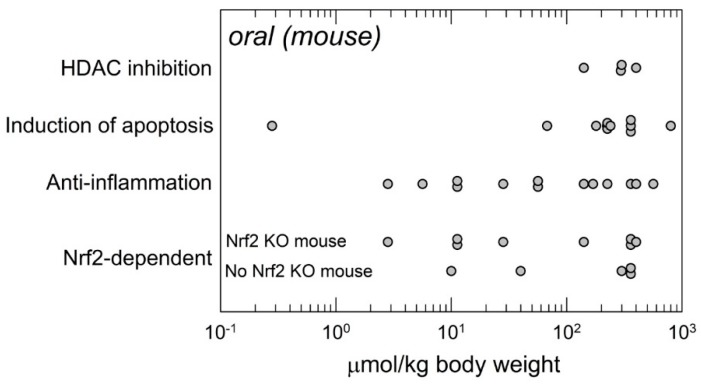
図3
サルフォラファンの経口投与量の分布について、生体内試験での基礎的メカニズムの実験的検討を含む研究において、マウスに投与されたサルフォラファンの経口投与量の分布。データは原著論文で報告され、解釈されたものである。掲載されているメカニズムは必ずしも排他的なものではない。Nrf2 KO:Nrf2ノックアウト。いくつかの研究では、Nrf2依存性を推測するために、野生型マウスとNrf2 KOマウスの応答の比較が含まれており、リストされているメカニズム(主に「抗炎症」)にも含まれている。
マウスに高用量のスルフォラファンを用いて実施されたいくつかの研究では、リスクとベネフィットの分析と治療または予防の指標の決定に注意を払う必要がある毒性が記載されている。Socalaら[43]は、単回投与の腹腔内注射後のマウスにおけるスルフォラファンの毒性プロファイルを検討した。スルフォラファンの高用量投与により、著しい鎮静(150-300 mg/kg低体温(150-300 mg/kg運動協調障害(200-300 mg/kg骨格筋力の低下(250-300 mg/kg死亡(200-300 mg/kg)が認められた。マウスにおけるスルフォラファンのLD50値は213 mg/kg i.p. (1203 µmol/kg)と推定された。この値は、マウスにおける有効性結果の中央値として報告されている用量の約10倍である。スルフォラファン(100 mg/kg)は、痙攣試験においてカルバマゼピンの抗けいれん作用を増強した。この薬物相互作用は自然界での薬物動態学的なものである可能性があり、ヒトでは観察されていない相互作用の一形態であると考えられる[44]。Shoreyら[45]は、発がん性物質ジベンゾ[def,p]クリセンに経産期および授乳期に曝露され、スルフォラファン(400ppm)またはその主要な全食源であるブロッコリースプラウト(10%wt/wt)を補給された母親から生まれた子供では、成人動物モデルにおける化学的保護作用の多くの報告とは対照的に、罹患率の増加および肺腫瘍発生の減少は認められなかったことを示した。潜在的に最も懸念されるのは、Taoら[46]の研究である。彼らは、カルバミン酸ビニルを用いた化学発がんモデル(A/Jマウス)と遺伝子モデル(LSL-K-rasG12D/+マウス)を用いて肺がんを誘導した。マウスに12.5mg/kg(75.5μmol/kg)を腹腔内投与した(5回投与、腫瘍誘導中は3日に1回または腫瘍誘導後1週間から3日に1回12.5mg/kgを腹腔内投与し、13週間(後処理)を行った。化学発がんモデルでは、前処理により腫瘍数が減少し、後処理により腫瘍がわずかに促進された。遺伝モデルでは、SFの前処理は腫瘍数に影響を与えなかったが、後処理は腫瘍数と大きさを増加させた。スルフォラファンの投与量が0.5μmol/kg未満でのヒトでの有効性が観察され、マウスからのアロメトリックスケーリングとi.p.投与によるバイオアベイラビリティーの改善を考慮すると、安全性の差は10倍程度しかないと考えられる。Kombairajuら[47]は、同じLSL-K-rasG12D/+マウスモデルにおいて、スルフォラファンの長期投与(0.5 mg, 5d/wk, 3ヶ月間、ネブライザーを用いて)は腫瘍形成を促進しなかったと報告していることに留意すべきである。スルフォラファンやブロッコリーベースの製剤を用いた長期の予防的介入を行う場合には、投与量、投与スケジュール、投与期間について慎重に検討する必要があると考えられる。
3. ブロッコリーを用いた臨床試験
3.1. スルフォラファンの薬物動態と薬力学
スルフォラファンは哺乳類細胞に入ると、GST触媒反応によりGSHと共役し、メルカプトウリン酸経路に入る(Scheme 1e)。スルフォラファンのグルタチオン共役体は、γ-グルタミルトランスペプチダーゼ(γGT)、システイニルグリシナーゼ(CGase)、N-アセチルトランスフェラーゼ(NAT)によって触媒される一連の連続的な変換を受けます。最終的には、スルフォラファン(メルカプトウリン酸)のN-アセチルシステイン抱合体が生成される。さらに、スルフォラファンは、エルシン[1-イソチオシアナト-4-(メチルチオ)ブタン]への相互変換を受けることができ、その後、スルフォラファンと同じ方法で代謝される[48,49]。
スルフォラファンとその代謝物(ジチオカルバメート)は、1,2-ベンゼンジチオールとのシクロ縮合により、ピコモル範囲の感度でまとめて定量することができる[50]。この高感度で簡便な方法は、ネズミやヒトにスルフォラファンを投与した後の血液、血漿、尿、組織中のスルフォラファンとその代謝物のレベルを測定するために広く利用されている。この方法を用いて、妊娠マウスにスルフォラファンを単回(5μmol)投与した後の2時間後の胚におけるジチオカルバメートの検出から、スルフォラファンが胎盤関門を通過することが明らかになった[51]。さらに、液体クロマトグラフィーとタンデム質量分析法(LC-MS/MS)で分離した後、個々の代謝物を分析する方法も開発されている[52,53]。さらに、スルフォラファン[1-イソチオシアナト-4-メチル-スルフィニル(1,1,2,2,3,3,4,4,4-2H8)ブタン]とそれに対応するメルカプトウリン酸経路共役体の安定同位体標識内部標準物質と結合した質量分析法を用いることで、スルフォラファンとその代謝物の定量的、精密、高感度、かつ特異的な分析が可能になる[54]。
これらの分析ツールを用いて、齧歯類およびヒトを対象とした多くの薬物動態試験が実施されてきた。例えば、10 週齢の雌スプラ グ・ドーリーラットに 150 μmol の超高用量スルフォラファンを経口投与したところ、血漿中のジチオカルバミン酸塩濃度は急速に上昇し、投与後 1 時間後に 60 μM のピーク(Cmax)に達し、濃度曲線下面積(AUC)は 491 h μmol/L、排泄定数(Kel)は 0.1 h-1,排泄半減期は 6.7 h であった [55] 。同様に、健康なヒトボランティア4名にブロッコリースプラウトイソチオシアネート200μmolを経口投与したところ、投与1時間後の血漿中ジチオカルバミン酸塩ピーク濃度(Cmax)は1.91±0.24(0.943~2.27)μMで、半減期は1.77±0.13時間、クリアランスは369±53mL/minであった[56]。スルフォラファンを200μmolのスルフォラファン含有粉末としてカプセルに封入して20名に投与した試験では、3時間後のCmaxは0.7±0.2μM、半減期は1.9±0.4時間であり、質量分析法で測定したスルフォラファン当量体の排泄は1.9±0.4時間であったと報告されている[57]。ブロッコリースープを単回投与した別の薬物動態試験では、スルフォラファン16μmolまたは52μmolのいずれかに相当する量を投与した場合、低用量では1.5時間、高用量では2.2±0.8μM、2時間では7.3±2.9μMのCmaxが報告されている[53]。84,280,または452μmolのグルコラファニンを単回投与したブロッコリースープ(グルコラファニン含有量が増加した植物から調製)を用いた二重盲検無作為化クロスオーバー試験では、それぞれ0.17±0.12,0.37±0.26,および0.61±0.40μMのピーク血漿中濃度(Cmax)が報告されている[52]。別の研究では、手術の1時間前に200μmolのスルフォラファンを投与したブロッコリースプラウト製剤の単回投与を受けた縮小乳房形成術を受けた8人の健康な女性で、右と左の乳房について、それぞれ0.92±0.72μMの血漿ジチオカルバメート濃度と1.45±1.12と2.00±1.95pmol/mg組織の平均上皮/間質濃縮乳房組織ジチオカルバメート濃度を報告している[55]。
前立腺生検のために来院した男性を対象とした二重盲検無作為化プラセボ対照試験では、4-8週間の介入期間の後、12時間間隔で100μmolのスルフォラファンを1日2回投与した場合,0.12μMのスルフォラファンとその代謝物の血漿中濃度が検出された [58]。変形性膝関節症で膝関節置換手術を受けた患者の血漿中に2.2μM、滑液中に500nMのイソチオシアン酸が検出された[59]。
111μmol相当のグルコシノレートまたはイソチオシアネートを含むブロッコリースプラウト抽出物を単回経口投与した健康な被験者を対象とした研究では、ジチオカルバミン酸塩の累積尿中排泄量は、イソチオシアネート製剤で88.9±5.5μmol、グルコシノレート製剤で13.1±1.9μmolであった[60]。この研究はさらに、イソチオシアネート製剤では25~200μmolの用量範囲で一貫して直線的に排泄されたのに対し、グルコシノレート製剤では個人間で排泄量に大きなばらつきがあることを明らかにした。これらの観察結果は、無作為化プラセボ対照二重盲検第I相臨床試験の結果とほぼ一致している。この試験では、イソチオシアネート(25μmol)またはグルコシノレート(25μmolまたは100μmol)を豊富に含む製剤を、健康なヒト被験者3人のコホートに8時間間隔で7日間経口投与した;各コホートの他の1人の被験者にプラセボを投与した[61]。特筆すべきは、この研究では、肝臓(トランスアミナーゼ)および甲状腺(TSH、T3,T4)機能検査を含む32種類の血液検査および化学検査に基づいて、臨床的に有意な有害事象の証拠は示されなかったことである。これに一致して、ランダム化臨床試験に参加した女性ボランティア45人から採取した血清中の甲状腺機能の生化学的パラメータの最近の分析では、40μmolのスルフォラファンと600μmolのグルコラファニンの組み合わせを含むブロッコリースプラウト飲料を12週間摂取して介入した後、ベースラインと比較して変化がないことが明らかになった[62]。
イソチオシアン酸塩と比較して、グルコシノレートの経口投与はバイオアベイラビリティが低く、排泄が遅く、排泄物の個人差が大きいという知見は、5日間のベースライン期間の後に、グルコシノレートまたはそれに対応するイソチオシアン酸塩のいずれかを含むブロッコリースプラウト飲料を7日間毎日投与し、5日間のウォッシュアウト期間を経て、反対の介入を7日間投与した大規模な(50人)クロスオーバー臨床試験によってさらに強化された[63]。24時間尿中排泄プロファイルが高い5人の被験者(「高転換者」)および排泄プロファイルが低い5人の被験者(「低転換者」)からの糞便サンプルの採取を用いて、生体外では、「高転換者」に由来する糞便細菌の培養物において、「低転換者」に比べてグルコラファニンの分解が大きいことが明らかになった[64]。これらの観察結果は、機械的洗浄や抗生物質処理が健康なヒト被験者のグルコシノレート変換を大幅に減少させることを示した以前の研究 [26] と一致しており、消化管微生物叢がグルコシノレート加水分解の程度を決定する上で重要な因子であることを示している。個人差に加えて、グルコシノレートのジチオカルバミン酸塩への変換には日内変動もあり、日中に変換が大きくなる [65]。対照的に、イソチオシアン酸塩からジチオカルバメートへの変換は夜間に高くなる。
全体的に、ヒトでは、スルフォラファンは個人差が小さく、典型的な尿中排泄量は投与量の 70-90%で、急速に吸収・排泄される。対照的に、グルコラファニンの変換は遅く、個人差が大きい。グルコラファニン含有製剤による介入後のスルフォラファン代謝物の尿中排泄量は、典型的には投与量の2%から15%の範囲であり、極端な場合は1%から45%である。スルフォラファンとグルコラファニンの個人差があることから、一見すると、スルフォラファンの使用は投与量の正確さを目的とした場合には魅力的である。しかし、安定なグルコシノレート前駆体とは対照的に、スルフォラファンは不安定であるため、α-シクロデキストリンでカプセル化されたスルフォラファン[66]や、プロスタファン®(Nutrinov, Noyal sur Vilaine Cedex, France)として知られる純粋な植物由来のスルフォラファンの安定化バージョンのような安定化製剤の開発が促されてきた。あるいは、活性ミロシナーゼを含むグルコラファニンが豊富な製剤も使用されている[67,68]。製剤のバイオアベイラビリティーが異なるため(これは、様々なヒトの研究で報告された薬物動態パラメータの違いを説明する可能性がある投与された製剤の量ではなく、尿中のスルフォラファン代謝物の排泄量が、実際の投与量のより信頼性の高い測定値を提供する[69]。
スルフォラファンの薬物動態の研究と同様に、スルフォラファンの薬物動態を扱ったほぼすべてのヒトの研究では、グルコラファニンまたはスルフォラファンを豊富に含むブロッコリーをベースとした製剤が使用されている。現在のところ、スルフォラファンがヒトにおいて特定の標的に関与していることを示す直接的な証拠はないが、スルフォラファンの薬力学的作用については明確な証拠がある。このように、アブラナ科野菜を摂取したヒトの血漿 [70] と唾液 [71] において、Nrf2 を標的とする酵素 A-class GSTs と NQO1 のレベルが上昇したことが報告されている。これと一致して、健康なボランティアへのグルコラファニン/スルフォラファニンに富んだ調製物の投与は、PBMC、皮膚パンチ生検、鼻や頬のスクレイピングと同様に、NQO1およびGSTsのmRNAまたはタンパク質レベルの増加をもたらした[72,73,74,75,76]。
ブロッコリーベースのグルコラファン/スルフォラファンを豊富に含む製剤は、発がん性の可能性のある食品汚染物質および大気汚染物質の解毒および排泄を促進することが示されており、汚染への避けられない暴露による集団全体のがんリスクの低減のための非常に魅力的な戦略を提供している。中国のQidongで実施されたヒトボランティア50人を対象としたクロスオーバー臨床試験では、スルフォラファンおよび/またはグルコラファンニンを豊富に含むブロッコリースプラウト由来の飲料を摂取した後、大気汚染物質アクロレインおよびベンゼンのグルタチオン由来の抱合体の尿中排泄レベルが20~50%の統計学的に有意に増加することが明らかになった [77]。その後、40μmolのスルフォラファンと600μmolのグルコラファニンを配合したブロッコリースプラウト飲料を用いて、同じ地域の291人の参加者を対象とした12週間のプラセボ対照無作為化臨床試験では、ベンゼンとアクロレインのグルタチオン由来の共役体の排泄レベルが、プラセボと比較して、ブロッコリースプラウト飲料を摂取したボランティアでは、それぞれ61%と23%と有意に増加したことが示され、これらの知見を確認し、拡張した[78]。最近、中国の同じ地域で実施されたブロッコリースプラウト飲料の無作為化プラセボ対照多用量介入試験では、スルフォラファンの尿中代謝物の用量依存性の排泄が示され、さらに、40μmolのスルフォラファンと600μmolのグルコラファニンを10日間毎日投与し、1日あたり約25μmolのスルフォラファン代謝物を尿中に排泄させる治療体制がベンゼンの解毒を促進することが明らかになった[69]。
前立腺癌のリスクが高い男性の前立腺における転写変化を評価するためのグローバルな遺伝子発現プロファイリングにより、ブロッコリーを多く含む食事を6ヶ月または12ヶ月間摂取すると、前立腺組織の炎症および発癌に関与するシグナル伝達経路の転写変化が生じることが明らかになった[79,80];重要なことに、これらの変化はグルコラファニンを多く含む食事を摂取した被験者では用量依存的に減衰する[80]。ヒトにおけるグルコラファニン/スルフォラファンの介入の他の薬力学的効果には以下のものがある。脳内還元型グルタチオンの増加 [81]、脂肪酸β酸化とTCAサイクル活性の統合強化 [82]、紫外線照射による皮膚紅斑の予防 [83,84]、血漿LDL-コレステロールの減少 [85]、2型糖尿病の調節障害を有する肥満患者における空腹時血糖値と糖化ヘモグロビン値の低下 [86]、自閉症スペクトラム障害を有する若年男性における社会的相互作用、行動、言語コミュニケーションの改善 [87]などが挙げられる。全体的に、正確な分子メディエーターは常に知られているわけではないが、ヒトにおけるグルコラファニン/スルフォラファンを豊富に含むブロッコリー製剤への介入が、多様な有益な効果をもたらすことは明らかである。
3.2. ブロッコリーベースの製剤を用いた臨床試験。有効性
ブロッコリーベースの製剤は、グルコラファニン、スルフォラファン、グルコラファニンに活性ミロシナーゼを加えたもの、生、調理、乾燥した野菜そのもの(ブロッコリーまたはブロッコリースプラウトまたはブロッコリーの種子やスプラウトの抽出物-グルコラファニンが豊富なもの、スルフォラファンが豊富なもの、またはその両方から構成されている。これらの研究はもちろん、すべてが単純ではなく、ブロッコリー由来の成分の測定は謎、難解化、混乱の原因となり、サプリメント業界によって容易に利用されている。それにもかかわらず、現在では多くの臨床研究が行われており、いくつかの包括的な知見が定式化され始めている。我々は、バイオアベイラビリティ、グルコラファニンのスルフォラファンへの変換、安全性、そしてこのレビューの前のセクションで議論された古典的なADME(吸収、分布、代謝、排泄)薬物動態パラメータの評価に多くの時間を費やしていた。有効性についての研究はあまり行われていないが、明らかになりつつある。特に注目されているのは以下の領域(アルファベット順)である。
3.2.1. アフラトキシン毒性
上海近郊の中国沿岸部の七東地域では、保存されている自給用の種子(トウモロコシおよびピーナッツ)からのアフラトキシンのレベルが、近年の歴史の中で非常に高く、関連する肝臓がんの発生率も高くなっている。ブロッコリースプラウトは予防的介入として試験的に成功しており、安全性と有効性[バイオマーカー]、地域住民による耐性と受容性について多くのデータが得られている[88,89]。
3.2.2. 大気汚染の無害化
七東の自然実験室では、さらにブロッコリーの噴出口が揮発性有機大気汚染物質の無害化に及ぼす影響を研究している[69,77,78,90]。他の環境では、ディーゼル排気(粒子状物質)やその他の大気汚染物質の影響を調べた研究もある[91,92]。
3.2.3. 関節炎
Healyと共同研究者による初期の研究では、軟骨細胞のせん断応力への影響が示唆されていた [93]。これは現在、ブロッコリーの摂取量を増やすことで、関節内へのイソチオシアネート(例えば、スルフォラファン)の取り込 みが促進され、それに伴って関節にも変化が生じることをエレガントに実証している[59]。スルフォラファンの抗炎症特性に関する他の多くの研究は、最終的には関節炎に関連しているかもしれない。
3.2.4. 喘息とアトピー性アレルギー反応
スルフォラファンの効果は比較的小さくても有意なものであり、多くの比較的複雑な実験系で実証されている [73,92,94,95,96,97]。
3.2.5. 癌のバイオマーカー
スルフォラファン治療後には、様々なバイオマーカーが報告されている。研究対象としている癌は以下の通りである。乳がん [55,98]、肺がん [99]、胃がん [100]、大腸・直腸がん [101]、前立腺がん [79,80,102,103]、皮膚がん [75,83,84,104]、頭頸部がん [72]、肝臓がん [90]などが研究されている。
3.2.6. COPD
スルフォラファンを豊富に含むブロッコリースプラウト抽出物を用いた90被験者3施設RCTが実施されたが、進行したCOPD患者には効果が認められなかった。事後的な推論では、被験者の気道の状態がすでに深刻に悪化しているため、使用された薬剤にかかわらず、反応性(Nrf2関連および抗炎症)が認められなかった可能性があることが示唆された[105]。追跡分析では、COPDを持つ現在および元喫煙者における抗酸化および抗炎症遺伝子発現のコンパートメンテーションがあったことが示唆されている [106]。
3.2.7. 心血管疾患
少なくとも3つの異なるグループが、生化学的マーカー[107]、血圧および流量媒介性拡張[108]、および血漿代謝物バイオマーカー[82,85]を含む効果を報告している。
3.2.8. 糖尿病、メタボリックシンドローム、および関連疾患
現在、少なくとも3つの異なるグループによる多くの臨床研究が発表されている。これらの研究では、グルコネオジェネシス [86]、炎症性マーカー [109]、インスリン抵抗性 [110,111,112]の低下に対する効果が示されている。
3.2.9. 一般
様々な研究における広範な対策により、主要な化学保護酵素のアップレギュレーションが記録されている。このレビューでは言及されていない研究をいくつか挙げると、以下の通りである。[113,114];
3.2.10. ヘリコバクター・ピロリ感染症
我々の最初の観察は、試験管内試験 および動物モデル [11] で、いくつかの感染者における H. pylori の植民地化と胃の炎症のレベルを減少させ、より重要なことに、いくつかの根絶に翻訳されている [115,116,117]。
3.2.11. NASH/NAFLD
肝機能マーカーの陽性の変化が観察されており [118] 、有望な前臨床試験に基づいて多くの関心が続いている。
3.2.12. 神経変性疾患
GSHレベルへの影響を示す小規模な研究や、特定の脳領域へのGSH上昇のマッピングは、多くの興奮を生み出している [5,81]。
3.2.13. 神経発達条件
ブロッコリースプラウトのスルフォラファンを摂取すると自閉症スペクトラム障害(ASD)の状態が改善することを示した成功した非常に目に見える研究 [87,119] が、現在、ASDの被験者を対象とした少なくとも5つの研究、2つの統合失調症と1つの精神病を対象とした研究のフォローアップが行われている。これらのフォローアップ研究のうち、これまでに発表されたのは1件のみである[120]。
3.2.14. 鎌状赤血球疾患
投与量のエスカレーションが行われた第 1 相試験は 1 回のみであるが、限られた数の疾患関連の薬力学的エンドポイントが照会され、安全性は比較的高 い計算用量で評価されている[74]。
3.3. スルフォラファン、グルコラファンまたはその混合物を用いた臨床試験の概要
表1は、ブロッコリーベースの製剤、スルフォラファンおよび/またはグルコラファニンを用いて実施された臨床試験の公表文献を要約したものである。また、ClinicalTrials.govに掲載されている、進行中であることが知られている臨床試験も含まれている。保留中の試験は含まれていない。スルフォラファンを直接投与した経口投与量は、1人1日あたり9.9~847μmol(中央値100μmolグルコラファンニンは1人1日あたり25~800μmol(中央値190μmol)であった。グルコラファニンとスルフォラファンの高用量使用の傾向は、飲料や栄養補助食品に外因性ミロシナーゼが含まれていない場合、グルコラファニンからスルフォラファンへの変換が制限されることを考慮した試験責任者の配慮を反映していると考えられる。
表 1 ブロッコリー、グルコラファニンまたはスルフォラファンを用いた臨床試験の概要
原文参照
スルフォラファンの高用量を摂取したほとんどの人が気づく、きつい味(別名、喉の奥が焼けるような感覚)は、研究者が認識し、予想していなければならない。被験者の中には、非常に不快な味だと考える人もいるかもしれないが、それを考慮しなければならない。これは、スルフォラファンの投与量の上限では特にそうであるが、グルコラファニン、あるいはグルコラファニン+ミロシナーゼの場合には、それほど気にする必要はない。グルコシノール酸-ミロシナーゼ-イソチオシアネート系を「からし油爆弾」として特徴づけたのは、この苛酷な、あるいは灼熱感である。
約100μmolを超える経口投与量のスルフォラファンの存在および/または酵素生産は、ほとんどの消費者が舌ではなく喉の奥に感じる灼熱感のある味を作り出する。このため、ブロッコリーやスルフォラファン製剤を摂取することができない人もいる。スルフォラファンの高用量投与は、主に吐き気、胸焼け、その他の胃腸の不快感などの有害事象の報告の増加につながる[44,67,87,119,122]。我々は、その非常に独特な味を隠したり、消費者の注意をそらしたりして、適切なプラセボの開発を促進するために、科学的に導かれた研究を実施していた[122,123]。
4. 今後の課題
4.1. 植物と個別の単離物との比較。食品対サプリメント
究極の公衆衛生のパラダイムとして、植物を直接食べることは、調理の有無にかかわらず、あるいは最小限の加工で、世界のほとんどの地域で解決策でなければならない。最も裕福な地域は、予防的介入としてサプリメントを買う余裕がある。化学的予防のアプローチを医薬品戦略に変えようとするのは無謀なことであるが、スルフォラファンが治療効果や治癒効果を持つことが証明されていれば、それは方向性の一つとなるだろう。予防効果を示すための臨床試験の設計・実施という観点からは、多くの課題がある。これまでにも取り上げてきたが[65,139,140]、繰り返しになるが、いくつかの問題点がある。
4.1.1. 第一
もし、究極のデリバリー・ビークルとなるのが本当に植物性食品であるならば、健康寿命の向上に成功した場合の莫大なアップサイドを共有することになるであろう食品会社は、これらの試験を実施するためのコストの一部を負担しなければならない。ビッグファーマ」(世界的には約1兆ドルの産業)の規模とロビー活動力については多くのことが語られてきたが、米国経済の食品部門だけでも、現在では約1.1兆ドルと評価されている[141]。
4.1.2. 第二
食品を用いた臨床研究では、投与量の標準化は非常に困難である。スルフォラファンが予防的なファイトケミカルとして科学的に信頼されるようになるにつれ、スルフォラファンをどのように、どのくらいの量を、どのくらいの期間、どのように投与し、どのように測定するかを決定することを目的とした臨床研究は、定義上、より大きく、より長く、より洗練されたものになっていくであろう。おそらく、ブロッコリーのような食品に品種名(例えば、リンゴに貼られているような気が遠くなるような小さなステッカー)とグルコラファニン価が表示され、消費者がヘルススパンでの購入を直接選択できるようになる時が来るだろう。一方で、ブロッコリーやブロッコリースプラウトを使って行った臨床研究は、すでに学術システムを限界点まで緊張させている[142]。食品業界はステップアップする必要がある。
我々や他の人たちは、本明細書で論じたようにスルフォラファン含有サプリメントやスルフォラファン生成サプリメントの使用に切り替えた。多くの粗悪なサプリメントと多くの不謹慎なサプリメントの供給者[143,144]があるので、しかし、市販のサプリメントの使用は危険に満ちている。堅牢な品質管理が不可欠である。したがって、より良い業界のモニタリングと規制、そしてラベルに記載された「用量」の研究者による厳密な検証が重要である。予測可能な将来において、ラベルに表示されているものが「投与量」(及び場合によっては植物体)の正確な表現であることを信頼することはできず、表 1 には、介入前又は介入中に投与量を測定するのではなく、ラベルの結果を使用した臨床研究を示している。
4.1.3. 第三
「汝の食べ物は汝の薬であり、汝の薬は汝の食べ物である」という概念に臨床医のバイインがなければならない。これは、おそらく誤って、ヒポクラテスに起因しているが、その起源に関係なく、ヒポクラテスの知的な子孫である医師は、餌を取るために立ち上がっていない。彼らは代わりに、大規模な製薬会社の餌を取っている、フックラインとシンカー、それは私たちの経済を沈めるために脅している。医薬品は、最も確かに彼らの場所を持っているが、我々は、よりしっかりと通路の食事側に少なくとも片足を配置するために、人々はまだ彼らの重要かつ予防的なケアの問題で信頼している私たちの社会の医師を募集しなければならない。
4.2. 投与量の定義の最適化
臨床化学予防試験、特に食品をベースとした試験の設計におけるいくつかの重要な課題は、介入物質の投与量、製剤、および投与スケジュールの選択である。投与スケジュールは、典型的には、1日のスケジュールの利便性と、スルフォラファンの短い生物学的半減期の知識によって決定される。他の要因はあまり限定されない。投与量の選択は、先に議論したように、グルコラファニンの前駆体として投与された場合と、スルフォラファン自体として投与された場合では、スルフォラファンのバイオアベイラビリティーが大きく異なるため、複雑なものとなる。図4は、中国のQidongで実施された4つの臨床試験の経験をまとめたもので、グルコラファン、スルフォラファン、またはその両方を濃縮したブロッコリーをベースとした介入を行ったものである。
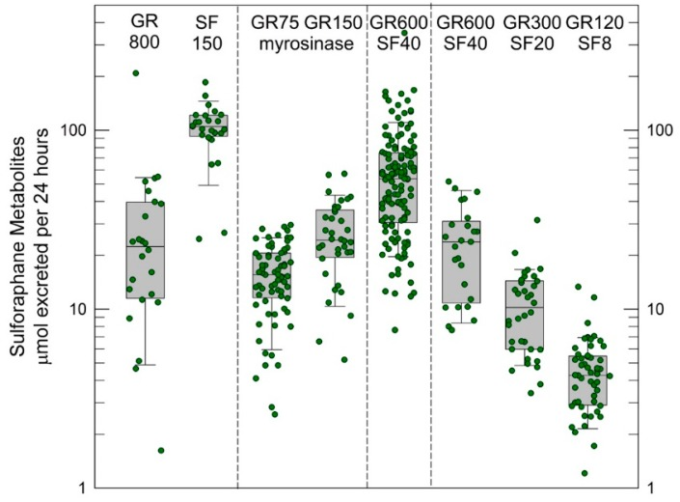
図4
中国の契東で実施された介入試験から、異なるブロッコリースプラウト製剤を初回投与した後の24時間あたりのスルフォラファン代謝物の尿中排泄物(「内服量」) [63,77,78]。分析はすべて同位体希釈質量分析法で行った。値は各参加者のスルフォラファン、スルフォラファン-システイン、およびスルフォラファン-N-アセチルシステインの合計。ボックスプロットは中央値、5%および95%信頼区間である。GR 800は、3日齢のブロッコリースプラウトの熱水抽出物を凍結乾燥し、マンゴージュースと水で再構成して800μmoleのグルコラファニン(GR)を含有する飲料であり、SF 150は、熱水抽出物を室温に冷却し、大根で処理してミロシナーゼを含有するようにした後、凍結乾燥し、マンゴージュースと水で再構成して150μmolのスルフォラファン(SF)を含有するようにした飲料であった。GR600 + SF 40は、凍結乾燥した粉末をパイナップルジュース、ライムジュース、水で再構成した飲料で、600μmolのGRと40μmolのSFを提供した。飲料に加えて、ミロシナーゼの存在下でグルコラファニン(75および150μmol)を提供するために、凍結乾燥したブロッコリースプラウトと細かく粉砕したブロッコリーの種子から構成される錠剤として配合された市販の栄養補助食品を用いた研究が実施された。
クロスオーバーデザイン研究では、排泄されたスルフォラファン代謝物(主にスルフォラファン-N-アセチルシステイン)の回収率は、グルコラファニンを豊富に含む飲料を投与した場合には約5%であり、1から45%の範囲であったが、スルフォラファンを豊富に含む飲料を使用した場合には約70%であり、個人間のばらつきはかなり狭い範囲であった[68]。このように、バイオアベイラビリティは、原料物質-前駆体または生理活性物質の機能として劇的に変化する。その後のいくつかの研究では、スルフォラファンとグルコラファニンを豊富に含む調合物のブレンドを使用してバイオアベイラビリティーと忍容性を改善し、用量反応関係を検討した[69,78]。摂取量の増加は達成されたが、個人間変動への影響はほとんどなかった。ブロッコリースプラウト抽出物の調製方法(例えば、グルコラファニンの外因性ミロシナーゼ触媒による加水分解の有無など)を反映した製剤は、バイオアベイラビリティに強く影響する。錠剤形態のグルコラファニンとミロシナーゼ(Avmacol®)の栄養補助食品製剤を使用して、個人間のばらつきを大幅に抑制した中央値20%のバイオアベイラビリティを観察した。Faheyら[67]は、異なる集団において、このサプリメントで約35%のバイオアベイラビリティを観察している。このように、グルコラファニン及び/又はスルフォラファンの投与量の報告は、スルフォラファンのバイオアベイラ ビオアベイラビリティ/バイオアクティブ量を測るには不十分である。その結果、スルフォラファン代謝物(スルフォラファン+スルフォラファンシステイン-グリシン+スルフォラファンシステイン+スルフォラファンN-アセチルシステイン)の24時間(2-3半減期)の尿中排泄量を「内服量」の指標とすることで、被験者へのスルフォラファンの投与量をより明確にし、一貫性を持たせることができると考えられる。内部投与量」の指標を用いることで、製剤、投与量、スケジュールと有効性の決定因子との関連性を最適化するこ とが容易になり、重要なことは、異なる臨床試験間での結果の比較をより簡単に行うことができるようになるであろう。
4.3. 動物試験と臨床試験の統合
疫学研究では、アブラナ、より具体的にはブロッコリーの摂取と疾病リスクの軽減との間に有益な関連性があることが強く示唆されている。しかし、ブロッコリー、ブロッコリースプラウト、由来成分、またはスルフォラファンそのものを用いた臨床試験を実施することが必要であることを示す強固な基盤を提供してきたのは、動物実験である。補足表S1-S4にまとめられているように、マウスやラットを用いた疾患の予防や治療におけるスルフォラファンの役割についての研究は多岐にわたっているが、動物実験ではすべての情報が得られているわけではない。
しかし、動物を用いた研究では、期待されるような結果は得られていない。図5に示されたデータから明らかなように、前臨床試験では、投与量(または投与経路)の選択とその臨床的有用性との関連性について慎重に検討されていないことがわかる。マウスやラットの経口投与を例にとると、動物実験の 3 分の 2 以上は、齧歯類とヒトとの間の等比スケーリングを考慮した後でも、ヒトで使用されているスルフォラファンの最高用量を超える用量を使用している。このように、マウスでの投与量が 4対数以上に広がっているのは、トランスレーショナルサイエンスの最適化というよりも、出版物での効果報告の必要性に起因しているように思われる。このレビューの著者は、多くの研究者の中で、この用量の偏りに貢献している。
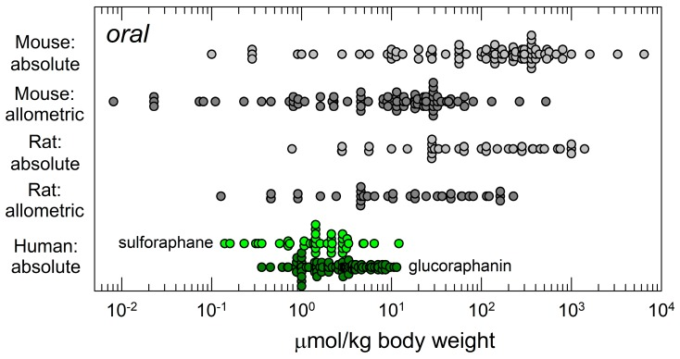
図5
公表されているマウスまたはラットに投与したスルフォラファンの経口投与量と、ヒトに投与したスルフォラファン(錠剤またはスルフォラファンに富むブロッコリー製剤)またはグルコラファニンに富むブロッコリー製剤の比較。マウス投与量の補正係数は 0.081,ラット投与量の補正係数は 0.162 を用いた [145]。ヒトの投与量は、各研究における体重 70 kg の推定値に基づいている。
ブロッコリーベースの製剤を用いた臨床試験の初期用量はどのように選定されたのか?ヒトにおける最初の研究が実施されたときにはすでに豊富にあった動物試験からは選択されていない。また、血漿中のピークレベル、半減期、代謝運命、スルフォラファンの組織内分布を定義するための齧歯類を用いた薬理学的研究からも選ばれていない。むしろ、Talalayらによる初期の慎重な定量的用量エスカレーション薬物動態研究[26,60,61]の後、臨床試験者は、薬力学的作用を特定するために、単純に濃縮された製剤の苦味を隠そうとすることによって、用量を忍容性の極限まで押し上げようとしたのである。これは、一貫して製剤化された安定で生物学的に利用可能なブロッコリー由来の製剤が開発されたことによって可能になった結果である。動物試験とヒト試験の間の断絶は、公衆衛生上の理由から、ブロッコリー由来の製剤を用いた最初のヒト試験を実施したいという願望(と規制上の必要性)があったために悪化していた。凍結乾燥させたブロッコリーや粉末ブロッコリーエキスを動物に与えることは、食事中に高いパーセンテージを必要とするため、全体的な栄養摂取量に影響を与える可能性があるため、好まれていなかったようである。現在、安定化スルフォラファンを用いた製剤が臨床使用されるようになったことで、製剤のギャップを埋めることができ、用量反応をより定量的に把握することができるようになるかもしれない[20,102]。いずれにしても、実験家は、ヒトで達成可能で忍容性のある用量とスケジュールの同等性を用いて、腹腔内ではなく経口投与で有効性とその基礎となるメカニズムを検討することに注意を払わなければならない。この考え方は、ヒトでも動物細胞株でも、試験管内試験 試験では、ヒト組織で達成可能なレベルをはるかに超えた濃度のスルフォラファンをピークレベルとして使用していることが多く、また、生体内での生物学的半減期が短く、曝露の持続時間がすぐに減衰することを考慮していないことが多い。
4.4. より良い有効性のバイオマーカー
現在、臨床試験で使用されているブロッコリーをベースとした製剤の薬物動態を最適化するための調達や製剤の改良には大きな進展があったが、それにもかかわらず、多くの臨床試験参加者に見られる薬物動態の個人間の大きなばらつきの一因となっている要因についての情報は限られていた。宿主因子(遺伝的多型やエピジェネティクス)や宿主-マイクロバイオーム相互作用がこのばらつきに重要な役割を果たしている可能性が高い。さらに、薬力学的作用の厳密なバイオマーカーを開発する必要がある。介入を最適化し、最も効果を発揮する可能性のある健康なグループやリスクの高いグループを特定するためには、前臨床試験で明らかにされた作用機序と臨床効果の機能的評価との間のより良い関連性が必要である。ブロッコリー、グルコラファニンを豊富に含むブロッコリー飲料、粉末、栄養補助食品、スルフォラファンの安定化製剤などの臨床研究に関する50以上の論文が発表されており、病気の予防や緩和への応用は今後も進化を続けていくことが期待される。ClinicalTrials.govには50件以上の臨床試験が追加掲載されており、このような期待を裏付けるものとなっている。ブロッコリーをベースとした戦略を用いた健康増進のために、既存の知見や新たな知見を迅速に展開するための指針となるためには、短期的な薬力学的作用のマーカー(おそらくはオミクスプラットフォームがサポートしている)が必要である。
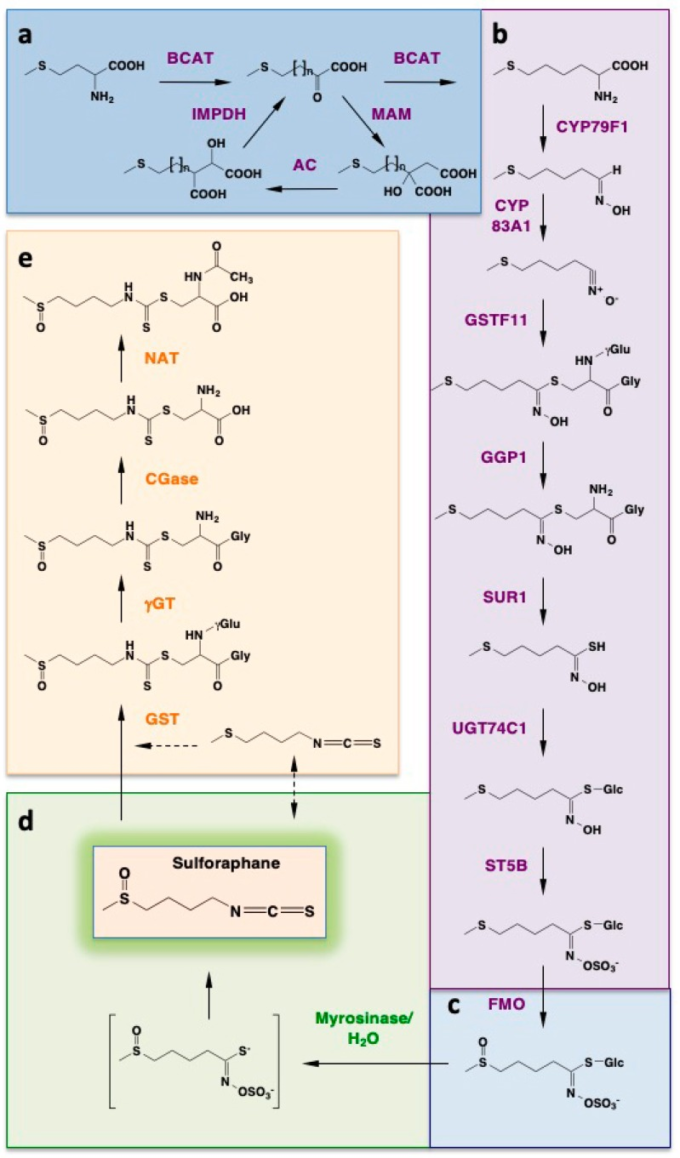
スキーム1
グルコラファニンの生合成、加水分解してイソチオシアン酸スルフォラファンを形成し、スルフォラファンの代謝を行っている。反応性の高いイソチオシアン酸スルフォラファンは、植物では不活性前駆体であるグルコシノール酸グルコラファニンとして生産される。その生合成経路はアミノ酸メチオニンに由来し、以下の3つの段階で進行する。(i)2つのメチレン基によるメチオニン側鎖の伸長(a)、(ii)コアとなるグルコシノレート構造の形成(b)、(iii)グルコシノレート側鎖の二次修飾(c)である。植物組織の完全性が破壊されると、グルコラファニンはミロシナーゼと接触し、これがグルコラファニンの加水分解を触媒してスルフォラファンを与える(d);哺乳類細胞では、スルフォラファンはメルカプトウリン酸経路を介して代謝され、また、エルシンへの相互変換を受けることができる(e)。