Contents
Anticholinergic Drug Exposure and the Risk of Dementia
A Nested Case-Control Study
jamanetwork.com/journals/jamainternalmedicine/fullarticle/2736353
キーポイント
質問
55歳以上の人の認知症リスクは、さまざまな抗コリン薬の使用と関連しているか?
所見
認知症と診断された患者58,769人と対照群225,574人を対象としたネステッド症例対照研究では、交絡変数を調整した後、抗コリン性抗うつ薬、抗パーキンソン薬、抗精神病薬、抗ムスカリン薬、抗てんかん薬への曝露と認知症リスクとの間に統計学的に有意な関連が認められた。
意味
特定のタイプの抗コリン薬について観察された関連性は,中高年においてはこれらの薬剤を慎重に処方すべきであることを示唆している.
要旨
重要性
抗コリン薬は短期的な認知副作用を有するが、長期的な使用が認知症リスクの増加と関連しているかどうかは不明である。
目的
55歳以上の人の抗コリン薬治療と認知症リスクとの関連を評価する。
デザイン、設定、および参加者
この入れ子になった症例対照研究は、QResearchのプライマリケアデータベースに登録されているイギリスの一般診療所で行われた。この研究では、認知症と診断された患者58,769人と55歳以上の対照者225,574人を対象に、抗コリン薬への曝露が認知症リスクと関連しているかどうかを、年齢、性別、一般診療所、暦でマッチさせて評価した。抗コリン作用の強い56剤の処方情報を用いて、抗コリン薬の累積曝露量の尺度を算出した。データは2016年5月から 2018年6月まで分析した。
曝露
主要曝露は、マッチドコントロールにおける認知症の診断日またはそれに相当する日(指標日)の1~11年前の1年間に処方された抗コリン薬の総標準化1日量(TSDD)であった。
主要評価項目
抗コリン薬への累積曝露に関連する認知症のオッズ比(OR交絡変数を調整。
結果
全集団(284343例の症例と対照群)のうち、179 365例(63.1%)が女性であり、全集団の平均年齢(SD)は82.2歳(6.8歳)であった。認知症の修正ORは、指標日以前の1~11年間に抗コリン薬の処方がなかった場合と比較して、全体の抗コリン薬曝露量が最も低いカテゴリー(総曝露量1~90 TSDDs)では1.06(95%CI、1.03~1.09)から、最も高いカテゴリー(1095 TSDDs以上)では1.49(95%CI、1.44~1.54)に増加した。抗コリン性抗うつ薬(調整後OR[AOR]、1.29;95%CI、1.24~1.34抗パーキンソン薬(AOR、1.52;95%CI、1.16~2.00抗精神病薬(AOR、1.16~2.00)では、認知症リスクの有意な増加が認められた。 00抗精神病薬(AOR、1.70;95%CI、1.53-1.90膀胱抗ムスカリン薬(AOR、1.65;95%CI、1.56-1.75および抗てんかん薬(AOR、1.39;95%CI、1.22-1.57)のすべてが1095件以上のTSDDであった。TSDDが1095例以上の場合、曝露を指標日より前の3~13年(AOR、1.46;95%CI、1.41-1.52)および5~20年(AOR、1.44;95%CI、1.32-1.57)に限定した場合でも、結果は同様であった。関連性は、80歳以前に診断された症例でより強かった。診断前1~11年間の総抗コリン薬曝露に関連する集団帰属率は10.3%であった。
結論と関連性
数種類の強力な抗コリン薬への曝露は認知症リスクの増加と関連している。これらの知見は、中高年における抗コリン薬への曝露を減らすことの重要性を強調している。
序論
2 高血圧、難聴、うつ病、糖尿病、喫煙などの修正可能な危険因子が認知症の約35%を占めている。抗コリン薬は、中枢神経系および末梢神経系の神経伝達物質であるアセチルコリンを阻害することで作用する幅広い薬剤群で、一部の抗ヒスタミン薬、抗うつ薬、胃腸障害や膀胱障害の治療薬などが含まれる。これらの薬剤は、高齢者では錯乱や記憶力低下などの短期的な副作用を示すことがある3-6が、長期使用により認知症のリスクが高まるかどうかについては、あまり明らかにされていない。
抗コリン薬と認知症リスクに関する観察研究7-10は、一般的に比較的小規模で、短期的な曝露しか評価されていないか、リコールバイアスの影響を受けている。また、これらの研究では、診断前の認知症の初期症状を治療するために抗コリン薬が処方されていることを考慮していないため、プロトパシーバイアスの影響を受けやすい。コホート研究11では、追跡調査の最終年に処方されたものを除外することで原病的バイアスを軽減したが、抗コリン薬の累積使用量が多いほど認知症のリスクが有意に増加することがわかったが、抗コリン薬の別のタイプの分析には限界があった。最近の大規模な研究12では、抗コリン薬の種類によってリスクに差があることが明らかになり、さらなる研究では個々の抗コリン薬のクラスを検討すべきであると結論づけられた。
本研究は、英国の代表的な大規模集団における抗コリン薬の累積使用と認知症リスクとの関連を評価することを目的とした。本研究の目的は、診断前20年までの処方箋の分析を含め、さまざまな種類の抗コリン薬と認知症リスクを推定することであった。
研究方法
スタディデザイン
これは、QResearchデータベース(バージョン41)に登録されている英国の診療所に登録されている患者のコホートを対象とした、入れ子になった症例対照研究である。QResearchは、1500以上の一般診療所の3,000万人以上の個人を対象とした匿名化された研究データベースで、日常的なヘルスケアからプロスペクティブに記録されたデータが含まれている。データには、人口統計学的情報、医学的診断、処方、紹介、検査結果、臨床値などが含まれている。
本研究は、East Midlands Derby研究倫理委員会との合意された手順に従って承認され、同定されていない患者データについては書面によるインフォームドコンセントを放棄している。
症例と対照の選択
ベースコホートは、研究期間中(2004年1月1日から 2016年1月31日まで)に登録された55歳以上の患者で、研究開始日(2004年1月1日患者の55歳の誕生日、診療所に登録した日+1年、診療所のコンピュータシステムを導入した日+1年と定義し、研究開始時に認知症の診断を受けていないものを対象とした。コホートは、死亡、他の診療所への転院、または研究終了日(2016年1月31日)のうち最も早い日まで追跡調査を行った。
症例患者は、追跡調査中に認知症と診断された患者で、診療記録に記録された臨床コード、または国家統計局の死亡記録にリンクされた臨床コードを用いて同定されたものとした。アセチルコリンエステラーゼ阻害薬(ドネペジル、ガランタミン、メマンチン、リバスチグミン)が処方されているが、認知症の診断が記録されていない患者も対象とした。ハンチントン病、パーキンソン病、クロイツフェルト・ヤコブ病、ヒト免疫不全ウイルス(HIV)に関連する特定のサブタイプの認知症の診断コードを持つ症例は、適応の偏りを減らすためにパーキンソン病、ハンチントン病、多発性硬化症と診断された患者と同様に除外した。
各症例患者は、発生密度サンプリングを用いて、年齢(1年以内性別、一般診療、暦年ごとに5人の対照群とマッチングされた13 。対照群は、パーキンソン病、ハンチントン病、または多発性硬化症の診断を受けていた場合は除外された。
一次解析では、抗コリン薬曝露を10年間の全期間(指標日の前の1年間を除く)にわたって評価できるように、症例患者および対照群は、指標日の前に少なくとも11年間の記録データを持っていた場合にのみ含まれた。
エクスポージャー
どの薬剤が抗コリン作用を有すると考えられるかについては、不完全なコンセンサスがある。我々は、米国老年医学会2012年ビアス基準アップデート専門家パネルによって強い抗コリン作用を有すると同定された薬剤を含めたGrayら11のアプローチを用いた14。また、Beers 2015年に更新された強力な抗コリン作用を有する薬剤のリスト15,抗コリン性認知負荷尺度で高い抗コリン作用を有すると記載されている薬剤16,またはシステマティックレビューで高い抗コリン作用を有すると同定されている薬剤17,さらに英国のナショナルフォーミュラーリーで実質的な抗コリン作用を有すると同定されている薬剤を追加した。補足資料の表1には、本研究に含まれている56種類の抗コリン作用を有する薬剤と、それらの薬剤が含まれている根拠の詳細が示されている。
また、本研究に含まれる抗コリン薬の処方の詳細を抽出した。原発性バイアスを減らすために、指標日の前の年に発行された処方箋は含まなかった。2つの追加分析では、診断の3年前までおよび5年前までに発行された処方箋のみを含めた。
主な曝露変数は抗コリン薬の累積曝露量であり、Gray er al)。11 が用いた方法に基づき、異なるタイプの抗コリン薬を組み合わせたものである。次に、これらの値を高齢者での使用が推奨されている最小有効1日量値で割って、各処方箋の標準化された1日量を求めた。我々は、入手可能な場合には『老年者用服用ハンドブック』18 の最小有効用量値を使用し、追加の薬剤については、英国国立処方箋に記載されている最低推奨用量値(記載されている場合には高齢者での)を使用した(補足のe表1を参照)。これらの標準化された値を、関心のある曝露時間帯に処方されたすべての抗コリン剤について合計し、各患者の1日の総標準化用量(TSDD)を求めた。
また、抗コリン薬の主要な適応(抗ヒスタミン薬、抗うつ薬、抗痙攣薬、抗パーキンソン薬、抗精神病薬、膀胱筋弛緩薬、骨格筋弛緩薬、消化管鎮痙薬、抗不整脈薬、抗てんかん薬、抗ムスカリン性気管支拡張薬)に基づいて、各タイプの抗コリン薬のTSDDを算出した。感度分析として、我々は、処方された用量を標準化するために、世界保健機関(WHO)が定義した1日用量(DDD)値(https://www.whocc.no/atc_ddd_index/)を使用した。
交絡変数
認知症や抗コリン薬使用の適応症の危険因子として同定された19-25の交絡変数としては、体重をキログラムで割った身長をメートル二乗で計算したボディマス指数、20 喫煙状況、26 アルコール消費量、27 タウンゼント剥奪スコア、21 自己申告民族グループ、28 併存疾患(冠動脈性心疾患、心房細動、心不全、高血圧)などがあると考えられる。高脂血症、糖尿病、脳卒中、くも膜下出血、一過性脳虚血発作、腎不全、喘息、慢性閉塞性肺疾患、不安、双極性障害、うつ病、ダウン症、重度の学習障害。統合失調症、重度の頭部損傷、認知機能の低下/記憶喪失および他の薬物の使用(降圧剤、アスピリン、催眠剤および抗不安剤、非ステロイド性抗炎症剤、スタチン)。これらの変数は、一次分析のための暴露ウィンドウの開始時に評価した。
統計的分析
交絡変数を調整したオッズ比(OR)を推定するために条件付きロジスティック回帰を用いた。主要解析における曝露窓は、指標日の1年前から11年前までを対象とした。我々は抗コリン薬曝露変数を5つのカテゴリー(0,1-90,91-365,366-1095,および1095以上のTSDD)に分類した11。データは2016年5月から 2018年6月まで分析した。
アルツハイマー病(混合型を含む血管性認知症、その他または特定できないタイプの認知症と診断された症例と、それぞれのマッチした対照群との間で、指標日の年齢別(80歳未満および80歳以上性別、および個別にサブグループ分析と相互作用検定を行った。
感度解析は以下のように行った。
(1)指標日の3年前から13年前までの3年間に処方されたものを除外して、指標日の3年前から13年前までの抗コリン作用曝露を評価した。
(2) 我々は、潜在的な原形質的バイアスをさらに低減し、より長期の曝露に関する関連性を評価するために、指標日の5~20年前の時間枠で抗コリン作用への曝露を評価した。
(3) 我々は、関連を直接比較できるように、Grayら11によって含まれていない抗コリン薬を削除した。
(4) 我々は、ボディマス指数、喫煙状況、およびアルコール消費量の欠落値を置き換えるために、連鎖方程式による多重入力を使用した。我々は、10個の多重インputedデータセットを作成し、Rubin規則29を用いて結果を結合した;および
(5)では、WHOのDDD値で標準化された累積曝露変数を用いて解析を繰り返した。
我々は、調整オッズ比(AOR)と抗コリン薬曝露の異なるカテゴリーにおける症例の割合を組み合わせることにより、集団帰属分率を算出した30,31 。すべての解析にStata(バージョン15.1)を使用した。
結果
ベースコホートは55歳から100歳までの3,638,582人である。20005,739人年の追跡調査期間中に128,517人が認知症と診断された。除外基準を適用した後、症例患者58,769人と対照群225,574人を対象とした(補足資料の図1)。症例患者の平均年齢(SD)は82.4歳(7.0歳)であり、63.1%(37 105人)が女性であった(表1);本補足の表2では、認知症の種類が記録されている36 666例のうち、アルツハイマー病(混合型を含む)と診断された患者は22 034人(60.1%血管性認知症と診断された患者は13 313人(36.3%その他の認知症と診断された患者は1319人(3.6%)であった。
併存疾患と処方された薬の情報を表2に示した。すべての併存疾患と処方された薬について、有病率は対照群よりも症例群の方がわずかに高かった。
抗コリン薬曝露
指標日以前の1~11年間に、少なくとも1種類の抗コリン薬が処方されていたのは、症例患者56.6%(33 253対照群51.0%(115 096)であり、中央値は症例患者で6種類、対照群で4種類であった(表3)。最も多く処方された抗コリン薬の種類は、抗うつ薬(症例27.1%、対照群23.3%抗眩暈・制吐薬(症例23.8%、対照群21.7%膀胱抗ムスカリン薬(症例11.7%、対照群8.3%)であった(補足資料のe図2参照)。本資料のe表3は、本研究に含まれる56種類の抗コリン薬についての記述情報であり、本資料のe表4とe表5は、それぞれ指標日以前の3年から13年、5年から 20年に処方された抗コリン薬についての記述情報である。
認知症との関連
指標日以前の1~11年の累計抗コリン性累積曝露に関連するAORは、非使用時と比較して、1~90TDDでは1.06(95%CI、1.03~1.09)から1095TDD以上では1.49(95%CI、1.44~1.54)へと増加した(表4)。結果は同様であったが、指標日より前の3~13年および5~20年に限定した場合のORはわずかに低かった;例えば、指標日より前の5~20年では、1095 TSDD以上でAORは1.44(95%CI、1.32~1.57)であった(表4)。
特定の種類の抗コリン薬の中では、抗うつ薬、抗パーキンソン薬、抗精神病薬、膀胱内抗ムスカリン薬、抗てんかん薬の使用に関連したリスクの有意な増加がみられた(表5)。最高曝露カテゴリー(>1095 TSDD)における調整オッズ比は、抗うつ薬で1.29(95%CI、1.24-1.34抗パーキンソン薬で1.52(95%CI、1.16-2.00抗てんかん薬で1.70(95%CI、1.16-2.00)であった。 抗精神病薬では1.70(95%CI、1.53~1.90膀胱抗ムスカリン薬では1.65(95%CI、1.56~1.75抗てんかん薬では1.39(95%CI、1.22~1.57)であり、いずれも不使用と比較した。抗てんかん薬/制吐薬については、表 5 に詳述したように、366~1095 の TSDD に関連するリスクの有意な増加が認められたが、最高曝露カテゴリーでは認められなかった。抗ヒスタミン薬、骨格筋弛緩薬、消化管鎮痙薬、抗不整脈薬、または抗ムスカリン性気管支拡張薬に関連したリスクの有意な増加はなかったが、骨格筋弛緩薬と抗不整脈薬では曝露された患者数は少なかった。リスクのパターンは、3~13年および5~20年の曝露期間では、5~20年の曝露期間では統計的に有意なリスクの増加は認められなかった抗精神病薬を除き、3~13年および5~20年の曝露期間でも同様であった(補足資料のe表6);1095例以上のTSDDの曝露におけるAORは1.23(95%CI,0.93~1.62)であった。一部の薬剤については、数が少なすぎて、指標日より前の5~20年を対象とした解析ができなかった(補足資料のe表7)。
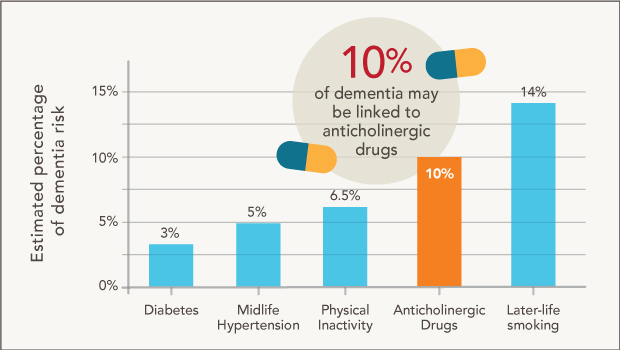
診断前1~11年の総抗コリン薬曝露に関連した集団帰属率は10.3%であった。診断前3~13年では9.0%、診断前5~20年では9.7%であった。
追加分析
80歳以前に診断された症例では、総薬剤曝露量、抗うつ薬、抗精神病薬、膀胱用抗ムスカリン薬のいずれにおいても、80歳以上の場合よりも強い関連性が認められた(補足資料のe表8)。総累積曝露量については、80歳以前に診断された1095例以上のTSDDのAORは1.81(95%CI、1.71-1.91)であったのに対し、80歳以上で診断された症例では1.35(95%CI、1.30-1.40)であった。関連性は男女で同様であった(補足のe表9)。
調整後オッズ比は一般に血管性認知症の方がアルツハイマー病よりも高かった(補足のe表10);例えば、1年から11年の曝露期間において、1095例以上のTDDのAORは血管性認知症で1.68(95%CI、1.57-1.79アルツハイマー病では1.37(95%CI、1.30-1.44)であった。
累積曝露量の算出にDDD値を使用した場合も結果は同様であった(補足資料のe表12)。多重被曝データを用いた感度解析(本補足のe表13)や、Grayら11による研究に含まれる抗コリン剤に限定した感度解析(本補足のe表14)では、研究結果に変化はなかった。
考察
この大規模なネステッド症例対照研究では、抗コリン薬の使用に関連して認知症のリスクが増加していることが明らかになった。抗コリン性の抗うつ薬、膀胱内抗ムスカリン薬、抗精神病薬、抗てんかん薬との関連性が最も強く、80歳以前と診断された症例でも関連性が認められた。また、80歳以前と診断された症例や、アルツハイマー病ではなく血管性認知症と診断された症例でも関連性が強かった。抗ヒスタミン薬、消化管鎮痙薬、抗ムスカリン性気管支拡張薬、抗不整脈薬、骨格筋弛緩薬については、骨格筋弛緩薬と抗不整脈薬を処方された患者数が少なく、不正確な推定値が得られたが、有意なリスク増加は認められなかった。
これは、高齢者に推奨されている最低有効量の強力な抗コリン薬1剤を3年間毎日使用したことに相当する。この観察研究では、関連性は示されているが、因果関係を評価することはできない。しかし、もしこの関連性が因果関係にあるとすれば、母集団帰属分率を見ると、認知症診断の約10%が抗コリン薬の服用に起因していることになり、例えば、英国で年間209,600人の認知症患者のうち約20,000人に相当する32。
血管性認知症が他のタイプの認知症よりも顕著に関連しているという知見は新しいものである。また、抗コリン薬が認知症のリスクを高めるメカニズムについても疑問を投げかけている。これには、血管や炎症性の変化33,34や慢性的なコリン作動性物質の枯渇というより明らかなメカニズムが含まれている可能性がある。抗コリン薬の潜在的な効果の根底にあるメカニズムは、アセチルコリンをブロックしてアルツハイマー病の過剰症を引き起こすだけではないかもしれないので、今後の研究ではその可能性のあるメカニズムを考慮する必要がある。
認知症と診断された患者と対照群の大規模な代表サンプルを対象とした。対象となる患者と対照者はすべて対象としたため、無反応による選択バイアスはなく、また、データはプロスペクティブに記録されているため、リコールバイアスの影響を受けない。処方に関する包括的なデータがあるため、処方された量と用量を考慮した総抗コリン薬曝露量の指標を導き出すことができた。
我々の知見は、3434人の参加者を対象とした米国のコホート研究11を含む他の研究と一致しており、最も高い曝露カテゴリー(1095 TSDD以上)のハザード比は1.54(95%CI、1.21-1.96)であり、我々のAORは1.49(95%CI、1.44-1.54)とほぼ同じであった。サンプルサイズが大きければ、特定のタイプの抗コリン薬を調べ、より広範な交絡因子を説明することも可能である。英国の別のプライマリケアデータベース(CPRD)を用いたRichardsonら12の研究では、含まれる薬剤、使用された曝露手段、曝露窓、交絡変数にいくつかの違いがあるにもかかわらず、我々と同様の結果が報告されている。例えば、我々は、米国老年医学会2012年Beers Criteria Update Expert Panelによって強い抗コリン作用を持つと同定された薬剤をベースにした薬剤を使用している14。これらの違いにもかかわらず、Richardsonら12は、抗うつ薬、泌尿器科薬、抗パーキンソン薬のグループでは認知症リスクが増加し、胃腸薬や抗ヒスタミン薬では関連性がないことを示している。これら3つの研究で得られた知見の一貫性は、異なる研究デザイン、国、設定の中での関連性の信頼性と頑健性を示す強力な証拠となっている。しかしながら、交絡因子の残留の可能性が残っており、認知症の非常に初期の前臨床症状に対する治療から生じる原病的影響を完全に排除することは不可能である。
限界
限界は、一部の患者が処方された薬を服用していなかったり、処方された用量を服用していなかったりして、曝露の誤分類につながる可能性があることである。この誤分類は、もし非分化的であれば、ORを減少させる傾向があり、抗ヒスタミン薬と抗ベルチゴ薬の最も高い曝露カテゴリーとの関連性の欠如を説明することができるかもしれない。我々の認知症患者の同定は、研究集団全体のスクリーニングではなく、記録された診断やアセチルコリンエステラーゼ阻害薬による治療に基づいている。これは、認知症の症例数が少ないことを意味し、対照者の中には診断されていない認知症があるかもしれないことを意味し、薬物曝露との関連を過小評価する傾向がある。
本解析では交絡変数の可能性を幅広く考慮したが、観察研究では交絡変数の残留や適応症のバイアスの可能性がある。我々は、感度解析において診断前1年および診断前3年および5年の処方を除外することにより、原疾患バイアスを低減するように努めた。主解析で特定の薬物群について同定されたリスクの増加は、抗精神病薬との関連を除き、これらの感度解析においても残存していたが、診断前5年の処方を除外した場合には有意ではなく、この関連は原形質バイアスに起因する可能性が示唆された。なぜなら、症状の発症から認知症診断までの期間は平均1~5年であるが、認知機能の低下やうつ病のような初期症状は診断の10年前までに出現する可能性があるからである39,40 。
結論
本研究では、強力な抗コリン薬、特に抗うつ薬、膀胱抗ムスカリン薬、抗パーキンソン薬、てんかん薬に関連する潜在的なリスクについてのさらなる証拠が追加されている。また、可能であれば、他の抗うつ薬やうつ病に対する非薬物療法、代替抗パーキンソン薬、過活動膀胱に対する膀胱トレーニングやミラベグロンなどの代替治療を検討すべきである42,43。
