Aetiology and treatment of nightmare disorder: State of the art and future perspectives
概要
このコンセンサス・ペーパーは、悪夢障害の病因と治療に関する研究の現状を概観し、これらの問題に関するさらなる展望を概説するものである。悪夢と悪夢障害の定義、疫学的知見、そしてトラウマを持つ人と持たない人の悪夢の病因に関する既存のモデルを説明している。
慢性的な悪夢は、過覚醒の亢進と恐怖消去の障害の相互作用によって発症する。この相互作用は、トラウマ体験、幼少期の逆境、形質的な感受性によって誘発され、また、思考抑制の亢進や睡眠呼吸障害の可能性によって促進されると考えられる。
そのため、悪夢の治療は、悪夢の意味、悪夢の慢性的な繰り返し、不適応な信念などに焦点を当てて行われる。臨床的には、悪夢障害に関する医療従事者の知識と、医療システムにおけるエビデンスに基づく介入の提供について議論した。
これらの知見をもとに,悪夢の治療法や悪夢の病因に関する研究の今後の展望と発展の可能性について述べた。
キーワード
不安、エビデンスに基づく医療、曝露、イメージ(心理療法)悪夢の脚本、傍睡眠、心的外傷後ストレス障害、PTSD、睡眠障害
1. 序論
悪夢障害は、社会的、職業的、またはその他の重要な機能領域において、臨床的に有意な苦痛または障害をもたらす悪夢が繰り返し起こることによって定義される。精神疾患の診断と統計マニュアルの第5版(DSM-5)米国精神医学会(APA)2013,睡眠障害国際分類の第3版(ICSD-3)米国睡眠学会(AASM)2014)。
ICSD-3(AASM 2014)とDSM-5(APA 2013)はともに、悪夢を「生存、安全、または身体的完全性に対する脅威を回避する努力を通常伴う」「延長された、極めて不快な」夢と定義している。悪夢は通常、レム睡眠中に発生し(Nielsen, 2000; APA, 2013, しかし、Solms, 2000を参照)発汗や息切れなどの身体的覚醒症状や、急速眼球運動(REM)睡眠中の周期性脚運動の指標がより上昇することと関連している(Germain & Nielsen, 2003)。有用な感情は恐怖であるが、怒り、恥、悲しみなどの他の感情が生じることもある(Köthe & Pietrowsky, 2001; Robert & Zadra, 2014, ただし、Phelps er al)。2018を参照)。これらの生理的な症状や感情は、夢を見ている間にも、不穏な夢から目覚めたときにも、後に夢の経験を思い出したときにも生じる。心的外傷後の悪夢と特発性の悪夢を区別することができる。心的外傷後の悪夢は、心的外傷後の出来事を直接再現するか、心的外傷に関連する感情や内容を象徴的に含んでいる。特発性悪夢は、より想像力に富んだストーリーを描いており、必ずしも外傷性イベントを反映しているわけではない。心的外傷後の悪夢は、特発性悪夢と比較して、より重度の覚醒、より多くの夜間覚醒、より強い攻撃性、より上昇した無力感をもたらす(Wittmann & De Dassel, 2015)。
夢が悪夢とみなされるために、夢主が異形の夢から覚醒する必要があるかどうかについては、現在も議論が続いている(Robert & Zadra, 2014)。以前のDSM診断マニュアル(DSM-IV、米国精神医学会(APA)1994)では、「拡張した非常に恐ろしい夢の詳細な記憶を伴う大睡眠期または昼寝からの繰り返しの覚醒[…]」と記述されていたが、より最近のDSM-5(APA 2013)では、この基準Aを以下のように定式化している。”拡張した、極めて不愉快な、よく覚えている夢の反復発生[…]”(p.404)。このように、DSM-5によれば、悪夢はしばしば覚醒につながるが、覚醒は悪夢障害の必要な診断基準ではない。頻度の基準はないが、DSM-5では、軽度の悪夢障害は平均して週に1回以下のエピソード、中等度の障害は週に1回以上のエピソードだが毎晩ではないエピソード、重度の障害は毎晩のエピソードとされている。急性エピソードは持続期間が1ヶ月以下、亜急性エピソードは持続期間が1ヶ月以上6ヶ月以下、慢性悪夢は持続期間が6ヶ月以上とされている(APA, 2013)。
夜驚症は、混乱した覚醒、不完全な覚醒、慰められないなどの症状を示するが、悪夢障害と診断された人は、完全に覚醒し、すぐに方向転換し、夢を鮮明に覚えている。また、悪夢は、ナルコレプシーによく見られる睡眠麻痺や睡眠時発症幻覚、睡眠時発症幻覚と誤認されることが多いであるが、睡眠麻痺型の悪夢も認められている(APA, 2013)。
上記のノソロジーにもかかわらず、実際には慢性悪夢障害と診断されることは稀である。なぜなら、慢性悪夢がしばしば独立した精神疾患や睡眠障害、あるいは他の精神疾患との共起障害を構成しているという事実を、開業医は知らないことが多いからである。その代わりに、開業医はほとんどのタイプの不穏な夢を、不安障害や心的外傷後ストレス障害(PTSD, Krakow, 2006; Spoormaker, Schredl, & Van Den Bout, 2006; Schredl, 2013; Thünker, Norpoth, Von Aspern, Özcan, & Pietrowsky, 2014; Nadorff, Nadorff, & Germain, 2015; Schredl & Göritz, 2014; Krakow, Kellner, Pathak, & Lambert, 1995)。) 全体として、一般成人の3.5~8.3%(Li, Zhang, Li, & Wing, 2010; Munezawa et al 2011; Sandman et al 2013; Schredl, 2010)小児の6.7~11.3%(Wiechers et al 2011)成人の精神科患者(不安障害とPTSD、それぞれSwart, Van Schagen, Lancee, & Van Den Bout, 2013)の15.6~66.7%が反復性の悪夢を報告している。すべての疫学的知見において、悪夢は男性よりも女性の方が頻繁に起こる(Li et al 2010; Munezawa et al 2011; Sandman et al 2013; Schredl, 2010; Swart et al 2013; Wiechers et al 2011)。頻繁な悪夢は、さまざまな精神的不定愁訴、睡眠障害、不眠症、すなわち、日中の機能の低下とともに、睡眠の開始と維持が困難になることと関連している(Cattarius & Schlarb, 2016; Krakow, 2006; Lancee & Schrijnemaekers, 2013; Lancee, Spoormaker, & Van Den Bout, 2010b)。さらに、起床時の疲労感、日中の眠気、エネルギー不足、小心者、集中力の低下、睡眠不足の心配(Lancee & Schrijnemaekers, 2013)精神的苦痛の増大、不安、抑うつ(Blagrove, Farmer, & Williams, 2004; Levin & Fireman, 2002)学業成績の低下(Wiechers et al, 2011)不適応なパーソナリティ機能(Köthe & Pietrowsky, 2001; Van Schagen, Lancee, Swart, Spoormaker, & Van Den Bout, 2017)がある。最後に、繰り返す悪夢は、性別、年齢、交際状況、雇用状況、喫煙、アルコールの使用、運動量、不眠症の症状、うつ病の症状、外傷体験、心的外傷後の症状、他の精神障害、向精神薬の使用をコントロールした後でも、自殺の試みおよび再試みのリスクを増加させる(Sjöström, Hetta, & Waerna, 2009)(Nadorff, Nazem, & Fiske, 2011; Sandman er al)。
悪夢の有病率が高く、精神的および身体的健康の障害に関連する特徴を考慮すると、悪夢は実質的な臨床的関連性がある。1980年代以降、悪夢障害を治療するための理論的・経験的に基づいたいくつかの試みが開発されてきた。この論文は,オーストリア,カナダ,デンマーク,フランス,ドイツ,オランダ,スイス,英国,米国の科学者や実務家が参加した悪夢治療に関する国際シンポジウムの結果をまとめたものである。このシンポジウムでは、悪夢障害の病因と治療に関する現在の知識を概説。さらに、悪夢の研究と治療の現状と今後の展望についても言及している。
1.1. 悪夢と悪夢障害の評価
悪夢の頻度や悪夢の苦痛を評価する方法はいくつかある。悪夢の頻度はNightmare Frequency Questionnaire (NFQ, Krakow, Schrader et al 2002)で評価できる。また、現在および幼少期の悪夢の頻度や、成人における悪夢の再発回数は、Mannheim Dream Questionnaire (MADRE, Schredl, Berres, Klingauf, Schellhaas, & Göritz, 2010)で評価することができる。悪夢に関連する苦痛に対処するために,参加者に悪夢の問題があるかどうかを尋ねる単一の質問を用いる著者もいる(Wood & Bootzin, 1990)。あるいは、Nightmare Distress Questionnaire (NDQ, Belicki, 1992)のような心理測定的に構築された尺度では、睡眠の質への影響や日中の信念や認識への影響など、悪夢に関する一般的な懸念を評価する(Böckermann, Gieselmann, & Pietrowsky, 2014)。SLEEP-50の下位尺度では、DSM-IVの基準を参照して悪夢の苦痛を評価している(Lancee, Spoormaker, & Van Den Bout, 2010a)。悪夢が社会的、睡眠的、健康的な領域に及ぼす影響に焦点を当てた他の質問票には、Nightmare Effects Survey (NES, Krakow et al 2000)やTrauma Related Nightmare Survey (TRNS, Davis & Wright, 2007)がある。Disturbing Dream and Nightmare Severity Index(DDNSI、Krakow, 2006)は、成人における悪夢の頻度と悪夢の効果を組み合わせたものであり、Nightmare Effects Questionnaire(NEQ、Schlarb er al)2016)は、14歳から 18歳までの青年における悪夢の頻度と悪夢の効果を組み合わせたものである。他の尺度は、Van Dream Anxiety Scale (VDAS, Agargün et al 1999)などの不安症状に焦点を当てたものや、Nightmare Behavior Questionnaire (NBQ, Pietrowsky & Köthe, 2003)などの行動結果に焦点を当てたものである。
最も頻繁に使用されている苦痛測定法であるNDQ(Belicki, 1992)では、悪夢の苦痛は悪夢の頻度よりも、不安や抑うつを含む他の精神保健上の訴えとより強く関連していることが示されている。さらに、悪夢の頻度と幸福度の関係は、NDQで評価された悪夢の苦痛によって媒介され(Blagrove et al 2004年)悪夢特異的治療は悪夢の頻度と悪夢の苦痛の両方を減少させるのに対し、非特異的治療は悪夢の頻度のみを減少させる(Gieselmann, Böckermann, Sorbi, & Pietrowsky, 2017,Van Schagen, Lancee, De Groot, Spoormaker, & Van Den Bout, 2015)。このような背景から、多くの著者は、悪夢の数の多さよりも、悪夢によって引き起こされる苦痛の方がメンタルヘルスに関連すると結論づけている(Belicki, 1992; Blagrove et al 2004; Gieselmann et al 2017; Levin & Fireman, 2002; Van Schagen et al 2015)。
2. ナイトメアの病因
ソルムス(2000)の夢生成の神経認知理論によると、夢は主にレム睡眠を司る脳幹によって生成されるのではなく、レム睡眠状態とは無関係に複雑な前脳のメカニズムによって生成されるという。彼はその根拠として、「中脳皮質-中脳辺縁系ドーパミン系が夢の生成に因果的な役割を果たしている」という大規模な臨床解剖学的研究から得られた神経心理学的知見を挙げている(Solms, 2000, p.847)。これらの経路の病変は、夢を見ることを抑制するが、レムの頻度、持続時間、密度には影響を与えない(Solms, 2000)。ソルムズ(1995年、p.61)は、今回の発見を「約100年前にフロイトが導入した古典的な夢の理論を裏付けるもの」と理解している。それによると、夢は睡眠を保護する機能を持ち、無意識の知識への入り口を提供する(フロイト、1900)。
他の研究グループは、悪夢障害の病因を、(a)過覚醒の亢進、(b)恐怖絶滅の障害、と説明している。
2.1. 過覚醒
悪夢障害の病因は、日中に蓄積され、夜間にも維持される過覚醒の亢進に影響されている可能性がある。過覚醒の亢進は、PTSDの中心的な病態生理因子として議論されているが(Buckley & Kaloupek, 2001; Kendall-Tackett, 2009; Pacella, Hruska, & Delahanty, 2013; Pole, 2007)不眠症でも同様である(統合的なレビューはRiemann et al 2010を参照)。不眠症と診断された患者は、良質な睡眠者に比べて、レム睡眠中に頻繁に(微小な)覚醒を起こし、レム睡眠の時間が断片化されていることがわかった(Feige er al)。 この覚醒亢進は、睡眠中の情報処理とβ活動を亢進させる(Perlis, Giles, Mendelson, Bootzin, & Wyatt, 1997)。つまり、過覚醒がPTSDと不眠症の両方に典型的な症状であるように、悪夢障害の病因を説明するのにも役立つかもしれないのである。
2.2. 恐怖の消極性の低下
正常な睡眠や夢を見ることで、恐怖の記憶を新規の解離した文脈と組み替えるプロセスを通じて、恐怖の絶滅が可能になるかもしれないが、悪夢障害のある人は、睡眠中に覚醒する記憶の断片を活性化し続け、恐怖の記憶を強化している(Germain, Buysse, & Nofzinger, 2008; Nielsen, 2017a; Nielsen & Levin, 2007)。情動ネットワーク機能不全モデル(AND;Nielsen & Levin, 2007)で規定されているように、情動負荷や情動苦痛が高い人は、特にこのような恐怖絶滅の障害を受けやすいとされている。「情動負荷」とは、ストレスやネガティブな感情を引き起こす出来事が自分の情動調節能力に及ぼす影響を示す状態因子であり、「情動苦痛」とは、ストレス要因に対してネガティブな情動や苦痛で反応する形質的な傾向であると定義されている。神経学的には、このプロセスは、扁桃体の過活動と、前頭前野、特に内側前頭前野(mPFC)の調節経路の障害として理解することができる。この脳の状態の弊害は、負の興奮と相容れない記憶の断片が連想ネットワークから取り出されず、恐怖を伴う記憶の断片がネットワークに統合されないことである。したがって、恐怖の絶滅が損なわれる(Germain et al 2008; Nielsen, 2017a; Nielsen & Levin, 2007)。
2.3. 過覚醒と恐怖絶滅の障害を促進する要因
悪夢障害と診断された患者において、覚醒亢進と恐怖絶滅の障害を促進する要因として、いくつか提案されている。これらの促進因子の全体像を描くことはできないが、ここでは、(a)トラウマ体験や幼少期の逆境、(b)特性感受性、(c)不適応な認知因子、(d)生理的因子によって引き起こされる特性情動の苦痛を取り上げる。
2.3.1. 心的外傷体験と幼少期の逆境
ANDモデルによると、恐怖絶滅能力はトラウマ体験の結果によって損なわれるが、幼少期の逆境のような発達上のストレスも同様のメカニズムを引き起こす可能性がある。幼少期の逆境は、mPFC-扁桃体回路の変化を引き起こすことが知られており、これらの回路は、脅威の知覚の高まり(Ochsner & Gross, 2005)や、おそらく、夢を見ることが困難になる(Nielsen & Levin, 2007)ことと関連していると考えられる。したがって、幼少期の逆境は、感情表現を含む情動制御の正常な発達を阻害し、その結果、恐怖記憶の発達を助長する可能性がある。この理論は最近、悪夢のストレス加速仮説(SAH, Nielsen, 2017a)によって明確にされた。SAHモデルでは、幼児期の健忘期間後に通常は抑制される初期の出来事の記憶(Madsen & Kim, 2016)が、夢を見ることや覚醒時の記憶に持続的な影響を及ぼす可能性が示唆されている。その証拠に、悪夢を見る人は幼少期の出来事を異常によく覚えていることを示す臨床研究(Hartmann, 1991)と実証研究(Nielsen, 2017b)がある。同様に、重度の幼少期の虐待歴は、より頻繁な乱れた夢、より高い悪夢の苦痛、および高い精神病理と関連しており(Duval, Mcduff, & Zadra, 2013)トラウマの重症度と量は、いずれもいくつかの夢と病理の測定値と相関している(Yu, 2014)。このような結果は、トラウマ体験と幼少期の逆境の両方が、情動の苦痛と悪夢障害の発症を促進するという仮説と一致する(Nielsen, 2017a; Nielsen & Levin, 2007)。
2.3.2. 形質的感受性(Trait susceptibility)
感受性の差の理論(Carr & Nielsen, 2017, c.f. Belsky & Pluess, 2009)は、ANDモデルやSAHモデルの発達論と一致しており、外傷体験や幼少期の逆境が感受性の高い人の形質感受性を増強すると仮定している。しかし、そのような特性感受性は、ネガティブな文脈だけでなく、ポジティブな文脈や支持的な文脈にも反応すると規定している。実証的には、悪夢障害や予期不安を抱える人は、新奇性を求める行動や報酬関連の行動が高いことがわかっている(Perogamvros et al 2015)。さらに、頻繁に悪夢を見る人は、ネガティブな意味刺激とポジティブな意味刺激の両方に対する処理の深さが増加し(Carr, Blanchette-Carrière, Marquis, Ting, & Nielsen, 2016)感情的なStroop課題において、ネガティブなディストラクタとポジティブなディストラクタの両方に対する反応でより多くのエラーを示す(Simor, Pajkossy, Horváth, & Bódizs, 2012)。これらの研究は、特徴的な感受性が感情の苦痛や悪夢障害の発症を促進する可能性を示唆しているだけでなく、悪夢を見る人はネガティブなトーンの感情刺激とポジティブなトーンの感情刺激の両方に敏感であることも示唆している。ポジティブな刺激に敏感であることから、ポジティブ心理学、支持的な社会環境、およびマインドフルネストレーニングなどの感情調整を強化する他の介入に特に影響を受けやすいのかもしれない(Carr & Nielsen, 2017)。
2.3.3. 不適応な信念
悪夢障害の病因には、不適応な信念が関与している可能性がある。望まない思考や感情を抑制しようとする自発的な試み(「思考抑制」)を取り上げた最新の研究によると、そのような試みは、抑制された思考が人の夢、特にレム睡眠中の夢で再燃する可能性を高めることがわかっている(Wegner, Wenzlaff, & Kozak, 2004)。さらに、内外の刺激を意図的に回避することは、悪夢の再発の有無と関連している(Kramer & Kinney, 2003)。実験では、意図的な思考抑制とそれに続く夢のリバウンドは、認知的負荷によって強化され(Bryant, Wyzenbeek, & Weinstein, 2011)、意図的な思考抑制を1週間にわたって実践すると、睡眠の質と精神的健康が悪化した(Kröner-Borowik et al 2013)。このように、意図的な思考抑制は、悪夢障害の発症を促進するもう一つのきっかけとなりうる。
2.3.4. 生理的要因
悪夢を見る患者の覚醒亢進を説明する生理学的要因の一つとして、閉塞性睡眠時無呼吸症候群や中枢性睡眠時無呼吸症候群(OSAやCSA)上気道抵抗症候群(UARS)や睡眠関連低換気症候群などによって引き起こされる深刻な睡眠の断片化が挙げられる。PTSD患者では、OSA、CSAまたはUARSが異常に高い確率で発生し(Jaoude, Vermont, Porhomayon, & El-Solh, 2015; Krakow, Melendrez et al 2002)(微小)覚醒につながることが注目されている。いくつかの研究では、睡眠呼吸障害と悪夢の関連性が描かれており、陽圧呼吸療法(PAP;Bahammam, Al-Shimemeri, Salama, & Sharif, 2013; Krakow et al 2000)や気分安定薬(Gupta, 2017)による治療で、OSA/CSA/UARSと悪夢を含むPTSD症状の両方が改善されたという。
同時に、神経伝達物質であるノルエピネフーリン、セロトニン、ドーパミンに影響を与える薬剤は、一部の患者で悪夢の発生と関連しており、一方、神経伝達物質であるγ-アミノ酪酸(GABA)アセチルコリン、ヒスタミンに影響を与える化合物は悪夢を誘発しにくいとされているが、この点についてはすべての結果が一致しているわけではない。さらに、レム睡眠を抑制する薬の離脱は悪夢を引き起こすことが報告されている(Morgenthaler et al 2018,Pagel & Helfter 2003)。これらの知見を合わせると、悪夢の発生を促進する化学センサー経路があることが示唆される。
2.4. 悪夢スクリプトの形成
上記のすべての要因が、再発する悪夢の要素を悪夢スクリプトに凝縮することに寄与していると考えられる。悪夢は学習された行動として持続すると考えられており、つまり「自分の人生」を歩むことになる(Ehlers & Clark, 2000; Hartmann, 1996; Krakow & Neidhardt, 1992など)。さらに最近では、再発夢の認知モデル(Spoormaker, 2008)によると、悪夢の持続は、悪夢を最初に引き起こした元のストレス要因がとっくに消えているにもかかわらず、固定された期待パターン(すなわち悪夢スクリプト)を再生するループによって引き起こされるという。この点で、悪夢は、元のストレス因子に類似した夢の要素に反応して悪夢スクリプトが活性化されることで発生し、悪夢は習慣的な形で永続する。
これらの悪夢誘発因子は、図1に示すような病態生理学的なパッチワークを構成していると考えられる。
図1 悪夢の病因の統合モデル
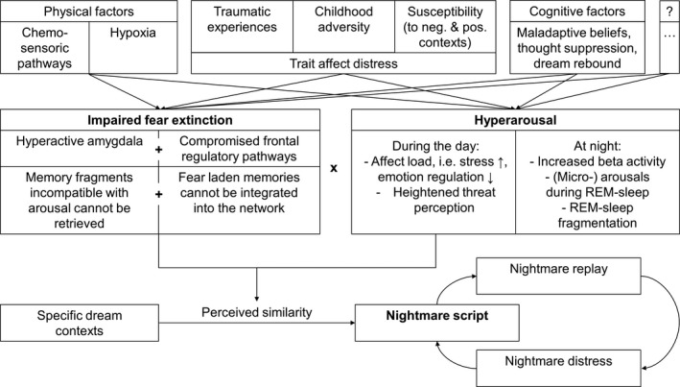
3. 悪夢障害の治療
悪夢障害は、治療されないまま何十年も続くことが多く(Schreuder, Kleijn, & Rooijmans, 2000)、特定の治療アプローチが存在するにもかかわらず、患者は治療を受けないか、不十分な治療を受けることが多い(Krakow et al 1995)。以下の考察は、異なる治療アプローチの主な影響に注意を向けるのに役立つかもしれない;これらは、強調する治療である。(a)悪夢の主観的な意味、(b)悪夢の病的な繰り返し、(c)悪夢に関する不適応な信念を重視した治療法である。
3.1. 悪夢の意味を対象とした治療アプローチ
悪夢の特定の意味は、心理力学的アプローチの一つの焦点である。心的外傷後の悪夢は、しばしば患者によってステレオタイプな再現性のある内容として描写される(Wittmann, Schredl, & Kramer, 2007)ことから、多くの治療アプローチでは、この再現性のある内容の潜在的な主観的意味を無視している。しかし、LanskyとBley(1995)は、いわゆる複製性悪夢が元のエピソード性トラウマ記憶とは異なり、重要な情報源を構成している可能性があるという広範な臨床的証拠を報告している。心理力学的な観点からは、悪夢の発生は、現在の心理的平衡が乱れていることを示すアラーム信号と考えることができ、心理力学的なアプローチは、アラーム信号だけに対処するのではなく、根底にある葛藤を特定し解決することを目的とすることができる。この作業には、個人の発達歴やトラウマ歴(Wittmann & De Dassel, 2015)エピソード記憶の痕跡との類似点や相違点の発見(Lansky & Bley, 1995)悪夢の発生を治療プロセスや現在の生活状況、対人関係のパターンと関連付ける(Wittmann & De Dassel, 2015)繰り返しの意味づけ(Gardner & Ørner, 2009)自分の感情調整プロセスを洞察するために暗黙的な意味を精緻化する(Moser & Von Zeppelin, 1996)など、複数のレベルの処理が含まれる。
夢の内容の変化は、トラウマ的な出来事の後に患者が経験する適応と不適応に対応し(Mellman, David, Bustamante, Torres, & Fins, 2001; Terr, 1983)、精神分析的な治療の過程における症状の変化や個人の成長を示すことがわかっている。しかし、悪夢の治療における精神力動的アプローチの有効性を示す証拠は、対照的でないケースシリーズに限られている(Gardner & Ørner, 2009; Lansky & Bley, 1990; Wittmann & De Dassel, 2015など)。
3.2. 悪夢の慢性的な繰り返しを対象とした治療アプローチ
悪夢の内容の慢性的な繰り返しを対象とした治療アプローチは、悪夢を過学習された行動であると考え、これらの習慣を学習解除することを目的としていることが多い。これらのアプローチは主に、以下に説明するように、(a)脱感作と暴露療法、(b)イメージリハーサル療法(IRT)、または(c)明晰夢の原則に基づいている。
3.2.1. 脱感作・暴露療法
脱感作療法と暴露療法は、悪夢を直接治療するために用いられた最初のアプローチである(Kellner, Neidhardt, Krakow, & Pathak, 1992; Miller & Dipalato, 1983)。脱感作法では、まず患者に筋弛緩法を紹介する。そして、悪夢を修正せずに想像し、緊張するたびにリラックスするように求められる。暴露療法では、患者は悪夢を鮮明に想像するよう求められるが、弛緩運動は伴わず、またストーリーラインを積極的に変更することもない(Kunze, Arntz, Morina, Kindt, & Lancee, 2017)。この方法は、PTSDを治療するための伝統的な技法から適応されている(Foa & Rothbaum, 1989など)。脱感作療法と暴露療法に共通する治療根拠は、悪夢に伴う恐怖や覚醒の症状が、より適応的な行動、認知、感情のプロセスによって上書きされるという、絶滅および/または抑制学習の原則に基づいている。いくつかの試験で、脱感作療法と暴露療法の有効性が実証されている(Davis & Wright, 2007; Hansen, Höfling, Kröner-Borowik, Stangier, & Steil, 2013)。Kunze et al 2017)は、純粋な曝露プロトコルが純粋なIRTプロトコルと同様の効果サイズを持つことを示した。しかし、減感作療法と曝露療法の大きな欠点の1つは、治療中に惹起される喚起が患者に深刻な苦痛を与える可能性があることである(Arntz, Tiesema, & Kindt, 2007, ただし、Kunze er al)。
3.2.2. イメージリハーサル療法(IRT)
悪夢を治療するためのIRTアプローチは、入手可能な最良のエビデンスに裏打ちされているため、Oxford Centre for Evidence Based Medicine(Cranston, Davis, Rhudy, & Favorite, 2011)やAASM(Aurora er al)。2010; Morgenthaler er al)。2018)では、悪夢障害のレベルA治療として推奨されている。IRTでは、患者は覚醒時に悪夢のストーリーを再記述するように指示される。当初の指示は “これは、悪夢の結末やその他の不穏な夢の構成要素を特定したものではないが、悪夢を「勝利」(Marks, 1978)「満足」、「より中立的な、あるいは楽しい」(Thünker & Pietrowsky, 2012)結末を持つように変更することを提案している人もいる。そして、この再記述された悪夢(もはや悪夢ではないように見える)は、患者の想像力の中で1日に2,3回リハーサルされる。Hansen et al 2013)のメタ分析では、IRTが悪夢の頻度(Hedges’ g = 1.04)と悪夢を見る週の回数(g = 0.99,gs ≥ 0. 80は大きな効果と考えられる)(他のメタアナリシスの同等の結果については、Augedal, Hansen, Kronhaug, Harvey, and Pallesen (2013)、Cranston et al (2011)、Casement and Swanson (2012)、Nadorff, Lambdin, and Germain (2014)、Seda, Sanchez-Ortuno, Welsh, Halbower, and Edinger (2015)を参照)。IRTは悪夢の頻度を減少させるだけでなく、PTSDの重症度を減少させ(g = 0.92,Hansen et al 2013年)睡眠の質を高め(Cohenのd = 0.68,Casement & Swanson 2012年)より一般的な精神衛生上の不満を減少させた。IRTによる治療を受けている患者では、副作用や症状の代替は報告されていない。
IRTにおける積極的な治療メカニズムについては、継続的な議論が行われている。IRTは多成分の治療パッケージで提供されることがほとんどであるため、特定の治療メカニズムを特定することは困難である。悪夢の修正は、嫌悪的な悪夢の内容への曝露なしにはほとんど起こらない(Lancee, Van Den Bout, & Spoormaker, 2010)し、ほとんどの治療マニュアルには、PTSDの治療から取り入れられた心理教育、睡眠日誌の作成、リラクゼーション演習、想像力のテクニックなども含まれている。このような治療要素を特定する試みでは、悪夢を日記に記録するだけで、悪夢の頻度や悪夢の苦痛が減少することが実証されている(Lancee et al 2010a; Neidhardt, Krakow, Kellner, & Pathak, 1992)。それにもかかわらず、補助療法としてのIRTは、日記も含む比較治療を上回る結果となった(Gieselmann et al 2017; Van Schagen er al)。 一方、詳細な物語形式の睡眠日記をつけることは、悪夢の頻度を減少させる上でIRT(日記を含む)と同等の効果があったが、悪夢の苦痛を減少させる上ではIRTが詳細な日記を上回ってた。興味深いことに、日記や宿題などの他の治療要素を一切排除し、最低限の心理教育のみを含む純粋なIRTプロトコルも有効であった(Kunze et al 2017)。このように、日記をつけることはIRTの必要な治療要素ではないかもしれない。さらに,IRTは最小限の曝露で効果を発揮するため,悪夢のコンテンツへの曝露は必要な治療要素ではないと主張されている(Krakow, Hollifield er al)。,2001)。しかし、リラクゼーショントレーニングと睡眠習慣修正の介入は、曝露とリスクリプトを含む完全なIRTプロトコルよりもパフォーマンスが悪くならないことを示唆する研究もある(Miller & Dipalato, 1983; Pruiksma, Cranston, Rhudy, Micol, & Davis, 2018)。このように、文献は依然として不明瞭であり、時には矛盾している。
3.2.3. 明晰夢療法
明晰夢療法は著しく異なるアプローチをとり、個人が夢を見ている間に夢に直接影響を与えることができるようにすることに焦点を当てている(Holtzinger, 2014)。明晰夢は、オリエンテーションの意識、つまり夢を見ている過程にあるという意識が特徴であり、しばしば、決定を下すことができるという意識も伴うため、夢のプロットを担当したり、責任を負ったりすることができる。例えば、夢の内容を変えたり、コントロールしたり、あるいは単に自分を目覚めさせたりするなど、自発的に行動できるようになることがある。実際には、目覚めたときに夢を直接書き留めて、夢の記憶を改善することを明確に意図して就寝してもらいます。また、「自分が夢を見ていることに気づくことができる」という確信を持つことで、明晰夢の頻度が高まることがわかった。明晰になったかどうかを確認するには、覚醒時に「これは本当に起こっていることなのか、それとも夢なのか」、「2度見ても同じように見えるか(例:時計は同じ時間を示しているかどうか?本のタイトルはまだ同じなのか、そうでないのか)』。ゲシュタルト療法のアドオンとしての明晰夢は、悪夢に明確な焦点を当てないゲシュタルト療法よりも、悪夢や睡眠関連の症状をより早く改善することがわかった(Holtzinger, Klösch, & Saletu, 2015)。しかし、大きな懸念として、Spoormaker and Van Den Bout(2006)が実証したように、すべての夢を見る人が明晰夢の状態に到達できるわけではなく、16人の患者のうち6人しか悪夢の中で明晰になることができなかったということがあった。興味深いことに、治療効果は、患者が夢の中で明晰になれたかどうかとは無関係に生じた。一方で、明晰夢の概念を紹介するだけで、安心感が得られることがわかった(Holzinger et al 2015)。
3.3. 不適応な信念をターゲットにした治療アプローチ
理論や実践でめったにターゲットにされないもう一つの側面は、不適応な信念の保持である。不適応な反芻やカタストロフィジング(例:「悪夢を見た後は汗びっしょり」、「悪夢を見た夜の後は、次の日は拷問になる」)は、患者の苦痛に影響を与えるのであろうか?悪夢の意味に関する不適応な特質的モデル(例:「実生活における将来の出来事に備えるために悪夢が必要である」)は、治療効果に役立つのか、それとも悪いのか?これらの信念の変化は苦痛を減少させるか?Harvey, Tang, and Browning(2005)は、不眠症の治療に認知療法を導入した。この流れの中で、彼らは行動実験と認知的再構築によって不適応な信念を変えることを推奨している。ネガティブな自己描写は、オリジナルのIRTプロトコルでも扱われており(Krakow & Zadra, 2006)エクスポージャーとIRTプロトコルの両方が、悪夢に関するネガティブな信念を改善することができた(Kunze er al)。 逆説的意図、つまり悪夢を見る人に悪夢を見るように促すことは、再発する悪夢の否定的評価に取り組む戦略として推奨されている(Spoormaker, 2008)。
3.4. 悪夢直接治療の積極的治療メカニズム
RousseauとBelleville(2018)は、特定の悪夢治療の報告された効果を説明する試みの中で、定性的な分析を行い、Germain et al 2004)やKrakow, Hollifield et al 2001)が提案したような、支配感の増大が、最も多く引用されたメカニズムであると結論づけている。著者らは、悪夢を自分でコントロールしているという確信には、認知的な要素だけでなく、感情的な処理も含まれると述べている。感情的な処理は、記憶の統合、すなわち、記憶ネットワークにおける意識的および無意識的な恐怖構造の再編成につながる。彼らは、ANDモデル(Nielsen & Levin, 2007)を参考にして、そのアプローチを論じた。それ以外にも、感情処理に類似したメカニズムは、PTSDの治療における積極的な治療メカニズムとして議論されており(下記参照、c.f. Kleim et al 2013)また、過覚醒を克服する際の認知・情動記憶内容の再構築の促進因子としてのレム睡眠に関連して議論されている(Feige et al 2008,2013,Perlis et al 1997,Riemann et al 2010)。
3.5. 薬理学的治療
悪夢の具体的な薬物治療については、ほとんどの試験で中枢神経系に作用するα1アドレナリン受容体拮抗薬であるプラゾシンが使用されている。AASMは、悪夢を含むPTSDの補助療法としてプラゾシンを推奨している(Aurora er al)。2010, on behalf of the AASM)。しかし、最近の大規模多施設試験では改善が見られず(Raskind et al 2018年)治療を中止すると患者がベースラインのレベルに戻ってしまう試験もあった(Raskind et al 2018)。これらの矛盾したデータにより、AASMはプラゾシンに関する助言を「推奨」から「使用してもよい」に格下げし、「使用してもよい」とする他の医薬品の名前を挙げた(Morgenthaler et al 2018,AASMを代表して)。
薬物療法の効果を評価する際には、医薬品は一般的に二重盲検法でプラシーボと比較して試験されることを考慮しなければならない。ほとんどの心理療法の臨床試験では、ナラティブベースの介入が行われているため、このような高い基準を満たすことができないことが多い。セラピストは通常、患者がどのグループに無作為に割り振られたかを知っており、ほとんどの介入はプラセボ薬と比較できない待機リスト対照条件でテストされる。同時に、悪夢障害の治療に遠慮なく推奨できる医薬品は現在のところ存在しない。
4. 異なる患者層における悪夢治療
4.1. PTSDにおける悪夢の治療
PTSDと診断された患者の最大67%が、苦痛を伴う夢の形で侵入してきたトラウマ記憶を再体験している。さらに、悪夢に伴う睡眠の断片化は、PTSD症状の回復を阻害する可能性が高い(Babson & Feldner, 2010; Germain et al 2008; Harvey, Jones, & Schmidt, 2003)。
特発性悪夢の場合と同様に、IRTはPTSD患者の悪夢の治療に有効な戦略である。暴力的な犯罪の被害者にIRTを含む1回のセッションを行った場合(Germain, Shear, Hall, & Buysse, 2007)や、性的暴行を受けた生存者にIRTを何も追加せずに行った場合、悪夢の症状と他の睡眠パラメータの両方が改善された(Krakow, Hollifield et al 2001)。さらに、IRTは他のPTSD症状を直接対象とせずに一般化すること、すなわち、侵入症状、回避症状、喚起症状の改善を引き起こすことが明らかになった(Seda er al)。2015)。悪夢やPTSD症状に対するIRTの有意な効果を示す研究は数多くある(Nappi, Drummond, Thorp, & Mcquaid, 2010など)。
プラゾシンとIRTの短期効果を比較したところ(Seda er al)。2015)どちらも悪夢やPTSD症状に対して同等かつ中等度の効果を示すことがわかったが、IRTと不眠症のためのCBT(CBT-i)を併用した研究では、プラゾシンを用いた研究に比べて全体的な睡眠の質の改善効果が高いことがわかった。IRTの研究では、治療プロトコルの提供方法(IRTとCBT-iまたは他のタイプの心理的介入の組み合わせなど)の異質性やバリエーションがかなり多く、結果に影響を与える可能性がある。対照研究からの初期の知見では、CBT-i単独(Ho, Chan, & Tang, 2016)、およびIRTと組み合わせたCBT-iが不眠症およびPTSD症状を効果的に軽減することが示されている(Margolies, Rybarczyk, Vrana, Leszczyszyn, & Lynch, 2013)。
4.2. 多様な他の精神障害を持つ患者の悪夢治療
IRTは,多様な精神障害を持つ外来患者にアドオン治療として使用した場合,悪夢の頻度と悪夢の苦痛に中程度の効果を示した。これらの患者は,通常通りの治療を受けた患者よりも悪夢の頻度と悪夢の苦痛が改善した(Van Schagen er al)。,2015)。その改善効果は、長期的に、つまり6か月後と9か月後のフォローアップでも維持された(Van Schagen, Lancee, Spoormaker, & Van Den Bout, 2016)。さらに、標準的な入院精神科治療にアドオンする形で悪夢を治療すると、自殺念慮のより大きな減少にもつながる(Ellis, Rufino, & Nadorff, 2019)。したがって、ナイトメア治療は、一般的な精神科診療における治療成績の向上に役立つと考えられる。一方で、治療効果は併存疾患のある患者とない患者で異なることがわかった:併存疾患が多いと治療成績の悪化が予測される(Thünker & Pietrowsky, 2012)。
4.3. 難民の悪夢のような治療
難民もまた、繰り返し見る悪夢をはじめとする多様な精神障害に悩まされることが多い集団のひとつである。その数は2017年末に新たなピークを迎え、全世界の難民数は2,540万人に達している(United Nations High Commissioner for Refugees (UNHCR), 2018)。世界の難民のおよそ30%がPTSDに苦しんでいると推定されている。2008年から 2012年にデンマークの救急車外来で精神科治療を受けたトラウマを抱えた難民752人のサンプルでは、99%が睡眠障害と再発性の悪夢を最も有病率の高い症状として報告している(Sandahl, Vindbjerg, & Carlsson, 2017)。しかし、一般的な治療マニュアルでは、効果的な治療を複雑にする言語的、文化的、組織的な障壁など、難民が経験する特殊な状況を考慮することはできない。難民の悪夢の場合、予備調査では、プラゾシン(Boynton, Bentley, Strachan, Barbato, & Raskind, 2009)とクロニジン(Kinzie, Sack, & Riley, 1994)の効果が取り上げられている。
4.4. 児童・青年期における悪夢の治療
悪夢やその他の副鼻腔は、子供や青年で頻繁に報告される。悪夢だけでなく、一人で寝るのが怖い、暗闇が怖いなどの症状を示すことも多い(Wiechers et al 2011)。子どもだけでなく、家族の少なくとも1人が、子どもの睡眠が原因で非回復性睡眠に悩まされることもよくある(Cattarius & Schlarb, 2016)。症状は通常、年齢が進むにつれて減少する。しかし、8~11歳のときに悪夢を見ていたことは、2年後に悪夢を見ていることを予測させるものであり、幼少期の悪夢は数年後にも残る可能性が高いことを示している(Schredl, Fricke-Oerkermann, Mitschke, Wiater, & Lehmkuhl, 2009)。子どもや青年を対象とした治療法としては、系統的脱感作法、IRT、リラクゼーション技法、消去法、眼球運動による脱感作法など、さまざまな手法が報告されているが、その知見は主に症例研究やサンプル数の少ない試験に限られている(子どもや青年の睡眠障害に関するレビューについては、Sadeh, 2005を参照)。主に不眠症を対象とした複合的な治療法を適用した様々な研究では、4歳までの子ども(Schlarb, Brandhorst er al)。2011)5~10歳の子ども(Schlarb, Velten-Schurian er al)。2011)大学生(Schlarb er al)。2017)で悪夢症状の有意な減少が認められた。悪夢を具体的に対象とした治療に関しては、IRTにより、6~11歳の子ども(Simard & Nielsen, 2009)および13~18歳の子ども(Krakow, Sandoval et al, 2001)で悪夢の頻度が有意に減少することが示された。
5. 悪夢の苦しみに関する知識の欠如と治療の可能性
精神科サンプルの患者の70%までが再発性の悪夢に苦しんでいるにもかかわらず(Swart et al 2013; Van Schagen et al 2017)悪夢のスクリーニングと治療は、睡眠センターでさえも稀なままである。それにもかかわらず、悪夢は最小接触の介入で治療できる。悪夢障害の治療は、1回のセッション(Neidhardt et al 1992年)掲載された自助書(Burgess, Marks, & Gill、1998年、Lancee, Spoormaker, & Van Den Bout 2011,Lancee et al 2010a)インターネットを利用した自助書(Gieselmann et al 2017)などで効果を上げている。しかし、悪夢に苦しむ患者の大多数は、専門家の助けを求めません。多くの患者は、他の選択肢を知らないために、悪夢と共存することを選択している。自分の悪夢が治療可能だと考えているのは3分の1以下で、医療機関に報告したのは38%にとどまっている(Nadorff et al 2015,Schredl 2013,Thünker et al 2014)。助けを求めた場合、ほとんどの患者は一般開業医(41%)または医療専門家(38%)に相談したが、彼らは悪夢障害の治療に関する専門知識をほとんど持ち合わせていなかった。専門家に助けを求めた悪夢症患者のうち、有益なアドバイスを受けたと報告したのは3分の1から5分の1以下であった(Nadorff et al 2015,Schredl & Göritz 2014,Thünker et al 2014)。
6. 将来の展望
悪夢の病因と治療はまだ比較的新しい分野であり、数多くの研究課題が未解決のままである。したがって、最後のセクションでは、(a)悪夢障害の病因、(b)悪夢治療の継続的な開発、(c)異なる亜集団への悪夢治療の適用、(d)悪夢治療の医療システムへの統合に関して、考えられる将来の展望を提示する。
6.1. 悪夢障害の病因に関する今後の展望
基礎科学の観点からは、悪夢に関する研究は、悪夢の発生が主観的な報告にのみ依存しているという事実によって妨げられることが多い。しかし、他の多くの現象にも同様の主観性の問題があり(例:恐怖、痛み、心の迷い、エピソード記憶、意識)このテーマの様々な側面を研究するための有効な実験モデルや評価ツールの開発を妨げるものではない。したがって、(a)共通の合意を客観化するのに役立つ悪夢の基準をより明確に定義すべきである。悪夢の苦痛が悪夢障害の重要な特徴であることを考えると、多様な評価ツールは異なる試験間での悪夢の苦痛の比較可能性を制限し、十分に確立された評価ツールは方法論的な理由で批判されている(Schredl, Landgraf, & Zeiler, 2003)。したがって、悪夢の基準をどのように定義するか、悪夢の苦痛をどのように運用するかについて、共通のコンセンサスを得ることが望まれる。さらに、(b)精神神経免疫学と精神神経内分泌学の分野(Buckley & Kaloupek, 2001; Kendall-Tackett, 2009; Pacella et al 2013; Pole, 2007)は、悪夢によって喚起される苦痛や、精神神経免疫学的および精神神経内分泌学的メカニズムと悪夢の発生との間の推定される因果関係について、さらなる洞察を与えるのに役立つかもしれない。悪夢を誘発する薬の役割は、そのようなメカニズムを明らかにするのに役立つかもしれないが、悪夢がある患者には起こるが、別の患者には起こらないなど、結果はまちまちである。c)睡眠呼吸障害の病態生理と悪夢の相互作用は、基礎科学の枠組みからもう一つの理解を深める可能性がある(Gupta, 2017; Jaoude er al)。
悪夢の実験モデルを開発するにあたっては、隣接する過覚醒と恐怖絶滅の分野から多くのことが学べることを提案する。過覚醒については、レム睡眠中の(微小な)覚醒やレム睡眠の断片化(Feige er al)。2008, 2013)などの現象が悪夢でも観察されるのかどうかを明らかにするための脳波研究が必要である。また、不眠症患者はレム睡眠時に覚醒していると感じることが多いのに対し、悪夢障害患者はレム睡眠時に悪夢を見ることが多い理由も明らかにする必要がある。悪夢を引き起こすためには恐怖の消極性の低下と覚醒度の上昇が必要であるという上述の理論は、依然として仮説的なものであり、実証的な調査が必要である。恐怖の消去に関しては、実験方法や神経回路が重なり合っているため、患者から健常者へ、動物から人間への知識の伝達が可能である。しかし、ヒトを対象とした研究で使用される無条件刺激は、一般的に手首への軽度の電気ショックであり、我々の知る限り、これによってヒト被験者に侵入型の記憶痕跡(例えば、フラッシュバックや嫌悪事象に関する自発的な思考)が生じることはない。このように、標準的な恐怖学習パラダイムは、人間の侵入記憶や悪夢の研究には最適ではないと考えられる。
興味深いことに、いくつかの研究グループが、短い映画の断片(Wegerer, Blechert, Kerschbaum, & Wilhelm, 2013)や、以前に見た長時間の映画のリマインダーキュー(Kunze, Arntz, & Kindt, 2015)など、非常に嫌悪感の強い映画クリップを無条件刺激として用いることで、恐怖条件付けと侵入的記憶形成の関係について取り組み始めている。さらに、感情的な刺激(映画の断片)が睡眠パラメータに及ぼす影響にも注目が集まっている(Talamini, Bringmann, De Boer, & Hofman, 2013; Werner, Schabus, Blechert, Kolodyazhniy, & Wilhelm, 2015)。昼間に自発的に発生することが、必ずしも睡眠中に自発的に発生することを意味しないため、恐怖条件付けされた侵入記憶の痕跡が、夜間にどの程度主観的に報告されるのかが中心的な問題として残っている。恐怖条件付けと恐怖絶滅に関するこの研究は、個人差を検討するための興味深いテーマとなりうる。さらに、今後の研究では、外部刺激法によって、睡眠実験室での実験制御を高めることができる。
さらに、思考抑制の役割をよりよく理解することが望まれる。現在のところ、特発性悪夢と心的外傷後の悪夢における思考抑制の影響は、議論されている概念の中で最も推測されていると考えられる。心的外傷後の悪夢では、認知的回避が悪夢の頻度を予測することは認められなかったが(Babson et al 2011)、認知的回避が思考抑制に包含されるものと一致するかどうかは不明である。しかし、これらの理論的枠組みは、特発性悪夢と心的外傷後悪夢における思考抑制と認知的回避の役割を検討するための、検証可能な研究方法の開発に役立つだろう。
6.2. 悪夢障害の治療に関する今後の展望
6.2.1. 異なる治療アプローチの場合
効果量が中程度から大きいにもかかわらず、治療成績にはまだ改善の余地がある。特に、異なるワークグループ間での大きな分散(Hansen er al)2013)はまだよく理解されていない。
IRTに代わる治療法を検討し、さらに研究すべきである。薬物治療の効果に関しては、より正確な知識が必要であり、それにより、より正確な推奨事項の策定が可能となる。さらに、特に多くの患者がPAP療法に耐えられないという背景から、PAP療法がどのように悪夢障害の臨床的改善をもたらすのかを探るためにRCTを開発すべきである(Bahammam et al 2013,Krakow et al 2000);それにもかかわらず、最近の研究では、オートバイレベルや適応サーボベンチレーションなどの高度なPAPモードを使用したPTSD患者において、通常よりも高いアドヒアランス率が示された(Krakow, Obando, Ulibarri, & Mciver, 2017)。さらに、治療としての明晰夢の可能性は、もっと注目されるべきである。可能であれば、夢を見ている間に確実に直接修正することができる技術を開発することができる。具体的には、これらの技術は、日中に悪夢のプロットを変更するよりも効果的であることを証明するかもしれない。現在のところ、多くの患者が明晰になれないため(Spoormaker & Van Den Bout, 2006)明晰夢の概念を紹介するだけで、それ自体が何らかの救済をもたらす可能性があるため(Holzinger et al 2015)明晰になることの必要性は疑問視されている。
心理力学的アプローチの効果を取り上げた研究は不足している。関連して、悪夢の内容に関連した悪夢治療の効果に関する研究もほとんどない。直近の悪夢の大規模なサンプル(N=1214)から得られた結果によると、危険や重要な他者の喪失といったトピックが頻繁に挙げられているが、診断基準にはあまり反映されておらず(Mathes & Schredl, 2014)これらのトピックに対して悪夢治療が他の悪夢のトピックと同様に効果があるかどうかはまだ明らかになっていない。さらに、いくつかの悪夢には自殺に関するテーマが含まれており、悪夢が持つカタルシス機能を背景に、より具体的に検討する必要がある。このような悪夢の発生や治療は、自殺の予防に役立つのだろうか?このように、悪夢の内容分析は、悪夢の「感情調整機能」の可能性に焦点を当てるべきである(Moser & Von Zeppelin, 1996)。さらに、悪夢が発生した具体的な生活状況を評価することで、根底にある関連する葛藤の正確な性質についての洞察が得られるかもしれないし(c.f. Lansky & Bley, 1995)、治療中の悪夢の内容の変化が予後の情報を提供するかもしれない(Mellman et al 2001; Terr, 1983)。夢の内容と治療過程、患者の現在の生活状況や対人関係のパターンとの間のアナロジーは、重要な現在の経験の認識を高めるのに役立つ(Wittmann & De Dassel, 2015)。
最後に、私たちの知る限り、不適応な信念、意味の特異なモデル、誤った自己描写を対象とした治療アプローチに関する研究はない。このように、IRTを超えて、連想分割がグリッドロックされた悪夢の脚本を解体するのに役立つかどうかは、まだ検証されていない。もともと強迫性障害(OCD, Moritz, Jelinek, Klinge, & Naber, 2007)の強迫観念を治療するために開発されたが、不要な侵入的思考などの他の症状の緩和にも有効であった(Rodríguez-Martín, Moritz, Molerio-Pérez, & Gil-Pérez, 2013)連想分割は、特に今後の研究に適した候補であると考えられる。同様に、Harvey et al 2005)の認知的再構成アプローチは、悪夢が未来を予言するとか、悪夢を見た夜は翌日の仕事や生活の問題に集中できないといった思い込みを患者が改めるのに役立つかもしれない。このような戦略が、単独の治療として、追加の方法として、あるいは複合的なアプローチとして適用されるのがよいかどうかは、まだ調査が必要である。
6.3. 悪夢を見る人のサブ集団に関する今後の展望
6.3.1. PTSD患者の場合
現在までに、トラウマ焦点CBTなどの心理療法を受けているPTSD患者の大半は、昼間の症状に焦点を当てて治療を受けている。改善は夜間の症状(睡眠障害など)に一般化すると想定されており、これは初期のエビデンスで支持されている(Woodward et al 2017)。一方、IRT治療は、主に夜間の症状に対処し、治療の利益は、今度は昼間の症状に一般化することがわかった(Krakow, Hollifield er al)2001)。昼間のPTSD症状の治療がどの程度、悪夢の症状に一般化するのか、またその逆はどの程度なのかをより明確にするためには、さらなる無作為化比較試験が必要である。さらに、治療反応の予測因子を確立し、どのような患者が他の治療法に比べて反応しやすいかを明らかにすることも有益であろう。これまでのところ、治療法の組み合わせによる効果についての知見は限られている。
ステップケアアプローチに関して、またIRTの介入が迅速かつ容易に提供できることを考慮すると、今後の研究では、IRTの短期経過をトラウマ焦点型心理療法と組み合わせて、あるいはその前に提供することの潜在的な有益性を確立すべきである(Nadorff et al 2014)。睡眠の質を改善することで、PTSD患者は、記憶のエンコーディングや記憶の統合が改善される可能性がある(Diekelmann, Wilhelm, & Born, 2009; Walker & Stickgold, 2006)。睡眠の質の改善は、PTSD症状を軽減することがわかっており(Ho er al)。 効果的なIRT治療の後には、多くの主要なPTSD症状がすでに正常化していることが考えられる。残りの症状は、トラウマに焦点を当てたCBTやその他のエビデンスに基づく治療アプローチ(図2参照)を用いて治療することができ、治療セッション数を減らせる可能性がある。トラウマに焦点を当てたCBTの前にIRTを行うことで、患者に報酬を与え、動機づけを行い、より長く、より厳しい、より複雑で、より苦痛を伴うトラウマに焦点を当てた介入によって引き起こされることがある望ましくない副作用を抑えることができる。実際、PTSDの第一選択の介入として悪夢を治療することの効果や、自殺念慮を減らす効果を調査する臨床試験が進行中である(例えば、https://tango.uthscsa.edu/ssads/507,テキサス大学;Nadorff er al)。2014)。
図2 頻繁に適用されるトラウマに焦点を当てた介入方法と提案されている代替アプローチ
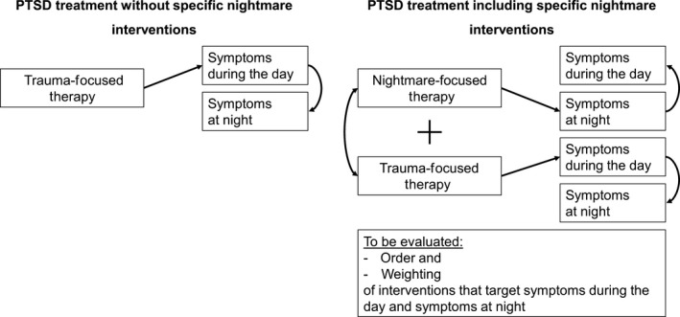
現在のところ、治療アルゴリズム、ステップケアの推奨はなく、PTSDのIRTとCBTのどちらが治療開始に最適かを推奨する経験的な証拠も不十分である。今後の研究では、PTSD治療におけるIRTの最適な選択とタイムポイントを決定する必要がある。さらに、PTSDの治療においては、曝露を行うことができず、そのためにイメージベースやマインドフルネスベースの介入を希望する患者や治療者のために、曝露を行わない選択肢を提供する介入法が登場している。悪夢のような介入とトラウマに焦点を当てたCBTや同様のPTSD治療の第一選択の両方の相乗効果の可能性に関する情報を含め、特定の患者の特徴に対する信頼できる治療アルゴリズムと治療法の選択を導き出すためには、今後の研究が必要である。
6.3.2. 異なる患者集団の場合
悪夢は統合失調症、境界性人格障害、解離性障害など多くの精神病理と関連することが示されているが、これらの障害に対する悪夢治療の影響を検討した研究はほとんどない(Swart er al)。 今後の研究では、他の多様な精神的愁訴を持つ治療を受けた患者が、複数の併存疾患を持たない患者ほど利益を得られない理由を明らかにしたり(Thünker & Pietrowsky, 2012)他の慢性疾患(てんかんや疼痛障害など)を患う患者における悪夢治療の効果を解明したりすることもできるだろう。悪夢障害の治療が患者の他の身体的・精神的愁訴にどのように影響するかを正確に明らかにするためには、さらなる研究が必要である(例えば、悪夢を治療することで抑うつ症状は軽減されるのか)。
難民は、長期的、反復的、世代を超えた、そして多くの場合、言語化できないトラウマに悩まされているだけでなく、亡命のステータスや居住地に関する不確実性、母国で安全でない家族への懸念、文化的・言語的困難、認識された差別や人種差別など、移住中や移住後のストレスを抱えていることが多いため、トラウマの影響を受けた難民を治療するためのアプローチはしばしば失敗する(Boynton et al 2009; Crumlish & O’rourke, 2010; Palic & Elklit, 2011)。異なる年齢層に関しては、同伴者のいない若い難民の特別なニーズに注目すべきである。さらに、PTSDや睡眠障害に苦しむ難民の睡眠障害や悪夢の治療に関する研究は不足しており、今後の注意が必要である。克服すべき課題は、翻訳された標準化された手段が利用できないことと、翻訳者の最適な雇用である。言語や文化の障壁があるため、薬理学的治療と心理学的治療を比較する試験が特に注目されている(Sandahl, Jennum, Baandrup, Poschmann, & Carlsson, 2017)。
ほとんどの研究は成人を対象としているが、年齢層を比較したものではなく、例えば、小児や青年におけるナイトメア障害の治療効果についてはほとんど研究されていない。しかし、成人患者に対する有望な結果と、思春期における初期の研究を考慮すると、子どもや思春期の悪夢の治療にIRTを使用することは、高い優先度を持つべきである。悪夢治療は、早期の治療開始が若年者の慢性的な悪夢障害の発症を防ぐのに役立つ可能性があるため、幼児や乳児、学童、思春期、高年齢の学生など、様々な年齢層に適応させるべきである。
6.4. 医療システムへの統合に関する今後の展望
医療機関で悪夢のスクリーニングが行われることは稀であり、また悪夢を医療機関に訴えない患者が多いため、無数の患者が治療を受けられずにいる。したがって、今後の研究では、このような診断上の欠点を理解し、それを克服する方法に大きな焦点を当てるべきである。そのためには、2つの政策目標が必要である。(a) プライマリーケアや小児科医の診察時間内にスクリーニングができるように効率化すること、(b) 医療従事者が適切な紹介ができるように教育すること。悪夢の存在は、重度の精神病理に共存するか、他の精神疾患を悪化させる影響があることを考えると(Van Schagen et al 2017年)不穏な夢は、個人がメンタルヘルスの治療を必要としていることを医療従事者に知らせるアラーム信号として役立つかもしれない。一方、悪夢が正常な小児期の発達の単なる副産物であるならば、小児科医が悪夢に対処すべきかどうかを判断するためのガイドラインを作成すべきである。要するに、悪夢の苦しみが正常な発達の範囲を超えている場合には、メンタルヘルス評価のための紹介が必要であることが示唆される。
治療へのアクセスを改善する試みとして、電話カウンセリング(Schredl et al 2016)インターネットベースのアプリケーションや自助的アプローチ(Gieselmann et al 2017;Lancee et al 2010a)などの閾値の低い介入がさらに開発され、一般市民に提供されるべきである。インターネットを利用した治療が有効であり、対面式の治療と同等の効果サイズがあることを示すエビデンスは豊富にある。このような新規のアプローチは、治療法の普及、簡素化、そしておそらくは治療効果の増大に役立つであろう(Andersson, Cuijpers, Carlbring, Riper, & Hedman, 2014; Cuijpers, Kleiboer, Karyotaki, & Riper, 2017)。同時に、このようなインターネットを利用したアプローチは、データセキュリティ、倫理、法的責任、緊急時の専門家の利用可能性、および専門家の行動と報酬に関する既存のルールに従って、このような治療法を精神医療システムに統合するという新たな課題をもたらす。
以上のように、悪夢障害の病因、悪夢治療の改善、さまざまな集団への悪夢治療の適用、医療システムへの悪夢治療の統合に関して、まだ答えの出ていない研究課題が数多くある。これらの未解決の問題に早急に取り組むことで、悪夢の苦しみについての理解が深まり、多くの恵まれない人々への精神医療の提供が促進されるであろう。今回のコンセンサス・ペーパーが、今後も続く障害の本質を明らかにし、この分野で大いに必要とされる研究を促進する一助となることを願っている。
