Contents
A Comprehensive, Multi-Modal Strategy to Mitigate Alzheimer’s Disease Risk Factors Improves Aspects of Metabolism and Offsets Cognitive Decline in Individuals with Cognitive Impairment
www.ncbi.nlm.nih.gov/pmc/articles/PMC7369137/
Ginger Schechter、a Gajendra Kumar Azad、b、c Rammohan Rao、a、d Allison McKeany、a Matthew Matulaitis、a Denise M. Kalos、a and Brian K. Kennedyb、d、e、f、g、*.
要旨
背景
アルツハイマー病(AD)は、時間の経過とともに進行する慢性疾患である。いくつかの治療法が開発されているが、どれも病気の進行を実質的に変えたものはない。一つの説明として、この疾患は多因子性疾患であるということが挙げられる。
目的
Affirmativ Health Personal Therapeutic Program(PTPr)を用いて、主観的認知障害、軽度認知障害、早期ADと診断された患者の認知機能と代謝機能を、包括的で個別化されたプログラムで改善できるかどうかを調べた。
方法
35人の患者が血液サンプルとモントリオール認知評価(MoCA)スコアを提出し、摂取に関する質問に答えた。本人と介護者は4日間のイマージョンプログラムに参加し、個人治療計画(PTP)、臨床家との相談、PTPrとPTPの説明を受けた。
参加者は、PTPr後3ヵ月から12ヵ月の間に少なくとも1回、血液サンプルの繰り返し分析、ライフスタイルの選択、現在の薬やサプリメントに関する最新情報、MoCA検査などの遠隔モニタリングによるフォローアップを受けた。
結果
ベースラインと追跡検査を比較することにより、血糖値、インスリン値、ビタミンB12、D3、Eのレベルを含むいくつかの危険因子のスコアが、参加者プール全体、または特定の因子の測定値が正常範囲外であった個人において改善したことが明らかになった。
MoCAスコアは参加者プール全体で安定し、ベースライン時のスコアが24以下の人で有意に改善した。
結論
我々の知見は、ADの危険因子を軽減するように設計された包括的で個別化されたアプローチが、危険因子スコアを改善し、認知機能を安定させることができるという証拠を提供するものであり、より広範なプラセボ対照臨床試験の実施が必要である。
キーワード
アルツハイマー病、代謝、軽度認知障害、個別化治療、主観的認知障害
はじめに
数多くの試みとリソースの膨大なコミットメントにもかかわらず、アルツハイマー病(AD)の進行を逆転させるか、あるいは鈍化させるための努力は、せいぜいわずかに成功している[1、 2]。これは多くの潜在的な理由に起因している。例えば、ほとんどの臨床試験は、病理学的に不可逆的な状態にまで進行している可能性がある比較的後期の病状進行期の患者を対象に行われてきたと主張されている[3]。
別の考えでは、治療法開発の主要標的であるアミロイドβプラークとタウタングルは、疾患の主要な推進因子ではないかもしれない、あるいは少なくともそれらの治療的クリアランスは疾患の進行を鈍化させるには不十分であるということを示唆している[4、 5]。むしろ、アミロイドβオリゴマーが主な原因かもしれないし、さらに問題なのは、病気の進行におけるアミロイドプラークの役割が過大評価されている可能性があるということである[6]。
実際、慢性炎症や代謝の変化などの他の因子の役割が明らかになってきている[7、8]。これらの経路がどのようにプラークやタングルと結びついているのかは、まだ十分に解明されていない。また、診断方法の改善により、加齢に伴う認知症は予想以上に多様であることがわかってきている[9]。
ADに対する治療的アプローチでは、危険因子の役割や早期疾患における危険因子の軽減が臨床的な進行を遅らせる可能性があるという考えが十分に示されていない[10-14]。これまでのほとんどの研究では、1つの危険因子、例えば低ビタミンD3レベル[15]を標的とした単独の介入が検討されているが、効果はほとんどないか、あるいは全くない。
しかし、ADに関連する遺伝的および生活習慣の危険因子は多く存在し、各個人は一部のサブセットでしか危険因子の影響を受けていない[16]。したがって、1つの危険因子を変更しても、わずかな転帰しかもたらさない可能性があり、研究はこの概念を支持し始めている[17-20]。
我々は以下の仮説に基づいて、より全体的な概念を検証した。1) ADの危険因子が疾患進行に寄与している、2)罹患した個人は危険因子のユニークな組み合わせを持っている、3) 危険因子が相加的または相乗的に作用して疾患進行を促進している、という仮説に基づいて、より全体的な概念を検証してきた。
したがって、関連するアプローチ[21、 22]で示されているように、それぞれの罹患者に特有の危険因子を特定し、減衰させるための個別化戦略は、病気の進行に大きな影響を与えるだろう。ここでは、その概念のパイロットデータテストを提示し、AD進行の初期段階にある人々にこのアプローチを拡大するためのケースを作る。
方法
スタディデザインと参加者
参加者は、オンラインのデジタル広告、ラジオ番組、参加者の紹介を含むマーケティングキャンペーンによって募集された。プログラムに連絡すると、個人は、ベースラインのモントリオール認知評価(MoCA)テスト、および人口統計学、現在の医療、過去の医療および手術歴、現在の病歴、タバコ、アルコールおよびレクリエーション薬物の使用、現在の薬やサプリメントの使用、家族歴、社会的履歴、現在の生活環境、AD症状、精神的健康歴、食事パターン、アレルギーおよび体組成計データを含む質問票を含む摂取プロセスを使用してスクリーニングされた。
上記の摂取を行った後、当社の研究プロファイルを満たした参加者は、ADの発症に関連する様々なパラメータの遺伝子検査と血液検査を受けた(表1)。データはその後、当社独自のソフトウェア技術を用いて処理され、記憶喪失の潜在的な原因を特定する個別化治療計画(PTP)が作成された。その後、データは、医師と登録栄養士によってスクリーニングされ、ADとは無関係に記憶に影響を与える可能性のある医学的疾患や指標を特定した。いくつかのケースでは、医療上の注意を必要とする新しい臨床状態が特定された。有資格者は、Affirmativ Health Personal Therapeutic Program(PTPr)に参加するように招待された。
表1 血液パネルの構成要素
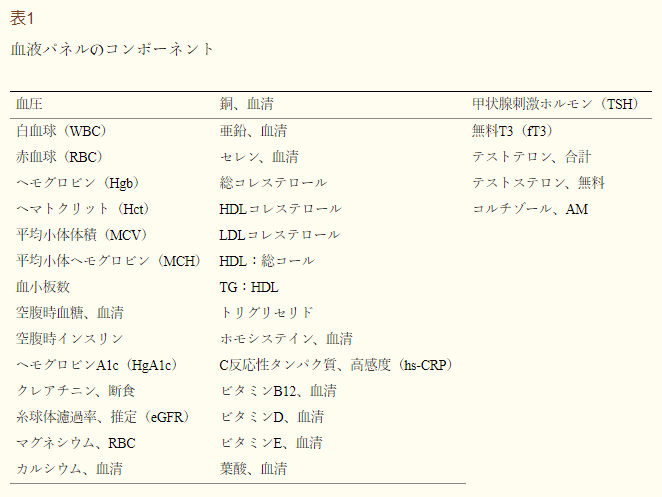
プログラム
PTPr(個別化治療計画)には、上記の事前テスト、PTPと4日間の対面式のイマージョンリトリート、継続的なコーチング、フォローアップテストが含まれてた。リトリートでは、参加者は、医師、栄養士、理学療法士、老人心理学者などを含む様々な専門家との個別化された交流を受けることができる。
さらに、参加者は、料理、ストレス管理、睡眠、運動プログラム、脳を刺激する活動の紹介など、健康的なライフスタイルの選択についても指導を受けます。最も重要なことは、参加者は、血液検査、遺伝子検査、認知検査の結果、個人の危険因子、認知の安定化および/または改善を達成するための最適な血液検査目標範囲(これまでに発表された研究で支持されている)を含むPTPの徹底的な見直しを受けることである。
また、これらのリスクを軽減するための戦略も提供される。前述したように、戦略には、個別化された食事と運動の推奨、ストレスの軽減、および必要かつ実行可能な場合にはサプリメントが含まれる。推奨されるすべてのサプリメント介入は広く使用されており、安全性の高いプロファイルを有している。
治療の一環として処方薬は推奨されなかった。4日間のリトリート終了時には、参加者には医師版のPTPが提供され、PTPに含まれている特定の臨床上の推奨事項でフォローアップが必要なものがあれば、その医師が責任を持ってプライマリケア医と話し合うことができる。
4日間のリトリート終了後、月に一度のフォローアップ・コーチング・コールが行われ、参加者のプログラムのアドヒアランスを支援し、アドヒアランス・データを収集する。フォローアップテストは、参加者が完全にアドヒアランスするまでにかかった期間に基づいて、3ヶ月または6ヶ月後に実施される。場合によっては、それ以降のテストも実施された。
統計分析
ヒトの介入サンプルから得られた様々なパラメータのデータセットを可視化するために、「折れ線グラフ」と「ボックスプロット」という表現方法を用いた。図に示すように、データセットのグループごとにボックスプロットを生成した。また、各ボックスプロットには、標準偏差とエラーバーを計算して追加した。
統計分析は、Graph Pad Prismソフトウェアを用いて行った。統計的有意性は、二尾の無対のStudentのt検定によって決定した。データは平均値±標準偏差(SD)で表され、0.05未満のp値は有意とみなされた。また、図1に示すように、MoCA前後の値の間の相関プロットを作成した。相関値(R2)を算出したところ、データポイントは正の直線的な関連性を示した(R2-0.87)。

図1
PTPrプログラムによる認知検査。A) プログラム開始後の参加者のMoCAテストスコアとベースラインおよび指示された時点(n = 26)。35名のうち、ベースラインとエンドポイントの両方のMoCAテストスコアを持つ参加者は26名のみである。B) 参加者プール全体(n = 26)でMoCAスコアが増加する傾向があるが、統計的有意性は得られなかった(p = 0.121、有意ではない)。統計解析には、参加者の最後のタイムポイントを使用した。C)ベースライン時のMoCAスコアが24未満の参加者では、統計学的に有意な増加が観察された(n = 9、p = 0.029)。
結果
合計35名がプログラムに登録され、初期テスト、4日間のリトリート、少なくとも1回のフォローアップ血液検査と認知機能検査を終え、有効性の統計的分析を可能にした。参加者には、いくつかのライフスタイルの変化とサプリメントを含む強固なプログラムの遵守が求められた。
アドヒアランスに関するフィードバックを作成したところ、アドヒアランスの平均スコアは69.67%、中央値は80%であった。参加者の統計を表2に示する。一般的に、参加者は高学歴で、太りすぎておらず、多くの場合、AD発症の主要な危険因子であるAPOE4対立遺伝子を少なくとも1つ持っている。
表2 勉強会の参加者
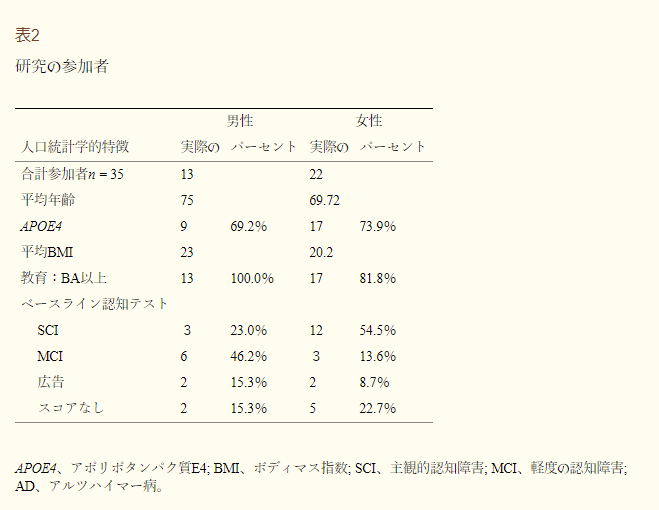
PTPrの第一の目標は、主観的認知機能障害(SCI)、軽度認知機能障害(MCI)、または早期ADを経験した後の認知パフォーマンスの維持または改善を支援することである。MoCAスコアは、ベースライン時とプログラム参加後の様々な時点で収集された。MCIとアルツハイマー病患者では認知パフォーマンスが着実に低下している。我々の仮説では、これはリスク因子を軽減する戦略によって予防できるか、あるいは逆転する可能性があるというものであった。
認知機能検査のフォローアップは、ほとんどのデータポイントがプログラム参加後3-6ヶ月の時点であったが、3ヶ月から18ヶ月の間に実施された(図1A)。統計的な妥当性を生み出すために、分析には最新のデータポイントを利用した。フォローアップ試験ではMoCAテストスコアに改善が見られたが、統計的有意性には至らなかった(p=0.12)(図1B)。
各サブフィグの参加者数およびp値の計算については、表3を参照のこと)。) 男女間の差は認められなかった。統計的有意性を達成するための制限の一つは、参加者の多くが治療開始時に高いMoCAスコアを持っていたことであり、これ は参加がSCI者にも開放されていたこともある。
治療開始時のMoCAスコアが低い参加者の変化を評価するために、スコアが24未満の人のデータを再分析した。この場合、有意な改善が観察された(p = 0.03)(図1C)。参加者数を増やし、プラセボ対照試験を含む追加試験を実施する必要があるが、これらの知見は、PTPrが認知機能の改善を遅らせたり、逆行させたりすることが期待できることを示している。
表3 各データ分析の参加者と統計的なp値
図 参加者数 p 値
1A 26 NA
1B 26 0.121
1C 9 0.029
2A 35 0.181
2B 20 0.015
2C 34 0.109
2D 23 0.0003
2E 20 0.000014
2F 16 0.012
2G 10 0.013
PTPrは、しばしば老化の他の慢性疾患にリンクされているこれらのパラメータを変更することができるかどうかをテストすることが可能になり、ADにリンクされている危険因子の範囲を相殺しようとしている。多くは本質的に代謝性であり、II型糖尿病、心血管疾患および他の条件を含む疾患にリンクされている[23-26]。
そこで、教育プログラムと介入によって個々のパラメータが改善されたかどうかを評価した。その結果、ベースライン時の空腹時血糖値が高かった参加者では、空腹時血糖値の有意な低下が観察された(>89 mg/dL; p = 0.02)(図2A、B)。
一般的に空腹時血糖値が高いとは、100mg/dl以上と定義されるが、我々は先行研究[27]に基づいて、より厳格な基準を選択した。89mg/dLを超える参加者には、食生活と運動に関する教育が、生姜とシナモンとともに推奨された [28-31]。125mg/dL以上の参加者には、ベルベリン500mgを1日2回、食事とともに投与し、その後8週間間隔でモニタリングを行うことが推奨された [32]。
空腹時インスリン値が高い人(4mU/L以上と定義)も、高血糖症の人に同様の推奨事項を採用した後、有意な改善が見られた(図2C、D)。同様に、ヘモグロビンA1CおよびHOMA-IR値も、ベースラインスコアが5.2%以上の参加者では低下した(図示せず)。これらの所見は、PTPrの参加者が代謝パラメータの改善を経験したことを示しており、したがって、他の加齢に関連した状態から保護されている可能性があることを示している。
図2 参加者間の危険因子レベルの変化

A)参加者プール全体の血糖値に変化はないが、(B)開始時に血糖値が上昇していた参加者の間で統計的に有意な減少が見られた。C)参加者プール全体の血中インスリン値に有意な変化はなかったが、(D)開始時に血糖値が上昇していた参加者の間で統計学的に有意な減少が見られた。プログラム開始時に血糖値が低かった参加者において、ビタミンD3(E)、E(F)、およびB12(G)のレベルが上昇した。
PTPrによって効果的に緩和された他の危険因子の中でも、ベースライン時に低値であると判断された参加者では、ビタミンD3、E、B12が統計的に増加していたことがわかった(図2E-G)。ベースライン値が500ng/dL未満の男性では、遊離テストステロン値も上昇していた(図示せず)。総テストステロン値は変化しなかった。
ベースライン時のレベルが低かった参加者では、亜鉛の直接補給により亜鉛の増加も観察された(図示せず)。コレステロールや炎症性マーカーを含む他のパラメータは、PTPrによる統計的に有意な影響を示さなかった。このことは、これらおよび他のリスク因子を効果的に軽減するプログラム戦略の改善が、認知パフォーマンスへのより大きな効果をもたらす可能性を示唆している。
考察
ADは500万人以上のアメリカ人に影響を与えている。慢性的で進行性の病気であるADは、最近の推定では、米国での死亡原因の第三位にリストされている。効果的な予防と治療法がない場合、将来の見通しは非常に懸念されている。1300 万人のアメリカ人と 1 億 6000 万人の市民が 2050 年までに AD を持っていると予測され、これはメディケアの破産の可能性を含む世界中の医療制度への影響についての懸念を提起する。過去10年間だけでも、何百ものADの臨床試験が数十億ドルもの費用をかけて実施されていたが、大きな成功はなかった[1、 2]。広範な資源が薬物試験に向けられており、これが、ADとその前身であるSCIとMCIのための薬物開発にほぼ独占的に焦点を当てるために取られたアプローチが最適なものであるかどうかを疑問視する声も聞かれるようになっている。最終的には、効果的な薬剤が開発されるかもしれないが、危険因子の治療などの他のアプローチは、その間に病気の発症と進行を減少させるかもしれない。
慢性疾患はライフコースを通じて増加する[33]。既知の疾患原因だけでなく、ライフスタイルの選択、ストレス、睡眠、栄養不足、メンタルヘルス、社会化、炎症、食生活など、疾患の進行や重症化に寄与する因子を対象とする多様なアプローチが必要であることを示唆している[22]。研究はADの単一の原因を治療することに焦点を当てていたが、今日まで医学的な治療法や単一の効果的な治療法はなく、複数の原因と解決策があることを示唆している。疾患の進行を予防、遅らせる、または逆行させる最も効果的な方法として、食事やその他のライフスタイルの変化を支持する証拠が増えてきている。また、最大の変化と改善をもたらすためには、個々の参加者に合わせた、より個別化された精密なアプローチが必要であることも研究で明らかにされている。
現在までのところ、ADの症状や進行の安定化や逆転をもたらした単一の介入はない。運動、ビタミン欠乏、ブドウ糖代謝などの単一の介入に注目した研究は数多くあるが、主に進行性で不可逆的であると考えられている病気に苦しんでいる人のための持続的な効果は報告されていない。
ADの遺伝的評価には、ADの最も強力な既知の予測因子であるAPOE遺伝子の検査が含まれることが多い[34]。APOE4遺伝子は、ADを含む人生後期の慢性炎症および慢性疾患と関連している[35]。しかし、ADの遺伝的素因があるとしても、生活様式因子が加齢に伴う認知健康の維持に強い役割を果たすという良い証拠がある。
公表されている研究を徹底的に検討した結果、私たちは、科学的に支持されている危険因子に対処するための包括的なアプローチを開発し、ADと認知症の領域における予防、回復力の向上、脳機能の安定化を促進するための介入として厳密に定義されている。最先端のテクノロジー(PTP)と対面でのコーチングやコンサルテーションを併用することで、マルチモーダルでパーソナライズされたアプローチが回復力の向上と最適な脳機能の回復を促進することを実証している。
PTPには、遺伝学、広範な血液パネル、生活習慣のデータが含まれており、認知機能の健康に関連する代謝因子や栄養素のレベルを評価する。認知機能の健康のために最適化されたレベルに到達することを目標としているため、PTPの実験室レベルの目標値は、標準的な実験室の範囲よりも厳しい場合がある。
認知機能の低下の潜在的な原因が早期に特定されればされるほど、それらを修正し、認知機能の健康を維持するために早期の措置を講じることができる。このことを知った上で、我々の第一の目標は、疾患の初期段階(SCI、MCI、および初期AD)にある参加者を募集することであった。ベースラインのMoCAスコアのデータは、8~30の範囲を示しており、大多数の患者は20~30の範囲でスコアを出していた。プログラムを受けた参加者は、ベースラインと追跡調査の間で安定していた。しかし、スコアが24未満の参加者は統計学的に有意な改善を示した(図1参照)。このことは、早期介入が重要であるという結論を支持するだけでなく、さらに疾患が進行しても改善が見られることを示唆している。また、36ヵ月間の追跡調査を延長した患者のデータポイントも含まれている。この患者は、この期間に短期および長期の進行性改善を示したことから、PTPrは短期および長期の両方の効果があることが示唆された。我々は、この長期参加者をプログラムの潜在的な効果を示す指標として挙げたが、もちろん、長期的な効果を確立するためには、より多くの研究が必要である。
我々の結果は、血糖代謝の影響が記憶力低下の改善と安定化に最も重要であることを明確に示している。空腹時血糖、空腹時インスリン、ヘモグロビンA1c、HOMAインスリン抵抗性スコアの4つのパラメータすべてが、PTPrで有意な改善を示した(図2参照)。ADは最近「III型糖尿病」としてラベル付けされているように、これは血糖値と認知機能低下への寄与に対処する必要性をさらに支持している[8、36]。
ビタミンD3、ビタミンE、ビタミンB12、亜鉛でも同様の結果が得られた(図2、図示せず)。これらのそれぞれが単独でAD [37-39]で研究されているが、どれも認知の改善や安定化との関連性が明確に示されていないことを考えると、我々の知見は治療へのマルチモーダルなアプローチを必要としている。より多くのデータが得られれば、一見別々の危険因子の間で、現在は知られていない特定のリンクを作ることも可能になるかもしれない。
PTPrの興味深い結果は、遊離テストステロンが改善されたという結果であった[40]。テストステロン補充の難しさと、この治療を安全かつ効果的に投与するために必要な綿密なモニタリングとしばしば専門化の必要性を考えると、参加者はテストステロン治療を追求するように求められなかった。我々は、胃腸系を含む参加者の代謝がPTPrの進行に伴って改善し始めると、ホルモンバランスの不均衡が自己修正されると推定している。
我々のアプローチでは、認知機能の低下に寄与することが知られている35以上の因子に注目しているが、我々の結果は、それらの因子の特定のものが他のものよりも影響を受けていることを示している。このことは、より多くのデータや研究が利用可能になるにつれて、我々のPTPrをさらに発展させる必要性があることを示している。また、このことは、ADに対する包括的な精密医療のアプローチに向かっていることを示唆している。さらに、本研究は、ワンサイズ・フィット・オールではなく、ワンサイズ・フィット・ワンに焦点を当て、関連するすべての危険因子を包括的に評価するアプローチに向けて、より多くの努力が必要であることを支持している。要約すると、このパイロット研究から得られた知見は、危険因子をターゲットとした個別化されたアプローチの潜在的な利点を強化し、さらなる検証を提供するために、より大規模なプラセボ対照研究を求めている。
