Contents
2020 Alzheimer’s disease facts and figures
alz-journals.onlinelibrary.wiley.com/doi/full/10.1002/alz.12068
要旨
本稿では、アルツハイマー病(AD)の発生率と有病率、死亡率と罹患率、ケアの利用と費用、介護者と社会への全体的な影響など、アルツハイマー病(AD)の公衆衛生への影響について解説している。特別報告書では、プライマリーケアに特に重点を置いて、米国で増加するアルツハイマー型認知症患者のケア需要を満たすための今後の課題を論じている。
今世紀半ばまでに、65歳以上のアルツハイマー型認知症患者は1,380万人に達すると予測されている。これは、現在の65歳以上のアルツハイマー型認知症の推定患者数580万人から急に増加したことを意味する。公式の死亡診断書は、データが入手できる最新の年である2018年にADによる死亡を122,019人記録しており、アルツハイマーは米国の死因の第6位、65歳以上のアメリカ人の死因の第5位となっている。
2000年から 2018年の間に、脳卒中、HIV、心臓病に起因する死亡は減少したが、報告されたアルツハイマー病による死亡は146.2%増加した。2019年には、1600万人以上の家族やその他の無給の介護者が、アルツハイマー病やその他の認知症の人に推定186億時間のケアを提供した。このケアは約2440億ドルと評価されているが、そのコストは、家族の介護者の感情的苦痛と負の精神的・肉体的健康のアウトカムのリスクの増加にまで及んでいる。
ADやその他の認知症を持つ65歳以上の受益者へのサービスに対するメディケアの一人当たりの平均支払い額は、これらの条件を持たない受益者への支払い額の3倍以上であり、メディケイドの支払い額は23倍以上である。認知症を持つ65歳以上の人々のヘルスケア、長期ケア、ホスピスサービスに対する2020年の支払い総額は3,050億ドルと推定されている。
アルツハイマー型認知症を患うアメリカ人の人口が増加するにつれ、その介護の負担も増加する。これらの課題は、認知症ケアの専門家の不足によって悪化しており、認知症患者へのケアを提供するプライマリ・ケア医師(PCP)の負担が増大している。
多くのPCPは、認知症ケアの責任を効果的に処理するための準備や訓練が不十分であると感じている。本報告書では、プライマリ・ケアにおける専門医の不足やトレーニングの課題に直面している中で、ケアの質を最大化するための提言が含まれている。
1 本報告書について
2020年アルツハイマー病の統計資料は、認知症の最も一般的な原因であるアルツハイマー病に関する米国のデータをまとめた統計資料である。データの解釈のための背景とコンテキストは、概要に含まれている。その他のセクションでは、有病率、死亡率、罹患率、介護、医療とサービスの利用とコストについて述べている。特別報告では、認知症ケアを提供する際のプライマリ・ケア医の経験、経験、トレーニング、態度、そして、アルツハイマー病やその他の認知症を抱える米国人の増加に対応するための将来的な準備を確保するための措置を検討している。
1.1 本報告書の具体的な内容
今年のアルツハイマー病の具体的な情報としては、以下のようなものがある。
- アルツハイマー病で起こる脳の変化。
- アルツハイマー型認知症の危険因子。
- アルツハイマー病の認知症を持つアメリカ人の数は、全国的に、各州のために。
- アルツハイマー型認知症を発症する生涯のリスク。
- 女性と男性のアルツハイマー型認知症と他の認知症の割合。
- 全国および各州のアルツハイマー病による死亡数、年齢別死亡率。
- 家族介護者数、提供された介護時間、無報酬介護の経済的価値の全国および各州別。
- 介護が介護者に与える影響。
- アルツハイマー型認知症やその他の認知症の人の介護にかかる全国的な費用(メディケアやメディケイドで支払われる費用とポケットから支払われる費用を含む)。
- 認知症の人のためのメディケアの支払いは、認知症のない人と比較して。
- 2050年に州が必要とする老年医の数
付録では、本報告書の統計を作成するために使用した情報源と方法を詳述している。
可能な場合には、アルツハイマー病に関する具体的な情報を提供しているが、それ以外の場合には、”Alzheimer’s or other dementias “のより一般的な情報を参照することもある。
2 アルツハイマー病の概要
アルツハイマー病は、冠動脈疾患が心臓病の一種であるように、脳の病気の一種である。また、退行性の病気であり、時間の経過とともに悪化していく。アルツハイマー病は、症状が出る20年以上前から発症すると考えられている1-6。脳の変化が何年も続いて初めて、記憶力の低下や言語障害などの顕著な症状が現れる。症状は、思考、学習、記憶(認知機能)に関わる脳の一部の神経細胞(ニューロン)が損傷したり、破壊されたりすることで起こる。病気が進行すると、脳の他の部分の神経細胞が損傷したり破壊されたりする。最終的には、歩行や嚥下などの基本的な身体機能を担う脳の一部の神経細胞が障害を受けます。寝たきり状態になり、24時間体制での介護が必要になる。アルツハイマー病は最終的には致命的である。
2.1 アルツハイマー病か認知症か?
アルツハイマー病と認知症の違いは何なのであろうか?
認知症とは、特定の症状群の総称である。認知症の特徴的な症状は、記憶力、言語、問題解決能力、その他の思考能力の障害であり、日常生活の遂行能力に影響を与える。認知症には多くの原因がある(表1参照)。認知症の原因の中で最も多いのはアルツハイマー病である。
表1. 認知症の一般的な原因と関連する特徴
原因/特徴
アルツハイマー病
アルツハイマー病は認知症の最も一般的な原因であり、推定60%から80%を占めている。最近の大規模な剖検調査では、アルツハイマー型認知症の人の半数以上が、アルツハイマー型認知症の脳の変化(病理)に加えて、脳血管疾患やレビー小体型疾患などの認知症の原因となる1つ以上の脳の変化を持っていることが明らかになっている。これを混合病態といい、生活の中で認識されると混合型認知症と呼ばれる。
最近の会話や名前、出来事を覚えていないことが初期の臨床症状であることが多く、無気力や抑うつも初期の症状であることが多い。後期症状としては、コミュニケーション障害、見当識障害、混乱、判断力の低下、行動の変化、最終的には会話、嚥下、歩行の困難などが挙げられる。
アルツハイマー病の特徴的な病態は、脳内の神経細胞の外側にβアミロイドというタンパク質断片(プラーク)が蓄積し、神経細胞の内側にはタウというタンパク質のねじれた鎖(もつれ)が蓄積することである。これらの変化は、神経細胞の死や脳組織の損傷を伴う。アルツハイマー病はゆっくりと進行する脳の病気で、症状が出る何年も前に発症する。
脳血管疾患
脳血管障害とは、脳の血管が損傷したり、血液や酸素、栄養が十分に供給されずに脳組織が傷ついたりすることをいいます。脳に脳血管障害が認められる認知症の人は、血管性認知症と言われている。しかし、認知症の人の多くは脳血管疾患とアルツハイマー病の脳の変化を呈しているため、混合病態としての認知症が多いです9,10。
判断力の低下や判断力の低下、計画性や整理能力の低下が初期症状として現れることがあるが、特に他の原因による認知症の脳の変化がある場合には、記憶力にも影響が出ることがある。認知機能の変化に加えて、血管性認知症の人は運動機能、特に歩行の遅さやバランスの悪さにも悩まされる。
血管性認知症は、血管の閉塞や損傷により、脳内に死滅した組織や出血が生じることが最も一般的である。脳の損傷の場所、数、大きさによって、認知症になるかどうかが決まり、その人の思考や身体機能にどのような影響を与えるかが決まる。
レビー小体症
レビー小体とは、神経細胞内のα-シヌクレインというタンパク質の異常な集合体(塊)のことである。レビー小体が大脳皮質と呼ばれる脳の一部に発生すると、認知症(レビー小体型認知症またはDLBと呼ばれる)になることがある。DLBの人は、アルツハイマー型認知症によくみられる症状の一部を呈するが、初期症状や初期症状として、睡眠障害や幻覚、視覚障害などの症状を呈することが多くなる。これらの症状は、重大な記憶障害がない場合にも起こるが、他の原因による認知症の脳の変化がある場合には特に、記憶喪失が起こることが多い。
認知症患者の約5%はDLBのみの証拠を示すが、DLBを有する人の多くはアルツハイマー病の病理学的特徴も併せ持っている。
前頭側頭葉変性症(FTLD)
FTLDには、行動変容型FTLD、原発性進行性失語症、ピック病、皮質基底変性症、進行性上核麻痺などの認知症が含まれる。
典型的な初期症状としては、人格や行動の著しい変化、および/または言語の生産や理解の困難が挙げられる。アルツハイマー病とは異なり、記憶は通常、疾患の初期段階では免れている。
脳の前部(前頭葉)と側部(側頭葉)の神経細胞が特に影響を受け、これらの領域が著しく萎縮(縮小)する。さらに、大脳皮質の上層部は通常、軟らかく海綿状になり、異常なタンパク質の包接体(通常、タウタンパク質や超活性応答DNA結合タンパク質であるTDP-43)を有している。
FTLDの症状はアルツハイマー病と同様に65歳以上で発症することがあるが、ほとんどの人は若い年齢で発症する。11 システマティックレビューでは、65歳以上の人を対象とした研究では認知症症例の約3%、65歳未満の人に限定した研究では認知症症例の約10%をFTLDが占めているとされている12。
パーキンソン病(PD)
運動障害(動きの遅さ、硬直、振戦、歩行の変化)はPDの一般的な症状である。認知症状は、運動症状の直前に、または疾患の後期に発症する。
PDでは、α-シヌクレインの集合体が黒質と呼ばれる脳の深部に出現する。この凝集体は、ドーパミンを産生する神経細胞の変性を引き起こすと考えられている13。
PDが進行すると、大脳皮質にα-シヌクレインが蓄積して二次的に認知症になることが多い(レビー小体型認知症に似ている)。
海馬硬化症(HS)
HSとは、脳の海馬の組織が硬くなることである。海馬は記憶の形成に重要な役割を果たしている。HSの最も顕著な症状は記憶喪失であり、アルツハイマー病と誤診されることもある。
HSの脳の変化は、しばしばTDP-43と呼ばれるタンパク質の誤った形態の蓄積を伴う。
HSは、85歳以上の「高齢者」に多くみられる認知症の原因である。
混合病態
認知症の原因が2つ以上の脳の変化を示す場合、混合型認知症が原因と考えられている。これらの病態が生活の中で認知症の症状を引き起こす場合、その人は混合型認知症と言われている。
アルツハイマー病センターで調査された認知症患者の50%以上が複数の認知症原因の病理学的証拠を持っている10。
2.2 アルツハイマー病に伴う脳の変化
健康な成人の脳には約1,000億個のニューロンがあり、それぞれのニューロンは長い枝分かれした延長を持っている。これらの延長線によって、個々のニューロンは他のニューロンと接続を形成することができる。シナプスと呼ばれるこのような接続では、情報が化学物質の微小なバーストで流れ、あるニューロンから放出され、別のニューロンによって検出される。脳には約100兆個のシナプスが存在する。シナプスがあることで、信号が脳の神経回路を高速で移動し、記憶、思考、感覚、感情、運動、技能などの細胞の基礎が作られているのである。
βアミロイドというタンパク質の断片(βアミロイド斑と呼ばれる)の神経細胞外への蓄積と、異常な形のタウというタンパク質の神経細胞内への蓄積(タウのもつれと呼ばれる)は、アルツハイマー病に関連したいくつかの脳の変化のうちの2つである。
プラークやオリゴマーと呼ばれるβアミロイドの小さな蓄積は、シナプスにおける神経細胞間のコミュニケーションを阻害することで、神経細胞の損傷や死(神経変性)に寄与すると考えられている。タウのもつれは、神経細胞内での栄養素やその他の必須分子の輸送を阻害する。事象の完全なシーケンスは明らかにされていないが、βアミロイドは異常なタウの前に蓄積を開始する可能性があり、βアミロイド蓄積の増加はその後のタウの増加と関連している。
その他の脳の変化としては、炎症や萎縮がある。有毒なβアミロイドやタウタンパク質の存在は、ミクログリアと呼ばれる脳内の免疫系細胞を活性化させると考えられている。ミクログリアは、死んで死にかけている細胞から有毒なタンパク質だけでなく、広範囲の破片を除去しようとする。ミクログリアがクリアする必要があるすべてのものに追いつけなくなると、慢性的な炎症が起こることがある。脳の萎縮、または収縮は、細胞の損失のために発生する。正常な脳機能は、さらにブドウ糖、その主な燃料を代謝する脳の能力の低下によってアルツハイマー病で損なわれている。
アルツハイマー病の原因となるまれな遺伝子変異を持つ人々を対象とした研究5では、症状が発現する22年前から脳内のβアミロイドのレベルが有意に上昇していることが明らかになった(これらの遺伝子変異を持つ人々は、通常、アルツハイマー病の親と同じか、ほぼ同じ年齢で症状が発現する)。ブドウ糖代謝の低下は予想される症状の18年前から始まり、脳の萎縮は予想される症状の13年前から始まった。
アルツハイマー病研究の分野では、病気に伴う脳の変化や病気の進行の仕方を理解する上で長年にわたって大きな成果を上げてきたが、これまでの研究の多くは、黒人/アフリカ系アメリカ人、ヒスパニック/ラテン系アメリカ人、アジア系アメリカ人/太平洋諸島人、ネイティブアメリカンの数が十分に含まれておらず、米国の人口を代表するものとなっていないことに注意することが重要である。さらに、いくつかの研究16-19では、黒人/アフリカ系アメリカ人やヒスパニック/ラテン系アメリカ人がアルツハイマー病のリスクが高いことが明らかになっているため、これらの人々の数が十分でないことは、これらの健康格差を理解するための厳密な研究の実施を妨げている。アルツハイマー病の包括的な理解を得るためには、十分な研究が必要である。
2.3 アルツハイマー病の連続性
アルツハイマー病の進行は、罹患した本人には気づかれない脳の変化から、記憶力に問題が生じ、最終的には身体的な障害を引き起こす脳の変化までをアルツハイマー病連続体と呼んでいる。
この連続体には、前臨床アルツハイマー病、アルツハイマー病による軽度認知障害(MCIアルツハイマー病による認知症の3つの段階がある(図1参照)20-23。
図1
アルツハイマー病(AD)の連続体。*MCIは軽度認知障害の頭文字をとったものである。
連続体は前臨床アルツハイマー病から始まり、重度のアルツハイマー病で終わることがわかっているが、連続体の各部分でどのくらいの期間を過ごすかは個人差がある。連続体の各段階の長さは、年齢、遺伝、性別、その他の要因の影響を受けている。
2.3.1 前臨床アルツハイマー病
この段階では、アルツハイマー病の初期徴候(バイオマーカー)を示す測定可能な脳の変化が見られるが、記憶喪失などの症状はまだ現れていない。測定可能な脳の変化の例としては、ポジトロン断層撮影(PET)スキャンや脳脊髄液(脳脊髄液)分析で示されるβアミロイドの異常値、PETスキャンで示されるブドウ糖代謝の低下などが挙げられる。アルツハイマー病の初期変化が起こると、脳はそれを補い、正常な機能を維持することができるようになる。
研究では、アルツハイマー病の初期の脳の変化を特定するためのツールや専門知識を持っているが、病院や医師のオフィス、その他の臨床現場で広く使用されるようになる前に、ツールの精度を微調整するための追加の研究が必要である。例えば、死亡時にβアミロイド斑を有していても、生活の中では記憶力や思考力に問題がなかった人もいる。
2.3.2 アルツハイマー病によるMCI
アルツハイマー病によるMCIを有する人々は、アルツハイマー病の脳の変化(例えば、βアミロイドの異常なレベル)に加えて、記憶や思考の微妙な問題を持つバイオマーカーの証拠を持っている。これらの認知機能の問題は、家族や友人には気づかれても、他の人には気づかれず、日常生活に支障をきたすことはない。思考能力の軽度の変化は、脳がもはやアルツハイマー病によって引き起こされる神経細胞の損傷と死を補うことができないときに発生する。
27 別の研究では、MCI患者の32%が5年以内にアルツハイマー型認知症を発症したという結果が出ている。しかし、MCIが正常な認知状態に戻る人もいれば、安定した状態が続く人もいる。MCIのどの患者がアルツハイマー病や他の認知症を発症しやすいかを特定することは、現在の研究の大きな目標となっている。
2.3.3 アルツハイマー病による認知症
アルツハイマー病による認知症は、アルツハイマー病に関連した脳の変化の証拠とともに、日常生活の機能を損なう顕著な記憶、思考、または行動の症状によって特徴づけられる。アルツハイマー型認知症の人は、数年の間に変化する複数の症状を経験する。これらの症状は、脳のさまざまな部分の神経細胞の損傷の程度を反映している。認知症の症状が軽度から中等度、重度へと進むペースは人によって異なる。
軽度のアルツハイマー型認知症
アルツハイマー型認知症の軽度の段階では、多くの人は多くの分野で自立して機能することができるが、自立性を最大限に高め、安全性を保つためには、いくつかの活動の支援が必要になる可能性がある。彼らはまだ運転したり、仕事をしたり、好きな活動に参加したりすることができるかもしれない。
中等度アルツハイマー型認知症
アルツハイマー型認知症の中等度の段階では、最長の段階であることが多く、コミュニケーションや日常生活動作(入浴や着替えなど)が困難になったり、失禁したり、不審感や焦燥感などの性格や行動の変化が見られるようになる。
重度のアルツハイマー型認知症
重度のアルツハイマー型認知症の段階では、日常生活動作の支援が必要となり、24時間体制での介護が必要となる可能性が高い。アルツハイマー病の身体的な健康への影響は、この段階では特に明らかになる。運動に関与する脳の領域への損傷のために、個人が寝たきりになる。寝たきりになると、血栓、皮膚感染症、敗血症などの状態に陥りやすくなり、全身の炎症を誘発して臓器不全に陥ることがある。嚥下を制御する脳の領域が損傷すると、飲食が困難になる。その結果、食物を食道(食物管)ではなく気管(気管)に飲み込んでしまうことがある。このため、食べ物の粒子が肺に堆積し、肺感染症を引き起こす可能性がある。このような感染症は誤嚥性肺炎と呼ばれ、多くのアルツハイマー病患者の死因となっている(「死亡率と罹患率」の項を参照)。
2.3.4 認知症様症状が認知症でない場合
アルツハイマー病や他の変性脳疾患のような進行性の脳の変化を伴わずに、認知症様の症状を呈する人がいることに注意が必要である。認知症様症状の原因としては、うつ病、未治療の睡眠時無呼吸、せん妄、薬の副作用、ライム病、甲状腺の問題、特定のビタミン欠乏、過度の飲酒などが挙げられる。アルツハイマー病や他の認知症とは異なり、これらの症状は治療によって元に戻ることが多い。症状の原因を判断するために医療専門家に相談することは、身体的にも精神的にも幸福になるために非常に重要である。
通常の加齢に伴う認知機能の変化とアルツハイマー型認知症の認知機能の変化には微妙な違いがある(表2参照)。認知機能の変化を経験した人は、その変化が年齢的に正常なものなのか、可逆的なものなのか、アルツハイマー型認知症や他の認知症の症状なのかを判断するために、医学的な助けを求めるべきである。認知機能の評価を含むメディケア年次健康診断は、65歳以上の人にとって、認知機能の変化について医師と話し合う好機である。
表2. アルツハイマー病やその他の認知症の兆候と典型的な年齢関連の変化*との比較
アルツハイマー病やその他の認知症の兆候 /典型的な加齢に伴う変化
- 日常生活に支障をきたす記憶障害 アルツハイマー病の最も一般的な徴候の一つは、記憶喪失であり、特に最近学んだ情報を忘れることである。その他には、重要な日付やイベントを忘れたり、同じ情報を何度も聞いたり、ますます自分で処理するために使用されていたもののためのメモリエイド(例えば、リマインダーノートや電子機器など)や家族に頼る必要がある。 名前や予定を忘れてしまうことがあるが、後で思い出してしまうこともある。
- 計画を立てたり、問題を解決したりすることへの挑戦。計画を立てたり、計画に従ったり、数字を使って作業したりする能力に変化を感じる人もいる。慣れ親しんだレシピに従ったり、毎月の請求書の記録をつけたり、お釣りを数えたりするのに苦労することがあるかもしれない。集中力に難があり、以前よりも時間がかかることがある。 小切手帳のバランスを取る際に、時々ミスをしてしまう。
- 家で、仕事で、または余暇で、慣れ親しんだ作業を完了することが困難になる。アルツハイマー型認知症の人は、日常のタスクを完了するのが難しいことが多い。時には、慣れ親しんだ場所への車での移動、職場での予算管理、好きなゲームのルールを覚えることが困難になることもある。 時には、電子レンジの設定を使用したり、テレビ番組を録画したりするのに助けを必要とすることもある。
- 時間や場所の混乱。アルツハイマー病の人は、日付、季節、時間の経過のトラックを失うことができる。それがすぐに起こっていない場合、彼らは何かを理解するのに苦労することがある。時々、彼らはどこにいるか、またはどのようにしてそこに着いたかを忘れてしまう。 週の日について混乱を得るが、後でそれを考え出す。
- 視覚イメージや空間関係を理解するのに問題がある。何人かの人々のために、ビジョンの問題を持つことは、アルツハイマー病の兆候である。彼らは、距離を判断し、運転に問題が発生する可能性がある色やコントラストを決定し、困難な読書を持っている可能性がある。 白内障、緑内障、加齢に伴う黄斑変性症に関連した視力の変化。
- 話すことや書くことにおける言葉の新たな問題。アルツハイマー型認知症の人は、会話についていけるか、会話に参加できないことがある。会話の途中で止まってしまったり、会話を続ける方法がわからなくなったり、繰り返してしまうことがある。彼らは、語彙に苦労することがある、右の単語を見つける問題を持っているか、または間違った名前(例えば、時計を「手の時計」と呼ぶ)で物事を呼び出すことがある。 正しい言葉を見つけるのに苦労することもある。
- 物を置き忘れたり、ステップを辿る能力を失ったりする。アルツハイマー型認知症の人は、いつもと違う場所に物を置いたり、物をなくしたりして、再びそれらを見つけるために自分のステップをさかのぼって行くことができなくなることがある。時には、盗みをしているのではないかと他人を非難することもある。このようなことは、時間が経つにつれてより頻繁に起こるかもしれない。 時々、物を置き忘れてしまい、それを見つけるために足取りを辿ることがある。
- 判断力の低下または低下。アルツハイマー型認知症の人は、判断力や意思決定の変化を経験することがある。例えば、お金を扱うときに判断力が低下したり、テレマーケティング業者に多額のお金を渡したりすることがある。身だしなみを整えたり、自分自身を清潔に保つことにあまり注意を払わないかもしれない。 時々悪い決定をすること。
- 仕事や社会活動からの撤退。アルツハイマー病の人は、趣味、社会活動、仕事のプロジェクトやスポーツから自分自身を削除することがある。彼らは、お気に入りのスポーツ チームに追いつくか、またはお気に入りの趣味を完了する方法を覚えているトラブルがある。また、経験した変化のために社交的になることを避けてしまうこともある。 時々、仕事、家族、社会的義務に疲れを感じる。
- 気分や性格の変化。気分とアルツハイマー病の人々 の人格を変更することができる。彼らは、混乱、疑わしい、落ち込んで、恐怖や不安になることができる。彼らは簡単に彼らの快適なゾーンから出ている場所では、自宅で、職場で、友人と一緒に、または場所で動揺することがある。 物事をするための非常に特定の方法を開発し、ルーチンが中断されたときに過敏になる。
*アルツハイマー病の症状についての詳細は、alz.org/10signsを見てほしい。
2.4 アルツハイマー病による認知症の診断
アルツハイマー病による認知症の検査は一つではない。その代わりに、医師は(多くの場合、神経内科医、神経心理学者、老年医、老年精神科医などの専門家の助けを借りて)診断を下すために様々なアプローチやツールを使用する。それらには以下のようなものがある。
- 精神科の病歴や認知・行動の変化の履歴など、個人の病歴や家族歴を入手する。
- 思考技能や行動の変化についての意見を提供するために家族に依頼する。
- 問題解決、記憶、その他の認知検査、身体検査、神経学的検査を実施する。
- 血液検査や脳の画像検査を行い、腫瘍や特定のビタミン不足など、認知症症状の原因となる可能性のあるものを除外する。
- ある状況では、脳のPET画像を用いて、アルツハイマー病の特徴であるβアミロイドが高値かどうかを調べる。
30 状況によっては、腰椎穿刺で脳脊髄液中のβアミロイドとある種のタウのレベルを測定し、正常値であればアルツハイマー病は認知症の原因ではないことを示唆している。
認知症かどうかはほとんどの場合、医師が判断できるが、正確な原因を特定するのは困難である。アルツハイマー病は認知症の最も一般的な原因であるが、他の原因もある32, 33 。表1に示すように、認知症の原因によって症状パターンや脳の異常が異なる。認知症の多くの人は、複数の認知症原因に関連した脳の変化を持っている9, 34-38。一部の研究9,10では、アルツハイマー型認知症の脳の変化を持つ人の大多数は、剖検で第二の原因の認知症の脳の変化も持つと報告している。
有病率の項で述べたように、アルツハイマー病やその他の認知症の診断基準を満たすであろう患者の多くは医師の診断を受けておらず、39-42,メディケアの請求記録にアルツハイマー病やその他の認知症の診断を受けているメディケア受給者の半数以下が診断を受けたと報告している(認知障害のために回答できない場合は介護者が報告している)43-46。また、認知症の特定の原因に応じた適切な治療やフォローアップケアを受けるために、正確な診断を受けることも重要である。
2.5 アルツハイマー型認知症の治療
2.5.1 薬物療法
現在、アルツハイマー型認知症のために利用可能な薬理学的治療法(薬)のどれも、アルツハイマー型認知症の症状を遅らせたり、アルツハイマー型認知症の症状を引き起こし、この病気を致命的なものにするニューロンの損傷や破壊を止めたりするものではない。米国食品医薬品局(FDA)は、アルツハイマー病の治療薬として、リバスチグミン、ガランタミン、ドネペジル、メマンチン、メマンチンとドネペジルを組み合わせた5つの薬を承認している。メマンチンを除くこれらの薬は、脳内の神経伝達物質と呼ばれる化学物質の量を増やすことで一時的に認知症状を改善する。メマンチンは、神経細胞にダメージを与える過剰な刺激から脳内の特定の受容体をブロックする。これらの薬の効果には個人差があり、効果が持続する期間も限られている。
アルツハイマー型認知症の中等度から重度の段階で発症する可能性のある行動症状や精神症状を治療するために、FDAによって特に承認されている薬はない。非薬物療法が成功せず、これらの症状が本人や他の人に害を及ぼす可能性がある場合、医師は他の疾患を持つ人の同様の症状に対して承認されている薬を処方することができる。抗精神病薬と呼ばれる薬の一種で、幻覚や攻撃性、焦燥感などを治療するために処方されることがある。しかし、いくつかの抗精神病薬が認知症患者の脳卒中や死亡のリスクを高めることが研究で示されている47, 48 抗精神病薬を使用するかどうかは、細心の注意を払って検討しなければならない。FDAは、抗精神病薬の製造業者に対し、抗精神病薬のリスクについての「ブラックボックス警告」と、認知症症状の治療薬として承認されていないことの注意喚起を表示するように命じている。
アルツハイマー病の効果的な治療法の開発が難しいことには、多くの要因が関係している。これらの要因には、臨床研究に十分な数の被験者や十分に多様な被験者を採用するペースが遅いこと、アルツハイマー病の原因となる脳内の正確な分子変化や生物学的プロセスに関する知識のギャップ、治験薬が病気の進行に影響を与えるかどうかを観察するのに比較的長い時間が必要であることなどがある。
研究者らは、アルツハイマー病の進行を遅らせたり止めたりして脳機能を維持するための将来の治療法は、アルツハイマー病によるMCIや前臨床アルツハイマー病の段階で、病気の進行の早い段階で投与することが最も効果的であると考えている。バイオマーカー検査は、これらの段階にある患者を特定するために不可欠であり、治療が可能になったときに治療を受けるべきである。また、バイオマーカーは治療の効果をモニターするためにも重要である。バイオマーカー検査はすでに医薬品開発において重要な役割を果たしているが、その理由は、バイオマーカー検査を行うことで、ある医薬品が影響を及ぼすように設計されたアルツハイマー病の脳内変化を有する患者のみを臨床試験に参加させることができるからである49 。
2.5.2 非薬物療法
非薬物療法とは、薬物を使用しない治療法のことである。アルツハイマー型認知症の人には、認知機能の維持や改善、生活の質の向上、日常生活動作の能力の向上などを目的として使用されることが多い。また、うつ病、無気力、徘徊、睡眠障害、焦燥感、攻撃性などの行動症状を軽減する目的で使用されることもある。最近の認知症患者の焦燥感や攻撃性に対する非薬理学的治療のレビューと分析では、非薬理学的介入の方が、薬理学的介入よりも攻撃性や焦燥感を軽減するのに有効であると結論づけられている51。現在の薬理学的療法と同様に、非薬理学的療法では、アルツハイマー病の症状を引き起こすニューロンの損傷や破壊を遅らせたり、止めたりすることはできず、アルツハイマー病を致命的なものにしてしまう。
非薬物療法の有効性を判断するのは、試験された治療法の数が多いこと、治療目的が多様であること(QOLの改善から特定の症状の改善まで認知症のステージが多様であること(軽度から中等度から重度まで混合型認知症が蔓延していることから特定の試験参加者の認知症のタイプが多様であること、個々の治療を実施するための標準的な方法がないことなどの理由から困難な場合がある。このような複数の要因を考慮する必要があるため、非薬物療法をグループ化して比較することは困難である。
それにもかかわらず、研究者は非薬物療法の複数の研究からデータをプールして、その潜在的な有効性についての洞察を提供している。
メタアナリシス52では、有酸素運動と有酸素運動と非有酸素運動の組み合わせがアルツハイマー型認知症患者の認知機能にプラスの効果があることが示されている。システマティックレビュー53では、運動は認知機能全体にプラスの効果があり、アルツハイマー型認知症の人の認知機能低下の速度を遅らせる可能性があることが示されている。
また、システマティックレビュー54では、認知刺激が認知機能とアルツハイマー型認知症の人の幸福度のいくつかの側面に有益な効果があることが報告されている。別のシステマティックレビュー55では、認知刺激は軽度から中等度のアルツハイマー型認知症患者のうつ病テストのスコア改善と関連していることが報告されている。2019年のシステマティックレビューの要約56では、認知刺激、音楽をベースとした治療、心理的治療(例えば、認知行動療法)が認知症の人のうつ病、不安、生活の質を改善したと報告されている。
軽度から中等度の認知症の人に対する認知訓練のシステマティックレビュー57の2019年の要約では、認知訓練は認知全体に少なくとも数ヶ月間持続する可能性のある何らかの効果を示す可能性があることが示されている。
2.6 アルツハイマー型認知症の積極的管理
研究では、アルツハイマー病やその他の認知症を積極的に管理することで、患 者やその介護者の生活の質が向上することが一貫して示されている58-60。
- 積極的な管理には以下が含まれる:利用可能な治療法の適切な利用。
- 積極的な管理には以下のようなものがある:利用可能な治療法を適切に利用すること。
- 介護者の日常生活を管理するための効果的な訓練を家族介護者に提供する。
- 医師、他の医療専門家、および一般の介護者の間でのケアの調整。
- 認知症の人にとって意味のある活動に参加し、生活に目的をもたらすこと。
- 認知症の人とつながる機会を持つこと。支援グループや支援サービスなどがその一例である。
- 認知症についての教育を受けること。
- 将来のための計画を立てること。
アルツハイマー病についての詳細や、アルツハイマー病との生活や介護者としての実践的な情報については、alz.orgを見てほしい。
2.7 アルツハイマー型認知症の危険因子
アルツハイマー型認知症を発症する人の大半は65歳以上である。これは後期発症型アルツハイマーと呼ばれている。専門家は、アルツハイマー病は、他の一般的な慢性疾患と同様に、単一の原因ではなく、複数の要因の結果として発症すると考えている。例外として、遺伝子の変化が原因でリスクが高まる場合もある。
2.7.1 年齢、遺伝、家族歴
後期型アルツハイマー病の最大の危険因子は、高齢61,62,遺伝63,64,アルツハイマー病の家族歴65-68である。
年齢
遺伝学
研究者たちは、アルツハイマー病のリスクを高めるいくつかの遺伝子を発見した。アポリポ蛋白質-e4 (APOE-e4) 遺伝子は、遅発性アルツハイマー病のリスクに最も強い影響を与える遺伝子である。APOE-e4 は、血流中のコレステロールを輸送するタンパク質の設計図を提供する。誰もが APOE 遺伝子 ・e2,e3 または e4 ・の 3 つのフォーム (対立遺伝子) の 1 つを継承する各親から 6 つの可能な APOE ペアになる:
e2/e2,e2/e3,e2/e4,e3/e3,e3/e4,e4/e4。研究者たちは、人種や民族によってこれらのペアの頻度に違いがあることを発見している。例えば、ヨーロッパ系アメリカ人よりも黒人/アフリカ系アメリカ人の方が、e4対立遺伝子のコピーを少なくとも1つ持っている割合が高いというデータがある(表3参照)。
表3. 特定のAPOEペアを有する黒人/アフリカ系米国人および欧州系米国人の割合
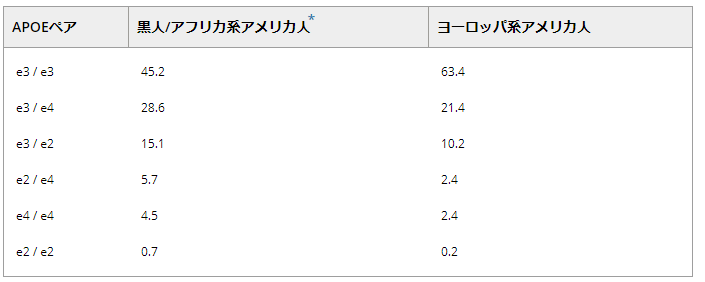
Rajan er al)。70 のデータを基に作成。
* 四捨五入のため、パーセンテージの合計は100ではない。
APOEのe4型を持つことは、e3型を持つことに比べてアルツハイマー病発症のリスクを高めるが、個人がアルツハイマー病を発症することを保証するものではない。e2型を持つ人はe3型を持つ人に比べてリスクが減少する可能性がある。e4型のコピーを1つ持っている人は、e3型のコピーを2つ持っている人に比べてアルツハイマー病の発症リスクが約3倍であるのに対し、e4型のコピーを2つ持っている人は8倍から12倍のリスクがあるとされている73-75。77 米国でアルツハイマー病と診断された人々のe4型の頻度を記述した20の論文を含むメタアナリシスでは、56%がAPOE-e4遺伝子を1コピー、11%がAPOE-e4遺伝子を2コピー保有していることが明らかになった。
しかし、黒人/アフリカ系アメリカ人のAPOEの状態に基づくアルツハイマー病リスクの研究では、一貫性のない結果が得られている。例えば、黒人/アフリカ系アメリカ人ではe4対立遺伝子を持っていてもリスクは増加しないとする研究もある71, 72, 80 が、他の研究では有意にリスクが増加するとする研究もある81, 82。
家族歴
アルツハイマー型認知症の家族歴は、個人がアルツハイマー型認知症を発症するために必要なものではない。しかし、親や兄弟(一親等親族)にアルツハイマー型認知症の患者がいる場合は、一親等親族にアルツハイマー型認知症の患者がいない場合に比べて発症する可能性が高い65, 73。大規模な人口ベースの研究では、親に認知症の人がいると、APOE-e4などの既知の遺伝的危険因子とは無関係にリスクが高まることが明らかにされている。
2.7.2 修正可能な危険因子
年齢や遺伝、家族歴は変えられないが、他の危険因子を変えたり、修正したりすることで、認知機能低下や認知症のリスクを減らすことができる。
2019年、世界保健機関(WHO)は、認知機能低下と認知症のリスクを減らすための推奨事項84を発表した。WHOは、認知機能低下や認知症のリスクを減らすために、身体活動、禁煙、高血圧や糖尿病の管理を強く推奨している。修正可能な危険因子の認知機能低下と認知症への影響に関するエビデンスの状況を評価した報告書85では、定期的な身体活動と心血管系危険因子(特に糖尿病、肥満、喫煙、高血圧)の管理が認知機能低下のリスク低下と関連しており、認知症のリスク低下と関連している可能性があることを、集団ベースの観点から十分に強いエビデンスがあると結論づけている。また、健康的な食生活、生涯学習、認知トレーニングが認知機能低下リスクの低下と関連しているという十分に強いエビデンスがあると結論づけている。全米医学アカデミー(旧医学研究所)の報告書では、認知機能低下の修正可能なリスク因子に関するエビデンスを検討し、同様の結論に達している。
認知機能低下や認知症の「リスクを減らす」ことは、認知機能低下や認知症を予防することと同義ではないことに注意することが重要である。リスクを減らすために対策を講じた人は、認知症を発症する可能性はあるが、認知症を発症する可能性が低くなったり、リスクを減らすために対策を講じなかった場合に比べて、認知症を発症する可能性が低くなったり、認知症を発症する時期が遅くなる可能性がある。また、認知機能の低下や認知症のリスクを増減させる要因は、必ずしもアルツハイマー病に関連する脳の変化に直接影響を与えるとは限らないことにも注意が必要である80 。例えば、喫煙が脳血管疾患に寄与して認知症のリスクを増加させる可能性はあるが、アルツハイマー病を特徴づけるアミロイド斑やタウ・タングルの発生に直接寄与するとは限らない。
心血管疾患の危険因子
脳の健康は、心臓と血管の健康に影響される。87 健康な心臓があれば十分な血液が脳に送り込まれ、健康な血管があれば酸素と栄養が豊富な血液が脳に届き、脳が正常に機能するようになる。
喫煙89-93,糖尿病94-97,糖尿病の前駆体であるブドウ糖の処理能力の低下も認知症リスクの増加につながるとする研究もある。例えば、中年期の肥満98, 101-104 高血圧98, 105-109 前高血圧(収縮期血圧120-139mmHg、拡張期血圧80-89mmHg)109 と高コレステロール110, 111 は認知症リスクの増加と関連している。しかし、晩年の肥満112と80113歳以降に発症した高血圧は認知症リスクの低下と関連している。修正可能ないくつかの危険因子の影響が加齢とともに変化する理由を理解するためには、さらなる研究が必要である。血圧に関しては、現在、大規模な臨床試験から、血圧を下げるための集中的な内科的治療が、高血圧症の高齢者におけるMCIと認知症の発生を安全に減少させる可能性があるというエビデンスが得られている114。
心臓の健康と脳の健康の関連性に基づき、研究者らは、心臓を保護する因子が脳を保護し、アルツハイマー病やその他の認知症の発症リスクを低下させる可能性があることを発見した。身体活動115-125は、これらの要因の一つであると考えられている。研究者は様々な運動を研究してきたが、具体的な運動の種類、運動の頻度、運動の持続時間などについては、リスクの低減に最も効果的であるかどうかはまだわかっていない。126-130 心臓に良い食事とは、果物、野菜、全粒粉、魚、鶏肉、ナッツ類、豆類を中心に、飽和脂肪、赤肉、糖分を制限することである。ビタミンC、D、E、オメガ3脂肪酸、イチョウ葉を含む(ただしこれらに限定されない)サプリメントの使用に関するシステマティックレビュー131では、認知機能の低下、MCIやアルツハイマー型認知症の予防にはほとんど効果がないことがわかった。
研究者たちは、危険因子の組み合わせが、個々の危険因子よりもアルツハイマー病や認知症のリスクをよりよく識別するかどうかを学ぶために、健康因子と生活習慣行動(例えば、健康因子としての血圧と生活習慣行動としての身体活動)の組み合わせの研究を開始している。また、複数の危険因子に同時に介入することが、単一の危険因子に対処するよりもリスクの低減に効果的であるかどうかも研究されている。実際、そのような研究の一つであるフィンランド老年医学介入研究(Finnish Geriatric Intervention Study to Prevent Cognitive Impairment and Disability (FINGER))132では、認知機能の低下や認知症のリスクが高い高齢者において、多面的な生活習慣の介入が認知機能に有益な効果をもたらすことが明らかになっている。FINGERの成功は、アルツハイマー病協会の米国研究「リスクを軽減するためのライフスタイル介入を通じて脳の健康を守る」(U.S. POINTER)など、他の国でもマルチドメイン・ライフスタイル介入研究が開始されるきっかけとなった。
教育
71, 134-138 一部の研究者は、教育年数が長いほど「認知的予備軍」を構築すると考えている。認知予備能とは、βアミロイドやタウの蓄積などの脳の変化139,140にもかかわらず、人が認知課題を遂行し続けることができるように、認知ネットワーク(神経細胞間のネットワーク)を柔軟かつ効率的に利用する脳の能力のことである。正式な教育を受けた年数だけが認知的予備能の決定要因ではない。精神的に刺激的な仕事をしたり、他の精神的に刺激的な活動に従事したりすることも、認知予備能の構築に役立つかもしれない141-144。
最近の研究145では、APOE-e4リスク遺伝子を持つ人は、初期の教育期間が長く、中年期に精神的にやりがいのある仕事をし、後期には余暇活動に参加し、後期には強い社会的ネットワークを持っていると、認知症発症リスクが低下することが明らかになった。
重要なことは、正式な教育とアルツハイマー病リスクの低下との関係の根本的な理由は明らかではないということである。社会経済的地位が高いほど正式な教育を受けた年数が多いことが、アルツハイマー病の予防因子になっている可能性がある。正規教育の年数が少ないことは、社会経済的地位の低さと関連している。
- 栄養不良を経験する可能性が高くなる。
- 脳の健康と密接に結びついている心血管疾患の危険因子の治療など、ヘルスケアや治療を受ける余裕のある人の能力を低下させる。
- 物理的に安全な住宅や雇用へのアクセスが制限され、大気汚染147,鉛148,殺虫剤などの神経系に有害な物質にさらされるリスクが高まる可能性がある。
また、教育年数の少ない人は、運動量が少ない150,糖尿病のリスクが高い151-153,高血圧154,喫煙の可能性が高い155など、アルツハイマー病の心血管系の危険因子が多い傾向がある。
ソーシャルと認知的エンゲージメント
116, 156-167 社会的・精神的に活動的な状態を維持することは、脳の健康を維持し、アルツハイマー病やその他の認知症のリスクを低下させる可能性があることが示唆されている。社会的・認知的関与と認知症リスクの低下との間に観察される関連性は、他の何かを反映している可能性がある。具体的には、認知障害があると、社会的・認知的スキルに関わる活動への関心や参加能力が低下する可能性がある。したがって、認知症リスクへの関与の影響というよりも、社会的・認知的関与に対する認知機能障害の影響を反映している可能性がある。社会的・認知的関与がリスクに影響を与える生物学的プロセスにどのように影響するかをよりよく理解するためには、さらなる研究が必要である。
外傷性脳損傷(TBI
TBIとは、頭部への打撃や衝撃、異物による頭蓋骨の貫通によって引き起こされる正常な脳機能の障害のことである。TBIは認知症のリスクを高める。
疾病対策予防センター(CDC)によると、情報が入手可能な最新の年である2014年には、約287万人のTBI関連の救急部門の受診、入院、死亡が発生している169。
TBIの重症度を分類するには、意識喪失または心的外傷後健忘症の持続時間170 と、15点満点のグラスゴー昏睡尺度の初期スコアの2つの方法がある171 。
- 軽度のTBI(脳震盪としても知られている)は、30分以内に持続する意識喪失や心的外傷後健忘、または初期のグラスゴースコアが13~15であることが特徴である。
- 中等度TBIは、意識消失または心的外傷後健忘が30分以上24時間未満持続すること、または初期のグラスゴースコアが9~12であることを特徴とする。
- 重度のTBIは、意識消失または24時間以上持続する心的外傷後健忘、または初期のグラスゴースコアが8以下であることを特徴とする。
168 軽度のTBIを経験した人でも、TBIを経験していない人に比べて認知症のリスクが高い。173 別の研究では、TBIの既往歴のある人がアルツハイマー病を発症するのは、TBIの既往歴のない人に比べて若い年齢であることが明らかになっている。
慢性外傷性脳症(CTE)は、コンタクトスポーツをしているときに起こる可能性があるような、頭部への繰り返しの打撃に関連した神経病理学的診断(剖検でしか特定できない脳の変化によって特徴づけられる)である。175 現在のところ、生きている間にCTEに関連した脳の変化があるかどうかを 判定する検査はない。175 現在のところ、CTEに関連した脳の変化を 生涯に発症するかどうかを判定する検査法はないが、 ある論文によると、CTEに関連した脳の変化を発症する 最大の危険因子は、反復的な脳外傷である。176 アルツハイマー病と同様に、CTEは脳内のタウ蛋白質の異常形 態のもつれを特徴とするが、アルツハイマー病とは異なり、CTEではβアミロイドプラーク はまれである。
2.7.3 リスクを増加させる珍しい遺伝的変化
特定の遺伝子変異やダウン症を特徴づける21番染色体の余分なコピーは、アルツハイマー病のリスクに強く影響する珍しい遺伝的要因である。
遺伝子変異
アルツハイマー型認知症のごく一部(推定1%以下)179は、3つの特定の遺伝子のいずれかの変異の結果として発症する。遺伝子の突然変異とは、遺伝子を構成する化学対の配列の異常な変化である。これらの変異には、アミロイド前駆体タンパク質(APP)の遺伝子やプレセニリン1,プレセニリン2の遺伝子が関与している。180 症状は65歳以前に発症する傾向があり、時には30歳という若さで発症することもあるが、アルツハイマー病の大多数は遅発性アルツハイマー病である。
ダウン症のトリソミー
ダウン症候群では、21番染色体のコピーが2つではなく3つ(トリソミー21と呼ばれる)で生まれる。ダウン症候群の人はアルツハイマー病を発症するリスクが高く、これはトリソミー21が関係していると考えられている。21番染色体には、APPの産生をコードする遺伝子が含まれており、アルツハイマー型認知症の人では、APPはβアミロイド断片に切断されてプラークに蓄積される。21番染色体の余分なコピーを持つことは、脳内でのβアミロイド断片の産生を増加させる可能性がある。
全体的に、ダウン症の人はダウン症のない人よりも早い年齢でアルツハイマー病を発症する。40歳までには、ダウン症のほとんどの人が脳内にβアミロイド斑とタウのもつれを持つようになる。全米ダウン症協会によると、50歳代のダウン症患者の約30%がアルツハイマー型認知症である58 。
2.8 将来を見据えて
アルツハイマー病のバイオマーカーを同定することにより、早期発見が可能となり、適切な人を確実に臨床試験に登録することで、新しい治療法の開発を加速させることができる。アルツハイマー病は発症の20年以上前から発症する可能性があることが明らかになったことで、病気の進行に介入するための時間的な余裕が生まれた。将来的には、どの治療法がアルツハイマー病のどの時点で最も効果的なのか、より多くのことが理解されることになるであろう。
アルツハイマー病をより深く理解するためには、その原因から予防、管理、治療の方法まで、他の重要な要素に依存している。これらの要因の中には、アルツハイマー病研究のすべての領域で多様な人種や民族からの参加者を含めることである。他のトップ10の死因の研究と一貫して、十分に代表されていない民族や人種のグループでのアルツハイマー病の研究は比較的まばらである。これは、黒人/アフリカ系アメリカ人、ヒスパニック/ラテン系アメリカ人、アジア系アメリカ人/太平洋諸島人、ネイティブアメリカンを臨床試験、観察研究、その他の調査に含めることで、アルツハイマー病の科学の進歩から誰もが利益を得ることができるようにするための現在および将来の研究の緊急の必要性を反映している。
3 有病率
何百万人ものアメリカ人がアルツハイマー病やその他の認知症を患っている。米国の65歳以上の人口が増加し続ける中、アルツハイマー病やその他の認知症を持つ米国人の数も増加すると予想されている。183, 184 ベビーブーム世代は、アルツハイマー型認知症のリスクが最も高い年齢層である65歳以上の年齢にすでに到達し始めている185 。
本節では、アルツハイマー型認知症が地域社会や医療システムに与える負担の大きさを説明するために、アルツハイマー型認知症患者の数と割合を報告する。アルツハイマー型認知症の有病率とは、ある時点でアルツハイマー型認知症になる人の数と割合のことである。罹患率とは、年間の新規患者数または罹患率のことである。アルツハイマー型認知症やその他の認知症の人の数や割合に関する研究の推定値は、それぞれの研究がどのように実施されたかによって異なる。本節では、いくつかの研究から得られたデータを用いる。
3.1 米国におけるアルツハイマー病およびその他の認知症の有病率
2020年には、65歳以上のアメリカ人の約580万人がアルツハイマー型認知症を患っていると推定されている1,62。
図2020年の65歳以上のアルツハイマー型認知症患者の数と年齢。
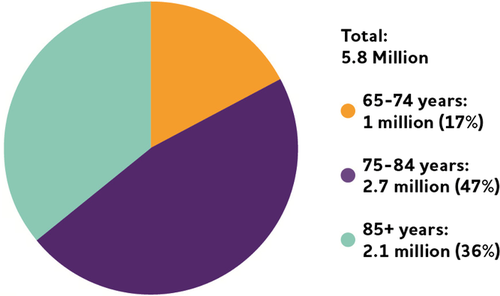
(Hebert er al)。2,62のデータを基に作成
米国の総人口のうち
- 65歳以上の10人に1人(10%)がアルツハイマー型認知症。
- 65歳から74歳の3%、75歳から84歳の17%、85歳以上の32%がアルツハイマー型認知症である62。
65歳以上のアルツハイマー型認知症の推定患者数は、2010年の米国国勢調査とChicago Health and Aging Project (CHAP)という高齢者の慢性的な健康状態を調査した人口ベースの調査の最新データを使用している62。
すべての認知症の有病率の全国的な推定値はCHAPからは得られていないが、高齢者の全国代表的なサンプルであるAging, Demographics, and Memory Study (ADAMS)を含む他の人口ベースの研究から得られている4,187, 188 ADAMSの推定値によると、米国では71歳以上の人の14%が認知症である。
これらの推定値は、記憶喪失や計画の立てにくさ、問題解決の難しさなどの症状に基づいてアルツハイマー型認知症の人を指す。バイオマーカーに基づく有病率の推定値は、報告されているアルツハイマー病患者の数に大きな影響を与える可能性がある。
現在アルツハイマー型認知症とされている人の中には、バイオマーカーではなく臨床症状に基づいて診断されたために、アルツハイマー型認知症に関連した脳の生物学的変化が見られない人もいる。剖検研究や臨床試験では、症状に基づいてアルツハイマー型認知症の基準を満たした人の15%から30%には、死亡時に必要とされるアルツハイマー型認知症に関連した脳の変化が見られなかったことがわかっている9, 69, 191-193。
同時に、バイオマーカーを用いた有病率推定では、アルツハイマー病による軽度認知障害(MCI)や前臨床アルツハイマー病など、現在のアルツハイマー病有病率推定にはカウントされていないアルツハイマー型認知症の人たちを含む、アルツハイマー型認知症の全領域の人たちが含まれることになるだろう。
3.1.1 プライマリーケアにおけるアルツハイマー病やその他の認知症の過少診断
CHAPやADAMSのような有病率研究は、研究対象者全員が認知症の評価を受けるように設計されている。しかし、研究の場以外では、アルツハイマー病やその他の認知症の診断基準を満たすであろう人々のかなりの部分は、医師から認知症と診断されていない39-42。さらに、メディケアの請求記録にアルツハイマー病やその他の認知症と診断されているメディケア受給者(認知障害のために回答できない場合はその介護者)の半数以下が診断を受けたと報告している43-46。アルツハイマー型認知症は過小診断されていることが多く、診断されてもそのことに気づかないことが多いため、アルツハイマー型認知症を持つアメリカ人の大部分は、自分がアルツハイマー型認知症であることに気づかないことがある。アルツハイマー病協会による最近の調査194では、平均して、プライマリーケアの医師は、認知機能障害が検出された場合、92%の頻度で患者に通知しており、64%の医師は、常に患者に通知していると報告していることがわかった。調査対象となった36%の医師のうち、常に患者に知らせていないのは、73%が完全な診断の前に知らせるのは時期尚早だからであり、41%が簡単な認知機能評価では偽陽性や偽陰性の割合が高いと答えている。
2011年以降、メディケアの年次健康診断では認知機能評価が必須となっている。アルツハイマー病協会による同様の調査では、高齢者の3人に1人の高齢者がこれらの訪問に認知評価が含まれるべきであると認識しているにすぎないことが明らかになった。ほとんど(93%)の高齢者は、記憶と思考の問題の検査を医師が推奨することを信頼していると答えているが、プライマリーケアの医師の94%が、すべての高齢者の認知機能障害を評価することが重要であると述べているにもかかわらず、それを行うための標準的なプロトコルであると答えたのは半数以下(47%)であった。調査した医師が高齢患者の認知機能障害を評価しない主な理由として挙げたのは、症状や訴えがない(68%時間がない(58%)というものであった。
3.1.2 自覚的認知機能低下の有病率
195-199 主観的認知機能の低下とは、認知検査や臨床診断、他の人が気づくこととは別に、記憶力やその他の思考能力の悪化を自分で感じていることである。200 自覚的認知機能の低下を経験した人のすべてがMCIや認知症を発症するわけではないが、多くの人が発症している。主観的認知機能の低下に関する質問を含む行動リスク因子サーベイランスシステム調査では、米国では45歳以上の11%が主観的認知機能の低下を報告しているが、報告した人の54%は医療専門家に相談していないことがわかった。
3.2 州別のアルツハイマー型認知症患者数の推計
表4は、2020年の州別の65歳以上のアルツハイマー型認知症患者数、2025年の予測数、2020年から 2025年までのアルツハイマー型認知症患者数の変化率の予測値を示したものである5,206。
表4. 州別の65歳以上のアルツハイマー型認知症患者数の予測
原文参照
(Weuve er al)。5,206によりアルツハイマー病協会に提供されたデータを基に作成
図3に示すように、2020年から 2025年の間に、全国のすべての州でアルツハイマー病患者数が少なくとも6.7%増加すると予想されている。これらの州では、65歳以上の人口が増加すると予測されているため、アルツハイマー型認知症の患者数は増加している。中年期の肥満や糖尿病などの認知症の危険因子は地域や州によって大きく異なるため、将来の負担の地域パターンはここで報告したものとは異なる可能性がある。これらの予測に基づいて、2020年から 2025年の間にアルツハイマー型認知症患者の割合が最も大きく増加するのは、西部と南東部であると予想される。これらの増加は、各州の医療制度やメディケイドプログラムにも大きな影響を与えるだろう。
図3 州別のアルツハイマー型認知症有病率の2020年から 2025年までの増加予測
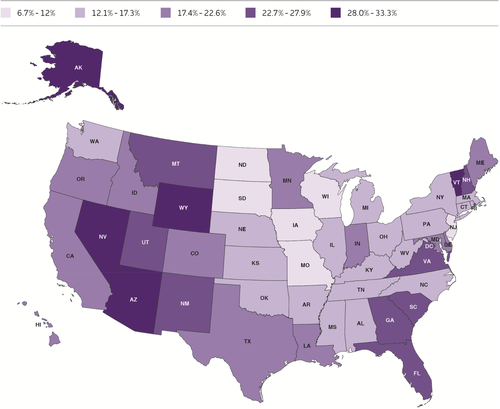
2020年から 2025年までのワシントンD.C.の変化:1.1%。Weuve er al)。5,206によるアルツハイマー病協会に提供されたデータを基に作成。
3.3 アルツハイマー型認知症の発症率
有病率とは、ある時点の母集団に存在する疾患の症例を指すのに対し、罹患率とは、定義された母集団(この場合、米国の65歳以上の人口)において、ある期間に新たに発症した疾患の症例を指する。発生率は、病気を発症するリスクの指標となる。確立された高齢者疫学研究のための人口集団のデータを用いたある研究によると、2020年に米国で65歳以上の人々が約491,000人のアルツハイマー型認知症を発症すると予測されている208。例えば、CHAPの推計によると、2011年に米国で65歳以上のアルツハイマー型認知症を発症した人は約91万人であり、CHAPの推計があれば2020年にはさらに多くの人が発症すると予想される。アルツハイマー型認知症の新規発症数は年齢とともに劇的に増加している。CHAPの推計によると、2011年の65~74歳の年間平均発症率は0.4%(2011年には65~74歳の1,000人に4人がアルツハイマー型認知症を発症したことになる75~84歳の年間発症率は3.2%(1,000人に32人85歳以上(「最高齢者」)の年間発症率は7.6%(1,000人に76人)となっている。 209 米国では高齢者を中心に65歳以上の人口が増加しているため、アルツハイマー型認知症やその他の認知症の新規発症数は2050年までに倍増すると予測されている。
3.4 アルツハイマー型認知症の生涯リスク
生涯リスクとは、特定の疾患を持たないある年齢の人が、残りの寿命の間にその疾患を発症する確率のことである。図4に示すように、45歳でのアルツハイマー型認知症の推定生涯リスクは、女性では約5人に1人(20%男性では約10人に1人(10%)であった。男女ともに、65歳ではわずかにリスクが高くなっている。
図4 45歳および65歳におけるアルツハイマー型認知症の推定生涯リスク、性別
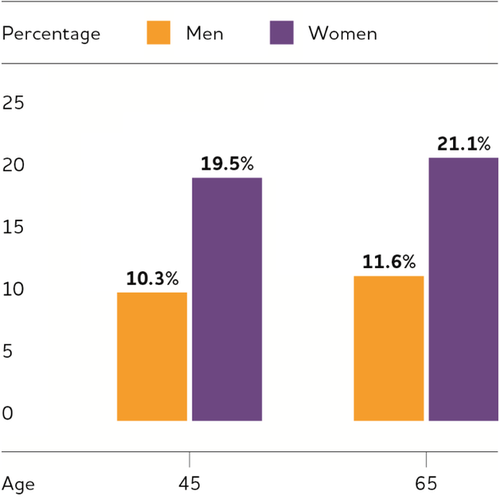
(Chene er al)。211のデータを基に作成
3.5 アルツハイマー病やその他の認知症の有病率とリスクにおける男女差
男性よりも女性の方がアルツハイマー病やその他の認知症に罹患している人が多い。7,62 米国の65歳以上のアルツハイマー病患者580万人のうち、女性が360万人、男性が220万人である。7,62 ADAMSの推計によると、71歳以上では女性の16%がアルツハイマー病やその他の認知症を持っているのに対し、男性の11%である。
211-213 しかし、同年齢の男女のアルツハイマー病やその他の認知症の発症リスクの違いについては、調査結果はまちまちである。71, 210, 213-215 しかし、ヨーロッパの研究では、年齢が高くなるほど女性の発症率が高くなるという報告があり、216, 217,イギリスの研究では男性の発症率が高くなるという報告がある。
219, 221 アルツハイマー病やその他の認知症のリスクに男女差があるとすれば、生物学的・社会的にいくつかの説明が考えられるが、その一つには、男女間の認知症の危険因子の分布や影響の違いが考えられる。アルツハイマー病やその他の認知症のリスクが女性の方が高いとすると、20世紀前半に生まれた男性よりも女性の方が教育水準が低いことが、認知症のリスク上昇の一因になっている可能性がある。興味深いことに、欧州の研究では、低学歴と認知症の転帰との関係は、実際には男性よりも女性の方が強いかもしれないという結果が出ている224, 225。224, 225 いくつかの研究では、認知症リスクに男女差があるとされているが、フラミンガム心臓研究のデータを用いた研究では、65歳を超えて生存し、研究に参加した男性は、心血管系のリスクプロファイル(男性は女性よりも中年期の心血管系疾患による死亡率が高い)が健康的であるため、認知症リスクが低いという「生存バイアス」が原因で、男性の認知症リスクが低いように見えることが示唆されている。
226 アルツハイマー型認知症の遺伝的危険因子として最もよく知られているAPOE-e4遺伝子型は、男性よりも女性の方がアルツハイマー型認知症227, 228および神経変性229との関連性が強いことが多くの研究で示されている。しかし、最近のメタアナリシスでは、APOE遺伝子型とアルツハイマー型認知症の関連性に男女差はないことが示されたが、ある年齢層ではAPOE-e4遺伝子型を持つ女性のリスクは高かった230。232 最後に、βアミロイドとタウのレベルが同程度であるにもかかわらず、女性の方が男性よりも急速な認知機能の低下や神経変性を示すことが示されており、アルツハイマー病の特徴である蛋白質が男性よりも女性に悪影響を及ぼす可能性があることを示唆している。
3.6 アルツハイマー病やその他の認知症の有病率における人種・民族の違い
非ヒスパニック系白人は、米国の他の人種・民族よりもアルツハイマー病やその他の認知症の患者数が多いが(非ヒスパニック系白人は米国最大の人種・民族グループであるため高齢の黒人・アフリカ系アメリカ人やヒスパニック・ラテン系は、高齢の白人よりもアルツハイマー病やその他の認知症になる可能性が高い16。17, 236-239 ほとんどの研究では、高齢の黒人・アフリカ系アメリカ人は、高齢の白人に比べてアルツハイマー病やその他の認知症になる可能性が約2倍であることが示されている18。19, 209 いくつかの研究では、高齢のヒスパニック/ラテン系住民は、高齢の白人に比べてアルツハイマー病やその他の認知症を発症する可能性が約1.5倍であることが示されている8, 19, 240, 241 しかしながら、ヒスパニック/ラテン系住民は、文化的歴史、遺伝的先祖、健康プロファイルの点で非常に多様な集団であり、有病率が特定のヒスパニック/ラテン系民族グループによって異なる可能性があるという証拠がある(例えば、メキシコ系アメリカ人とカリブ系アメリカ人を比較した場合など)。
アルツハイマー型認知症の有病率が白人に比べて少数派の人種・民族グループで高いのは、これらのグループの認知症発症率が高いためであると考えられる。アルツハイマー病やその他の認知症に対する遺伝的危険因子の影響は人種によって異なる可能性があるという証拠がいくつかあるにもかかわらず、80, 82, 245 遺伝的因子は人種間の有病率や発生率の大きな差を説明するものではないようである。246 代わりに、アルツハイマー病やその他の認知症のリスクの増加と関連する心血管疾患や糖尿病などの健康状態が、黒人/アフリカ系アメリカ人やヒスパニック/ラテン系の人々に多く見られることから、これらの違いを説明していると考えられている247。248 教育のレベルや質の低さ、貧困率の高さ、逆境や差別にさらされることの多さなどの社会経済的特徴もまた、黒人/アフリカ系アメリカ人やヒスパニック/ラティーノのコミュ ニティにおけるリスクを増加させる可能性がある(ひいては、上記の健康状態に寄与する可能性がある)80, 247-249。
250, 251 65歳以上のメディケア受給者のデータによると、アルツハイマー病やその他の認知症と診断されたことがあるのは、白人の10.3%、ヒスパニック・ラテンアメリカ人の12.2%、黒人・アフリカ系アメリカ人の13.8%であると推定されている。黒人・アフリカ系アメリカ人の診断率は白人よりも高かったが、医療制度の利用にかかわらず認知症の人をすべて検出する有病率調査によれば、黒人・アフリカ系アメリカ人の診断率はさらに高いはずである。
白人、黒人・アフリカ系アメリカ人、ヒスパニック・ラテン系以外の人種・民族におけるアルツハイマー病やその他の認知症の全国的な有病率については、集団ベースのコホート研究のデータが少ない。しかし、カリフォルニア州の大規模ヘルスプランの会員の電子カルテを調査した研究では、認知症の発症率(会員のカルテに認知症の診断があるかどうかで決まる)は、黒人/アフリカ系アメリカ人が最も高く、ラティーノ(この研究ではラティーノやヒスパニックと自己申告した人のことを指す)と白人では中間的で、アジア系アメリカ人では最も低いことが示されている。最近の文献レビューでは、日系アメリカ人は唯一信頼できる有病率データを持つアジア系アメリカ人のサブグループであり、他のすべての民族グループと比較して認知症の有病率が最も低いことが明らかになった。
3.7 アルツハイマー型認知症の有病率と発生率の推移
米国をはじめとする欧米の高所得国におけるアルツハイマー病やその他の認知症の有病率223, 255-263,発生率218, 259, 263-270は、過去25年間で減少している可能性があることを示す研究が増えているが、結果はまちまちである61。209, 271, 272 これらの減少は、教育水準の向上と心血管系の危険因子のコントロールの改善に起因している223, 258, 264, 267, 273, 274 これらの知見は有望であり、アルツハイマー病やその他の認知症の危険因子を特定して減らすことが有効であることを示唆している。これらの知見は、任意の年齢での認知症リスクがわずかに減少している可能性を示しているが、米国をはじめとする欧米の高所得国では、高齢者の増加により、アルツハイマー病やその他の認知症の総患者数は今後も劇的に増加すると予想されている。
アルツハイマー型認知症の潜在的な危険因子である糖尿病や肥満の増加が今後数年で認知症リスクを回復させる可能性があるという世界的な傾向を考えると、このような好ましい傾向が今後も続くのか、それともこのような好ましい傾向がすべての人種・民族に当てはまるのかは不明である(209, 255, 273, 274, 277)。さらに、2050年までに世界の認知症の有病率と負担が増加すると予測されているが、その68%は中低所得国で発生することになる。
3.7.1 将来を見据えて 団塊の世代の高齢化
団塊の世代である米国の人口の大部分は、アルツハイマー病やその他の認知症のリスクが高まる65歳以上に達している。2030 年までには、65 歳以上の人口は大幅に増加し、7,400 万人の高齢者が総人口の 20%以上を占めると予測されている(2020 年の 16%から増加)。
2025年までに、65歳以上のアルツハイマー型認知症患者数は710万人に達すると予測されており、2020年の580万人からほぼ22%増加すると予測されている10,62。
2050年までに、65歳以上のアルツハイマー型認知症患者数は1380万人に達すると予測されており、アルツハイマー型認知症を予防、遅らせる、または治すための医学的ブレークスルーの開発を待たずして、アルツハイマー型認知症の患者数は1380万人に達すると予測されている。
イメージ
図5 米国における65歳以上のアルツハイマー型認知症患者数の予測(2010年~2050)
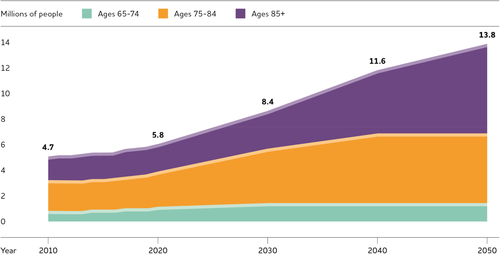
(Hebert er al)。9,62のデータを基に作成。
3.7.2 高齢者人口の増加
平均寿命の延長と大規模なベビーブーム集団の高齢化により、高齢者である 85 歳以上の米国人の数と割合が増加することになる。現在から 2050 年までの間に、米国の 65 歳以上の人口に占める高齢者の割合は、2020 年の 10%から 2050 年には 19%に増加すると予想されている。
- 2020年には85歳以上のアルツハイマー型認知症患者は約210万人となり、アルツハイマー型認知症患者の35%を占めている62。
- 団塊の世代の第一波が85歳に達すると(2031年85歳以上の300万人以上がアルツハイマー型認知症になると予測されている62。
- 2050年には、85歳以上で700万人がアルツハイマー型認知症になると予測され、65歳以上のアルツハイマー型認知症患者の約半数(51%)を占めている62。
4 致死率と病的状態
アルツハイマー病は、公式には米国における死因の第6位に挙げられている280 。また、アルツハイマー病は、障害や健康状態の悪化を引き起こす主な原因でもある。アルツハイマー型認知症の人は、死亡する前に、病気の進行に伴って何年にもわたって罹患しながら生活していくことになる。
4.1 アルツハイマー病による死亡例
アルツハイマー病が原因で毎年何人の死亡者が出ているかは、死因の記録方法の関係上、判断が難しい。疾病対策予防センター(CDC)のデータによると、データが入手可能な最新の年である2018年には、122,019人がアルツハイマー病で死亡している。
米国では、アルツハイマー病はがんや心臓病などの他の有力な死因と比較してランク付けできる死因としてカウントされているが、臨床的に診断された他のタイプの認知症による死亡はこのようにランク付けされていない。報告されているアルツハイマー型認知症による死亡数よりも、何らかの型の認知症による死亡数の方がはるかに多いのである。2018年には、何らかの認知症が266,957人の死因として公式に記録されている(これにはアルツハイマー病による122,019人が含まれている)。
さらに複雑なことに、アルツハイマー病や認知症を死因として記載されている死亡診断書の大部分は、剖検では確認されておらず、調査によると、生存中にアルツハイマー型認知症と診断された人の約30%は、実際にはアルツハイマー型認知症による認知症ではなく、別の原因による認知症であることが示されている(表2参照)。そのため、アルツハイマー型認知症と記載された死因が正確でない場合がある。ここでいう「アルツハイマー病による死亡」とは、死亡診断書に正式に記載されているものであり、報告者がアルツハイマー病による認知症が死因であると考えていることを理解した上で、通常は病理学的な確認なしに報告している。
重度の認知症では、不動や嚥下障害、栄養失調などの合併症が頻発し、死に至る重篤な急性疾患のリスクを著しく高める。284, 285 ある剖検調査では、アルツハイマー型認知症患者の半数以上で呼吸器系疾患が即死原因であり、次いで循環器系疾患が約4分の1であった。286-288 その結果、死亡診断書に記載されている急性疾患の原因がアルツハイマー病であっても、これらの急性疾患が原因で死亡したアルツハイマー型認知症の人は、アルツハイマー型認知症で死亡した人の数にカウントされないことがある。このように、死亡診断書を用いてアルツハイマー病やその他の認知症による死亡者数を決定することの難しさは、「認知症による死亡と認知症による死亡の区別が曖昧になっている」と呼ばれている。
アルツハイマー型認知症による死亡者数を決定するもう一つの方法は、アルツハイマー型認知症の人の死亡リスクの推定値と、アルツハイマー型認知症でない人の死亡リスクの推定値を比較する計算である。Rush Memory and Aging Project と Religious Orders Study のデータを用いた研究では、2010 年に米国で 75 歳以上の人々のうち 50 万人がアルツハイマー型認知症に起因すると推定されている(65 歳から 74 歳の推定値は得られていない)が、これは、アルツハイマー型認知症を持たない人々がその年に死亡するとは考えられないことを意味している。
アルツハイマー病による本当の死亡数は、死亡診断書に記録されているアルツハイマー病による死亡数と、死亡時にアルツハイマー病と診断された人の数との間にある。2014年のメディケアの請求データによると、ある年に死亡したメディケア受給者の約3分の1がアルツハイマー病または他の認知症と診断されている。死亡時にアルツハイマー型認知症を発症した高齢者の中には、アルツハイマー型認知症とは無関係の原因で亡くなる人もいるが、アルツハイマー型認知症そのものや肺炎などアルツハイマー型認知症が原因で亡くなる人も少なくない。
死因にかかわらず、70 歳では、アルツハイマー型認知症の人の 61%が 80 歳までに死亡すると予想されているのに対し、アルツハイマー型認知症の人はそうでない人の 30%が死亡すると予想されている。
4.2 アルツハイマー病による死亡が公衆衛生に与える影響
他の主要な死因による死亡数は大幅に減少またはほぼ横ばいとなっているが、公式の記録によると、アルツハイマー病による死亡数は大幅に増加している。2000年から 2018年の間に、死亡診断書に記録されたアルツハイマー病による死亡数は146%増と2倍以上に増加しているが、死因の第1位(心臓病)による死亡数は7.8%減少している(図6)。 281, 294 アルツハイマー病を死因とする死亡診断書の増加は、高齢化に伴いアルツハイマー病が一般的な死因となってきたこともあり、実際のアルツハイマー病による死亡数が増加したことと、医師、検視官、その他死因を特定する者による死亡診断書へのアルツハイマー病による死亡の報告が時間の経過とともに増加したことの両方を反映していると考えられる。
図6 2000年から 2018年の間に選択された死因(全年齢)の変化率
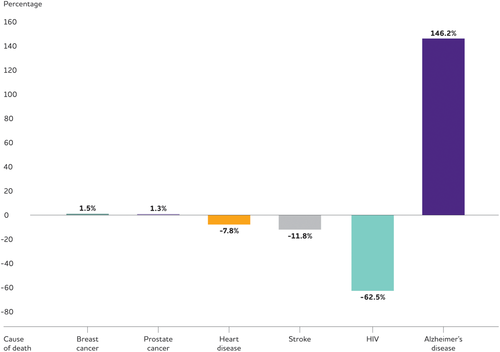
国立健康統計センターのデータを基に作成。
4.3 アルツハイマー病による死亡者数の州別推移
表5は、州別データが入手可能な直近の年である2018年の州別アルツハイマー病による死亡者数の情報を示している。この情報は死亡診断書から得られたもので、医師が死因として特定した状態を反映している。また、この表では、人口規模の異なる州間でアルツハイマー病による死亡リスクを比較するために、州別の年間死亡率を示している。米国全体では、2018年のアルツハイマー病の死亡率は人口10万人あたり37.3人であった。
表5. 州別アルツハイマー病による死亡数と年間死亡率(10万人あたり)2018年
州別死亡者数 死亡率
アラバマ州 2,616 53.5
アーカンソー州 131 17.8
アリゾナ州 3,012 42
アーカンソー州 1,457 48.3
カリフォルニア州 16,627 42
コロラド州 1,649 29
コネチカット州 986 27.6
デラウェア州 412 42.6
コロンビア特別区 105 14.9
フロリダ州 6,725 31.6
ジョージア州 4,513 42.9
ハワイ州 480 33.8
アイダホ州 666 38
イリノイ州 4,030 31.6
インディアナ州 2,668 39.9
アイオワ州 1,439 45.6
カンザス州 899 30.9
ケンタッキー州 1,674 37.5
ルイジアナ州 2,166 46.5
メイン州 580 43.3
メリーランド州 1,122 18.6
マサチューセッツ州 1,823 26.4
ミシガン州 4,474 44.8
ミネソタ州 2,436 43.4
ミシシッピ州 1,547 51.8
ミズーリ州 2,641 43.1
モンタナ州 310 29.2
ネブラスカ州 683 35.4
ネバダ州 704 23.2
ニューハンプシャー州 487 35.9
ニュージャージー州 2,710 30.4
ニューメキシコ州 583 27.8
ニューヨーク州 3,755 19.2
ノースカロライナ州 4,495 43.3
ノースダコタ 356 46.8
オハイオ州 5,391 46.1
オクラホマ州 1,739 44.1
オレゴン州 1,868 44.6
ペンシルバニア州 4,064 31.7
ロードアイランド 470 44.5
サウスカロライナ州 2,616 51.5
サウスダコタ 437 49.5
テネシー州 3,488 51.5
テキサス州 9,763 34
ユタ州 1,024 32.4
バーモント 333 53.2
バージニア州 2,592 30.4
ワシントン州 3,752 49.8
ウェストバージニア州 791 43.8
ウィスコンシン州 2,453 42.2
ワイオミング 277 47.9
米国合計 122,019 37.3
National Center for Health Statisticsのデータを基に作成。
4.4 アルツハイマー型認知症の死亡率
図7に示すように、アルツハイマー病による死亡率は2000年以降、大幅に上昇している。281 表6によると、アルツハイマー病による死亡率は年齢とともに劇的に上昇し、特に65歳以降では顕著に増加している11,281。CDC の報告書によると、年齢分布の違いを調整した後でも、1999 年から 2014 年の間に米国の年間アルツハイマー病死亡率は大幅に増加した。他に考えられる理由としては、心臓病や脳卒中などの他の一般的な老年期の死因による死亡が減少したこと、アルツハイマー型認知症の診断が増加したこと、死亡診断書に記入する医師などによるアルツハイマー型認知症を死因とする報告が増加したことなどが挙げられる。
図7 米国の年間アルツハイマー病死亡率(10万人あたり)の年別推移
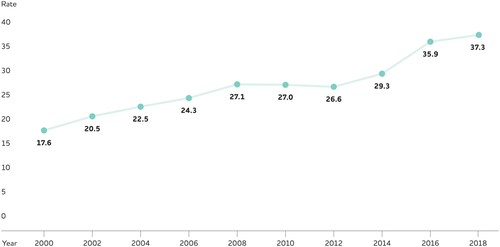
国立健康統計センターのデータを基に作成。
表6. 米国の年間アルツハイマー病死亡率(10万人あたり)年齢および年別
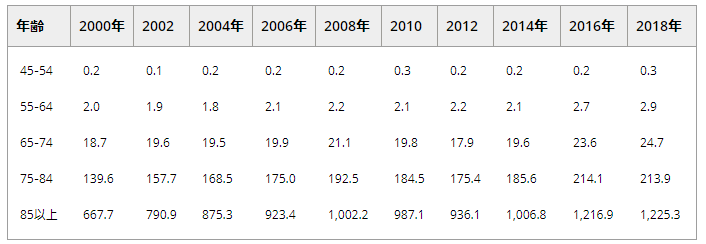
4.5 診断から死亡までの期間
研究によると、65歳以上の人はアルツハイマー型認知症と診断されてから平均4~8年で生存するが、中には20年も生きる人もいる210, 296-303。アルツハイマー型認知症で70歳から80歳まで生きる人は、この期間の平均40%を重度のステージで過ごすことになる。293 認知症で亡くなる人の約3分の2が老人ホームで亡くなるのに対し、がん患者の20%、その他の疾患で亡くなる人の28%が老人ホームで亡くなると推定されている。
4.6 アルツハイマー病の負担
アルツハイマー病は、生前の病気の期間が長いことから、その時間の多くが障害と依存の状態で過ごされるため、公衆衛生上の影響が大きいと考えられている。科学者たちは、さまざまな疾患が母集団に及ぼす負担を測定し、比較する方法を開発してきたが、これには疾患を持つ人の数だけでなく、その疾患のために失われた人生の年数や、障害の状態にあることによって失われた健康な人生の年数も考慮している。疾患負担の主要な指標は、障害調整済生存年数(DALYs)と呼ばれるもので、これは、早死にによって失われた年数(YLLs)と障害を抱えて生きた年数(YLDs)の合計であり、疾患や障害を持つすべての人を対象としている。これらの指標は、アルツハイマー病が本人だけでなく、その家族やインフォーマルな介護者にとっても非常に負担の大きい病気であることを示しており、米国では近年、アルツハイマー病の負担が他の病気の負担よりも劇的に増加していることを示している。最新のGlobal Burden of Disease分類システムによると、アルツハイマー病は、1990年に米国で12番目に負担の大きい病気や障害であったが、2016年にはDALYsの観点から6番目に上昇した。2016年には、アルツハイマー病はYLLs換算で4位、YLDs換算で19位となっている。
これらの統計を総合すると、アルツハイマー病はより多くのアメリカ人の死の原因となっているだけでなく、アメリカではより多くの健康不良や障害の原因となっていることがわかる。
5 介護
介護とは、別の人の健康上の必要性と幸福に出席することを指する。介護には、入浴や着替えなどの 1 つ以上の日常生活動作(ADL)や、請求書の支払い、買い物、交通機関の利用などの複数の日常生活動作(IADL)の介助が含まれることが多い306, 307 介護者は、アルツハイマー型認知症の人に感情的なサポートを提供するだけでなく、他の多くの支援(例えば、他の家族や医療提供者とのコミュニケーションやケアの調整、自宅や他の場所での安全の確保、健康状態の管理など)も行う。アルツハイマー病やその他の認知症の人の介護者についての記述情報を提供することに加えて、このセクションでは、認知症の人の介護者を他の病状の人の介護者と比較したり、比較できない場合は介護者以外の人と比較したりしている。
表7. 認知症の介護の仕事
家事、買い物、食事の準備、移動手段の提供、医師の予約の手配、財政や法律問題の管理、電話応対などの日常生活の道具的活動(lADL)の援助。
リマインダーや直接投薬を行うことで、利用者が正しく薬を服用できるように支援する。
認知症やその他の病状に対する治療のアドバイスに従うための支援。
入浴、着替え、グルーミング、食事などの日常生活動作(ADL)の支援、歩行、ベッドから椅子への移動、トイレの使用、失禁の管理など。
攻撃的な行動、徘徊、抑うつ的な気分、焦燥感、不安感、反復活動、夜間障害などの行動症状の管理。
サポートグループや成人向けデイサービスプログラムなどの支援サービスを探して利用する。
有料の居宅介護、介護施設、または補助生活介護の手配。
介護を提供する他の人を雇い、監督する。
必ずしも特定の仕事ではないが、以下のような追加の責任を負う。
- 一日を乗り切るための全体的な管理を提供する。
- 主な介護者のためのケアプラン、意思決定やレスパイトの手配について他の家族とのコミュニケーションを含む、アルツハイマー病を持つ親族の介護に関連する家族の問題に対処する。
- 関節炎、糖尿病、癌などの他の健康状態(すなわち、「併存疾患」)の管理。
- 感情的な支援と安心感の提供。
5.1 無給の介護者
308 高齢者に援助を提供する介護者の半数近く(48%)が、アルツハイマー病や他の認知症の人のために援助を行っている。
12 アルツハイマーやその他の認知症の人の介護者数は、データが入手可能な最新の日付である2009年のデータを一部取り入れたモデルを使用して計算されていることに注意することが重要である。過去10年間で、すべての高齢者のアメリカ人の家族介護者の数が減少している可能性が示唆されている。アルツハイマー協会は、認知症介護者に関する新しいデータや最近発表された州別のデータを調査し、専門家と協力して、これらの最近の傾向を考慮に入れてモデルを改訂している。予備的な評価によると、過去と比較して家族介護者の総数は減少しており、個々の介護者は介護時間を大幅に増やすことで、より大きな負担を経験している。この予備的な分析が維持されれば、将来のアルツハイマー病と認知症の介護者数の全国および各州の推計値は、現在の推計値よりも低くなるだろう。
2019年には、アルツハイマー病やその他の認知症の人の介護者は、推定186億時間の非公式な(つまり無給の)援助を行っており、国への貢献度は2,440億ドル近くに上る。これは、2019年のウォルマートの純額(5,144億ドル)310の約47%、2018年のマクドナルドの純額(210億ドル)の11倍である311 認知症の人の生涯介護費用の総額は、2019年のドルで357,297ドルと推定されている。生涯介護費用の70%は家族介護者が負担しており、その内訳は、認知症の人のための薬から食 事に至るまでの項目の未払いの介護費用や自己負担額の範囲内である312,313。
介護者がアルツハイマー型認知症や他の認知症の人に介護や援助を提供する主な理由は、(1)家族や友人を自宅に置いておきたい(65%(2)認知症の人との距離が近い(48%(3)認知症の人に対する介護者の義務感(38%)の 3 つである13 。316 認知症の高齢者のうち、家族やその他のインフォーマルな介護者からの援助を受けていない人は、認知症の高齢者のごく一部にすぎない(8%)。316 終末期にある認知症の配偶者の介護者のうち、半数近くが他の家族や友人の助けを借りずに介護を行っている。317 認知症の一人暮らしは、レズビアン、ゲイ、バイセクシュアル、トランスジェンダー(LGBT)などの特定のサブグループにとっては特に困難である。
5.1.1 介護者は誰か?
米国のアルツハイマー病やその他の認知症患者の家族介護者の人口統計学的背景を調査したところ、以下のような結果が得られた。その結果、以下のようなことがわかった:13,319-323
- 認知症介護者の約3分の2は女性である。
- 介護者の約 3 割が 65 歳以上 13.13
- 介護者の 60%以上が結婚しているか、パートナーと同居しているか、長期的な関係にある 13,320
- 介護者の半数以上が認知症の親や義理の親に援助を提供している。
- 介護者の3分の2は非ヒスパニック系の白人13,319,320,323で、10%が黒人/アフリカ系アメリカ人、8%がヒスパニック/ラテン系、5%がアジア系である13。
- 認知症介護者の約40%は大卒以上の教育を受けている13,320,323。
- 介護者の41%は世帯収入が5万ドル以下である13。
- 認知症の人のプライマリーケア(親族の援助に最も責任を持っている人)の中では、半数以上が親の介護をしている。
- 介護者のほとんど(66%)が認知症の人と地域で一緒に暮らしている。
- 認知症介護者の約4分の1は「サンドイッチ世代」の介護者である。
5.1.2 介護と女性
認知症の人を介護する責任は女性にあることが多い。前述のように、認知症介護者の約3分の2は女性である13,319, 320, 325, 326 認知症介護者の3分の1以上は娘である。男女ともに調査した2014年のアルツハイマー協会女性・アルツハイマー世論調査によると、週に21時間以上の介護を提供している人のうち、67%が女性であった328。認知症の人を 5 年以上介護している人のうち、63%が女性である。329, 330 個別カウンセリングやレスパイトケアの必要性を示した認知症介護者のうち、大多数は女性である(個別カウンセリング 85%、レスパイトケア 84%)。
5.1.3 介護の仕事
アルツハイマー病やその他の認知症の人に提供されるケアは多岐にわたっており、場合によってはすべてを網羅している。表7は、最も一般的な認知症ケアの種類をまとめたものである。
アルツハイマー型認知症やその他の認知症の人の家族が提供するケアは、他の疾患の人の介護者が提供するケアと似ているが、認知症の介護者はより広範な支援を提供する傾向がある。認知症の人の家族介護者は、認知症のない人の介護者よりも、介護を受ける人の健康状態をモニタリングする傾向が強い(79%対66%)。 331 2011年のNational Health and Aging Trends Studyのデータによると、認知症の人の介護者は、認知症のない人の介護者に比べて、セルフケアや移動の支援(85%対71%健康や医療のケア(63%対52%)を提供する傾向が高いことが示されている309, 319 図8は、認知症の人の家族介護者が他の高齢者の介護者に比べて、ADLの支援を提供する傾向が高いことを示している。
図8 アルツハイマー型認知症またはその他の認知症の人の介護者と、特定の日常生活動作の援助を提供するその他の高齢者の介護者の割合、米国、2015年
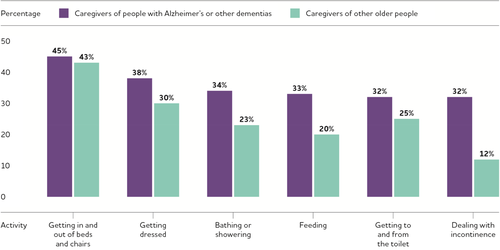
National Alliance for CaregivingおよびAARPのデータを基に作成。
ADL の支援に加えて、アルツハイマーやその他の認知症の人の介護者は、認知症のない人の介護者(46%、50%)に比べて、地域の機関や介護提供者との連携(65%)や財政管理(68%)を行う人が多い。 323 アルツハイマーやその他の認知症の人の介護者は、認知症のない人の介護者(それぞれ27%、59%)に比べて、外部サービスの手配(46%)や医療専門家とのコミュニケーション(80%)を行っている。認知症の人を介護することは、神経精神症状(例えば、不安、無気力、抑制力の欠如など)や重度の行動問題など、他の病気の人の介護者が直面することのない症状を管理することでもある。アルツハイマー病やその他の認知症の人の家族介護者は、認知症のない人の家族介護者に比べて、情緒的・精神的な健康問題(41%対16%)や行動問題(15%対4%)を支援する傾向がある。323 認知症の人は、認知症のない人に比べて家族や友人の介護に関わるネットワークが広い傾向があり、家族や友人は特定の介護課題に集中する傾向がある。
アルツハイマー型認知症や他の認知症の人が介護付き住宅や老人ホームに移った場合、家族介護者が提供する支援は、通常、表 7 にまとめた包括的なケアから、感情的な支援、施設スタッフとの交流、適切なケアのためのアドバイスへと変化していく。しかし、家族介護者の中には、入浴、着替え、その他のADLの支援を続けている人もいる。
5.1.4 介護の期間
別の調査によると、アルツハイマー病やその他の認知症の人の家族介護者の半数以上(57%)が4年以上介護をしたことがあると回答している。アルツハイマー型認知症の介護者の10人に6人以上(63%)が今後5年間介護を続けると予想しているのに対し、認知症のない人の介護者の半数以下(49%)である323。
5.1.5 無報酬の介護時間と介護の経済的価値
2019年には、アルツハイマー病やその他の認知症の人の家族やその他の無給の介護者1,630万人が、推定186億時間の無給ケアを提供した。この数字は、介護者 1 人当たりの平均介護時間が週 21.9 時間、介護者 1 人当たりの年間介護時間が 1,139 時間に相当する14 。この介護の価値は 1 時間当たり 13.11 ドル15 であり、全米の認知症患者の家族やその他の無報酬介護者が提供した介護の経済的価値は、2019 年には 2,440 億ドル近くになった。表 8 は、米国と各州における家族やその他の無報酬介護者が提供したケアの価値と、無報酬ケアの総時間を示したものである。アルツハイマー病やその他の認知症の人の無給介護者は、22 州の各州で 40 億ドル以上の価値のあるケアを提供した。カリフォルニア州、フロリダ州、ニューヨーク州、テキサス州の4つの最も人口の多い州では、それぞれ150億ドル以上の介護を提供している。認知症の人の家族介護の金銭的価値を縦断的に調査したところ、毎日の家族介護の全体的な価値は、介護を1年続けるごとに18%増加し、介護を受ける人の認知能力が低下するにつれて、介護の価値はさらに増加することがわかった336,337。
表8. アルツハイマー病やその他の認知症の人の介護者数、無給ケアの時間数、無給ケアの経済的価値、州別、2019年*。
州 介護者数(単位:千人) 未払い介護時間(単位:百万時間) 未払い介護の金額(単位:百万ドル
アラバマ州 306 349 349 $4,576
アラスカ州 33 38 495
アリゾナ州 346 394 5,165
アーカンソー州 178 203 2,663
カリフォルニア州 1,624 1,849 24,245
コロラド州 256 292 3,825
コネチカット州 178 203 2,655
デラウェア州
コロンビア特別区 29 33 433
フロリダ州 1,152 1,312 17,206
ジョージア州 540 615 8,063
ハワイ 65 74 975
アイダホ州 87 99 1,299
イリノイ州 587 668 8,759
インディアナ州 342 390 5,112
アイオワ州 136 155 2,036
カンザス州 152 173 2,268
ケンタッキー州 274 312 4,089
ルイジアナ 231 264 3,456
メイン州 70 79 1,042
メリーランド州 294 335 4,389
マサチューセッツ 340 387 5,075
ミシガン州 518 590 7,733
ミネソタ州 257 293 3,838
ミシシッピ州 207 235 3,085
ミズーリ州 319 363 4,755
モンタナ州 51 58 757
ネブラスカ州 83 95 1,240
ネバダ州 153 175 2,289
ニューハンプシャー州 68 78 1,016
ニュージャージー州 448 510 6,684
ニューメキシコ州 108 123 1,617
ニューヨーク 1,011 1,151 15,089
ノースカロライナ州 479 545 7,151
ノースダコタ州 30 35 454
オハイオ州 604 688 9,018
オクラホマ州 226 257 3,371
オレゴン州 188 214 2,810
ペンシルバニア州 677 771 10,104
ロードアイランド州 54 61 800
サウスカロライナ州 318 362 4,749
サウスダコタ州 39 44 575
テネシー州 444 506 6,628
テキサス州 1,449 1,650 21,628
ユタ州 159 181 2,366
バーモント 30 34 449
バージニア州 467 532 6,970
ワシントン州 353 402 5,268
ウエストバージニア州 105 120 1,574
ウィスコンシン州 195 223 2,918
ワイオミング 28 31 413
米国 TOTAL 16,343 18,611 $243,994
* 四捨五入のため、州の合計が米国の合計に加算されない場合がある。
2009年行動リスク因子サーベイランスシステム調査、米国国勢調査局、メディケア・メディケイド・サービスセンター、全米介護アライアンス、AARP、および米国労働省のデータを基に作成12,14,15
認知症の人の介護者は、認知症のない人に比べて月平均27時間以上(92時間対65時間)の介護を行っていると報告されている。1999 年から 2015 年までの全国の介護の傾向を分析したところ、認知症の介護者の 1 週間の平均介護時間は 1999 年の 45 時間から 2015 年には 48 時間に増加したが、同時期に認知症以外の介護者の 1 週間の介護時間は 34 時間から 24 時間に減少した。
5.1.6 アルツハイマーの介護の影響
アルツハイマー型認知症や他の認知症の人の介護は、特別な課題を伴う。たとえば、アルツハイマー病の中間から後期の段階では、判断力、方向性、および理解し、効果的にコミュニケーションする能力の損失を経験する。家族の介護者は、アルツハイマー型認知症の人がこれらの問題を管理するのを助けなければならないことが多い。339-341 アルツハイマー型認知症の人は、病状が進行するにつれ、監督やケアのレベルが上がっていく。症状が悪化すると、家族が必要とするケアは、介護者の精神的ストレスや抑うつ状態の増加、新たな健康問題の発生や悪化、雇用の中断や自分自身や認知症とともに生きる人々のためのヘルスケアやその他のサービスへの支払いのための収入や財政の枯渇などの結果となる可能性がある。
介護者の感情と社会的幸福
介護者と認知症の人との間にある親密な関係、共有された経験や思い出は、アルツハイマー病の進行に伴う記憶喪失、機能障害、精神・行動障害のために脅かされる可能性がある。しかし、全国世論調査では、認知症の人の介護者の45%が、認知障害のある人を助けることは非常にやりがいがあると答えている。
負担とストレス
- 認知症の介護者は、認知症のない人の介護者よりも、認知症の介護者の方が負担が大きいと分類されている(46%対38%)。
- 認知症のない人の介護者に比べて、認知症の人の介護者の2倍もの人が、精神的、経済的、身体的に相当な困難を指摘している。
- 13 認知症の介護者の半数近く(49%)が、介助をすることが非常にストレスになると回答しているのに対し、認知症のない人の介護者は35%であった。
図9 アルツハイマー病やその他の認知症の人の介護者のうち、介護による精神的・身体的ストレスが高いか非常に高いと報告する人の割合
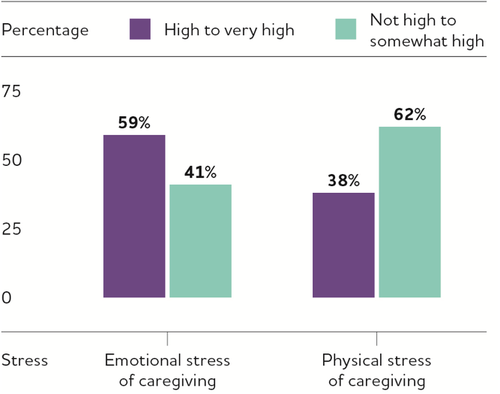
アルツハイマー病協会のデータから作成13
うつ病とメンタルヘルス
- メタアナリシスでは、認知症の人の介護者は、非介護者に比べてうつ病や不安を経験する可能性が有意に高いことが報告されている。
- うつ病の有病率は、統合失調症(20%)や脳卒中(19%)など、他の介護者よりも認知症介護者(30%~40%)の方が高い。
- メタアナリシスでは、関係の種類が介護者のうつ病の最も強い予測因子であり、配偶者の介護者は、配偶者ではない人の介護者に比べて、うつ病になる確率が2.5倍高かった362。
認知症の介護者における不安の有病率は44%であり、脳卒中の介護者(31%)よりも高い。 - アルツハイマー病患者の介護者は、年齢や他の特徴を考慮した非介護者と比較して、主観的な認知問題(例えば、記憶力の問題)が多く、時間の経過とともに認知力が低下することを経験している。
- 4 つ以上の行動・心理的症状(例えば、攻撃性、自傷行為、徘徊など)がある認知症の人の介護は、臨床的に意味のある抑うつや負担(つまり、介護を提供することに対する否定的な感情反応)を報告する可能性が高いため、家族介護者にとっては「転換点」となる。
重圧
- アルツハイマー病やその他の認知症の人の介護者は、認知症のない人の介護者に比べて、医療・看護関連の仕事(例えば、注射、経管栄養、カテーテル・コロストミーのケアなど)を完了するのが難しいと報告する可能性が2倍(22%、11%)であった331。
- アルツハイマー型認知症や他の認知症の介護者の約半数(51%)は、医療・介護関連業務の経験がないと報告しており、複雑な薬物療法を管理するために必要な情報やリソースが不足していることが多い。
- 2014年のアルツハイマー病協会の介護者を対象とした世論調査によると、回答者は介護者の役割を引き受けることに選択肢がないと考えていることが多い13。
- この世論調査では、18 歳未満の子供を持つ女性の半数以上が、認知症の人の介護は子供の介護よりも困難だと感じていることもわかった(53%)13。
- 13 アルツハイマー病やその他の認知症の人の介護者の多くは、一人で介護を行っている。2014年のアルツハイマー病協会の世論調査では、認知症の介護者の41%が、他の誰も無給の援助をしていないと報告している13。
- 認知症介護者を対象とした人口ベースのサンプルでは、認知症介護者は非認知症介護者よりも大きな負担を示しているが、白人と黒人・アフリカ系アメリカ人の認知症介護者の間では負担に大きな差は見られないことがわかった。
介護移行のストレス
親族を居住用ケア施設に入所させることは、家族介護者の情緒的および心理的な幸福に様々な影響を及ぼす。一部の研究では、親族が住宅介護施設に入所しても苦痛は変化しないか、あるいは増加することさえ示唆しているが、他の研究では入所後に苦痛が減少することが明らかにされている。
376 認知症の人が亡くなる前の年には、介護者の 59%が 1 日 24 時間「当直」であると感じており、この間の介護は非常にストレスが多いと感じていた。
介護者の身体の健康
介護者の中には、介護の要求が自分自身の健康状態を悪化させる場合もある。図9に示すように、アルツハイマー病やその他の認知症の介護者の38%が介護の身体的ストレスが高いか非常に高いと回答している13。379-381 認知症の人の介護者は、介護者ではない同年代の人と比較して、週に2.4時間から3.5時間の睡眠時間を失っていると推定されている。
一般的な健康
アルツハイマー型認知症やその他の認知症の人の介護者の 74%が、介護者になってから自分の健康を維持することについて「やや心配」から「非常に心配」と答えている13。また、アルツハイマーや他の認知症の人の介護者の35%が、介護責任のために健康状態が悪化したと報告しているのに対し、認知症のない人の介護者は19%であった。2017年の世論調査によると、認知症の介護者の27%が、自分の健康を維持するためにやるべきことを遅らせたり、やらなかったりしていると報告されている。認知症の介護者は、非介護者よりも健康に関連した生活の質が低く、非介護者や他の介護者よりも健康状態が「まあまあ」または「悪い」と報告する可能性が高い。348, 382, 384 Health and Retirement Studyのデータによると、配偶者に介護を提供した認知症の介護者は、同年齢の他の配偶者介護者に比べて、介護者になってから配偶者が亡くなるまでの間に、ますます虚弱になる可能性が高い(41%のオッズ増加)ことが示されている。
最近の研究では、多様な人種・民族背景を持つ認知症介護者の自己評価の健康状態の変化が調査されている。家族や友人からの支援は、黒人やアフリカ系アメリカ人の認知症介護者の自己評価の向上と関連しているが、白人やメキシコ系アメリカ人の介護者では関連していない。介護者と認知症の人との間に肯定的な関係があることは、黒人/アフリカ系アメリカ人介護者と白人介護者の間で自己評価の高い健康状態と関連している。
生理的変化
介護の慢性的なストレスは、高血圧症の発症率の増加342, 388-395,および高レベルのストレスホルモン388,免疫機能の低下342, 389,創傷治癒の遅れ390,冠動脈性心疾患など、慢性疾患の発症リスクを高める多くの生理学的変化と関連している可能性がある。396 介護の生理的影響をよりよく理解するためには、介護開始前と介護開始後の生理的変化について、多様な集団を対象にした追加の研究が必要である。
健康管理
認知症の人の介護者で、抑うつ症状や行動障害、機能状態が低下している人は、これらの症状がない認知症の人の介護者よりも、入院や救急外来を受診する可能性が高い397, 398。介護者の抑うつ症状の長期的な増加は、医師の受診頻度の増加、外来での検査や処置の増加、市販薬や処方薬の使用量の増加と関連している。
死亡率
例えば、入院して認知症になった配偶者の介護者は、入院していたが認知症にならなかった配偶者の介護者よりも翌年に死亡する可能性が高い(介護者の年齢差を考慮した場合)。対照的に、Health and Retirement Studyの参加者を対象とした縦断的研究では、認知症の介護者は、同年齢の介護者ではない人に比べて、12年間で死亡する可能性が低いことが明らかになっている。399 この結果は、認知症介護の役割を担う人は、初期の健康状態がそれを可能にしていることもあり、認知症介護の役割を担っている可能性と一致している。配偶者介護者の18%が認知症のパートナーより先に死亡している。
介護士の雇用と家計
アルツハイマーや他の認知症の人の介護者の10人に6人が、介護をしている間に雇用されていたか、または前年に雇用されていた。認知症の介護者の18%が介護の責任のために労働時間を短縮したのに対し、非認知症の介護者の13%であった。過去 1 年間に雇用された認知症介護者と非認知症介護者のその他の業務関連の変化は、図 10.323 にまとめられている。
図10 アルツハイマー型認知症やその他の認知症の人の介護者の中で、介護を始めてからいつでも雇用されていた人の仕事に関連した変化
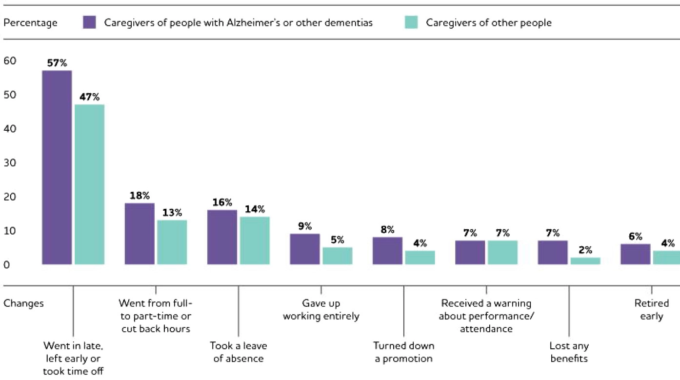
National Alliance for Caregiving と AARP のデータから作成された。
雇用主が認知症の介護にかかる費用には、介護責任を理由に辞めた従業員の代替費用や、欠勤や勤務の中断にかかる費用などが含まれる可能性がある。
2019 年には、認知症の介護者は、認知症の介護者以外の介護者に比べて、平均 2 倍近くの費用(例えば、医療費、認知症の本人の個人的なケアや家計費、介護者の個人的な費用やレスパイトサービスなど)を負担していると推定される(11,372 ドル対 6,121 ドル)。 407 2016 年のアルツハイマー病協会の「Family Impact of Alzheimer’s Survey」のデータによると、介護貢献者(認知症の人に認知症の費用を支払った友人や親戚で、前年に月に 1 回以上認知症の人の介護を行った人)の間では、48%が支出を削減し、43%が認知症の人への援助にかかる費用のために貯蓄を削減していることが示されている。調査の前年に介護の責任があったため、10 人に 4 人近くが「買ってきた食事が続かず、買い足すお金がない」と答え、10 人に 3 人が介護関連の費用のために食事を減らしたと答えている。
介護者のストレスが認知症の人に与える影響
介護者のストレスが認知症の人や医療サービスの利用に及ぼす影響についての研究が出てきている。例えば、家族介護者の苦痛は、認知症の人の施設入所の可能性の増加、認知症の人の行動的・心理的課題の悪化、認知症の人が虐待を受ける可能性の増加と関連している。
5.1.7 介護者の支援を目的とした介入
30 年以上にわたり、認知症の人の家族介護者を支援するための戦略が開発され、評価されてきた。これらの戦略の種類と焦点(「介入」と呼ばれることが多い)は、表9.347,409にまとめられている。
表 9. 介護者の介入の種類と焦点
タイプ/フォーカス
ケースマネジメント 家族の介護者のために、評価、情報、計画、紹介、ケア調整、および/またはアドボカシーを提供する。
精神教育的アプローチ 疾患、資源、サービス、および疾患の症状(例えば、認知機能障害、行動症状、介護関連のニーズ)に効果的に対応するためのスキルの拡大方法に関する情報を提供する構造化されたプログラムを含みます。講義、考察、文書による資料を含み、専門的な訓練を受けた専門家が指導する。
カウンセリング 介護を複雑にする既存の個人的な問題を解決し、介護者と介護を受ける人との間の葛藤を減らし、家族の機能を向上させることを目的としている。
心理療法的アプローチ 介護者と専門のセラピストとの間の治療関係の確立を伴う(例えば、介護者のための認知行動療法では、感情的苦痛に関連する信念の特定と修正、介護の要求に対処するための新しい行動の開発、介護者の幸福を促進することができる活動の育成に焦点を当てている)。
レスパイト 代替ケアの提供を通じて、計画された一時的な緩和を介護者に提供する;例としては、成人のデイサービスや、週に一定の時間数の在宅または施設でのレスパイトケアがある。
サポートグループは、精神教育的介入や心理療法的介入よりも構造化されていない。サポートグループは、介護者が個人的な感情や懸念事項を共有して孤立感を克服する機会を提供する。
多成分アプローチは、教育、支援、レスパイトなどの複数の形態の介入を1つの長期的なサービスに組み合わせた集中的な支援戦略が特徴である(多くの場合、12ヵ月以上にわたって提供される)。
(Pinquart er al)。およびGaugler er al)。346, 409のデータを基に作成。
一般的に、介入の目的は、介護の負の側面を緩和することで認知症の介護者の健康と幸福を改善することである。また、介護者にスキルやリソース(感情的、社会的、心理的、技術的)を提供し、在宅での親族や友人の支援を継続できるようにすることで、認知症の人の介護施設入所を遅らせることを目的としたものもある。様々な介入で用いられる具体的なアプローチとしては、介護者への教育の提供、介護者の認知症関連症状の管理の支援、介護者の社会的支援の改善、介護者への介護業務からの一時的な休息の提供などがある。
7つのメタアナリシスとランダム化比較試験の17の系統的レビューをレビューした認知症介護者介入に関する出版物によると、以下の特徴が効果的な介入を区別している:家族介護者が受動的に情報を受け取るのとは対照的に、積極的に介入に関与していること、親族の認知症の経過中に変化する家族介護者のニーズを満たすように介入が調整され、柔軟であること、介護者だけでなく認知症とともに生きる人々のニーズを満たしていること。2012年の報告書では、介護者の介入に関する無作為化対照研究を調査し、認知症の個人と介護者に利益をもたらす44の介入を特定した。411-416 最も有益な認知症介護者介入の構成要素を検討したメタアナリシスでは、最初に介護能力を高め、徐々に認知症本人の介護ニーズに対応し、必要に応じて喪失や悲しみに対する感情的なサポートを提供する介入が最も効果的であることが明らかになった。
科学的評価で有効性が実証されている認知症介護者向けの介入は、地域社会で徐々に実施されてきているが、まだ普及していないし、すべての家族介護者が利用できるわけではない。介入が実施されると、一般的には介護者のサービス提供方法の改善に成功し、多くの家族に届く可能性があると同時に、介護者の責任への対処を支援することにもなる。このケアモデルは、インディアナポリスの医療システムで10年近く成功を収めている。他の取り組みでは、テクノロジー(例えば、テレビ電話配信やオンライントレーニング)を利用して、認知症介護者への介入の手の届く範囲とアクセスのしやすさを広げる試みが行われている435-442。Pragmatic AD/ADRD Clinical Trials (IMPACT) Collaboratory. この共同研究機関には、30以上のトップ研究機関の専門家が参加しており、今後5年間で、認知症とともに生きる人々のために、非薬物的でケアに基づいた介入を試験するための最大40のパイロット試験を支援する予定である。IMPACTの目標は、認知症の人とその介護者のケアを改善するために、現実世界での研究実施のタイムラインを加速させることだ。
介護者と介護を提供する環境は多様であるため、どの介入が特定の状況に最も効果的であるか、またその介入がどのように成功しているかを定義するために、より多くの研究が必要とされている。444-447 介護者の利益を最大化するために介護者のサービスをパーソナライズするための改善されたツールと手段は、新たな研究分野である。また、人種、民族、社会経済的背景が異なり、地理的環境が異なる家族のために、実証済みの介入を適応させたり、新たな介入アプローチを開発したりするために、より多くの研究が必要とされている。455-469 疾患ステージに焦点を当てた介入に関する追加研究や、LGBT 介護者のための特定の介入ニーズに関する研究も必要である。
5.2 有給の介護士
5.2.1 アルツハイマー型認知症などの認知症の人の直接介護者
看護師のエイド、訪問看護のエイド、パーソナルケアおよび訪問介護のエイドなどの直接介護労働者は、在宅または住宅地で暮らす高齢者に有給の長期ケアの大部分を提供している470,471。看護助手のほとんどは女性であり、民族、人種、地理的背景はますます多様化している。472-474 介護助手は、入浴、着替え、家事、食事の準備、その他の活動を手伝う。看護助手のほとんどは女性であり、民族、人種、地理的背景はますます多様化している。
直接介護労働者は仕事が難しく、認知症ケアを提供するために必要な訓練を受けていない場合もある。476, 478 不十分な教育と困難な職場環境もまた、介護環境の違いによる介護スタッフの離職率の上昇の一因となっている。479 介護施設や病院における認知症ケアの質を向上させるための職員研修プログラムは、それなりの効果があることが研究で示されている。475, 480-484 全米科学・工学・医学アカデミーは、研修時間を 75 時間から 120 時間に増やすことを含め、一般的な直接介護職員研修の連邦要件の変更を推奨している。
アルツハイマー病やその他の認知症の人の介護に関連した知識やスキルに重点を置いた指導内容を提供している。
5.2.2 老人医療従事者の不足
高齢者の介護において特別な訓練を受ける可能性のある専門家には、医師、看護師、正看護師、ソーシャルワーカー、薬剤師、 医師助手、ケースワーカーなどが含まれる476 。2016年の時点で、米国の認定老年医は7,293人、つまりケアを必要としている65歳以上の米国人1,924人に1人の老年医がいることになる486。米国老年医学会は、老年医療を必要とする脆弱な高齢の米国人が増加していることから、現在から 2030年までの間に、高齢化する米国の人口のニーズを満たすために、さらに2万3,750人の老年医を養成する必要があると推定している487(追加情報は特別報告書を参照)。2019 年の米国における看護師開業医は 272,000 人であった。476 ソーシャルワーカーの 73%が 55 歳以上のクライエントにサービスを提供しているが、老人福祉の正式な資格を持っているのはわずか 4%である。
5.2.3 家族介護者の健康管理の充実
アルツハイマー病やその他の認知症の人を介護する専門家は、家族介護者が認知症の治療を促進する役割を認識すべきであり、専門家は認知症の人の全体的な疾患管理を改善するために家族介護者の幸福度を評価すべきであるというコンセンサスが高まってきている。489-493 認知症患者の複雑なケアの課題には、専門職間の連携と教育も必要である。494-497 認知症の人のための伝統的なプライマリーケアに革新的なケアマネジメントの実践を統合しようとする試みは、現在進行中である。その一例として、熟練した専門職が認知症の人のケアマネージャーとしての役割を果たすことが挙げられる。ケアマネージャーはプライマリ・ケアの医師や看護師と協力して、個別化されたケアプランを作成する。この計画では、家族の介護者をサポートし、認知症の人がケアの移行(例えば、ケア提供者の変更やケアの場所の変更)を管理し、認知症の人が適切な地域のサービスを利用できるようにすることができる。その他のモデルとしては、認知症の人の包括的な疾患管理と同時に家族介護者のニーズにも対応し、認知症の人の生活の質を向上させるというものもある。498 いくつかの評価では、このようなアプローチは認知症患者とその家族介護者の転帰を改善する可能性が高いことが示唆されている(例えば、介護施設入所の遅延や介護者の苦痛の軽減など)。499-508 現在の研究では、これらのモデルが現在実施されている専門的な設定の範囲を超えて、その実現可能性を判断しようとしている。509-512
2016年、全米科学・工学・医学アカデミー(National Academies of Sciences, Engineering, and Medicine)は、「Families Caring for an Aging America」という画期的な報告書を発表した。404 これらのサービスモデルでは、家族がケアを提供する上で重要な役割を果たしていることを認識し、認知症の親族への医療提供の際に家族介護者を取り入れることになっている。さらに、医療提供者は、介護者と認知症の人の両方にエビデンスに基づいたサービスと支援を提供することを奨励している。404, 513
2017年1月、メディケアは、包括的な認知症ケア計画に基づいて訪問診療を行った場合、医師、医師助手、看護師、臨床看護師の専門家に報酬を支払うようになった。包括的なケアプランは、効果的な認知症ケアマネジメントの中核的要素であり、認知症の人とその介護者の生活の質を潜在的に高めるサービスの提供につながる可能性がある。ケアプランニング給付金が利用できるようになった最初の年(2017)では、アルツハイマー病やその他の認知症の人のうち、包括的な認知症ケアプランを受けている人は1%にも満たなかった。7つの州(アラスカ州、モンタナ州、ニューハンプシャー州、ノースダコタ州、ロードアイランド州、サウスダコタ州、バーモント州)とコロンビア特別区では、有料サービスのメディケア受給者で包括的な認知症ケアプランを受けた人はいなかった。メディケアのケアプラン給付金の利用は年間を通じて増加しており、第4四半期の利用率は3.3倍となっている。2017 年第 1 四半期と比較して、2017 年第 4 四半期の利用率は 3.3 倍であった。514 アルツハイマー協会は、ケアプランニングキット(alz.org/careplanning)を作成し、認知症の人とその家族の介護者に効果的なケアプランを提供するための指針としている。
5.3 認知症介護の動向
家族が認知症の親族に提供するケアの管理が、昔に比べて上手になっていることが示唆されている。1999年から 2015年にかけて、認知症介護者は、介護に関連した身体的困難(1999年30%→2015年17%)と経済的困難(1999年22%→2015年9%)を報告する可能性が有意に減少した。また、認知症介護者によるレスパイトケアの利用は大幅に増加している(1999年の13%から 2015年には27%に)338 。しかし、前述のように、認知症介護者のための介入が利用可能であり、必要な人が利用できるようにするためには、より多くの研究が必要である。高齢者法の全国家族介護者支援プログラムに関する2016年の調査では、高齢化地域機関の半数以上(52%)が、エビデンスに基づいた家族介護者の介入を提供していないことが明らかになった。
アルツハイマー病協会は、認知症ケアの研究と提供方法を改善するためにいくつかの取り組みを行ってきた。最近の認知症ケアの実践に関する提言516 では、認知症の人とその介護者をケアの提供方法の中心に据えている(図11参照)。このモデルに不可欠なのは、認知症による能力の喪失に焦点を当てたアプローチから、本人の固有のニーズ、個人的な経験、強みを重視したアプローチへと移行することで、認知症の人のケアの測定方法や設計方法を再考する必要があるということである。この新しい枠組みは、研究者やケア提供者の認知症に対する考え方を変えることを目的としており、認知症とともに生活する際の回復力や適応力、スキルや能力の維持・向上の可能性をより深く理解するための道を示すものとなるかもしれない517。519 このフレームワークや他のフレームワークの中核的な要素は、すべての経験や相互作用が有意義な関わりを持つ機会とみなされ、認知症の人の生活の質を向上させるのに役立つことを保証することである。
図11 人を中心としたケアの提供
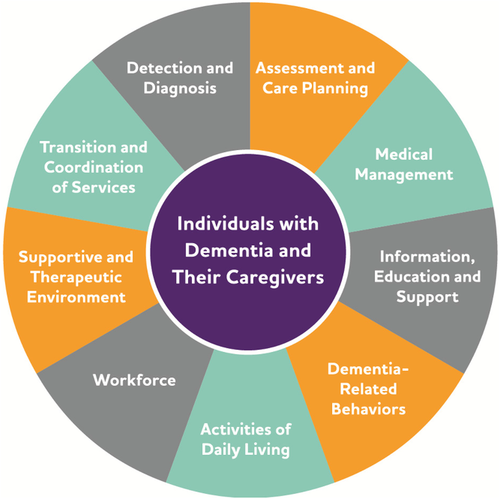
アルツハイマー病協会のデータから作成。
6 医療、長期療養、病院の利用と費用
アルツハイマー型認知症やその他の認知症の人の医療費や長期ケアの費用は相当なものであり、認知症は社会的に最もコストのかかる疾患の一つである。メディケアとメディケイドは、アルツハイマーやその他の認知症の人たちのヘルスケアと長期ケアの支払い総額の67%にあたる2060億ドルをカバーすると予想されている。ポケットからの支出は660億ドル(支払い総額の22%)になると予想されている16。
図12 アルツハイマー型認知症またはその他の認知症を持つ65歳以上の米国人の支払源別のケアにかかる総費用の分布、2020年
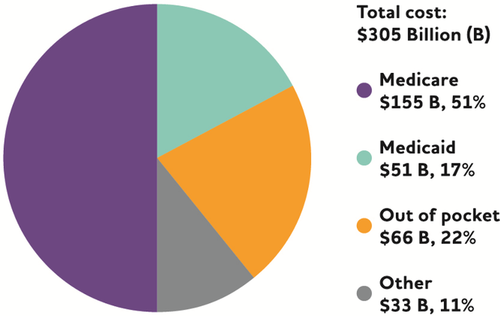
データは2020年ドル。四捨五入のため、パーセンテージの合計は 100 ではない。16 「その他」の支払源には、民間保険、健康維持機関、その他のマネージドケア機関、補償のないケアが含まれる。
6.1 医療および長期ケアの総費用
表 10 は、65 歳以上のメディケア受給者(アルツハイマー病やその他の認知症の有無に関わらず)の医療・介護サービスに対する一人当たりの年間平均支払額を報告している。アルツハイマー型認知症やその他の認知症を持つメディケア受給者の2019年の一人当たりの医療・介護サービスの支払い総額は、同じ年齢層の他のメディケア受給者の支払い総額の3倍以上であった(認知症を持つ人は一人当たり50,201ドル、認知症を持たない人は一人当たり14,326ドル)。
表10. 医療および長期介護サービスの支払い源別平均年間一人当たりの支払い額
メディケア受給者の年齢65歳以上、アルツハイマー病またはその他の認知症の有無、2019年のドル数
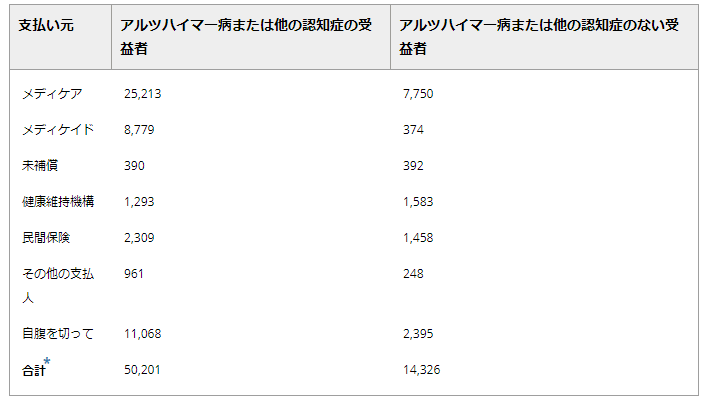
* 源泉からの支払いは、人口の重み付けの影響により、支払い総額と正確には一致しない。アルツハイマー型認知症またはその他の認知症を持つすべての受益者に対する支払いには、地域居住者および施設居住者に対する支払いが含まれている。
メディケア現受給者調査(2011)の未発表データを基に作成。
メディケアに加入しているアルツハイマーやその他の認知症の高齢者の27%がメディケイドにも加入しているのに対し、認知症のない高齢者は11%である。207 メディケイドは、非常に低所得で資産の少ない一部の人々のために、介護施設やその他の長期介護サービスに支払いを行っており、認知症の人々がこれらのサービスを多く利用しているため、メディケイドへのコストが高くなっている。アルツハイマーやその他の認知症を持つメディケア受給者の一人当たりの平均年間メディケイド支払額(8,779 ドル)は、アルツハイマーやその他の認知症を持たないメディケア受給者の平均メディケイド支払額(374 ドル)の 23 倍であった(表 10)。
このような経済的支援を受けているにもかかわらず、アルツハイマー型認知症やその他の認知症の人は、高額の生活費を負担している。これらのコストは、メディケア、他の健康保険料、控除額、自己負担額、メディケア、メディケイド、またはサポートの追加の情報源でカバーされていないサービスのためのものである。平均して、65 歳以上のアルツハイマー病やその他の認知症のメディケア受給者は、他の支援源ではカバーされていない健康管理や長期介護サービスのために、年間 11,068 ドルをポケット外に支払っている(表 10)。
研究者たちは、認知症の追加的、あるいは「増分的」な医療費、住宅長期介護費、家族介護費(つまり、同じ病状や人口統計学的特徴を持つ認知症のある人とない人を比較したときに、認知症に特に起因する費用)を評価してきた。ある研究グループでは、認知症患者の医療費と介護施設費の増分は、2010年には一人当たり年間28,501ドル(2019年には36,400ドル)であった19,520。 524 さらに、女性は寡婦になりやすく、貧困の中で生活しているため、アルツハイマー型認知症に関連したメディケイドの増分費用は男性よりも女性の方が70%高くなっている。第三の研究者グループは、生活費、メディケアやメディケイドの支出、インフォーマルな介護の価値を含めた生涯介護費用は、2015年ドルでアルツハイマー型認知症患者一人当たり321,780ドル(2019年ドルでは357,297ドル)であることを明らかにした。 312 アルツハイマー型認知症の人の生涯介護費用は、アルツハイマー型認知症のない人の2倍以上で、アルツハイマー型認知症の増分生涯費用は184,500ドル(2019年ドルで204,864ドル)であった。
いくつかの研究グループが、アルツハイマー型認知症やその他の認知症の人が負担する追加の費用を調査している。最近の認知症の生涯増分コストの分析では、認知症の人は 65 歳から死亡までの間に、介護施設でのケアのために、38,540 ドル(2014 年ドル、2019 年ドルでは 43,920 ドル)の費用負担が増加していることがわかった。別の研究グループによると、65歳以上のアルツハイマー型認知症の地域居住者は、アルツハイマー型認知症のない人に比べて、患者の特徴の違いをコントロールした後、年間の医療費が1,101ドル(2012年ドル、2019年は1,316ドル)高くなっており、その差の最大の部分は在宅医療と処方薬への支出の増加によるものである526。さらに、アルツハイマー型認知症の人は収入の12%を医療費に費やしているのに対し、アルツハイマー型認知症のない人は7%である527 。別の研究チームによると、認知症の5年間の増分コストは15,704ドル(2017年ドル、2019年は16,389ドル)で、診断後1年目の追加ケア費用が5年間の増分コストの46%を占めている527 。
他の研究者が認知症のある人とない人の終末期の費用を比較したところ、人生の最後の 5 年間にかかる費用の総額は、認知症のある人では 2010 年のドルで 287,038 ドル、認知症のない人では 183,001 ドル(2019 年のドルではそれぞれ 366,593 ドル、233,721 ドル)で、57%の差があることがわかった。
6.2 医療サービスの利用と費用
6.2.1 ヘルスケアサービスの利用
291 さらに、他の重篤な病状の人の医療サービス利用は、認知症の有無に大きく影響される。特に、冠動脈疾患、糖尿病、慢性腎臓病、慢性閉塞性肺疾患(COPD脳卒中、がんなどで、アルツハイマー病やその他の認知症を併発している人は、これらの病状を持っていても認知症を併発していない人に比べて、医療サービスの利用とコストが高い。
入院日数が多いだけでなく、アルツハイマー病やその他の認知症を持つ高齢者は、他の高齢者よりも年間の熟練した介護施設での滞在や在宅医療の訪問回数が多い。
- 病院。291 2012 年の認知症の人の平均入院日数は 23 日(病院や介護施設での入院日数と定義される)であったのに対し、メディケア人口全体では 5 日であった。アルツハイマー型認知症の人の入院理由で最も多いのは、失神(失神転倒、外傷(26%虚血性心疾患(17%消化器疾患(9%)である(図 13)530 。60 歳以上の成人の入院患者を対象とした研究では、アルツハイマー型認知症の人は、アルツハイマー型認知症のない人に比べて、入院中に死亡するリスクが 7%高く、入院期間が 1 日近く長くなっていた531 。532 直接比較はできないが、メディケア受給者の一部を対象としたある研究では、全体の再入院率は18%であることが示されている。
- 救急科。532 直接比較できるものではないが、メディケアの受益者のサブセットの利用パターンのレビューに基づいて、メディケアの受益者1,000人当たりの年間救急部門受診数は640件であった533。メディケア受給者1,000人当たりのアルツハイマー病やその他の認知症の人の救急部門受診は、2007年から 2017年の間に22%増加した(1,265人から1,548人へ)が、がん、虚血性心疾患、心不全の人の救急部門受診の増加と同様である(図14)532。
- 熟練看護施設。534 アルツハイマー病やその他の認知症の受益者1,000人あたりの年間の熟練看護施設滞在数は283人であるのに対し、そうでない受益者1,000人あたりの滞在数は73人であり、その割合は4倍近くになる。
- 在宅医療。アルツハイマー病やその他の認知症を持つ65歳以上のメディケア受給者の25%が1年間に少なくとも1回は在宅医療を受けているのに対し、アルツハイマー病やその他の認知症を持たない65歳以上のメディケア受給者の10%である。291 メディケアは、パートタイムの熟練した介護、在宅医療補助(個人的なハンズオン)ケア、治療、医療ソーシャルサービスなどの在宅医療サービスをカバーするが、ホームメーカーやパーソナルケアサービスは含まれない。
イメージ
図13 アルツハイマー型認知症患者の入院理由
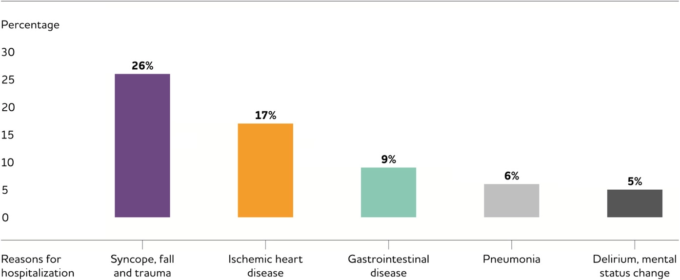
入院診断別の入院者の割合。アルツハイマー型認知症の可能性が高い、または高い可能性があると診断された人の入院はすべてパーセンテージを計算するために使用された。残りの37%の入院は他の理由によるものである。Rudolph er al)。530のデータを基に作成。
イメージ
図14 2007年から 2017年の間に選択された健康状態について
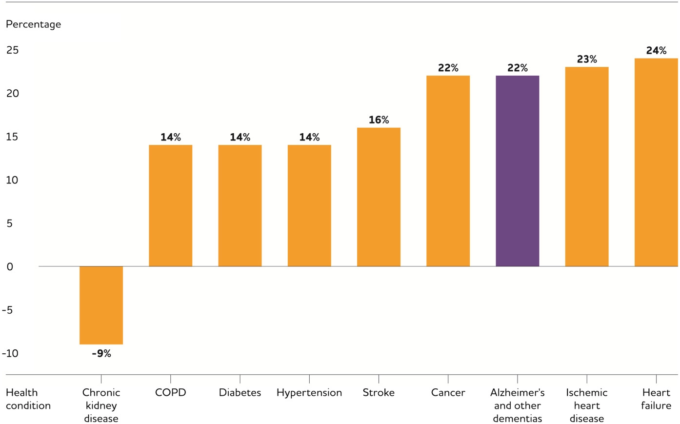
有料サービスのメディケア受給者1,000人当たりの救急部門受診数の変化率。各慢性疾患のクレームベースの診断を受けたメディケア受給者を含む。受給者は複数の慢性疾患を持っている可能性がある。米国メディケア・メディケイド・サービスセンター(Centers for Medicare & Medicaid Services)のデータを基に作成。
6.2.2 医療サービスにかかる費用
医療サービス(病院、医師、その他の医療提供者、介護施設、熟練した介護施設、ホスピス、在宅医療)と処方薬に対する一人当たりの平均支払額は、アルツハイマー病やその他の認知症を持つメディケア受給者の方が、同じ年齢層の他のメディケア受給者よりも高かった(表 11)207。
表11. 医療および長期介護サービスに対するサービスの種類別平均年間一人当たりの支払い額
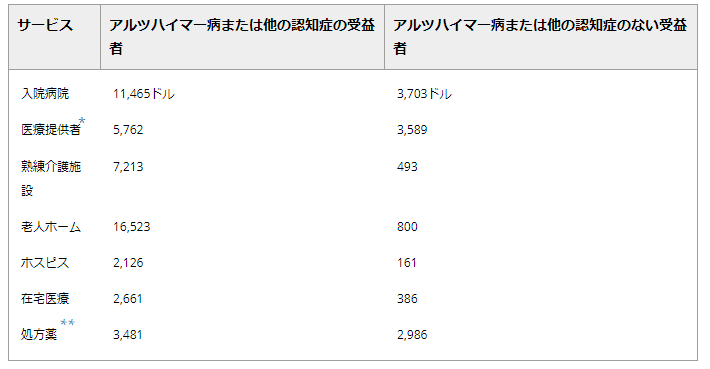
65歳以上のメディケア受給者(アルツハイマー病またはその他の認知症の有無にかかわらず2019年のドル数
サービス受給者 アルツハイマー型認知症またはその他の認知症の受給者 アルツハイマー型認知症またはその他の認知症の受給者 アルツハイマー型認知症またはその他の認知症の受給者 アルツハイマー型認知症またはその他の認知症の受給者
* 医療提供者」には、医師、その他の提供者、検査サービス、医療機器や消耗品が含まれる。
** 処方箋薬の支払いに関する情報は、地域社会で生活していた人のみを対象としており、老人ホームや介護施設ではない。
メディケア現受給者調査(2011)の未発表データを基に作成。
6.2.3 州別の医療サービスの利用と費用
アルツハイマー型認知症やその他の認知症を持つ人の医療利用とメディケアの支払いには、他の病状を持つメディケア受給者の場合と同様に、地理的に大きな差がある(表 12)。535 救急部門の受診は、サウスダコタ州では受給者 1,000 人当たり 1,134 人からウェストバージニア州では受給者 1,000 人当たり 1,828 人までとなっており、30 日以内に病院に入院した後に再入院した割合は、ユタ州では 15.4%からコロンビア特別区では 26.8%までとなっている。一人当たりのメディケア支出は、ノースダコタ州の17,572ドルからネバダ州の34,875ドル(2019年ドル)までの範囲である。
表12. アルツハイマー型認知症またはその他の認知症を持つメディケア受給者による救急部(ED)の訪問、病院の再入院、および2019年の一人当たりメディケア支払い額(2017年)州別
州 受給者1,000人当たりのED受診者数 30日以内に再入院した入院の割合 人頭当たりのメディケア支払い額
アラバマ州 1,426.8 21.5 22,555
アラスカ州 1,447.9 19.6 24,801
アリゾナ州 1,491.3 20.6 25,490
アーカンソー州 1,563.6 21.8 22,373
カリフォルニア州 1,497.6 23.1 32,940
コロラド州 1,437.1 18.3 23,060
コネチカット州 1,568.0 22.0 28,461
デラウェア州 16,000.0 21.8 28,260
コロンビア特別区 1,698.5 26.8 31,993
フロリダ州 1,564.9 23.4 28,606
ジョージア州 1,568.5 21.9 24,228
ハワイ州 1,225.2 17.4 20,009
アイダホ州 1,401.8 17.0 21,051
イリノイ州 1,611.9 23.1 28,485
インディアナ州 1,510.5 21.0 25,572
アイオワ州 1,344.7 18.5 18,715
カンザス州 1,394.1 19.4 22,787
ケンタッキー 1,718.4 23.0 24,991
ルイジアナ州 1,770.8 22.1 29,001
メイン州 1,666.3 19.8 21,787
メリーランド州 1,525.6 24.6 30,331
マサチューセッツ州 1,618.0 24.3 30,535
ミシガン州 1,711.5 24.1 28,325
ミネソタ州 1,447.9 21.0 22,830
ミシシッピ州 1,723.3 22.6 26,566
ミズーリ州 1,515.1 22.4 23,441
モンタナ州 1,307.1 17.5 18,664
ネブラスカ州 1,166.5 18.1 21,012
ネバダ州 1,712.2 25.4 34,875
ニューハンプシャー州 1,508.9 21.6 25,147
ニュージャージー州 1,459.8 23.0 30,930
ニューメキシコ州 1,566.1 20.7 22,711
ニューヨーク 1,446.1 23.7 31,353
ノースカロライナ州 1,699.3 21.5 23,226
ノースダコタ州 1,193.4 19.2 17,572
オハイオ州 1,633.7 22.6 26,502
オクラホマ州 1,700.7 21.5 26,351
オレゴン州 1,582.9 18.5 21,210
ペンシルバニア州 1,477.7 22.4 26,839
ロードアイランド州 1,614.9 22.8 26,876
サウスカロライナ州 1,563.8 21.4 23,917
サウスダコタ州 1,134.0 19.1 19,070
テネシー州 1,574.3 22.1 24,199
テキサス州 1,544.9 22.0 30,383
ユタ州 1,205.4 15.4 22,229
バーモント 1,485.6 19.2 22,588
バージニア州 1,637.2 22.0 23,846
ワシントン州 1,483.7 18.5 22,007
ウエストバージニア州 1,827.7 23.6 24,762
ウィスコンシン州 1,510.4 20.1 21,516
ワイオミング州 1,436.6 16.1 21,815
米国平均 1,547.7 22.3 27,101* 米国平均 1,547.7 22.3 27,101
* 一人当たりの平均メディケア支払い額は、基礎となるデータソースが異なるため、表10の数値とは若干異なる。米国メディケア・メディケイド・サービスセンター(Centers for (Medicare & Medicaid Services)のデータを基に作成。
6.2.4 認知機能障害の範囲における医療サービスの利用とコスト
医療費は認知症の存在とともに増加する。70~89歳の成人を対象とした人口ベースの研究では、認知症のある人の年間医療費は、軽度認知障害(MCI)のある人、ない人に比べて有意に高かった536 。
いくつかの研究グループは、アルツハイマー病や他の認知症と診断されていない同様の人と比較して、診断前の1年間、537-539,診断2年前、540,診断後1年後、527, 537, 538で医療費と処方薬の支出が有意に高いことを明らかにしているが、支出の増加源には違いがある。ある研究では、最大の差は入院治療と急性期後のケア538 であり、別の研究では、支出の差は主に外来治療、在宅ケア、医療デイサービスによるものであった539。さらに、3つの研究者グループは、診断後1年間の支出が、診断を受けていない人と比較して、診断後1年間の支出が高いことを明らかにしており、その金額は、2017年のメディケアの有料サービスの適用を受けている人を基準にした7,264ドル(2019年の7,581ドル)527から、メディケアの有料サービスの適用を受けている別のグループの人を基準にした2014年の追加費用17,852ドル(2019年の20,344ドル)までの範囲内である538。アルツハイマー病や他の認知症と診断される直前と直後の1年間に医療費が急増した理由の1つは、タイムリーな診断の遅れに関係している可能性がある。ある研究グループは、専門医(神経内科医、精神科医、老年医など)に診てもらった認知機能低下者は、アルツハイマー病の診断までの期間が短いことを明らかにした。ある研究チームは、認知症と診断された後の最初の4年間はそれぞれ医療費が高くなるが、診断後5年目には有意差がないことを発見した527。
6.2.5 アルツハイマー病やその他の認知症が、共存する病状の人の医療費や利用に与える影響
291 アルツハイマー病やその他の認知症を持つメディケア受給者は、認知症のない人よりも他の慢性疾患を持つ可能性が高い。情報が入手可能な最新の2014年には、65歳以上の認知症のメディケア受給者の38%が冠動脈疾患、37%が糖尿病、29%が慢性腎臓病、28%がうっ血性心不全、25%が慢性閉塞性肺疾患を併発していた。
表13. 特定の共存状態にあるアルツハイマー病またはその他の認知症のある65歳以上のメディケア受給者の割合
既存条件の割合
冠動脈疾患 38
糖尿病 37
慢性腎臓病 29
うっ血性心不全 28
慢性閉塞性肺疾患 25
ストローク 22
がん13
2014年の全国5%サンプルのメディケア診療報酬受給者の未発表データを基に作成。
アルツハイマー病やその他の認知症と共存する医療状態のメディケア受給者は、認知症のない同じ医療状態のメディケア受給者よりも、ほとんどの医療サービスに対する一人当たりの平均支払額が高い。表 14 は、アルツハイマー型認知症やその他の認知症を持つ受給者とアルツハイマー型認知症やその他の認知症を持たない受給者の間の 7 つの特定の医療状態に対するメディケアの一人当たり平均支払額を示している。542 さらに、認知症や行動障害のある人の方が、抗高血圧薬、認知症治療薬、抗精神病薬、抗うつ薬、抗てんかん薬、催眠薬などの薬物を使用している割合が高い。
表14. 65歳以上のメディケア受給者(アルツハイマー病やその他の認知症の有無にかかわらず)に対するサービスの種類と既存の医療条件別の平均年間一人当たりの支払い額(2019年)ドル*)
* この表にはすべての種類のメディケアサービスに対する支払いは含まれておらず、その結果、特定のメディケアサービスに対する一人当たりの平均支払い額は、一人当たりのメディケア支払い総額には加算されていない。
全国 5%サンプルのメディケアサービス費受給者の 2014 年の未発表データを基に作成。
6.3 介護サービスの利用と費用
207 アルツハイマー型認知症やその他の認知症の高齢者の推定70%が地域社会で生活しているのに対し、アルツハイマー型認知症やその他の認知症のない高齢者の98%は地域社会で生活している。認知症の多くの人は、在宅でも有料サービスを受けているが、成人デイセンターや介護施設、老人ホームなどでも有料サービスを受けている。メディケイドは、認知症患者の多くが病気の末期に必要とする長期の介護施設滞在をカバーする唯一の公的プログラムである。
6.3.1 長期介護サービスの利用状況
在宅で生活するアルツハイマー型認知症やその他の認知症の人の多くは、家族や友人からの無報酬の援助を受けているが、中にはパーソナルケアや成人式デイケアなどの在宅・地域密着型のサービスを受けている人もいる。アルツハイマー型認知症やその他の認知症の人は、成人向けデイサービスや介護施設で介護を受ける高齢者の中で大きな割合を占めている。
- 在宅医療サービス。在宅医療サービスを利用している人の32%がアルツハイマー型認知症やその他の認知症を持っている。
- 成人向けデイサービス。全体では、成人デイサービスの 69%がアルツハイマーやその他の認知症の人のための特定のプログラムを提供しており、成人デイサービスセンターの 14%が主にアルツハイマーやその他の認知症の人にサービスを提供している。
- 居住用介護施設。介護付き高齢者向け住宅を含む居住用介護施設(服薬管理や食事などの日常生活を支援するサービスを含む住宅)の入所者の 42%がアルツハイマー病やその他の認知症を患っている543。小規模施設(4~25 床)では、大規模施設に比べてアルツハイマー病やその他の認知症の入所者の割合が高い(4~25 床の施設では 51%、26~50 床の施設では 44%、50 床以上の施設では 39%)545 。
- 介護施設の介護。全体では、介護施設入居者の48%がアルツハイマー型認知症またはその他の認知症を有している543 が、ショートステイ(100日未満)の介護施設入居者の37%がアルツハイマー型認知症またはその他の認知症を有しており、ロングステイ(100日以上)の入居者の59%がこれらの状態を有している。2014年には、アルツハイマー型認知症またはその他の認知症を持つ老人ホーム入居者の61%が中等度または重度の認知障害を有していた。
- アルツハイマー型認知症特養ユニットと専用施設 アルツハイマー型認知症特別ケアユニットとは、アルツハイマー型認知症やその他の認知症を持つ人のためにカスタマイズされたサービスを提供する介護施設やその他の居住施設にある専用のユニット、棟、フロアのことである。メディケア受給者の 72%がアルツハイマー型認知症であるにもかかわらず、介護施設の 15%、その他の居住型ケア施設の 14%が認知症特養を設置している543 。
在宅と地域社会で提供される介護サービス
全国的に、各州のメディケイドプログラムは、不必要なコストを削減し、高齢者によるこれらのサービスに対する需要の高まりに対応するための手段として、長期ケアサービスを施設ケアから在宅や地域に根ざしたサービスへと移行させている。連邦政府と州政府がプログラムの管理と資金を共有しており、州によってメディケイドプログラムでカバーされるサービスが大きく異なる。548 2013年から 2016年の間に、在宅・地域密着型サービスへのメディケイド支出は全体で26%増加したが、施設ケアへの支出は同期間でわずか1.5%の増加にとどまった。さらに、アルツハイマー型認知症やその他の認知症を持つメディケア受給者の在宅ケアへの支出は 2004 年から 2011 年の間に約 2 倍に増加しているが、支出の増加は、アルツハイマー型認知症と診断される人の増加、在宅ケアを利用する人の増加、併存する病状の増加、在宅ケアサービスのより集中的な利用、高齢者のメディケイド加入率の増加など、様々な要因によるものと考えられる。549 認知症患者に対する在宅支援介入の費用対効果に関する最近の2つの系統的レビューでは、作業療法、在宅ベースの運動、心理学的・行動学的治療を費用対効果の高いアプローチとして支持するエビデンスがあることが示されたが、在宅支援介入の費用と便益の両方を評価した研究は乏しい。
ケア設定間の移行
認知症の患者は、介護施設だけに留まるのではなく、介護施設、病院、在宅の間を移動することが多い。認知症のプライマリーケア患者を対象とした縦断的な研究では、介護施設から退院した人は、病院への退院(44%)とほぼ同程度の確率で在宅退院(39%)していることがわかった。他の研究者によると、介護施設の入居者は、人生の最後の月に集中治療室への入所やホスピスへの後期登録など、人生の終わりに負担のかかる移行を頻繁に経験することが示されている。
6.3.2 介護サービスにかかる費用
介護サービスには、在宅・地域密着型サービス、アシストリビング、介護付有料老人ホームなどがある。以下の試算は、これらのサービスの利用者全員を対象としている。
- 在宅ケア。有給の非医療系在宅医療エイドの費用の中央値は、1時間あたり23ドル、1週間あたり1,012ドルである。
- 成人デイセンター。成人向けデイサービスの費用の中央値は 1 日あたり 75 ドルである。
- 介護付有料老人ホーム。援助生活施設でのケアにかかる費用の中央値は、1 か月あたり 4,051 ドル、または 1 年あたり 48,612 ドルである。
- 老人ホーム。老人ホームの個室の平均費用は 1 日あたり 280 ドル(年間 102,200 ドル半個室の平均費用は 1 日あたり 247 ドル(年間 90,155 ドル)である。
長期介護サービスの手頃な価格
アルツハイマー型認知症やその他の認知症を持つ人の中には、十分な介護保険に加入している人や、介護サービスが必要とされている限り、介護サービスの費用をポケットから出して支払う余裕のある人はほとんどいない。
- アルツハイマー型認知症やその他の認知症の人の所得や資産のデータはないが、メディケア受給者の50%は2016年の所得が26,200ドル以下(2019年は27,852ドル25%は2016年の所得が15,250ドル以下(2019年は16,212ドル)となっている。
- メディケア受給者の50%が2016年ドルで74,450ドル以下(2019年ドルでは79,145ドル25%が2016年ドルで14,550ドル以下(2019年ドルでは15,468ドル8%が貯蓄なしまたは借金をしていた。貯蓄額の中央値は、黒人/アフリカ系アメリカ人およびヒスパニック/ラテン系の受給者では、白人のメディケア受給者よりも大幅に低かった556。
介護保険
介護保険は一般的に、老人ホーム、補助生活施設、アルツハイマー型認知症の特別養護施設で提供される介護費用、成人デイケアなどの地域密着型サービス、介護や身の回りの世話の手伝いを含む在宅で提供されるサービスなどをカバーしている57。2016年のアルツハイマー病協会の家族影響調査の結果から、成人の28%がメディケアがアルツハイマー病患者の介護施設ケアの費用をカバーしていると考えており、37%が介護施設ケアの費用をカバーしているかどうかを知らないことが明らかになった349。
業界レポートによると、2014 年には約 720 万人のアメリカ人が長期介護保険に加入していたと推定されている559 。長期介護保険に加入している個人の所得の中央値は 2010 年ドルで 8 万 7500 ドル(2019 年ドルでは 10 万 2,373 ドル)で、77%が年収 5 万ドル以上(2019 年ドルでは 5 万 8,499 ドル82%が 7 万 5,000 ドル以上(2019 年ドルでは 8 万 7,748 ドル)の資産を持っていた。 559 民間の医療保険と介護保険は、2013 年の介護支出総額の約 8%にすぎず、2013 年のドルでの総額 3,100 億ドル(2019 年のドルでの総額 3,400 億ドルのうち 272 億ドル)のうち 248 億ドルに相当する560 。2000 年には、長期介護保険に加入している個人の 41%が 5 大保険会社のいずれかの保険に加入していたのに対し、2014 年には 56%であった。
民間の介護保険の選択肢が乏しく、介護サービスの費用が高いことに対処するために、ワシントン州は、州が運営する公的な介護保険プログラムを創設する法律を可決した全米初の州となった561 。このプログラムは現在、2025年に始まる生涯給付金で最大36,500ドルを支払うように構成されている。
メディケイドのコスト
メディケイドは、ケアのレベル、所得、資産に関するプログラムの要件を満たす個人を対象に、地域社会における介護施設のケアと長期ケアサービスをカバーしている。保険を受けるためには、受益者は低所得でなければならない。メディケイドの対象となる老人ホームの住民のほとんどは、ごくわずかな個人的ニーズ手当を除いて、社会保障費やその他の月収のすべてを老人ホームケアの支払いに充てなければならない。メディケイドが差額を補填するのは、老人ホーム入居者が介護費用の全額を支払うことができない場合や、配偶者が経済的に扶養されている場合のみである。メディケイドは介護施設でのケアの費用をカバーしているが、補助生活介護、在宅での熟練した介護、介護の手伝いなど、多くの長期ケアやサポートサービスのカバー範囲は州によって異なる。
アルツハイマー型認知症やその他の認知症の人のためのメディケイド支出総額は、2020年には510億ドル(2020年ドル)になると予測されている16 。207 アルツハイマーやその他の認知症を持つ 65 歳以上のメディケア受給者とその他の受給者の支払いの差の多くは、長期介護(老人ホームや補助生活施設などの入所介護施設)に関連する費用と、メディケイドの対象となる認知症の人の割合が多いことによるものである。
表15. アルツハイマー病やその他の認知症と暮らす65歳以上のアメリカ人へのメディケイド支払い総額(州別*)
州 2020年(単位:百万ドル) 2025年(単位:百万ドル) 増減率
アラバマ州 $925 $1,127 21.8
アラスカ州 76 110 44.6
アリゾナ州 414 545 31.7
アーカンソー 396 454 14.6
カリフォルニア州 4,197 5,235 24.7
コロラド州 635,789 24.1
コネチカット州 1,022 1,187 16.1
デラウェア 253 313 23.6
コロンビア特別区 126 135 6.8
フロリダ州 2,689 3,453 28.4
ジョージア州 1,265 1,594 26.0
ハワイ 240 285 18.7
アイダホ 149 196 31.2
イリノイ州 1,787 2,199 23.1
インディアナ州 1,054 1,233 17.1
アイオワ州 676,792 17.2
カンザス州 473 543 14.6
ケンタッキー州 803 949 18.2
ルイジアナ州 765 934 22.1
メイン州 212 274 29.5
メリーランド州 1,231 1,535 24.7
マサチューセッツ州 1,753 2,031 15.9
ミシガン州 1,487 1,738 16.9
ミネソタ州 905 1,087 20.1
ミシシッピ州 606 729 20.4
ミズーリ州 973 1,137 16.8
モンタナ州 166 203 22.2
ネブラスカ州 372 411 10.3
ネバダ州 203 277 36.5
ニューハンプシャー州 254 335 31.9
ニュージャージー州 2,186 2,614 19.6
ニューメキシコ州 227 279 22.9
ニューヨーク州 5,453 6,306 15.6
ノースカロライナ州 1,332 1,628 22.2
ノースダコタ 190 215 13.2
オハイオ州 2,534 2,940 16.0
オクラホマ州 516 611 18.3
オレゴン 253 317 25.4
ペンシルバニア州 3,658 4,029 10.2
ロードアイランド 470 565 20.1
サウスカロライナ州 652 818 25.4
サウスダコタ 182 212 16.6
テネシー州 1,109 1,377 24.2
テキサス州 3,202 3,949 23.3
ユタ州 185 235 27.0
バーモント 116 146 26.4
バージニア州 1,000 1,266 26.6
ワシントン州 547 689 26.0
ウェストバージニア 445 521 17.1
ウィスコンシン 777 924 18.9
ワイオミング 86 111 28.8
米国平均 $51,226 $61,581 20.2
* AIIのコストは2020年ドルで報告されている。四捨五入の関係上、州の合計が米国の合計に加算されない場合がある。Lewin モデルのデータを基に作成。
6.3.3 終末期のケアの利用と費用
ホスピスケアは、アルツハイマー病やその他の認知症の人を含め、死期を迎えようとしている人に対して、施設や自宅で医療ケア、痛みの管理、感情的・精神的なサポートを提供する。ホスピスケアはまた、死期を迎える人の家族のために、感情的・精神的なサポートと死別のサービスを提供する。ホスピスの主な目的は、終末期の病気に伴う痛みやその他の苦しい症状を伴わずに、尊厳を持って死ねるようにすることである。ホスピスケアの主な支払い源はメディケアであるが、民間保険、メディケイド、その他の支払い源からもホスピスケアの支払いが行われている。2008年から 2011年の全米ホスピス調査のデータによると、ほぼすべてのホスピスが認知症の人をケアしていた(99%)が、認知症の一次診断を受けた人をケアしていたのは67%にすぎなかった562。営利ホスピスと非営利ホスピスの認知症患者の割合の違いの根本的な理由を理解するためには、より多くの研究が必要である。
291 ホスピスケアの拡大は、人生の最後の90日間に、何らかの理由で2回以上の入院をしたり、肺炎、尿路感染症、脱水症、敗血症で1回以上の入院をした認知症患者の数が少ないことと関連している。2017年には、在宅、補助生活施設、長期療養施設、非熟練看護施設、熟練看護施設、入院病院、入院ホスピス施設、その他の施設でホスピスケアを提供していたホスピス会社は米国内に4,254社あった564。さらに、ホスピスケアを受けたメディケア受給者の18%がアルツハイマー型認知症を含む認知症の一次診断を受けていた(表16)564。2014年のホスピス利用者の45%がアルツハイマー病やその他の認知症の一次または二次診断を受けており、ホスピス利用者の多くがアルツハイマー病を併存疾患としていることが示唆されている。2008年から 2011年の全国ホスピス調査のデータによると、認知症の一次診断を受けた人のホスピス滞在期間の平均は、他の一次診断を受けた人よりも50%以上長かった。
表16. 認知症の一次診断でホスピスに入院したメディケア受給者の数と割合、2017年、州別
州 受給者数 受給者の割合
アラバマ州 5,867 18
アラスカ 95 14
アリゾナ州 7,229 18
アーカンソー州 3,133 18
カリフォルニア州 30,045 20
コロラド州 3,254 15
コネチカット州 2,380 15
デラウェア州
コロンビア特別区 263 18
フロリダ州 19,897 15
ジョージア州 10,435 21
ハワイ 943 16
アイダホ州 1,566 17
イリノイ州 9,795 18
インディアナ州 5,922 17
アイオワ州 3,278 17
カンザス州 2,770 18
ケンタッキー州 2,895 15
ルイジアナ州 4,786 19
メイン州 1,494 19
メリーランド州 4,072 17
マサチューセッツ州 7,245 23
ミシガン州 9,001 16
ミネソタ州 5,399 21
ミシシッピ州 3,547 20
ミズーリ州 5,991 17
モンタナ 507 11
ネブラスカ州 1,648 18
ネバダ州 2,167 17
ニューハンプシャー州 1,007 17
ニュージャージー州 8,207 23
ニューメキシコ州 1,523 15
ニューヨーク 7,669 16
ノースカロライナ州 8,486 17
ノースダコタ 468 18
オハイオ州 12,656 17
オクラホマ州 4,102 18
オレゴン州 3,565 17
ペンシルバニア州 12,384 17
ロードアイランド州 1,657 25
サウスカロライナ州 6,038 20
サウスダコタ州 421 13
テネシー州 6,435 19
テキサス州 26,672 22
ユタ州 2,506 19
バーモント州 543 17
バージニア州 6,440 19
ワシントン州 5,459 20
ウエストバージニア州 1,552 15
ウィスコンシン州 5,086 16
ワイオミング 89 7
米国 合計 278,192 18
米国メディケア・メディケイド・サービスセンターのデータを基に作成。
207 2016年、在宅ホスピスサービスに対するメディケアの報酬は、各施設の単純な日額から、1日目から60日目まではそれ以降の日額よりも高い報酬を提供する2段階のアプローチに変更された。2020年度の通常の在宅ケアの料金は、1日目から60日目までが194.50ドル、61日目以降が153.72ドルである。566 この診療報酬の変更がメディケアのコストを削減するかどうかを評価するためのシミュレーションでは、研究者グループは、ホスピスケアを受けている認知症の人は、ホスピスケアを受けていない認知症の人に比べてメディケア全体の支出が高くなるが、新しい診療報酬のアプローチはメディケアのコストを削減すると予想されることを発見した。
さらに、ホスピスケアに登録されている人は、人生の最後の 30 日間に入院する可能性が低く569 、痛みのための定期的な治療を受ける可能性が高い。547 ホスピスケアに登録されている認知症の家族は、ホスピスケアに登録されていない認知症の家族よりも、ホスピスケアに登録されている認知症の家族の方が、医療ケアに対する満足度が高い。
終末期における給餌チューブの使用
529 終末期に栄養チューブを挿入する確率は国によって異なり、重症度、人工的な水分補給や栄養補給の制限、民族、性別では説明できない。研究者らは、専門外の医師、または専門外の医師と開業医の両方が管理している認知症患者では、人工栄養チューブの使用率が最も高いことを明らかにした。573,574 メディケアによるホスピスケアの拡大に伴い、アルツハイマー病やその他の認知症の患者では、人生の最後の90日間での給餌チューブの使用が減少している。
アルツハイマー病やその他の認知症の方の死亡場所
1999 年から 2017 年の間に、介護施設で死亡したアルツハイマー型認知症患者の割合は 68%から 51%に減少し、医療施設で死亡した割合は 15%から 5%に減少した(図 15)。
図15 アルツハイマー病による死亡場所、1999年から 2017年まで
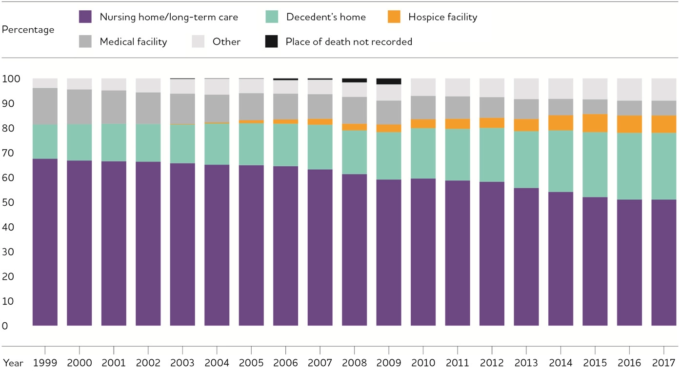
国立健康統計センターのデータより作成.575
6.4 人種・民族別の医療・介護サービスの利用と費用
アルツハイマー病やその他の認知症のメディケア受給者の中では、黒人・アフリカ系アメリカ人の一人当たりの年間メディケア支払額が最も高かったのに対し、白人の支払額は最も低かった(それぞれ28,633ドル対21,174ドル)(表17)。支払額の差が最も大きかったのは病院ケアで、黒人・アフリカ系アメリカ人の病院ケア費用は白人の1.7倍(9,566ドル対5,683ドル)であった(表17)。
表17. アルツハイマー型認知症またはその他の認知症を持つ65歳以上のメディケア受給者の、サービスの種類と人種・民族別の年間平均支払額(2019年)ドル
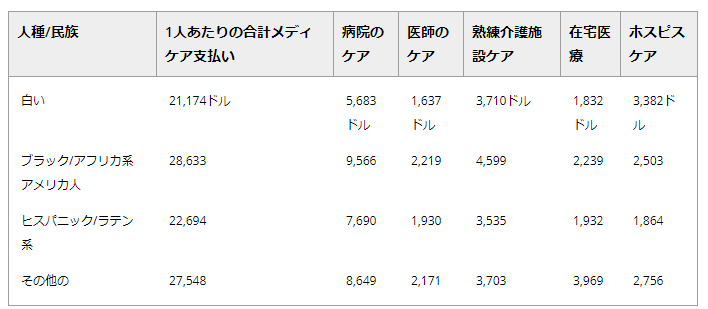
2014年の全国5%サンプルのメディケア診療報酬受給者の未発表データを基に作成。
576 これらの結果から、黒人/アフリカ系アメリカ人は白人やヒスパニック/ラテンアメリカ人に比べてケアコストが有意に高く、その主な原因は入院ケアの増加と併存疾患の増加であることが明らかになった。これらの違いは、ケアを受けている間の障害レベルの上昇、タイムリーなプライマリーケアへのアクセスの遅れ、ケア調整の欠如、プロバイダー間でのサービスの重複、またはケアへのアクセスの不公平につながる後期診断に起因している可能性がある。しかし、このような医療格差の理由を理解するためには、より多くの研究が必要である。
6.5 ヘルスケアおよび長期ケアサービスの回避可能な利用
6.5.1 予防可能な入院
予防可能な入院は、医療の質を測る一般的な指標の一つである。予防可能な入院とは、予防ケアやプライマリーケアへのアクセスや質が高ければ回避できた可能性のある状態の入院のことである。30日以内の計画外の再入院も、退院後の適切なケアがあれば回避できた可能性のある入院の一種である。2013年には、アルツハイマー病やその他の認知症を持つ有料サービスのメディケア登録者の入院の21%が、30日以内の計画外の再入院、または外来ケアに敏感な状態(つまり、タイムリーで効果的な外来ケアを行えば回避できる可能性のある状態)によるものであった。これらの予防可能性のある入院のメディケアへの総費用は47億ドル(2013年ドル、2019年は54億ドル)であった。30日以内に再入院した人のうち、27%が2回以上再入院している。メディケア登録者の10%が外来ケアに敏感な状態のために少なくとも1回入院しており、アルツハイマー病やその他の認知症のメディケア登録者の総入院の14%が外来ケアに敏感な状態のために入院していた。
2010年から 2015年までのメディケアの管理データによると、予防可能な入院はアルツハイマー病やその他の認知症患者の総入院の23.5%を占めていた。
Health and Retirement Studyとメディケアのデータに基づいて、人口統計学的、臨床的、健康リスク因子をコントロールした後、認知症の人は、神経精神疾患(認知症、うつ病、認知症を伴わない認知機能障害)を伴わない人に比べて、予防可能な入院のリスクが30%高くなってた。さらに、認知症とうつ病の両方を持つ人は、神経精神障害のない人に比べて、予防可能な入院のリスクが70%高かった579 別の研究グループは、認知症の人とうつ病の介護者は、認知症の人とうつ病のない介護者に比べて、6ヶ月間の救急外来の利用率が73%高かったことを発見した580。
291 ある研究チームによると、心不全で入院した人は、認知機能に障害がある場合、退院後に再入院したり死亡したりする可能性が高いとの結果が出ている。別の研究チームは、アルツハイマー病やその他の認知症を持つメディケア受給者は、糖尿病合併症や高血圧のための入院を回避できる可能性が高いことを発見した。
図16 アルツハイマー病やその他の認知症の有無にかかわらず、特定の持病を持つ 65 歳以上のメディケア受給者 1,000 人当たりの入院日数

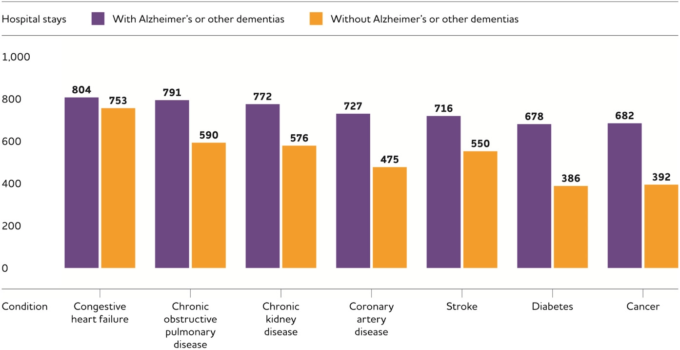
2014 年。2014 年の全国 5%サンプルメディケア有料サービス受給者の未発表データを基に作成。
認知症のある人とない人の医療利用の違いは、地域に住む人で最も顕著である。健康とリタイアメント調査のデータによると、地域に住む認知症の人は、予防可能な入院、回避可能な救急科受診、および/または入院に至った救急科受診の可能性が高かった。
6.5.2 回避可能な医療および介護施設の利用を減らすための率先取り組み
最近の研究では、2つのタイプのプログラムが回避可能な医療や介護施設の利用を減らす可能性があることが示されている。介護のセクションでは、多くの介護者支援プログラムについて説明しているが、これらのプログラムの中には、アルツハイマー病やその他の認知症患者の入所ケアへの移行を減らすことが期待されているものもある。さらに、共同ケアモデル(老人科医だけでなく、ソーシャルワーカー、看護師、医療助手なども参加するモデル)は、ケアの調整を改善し、それによって入院、救急部門の受診、その他の外来受診に関連する医療費を削減することができる。例えば、専門家間のメモリーケアクリニックでは、プライマリケア提供者のみがケアを監督していた記憶に問題のある人と比較して、記憶に問題のある人は、1人当たりの医療費を1年間で2012年に3,474ドル(2019年には4,153ドル)削減することが示されている。このプログラムは、1人あたりの年間平均コストが618ドル(2019年のドルで739ドル)と比較的低コストであり、ほぼ6対1の投資収益率であった。しかし、別の研究者グループは、ナースプラクティショナーと医師を用いて患者を共同管理する認知症ケアプログラムは、プログラムのコストと、長期療養型老人ホームへの入院が減少したことによるコスト削減を考慮した結果、コスト中立であることを明らかにした585。
ある研究者グループは、少数の臨床医にケアが集中している認知症患者は、より多くの臨床医にケアが分散している患者に比べて、入院や救急部門の受診が少なく、全体的に医療費が低いことを明らかにした。
6.6 将来の予測
アルツハイマー病やその他の認知症を持つ人々のヘルスケア、長期ケア、ホスピスケアに対する年間の支払い総額は、2020年の3050億ドルから 2050年には1兆1,000億ドル以上に増加すると予測されている(2020年ドル換算)。この劇的な増加には、メディケアとメディケイドの下での政府の支出とポケットからの支出の両方が約4倍に増加することが含まれている16。
6.6.1 アルツハイマー病の軌道修正による潜在的な影響
現在、アルツハイマー病の予防や治療、進行を遅らせるFDA承認の薬理学的治療法は存在しないが、いくつかの研究者グループは、認知症の発症を遅らせたり、症状を軽減したりする将来の介入のコスト削減を見積もっている。588, 590 ある研究者グループは、2025 年にアルツハイマー病の発症を 5 年遅らせる治療法を導入した場合、2050 年には総医療費が 33%、ポケットからの支払いが 44%削減されると推計している。588 第二の研究者グループは、アルツハイマー病の発症を 1 年から 5 年遅らせることで、2050 年には総医療費が 14%、3 年遅らせることで 27%、5 年遅らせることで 39%減少すると予測している。第3の研究者グループは、機能低下の速度を10%遅らせる治療法は、2015年の1人当たりの平均生涯コストを3,880ドル(2019年は4,308ドル)削減すると推定し、行動的・心理的症状の数を10%減らす治療法は、1人当たりの平均生涯コストを680ドル(2019年は755ドル)削減すると推定している。
アルツハイマー病協会は、アルツハイマー病を発症する人の88%が認知症の段階ではなくMCIの段階で診断されるか、あるいは全く診断されないと仮定して、早期診断による潜在的な費用節約の可能性についての調査を委託した590。2018 年に生きていてアルツハイマー病を発症する人の医療費と長期介護費を約 7 兆ドル節約することができる。コストの節約は、1)診断が高額な認知症の段階ではなく、MCIの段階で行われているため、診断の直前と診断後のコストのスパイクが小さくなったこと、2)MCIと認知症を診断して管理している個人の医療費と長期ケア費が、管理していないMCIと認知症の個人と比べて低くなったことによるものである。
疾患の予防、治癒、進行を遅らせる治療法は、米国の医療制度の大幅な節約につながる可能性がある。しかし、米国の医療制度の構造に変化がなければ、アルツハイマー病の新しい治療法へのアクセスは、キャパシティの制約により深刻に制限される可能性がある。例えば、ある研究者グループは、2020年までに新しい治療法が導入された場合、患者は平均19ヶ月間治療を待つことになると推定したキャパシティ制約のモデルを開発した。このモデルでは、仮想的な治療法として、輸液センターでの輸液が必要であることと、アミロイドPETスキャンで評価された人に依存することを想定している。アルツハイマー病の予防、治癒、進行を遅らせる新しい治療法の導入は、アルツハイマー病の発症率や重症度に劇的な効果をもたらす可能性があるが、その有効性は、医療システムのキャパシティと保険償還の両方の制約によって制限される可能性があることは明らかである。
7 スペシャル・レポート:最前線。アメリカにおけるプライマリケア医とアルツハイマー病ケア
アルツハイマー病をはじめとする認知症は、アメリカの危機が高まっている。今年のアルツハイマー病の事実と数字の有病率のセクションで報告されているように、現在、500万人以上のアメリカ人がアルツハイマー型認知症と生活しており、2050年までに1400万人近くに増加すると予測されている。一方で、米国ではアルツハイマー型認知症を持つ人々の数が増え続けているため、専門医の不足が問題となっている。その結果、主にプライマリ・ケア医が医療を担うことになっている。本特別報告書では、アルツハイマー病やその他の認知症の専門医療における現在の格差と将来の不足予測を検証し、プライマリ・ケアの課題を探る。また、高齢化が進む米国において、現在アルツハイマー病を患っている患者のケアを行う上で、プライマリ・ケア医が直面している課題を探っている。本報告書は、より多くのアメリカ人が認知症ケアにアクセスできるように、これらの不足や課題に対処するための提言で締めくくられている。
7.1 誰が診断し、医療ケアを提供するのか?
アルツハイマー病やその他の認知症の人々の医療ケアには、医師、神経心理学者、作業療法士や理学療法士、在宅医療補助員などの医療従事者を含む幅広い専門家が関与している。本報告では、プライマリケア医(家庭医学、内科、一般診療)と、老年医、神経内科医、老年精神科医、神経心理学者などの専門医に焦点を当てている。認知症患者の診断と治療管理の複雑さを考えると、認知症患者のケアを最適化するためには、専門医が充実していることが理想的であるという意見は一般的に一致している。しかし、現実には、そのような専門家が不足しているため、認知症の診断と治療の責任はプライマリ・ケア医にあるのが現状である。
例えば、最近の研究597では、認知症と診断された高齢者の大多数は認知症ケアの専門家を受診したことがなく、圧倒的に専門家ではない医師に診断・ケアされていることが明らかになった。具体的には、最初に認知症と診断された人の85%が、非認知症の専門家、通常はプライマリ・ケア医である専門家によって診断されているという研究結果が出ている。同じ研究では、診断から1年後に認知症専門医を受診したことがある患者は4分の1以下であった。5年後には、認知症専門医を受診したことがある患者の割合は36%にまで増加した。専門的なケアは、特にヒスパニック系とアジア系の人々では低かった。
7.2 ニーズの高まりと専門医不足の予測
有病率の項で述べたように、2020年から 2050年の間に、アメリカの高齢者人口(65歳以上)は飛躍的に増加すると予想されている。高齢者人口の増加に伴い、アルツハイマー型認知症の患者数も増加すると予想される。現在、65歳以上の約10人に1人がアルツハイマー型認知症になっている。しかし、その一方で、高齢者をケアするための労働力が不足しているのが現状であり、今後も不足する可能性が高い。
National Center for Health Workforce Analysis,598 によると、2013 年にはすでに老年医が不足しており、2025 年までには供給量の緩やかな増加が予測されているが、需要を満たす見込みはないという。医療研修の動向も、将来的に老年医の不足が深刻化することを示唆している。例えば、老年医学関連の大学院医学教育プログラムは、2001-2002年の学術年から 2017-2018年の学術年までにわずか1.1%しか成長していない599 同様に、現在および将来の米国の神経内科医の労働力に関する研究では、2025年までに神経内科医が19%不足すると予測されている600。
2050年には、アルツハイマー型認知症の人をケアするための専門医の必要性が大幅に増加すると予測している。表18は、2050年に必要とされる老年医の数を州別に予測したものである。国として、2050年にアルツハイマー型認知症になると予測される65歳以上の人(65歳以上の人口の約10%)をケアするのに十分な老年医を確保するためには、2019年に開業していた老年医の数を3倍に増やす必要がある。しかし、National Center for Health Workforce Analysisが推計した65歳以上の人口の30%が老人医療を必要としているため、老人医療従事者の数を9倍に増やす必要がある。同様の分析では、神経内科医、老年精神科医、神経心理学者、認知症の診断とケアに重要な専門知識を提供する専門家に対する大きなニーズが予測されていることも示されている。
表18. 州別の2050年の老年医ニーズの予測
2019年の州の老年医数 65歳以上の10%にサービスを提供するために2050年に必要な老年医数 65歳以上の30%にサービスを提供するために2050年に必要な老年医数
アラバマ州
アラスカ 6 31 92
アリゾナ州 89 363 1,089
アーカンソー州 51 134 402
カリフォルニア 590 1,676 5,029
コロラド州 89 289 867
コネチカット 99 166 497
デラウェア州
コロンビア特別区 37 28 83
フロリダ州 348 1,365 4,096
ジョージア州 96 492 1,476
ハワイ 61 64 192
アイダホ州 10 87 261
イリノイ州 218 517 1,551
インディアナ州 65 299 897
アイオワ 24 142 426
カンザス州 23 121 364
ケンタッキー34 207 622
ルイジアナ 31 198 595
メイン州 37 71 213
メリーランド州 150 288 865
マサチューセッツ 206 347 1,042
ミシガン州 169 465 1,394
ミネソタ州 93 270 811
ミシシッピ 25 124 373
ミズーリ州 103 283 849
モンタナ州 8 59 177
ノースカロライナ州 159 535 1,606
ノースダコタ州 15 34 103
ネブラスカ州 23 84 253
ネバダ州 40 158 474
ニューハンプシャー州 30 72 217
ニュージャージー 205 398 1,193
ニューメキシコ 29 93 279
ニューヨーク 605 818 2,454
オハイオ州 163 537 1,611
オクラホマ 28 171 512
オレゴン州 62 232 695
ペンシルバニア州 278 601 1,803
ロードアイランド州 32 49 147
サウスカロライナ州 66 288 865
サウスダコタ州 10 44 131
テネシー州 40 343 1,029
テキサス州 342 1,255 3,766
ユタ州 21 114 341
バーモント 5 32 95
バージニア州 103 406 1,218
ワシントン州 132 399 1,198
ウェストバージニア州 19 83 250
ウィスコンシン 84 273 820
ワイオミング 4 26 79
米国 合計 5,218 15,417 46,252
注釈。10%の欄は、2050年にアルツハイマー型認知症になると予測される65歳以上の人の割合が10%のままであると仮定した場合、65歳以上の人だけに老年医が何人必要になるかを示したものである。30%の欄は、National Center for Health Workforce Analysisによると、認知症の有無にかかわらず、老人医療を必要とする65歳以上の30%の人々に対応するために、何人の老人医療従事者が必要になるかを示している598。598 クラリタスの 2050 年の 65 歳以上の人口の州別推計は、クラリタスの「Pop-Facts 2020」によって提供されたものである。
これらの不足は、各州によって影響が異なる。いくつかの州では、格差は小さい。例えば、ニューヨーク州、ハワイ州、ワシントンD.C.は、必要とされる比較的緩やかな増加を達成するのに十分な位置にあるように見える。対照的に、14の州では、アルツハイマー型認知症になると予測される65歳以上の人々をケアするために、2050年までに老年医の数を少なくとも5倍に増やすか、老年医によるケアが必要と予測される65歳以上の人口の30%をケアするために15倍に増やす必要がある。テネシー州とアイダホ州の2つの州では、アルツハイマー型認知症と予測される人々のケアのニーズを満たすためだけに9倍、あるいは老年医のケアを必要とすると予測されるすべての人々のニーズを満たすために26倍に老年医の数を増やす必要がある。
7.3 プライマリ・ケア医
米国では、現在および将来のアルツハイマー型認知症ケアのニーズを満たす専門医が不足しており、プライマリ・ケア医は、認知症の予兆の特定から適切な診断、複雑で進行性があり、最終的には致命的な疾患を抱える患者の継続的なケアとサポートのニーズを満たすことまで、疾患の連続したケアにおいてますます重要な役割を果たすことになるだろう。
PCPが最前線にいるのは明らかであるが、臨床現場での認知症ケアの需要の高まりに対応するためのPCPの心構えについては、ほとんど知られていない。アルツハイマー病協会は、認知症ケアにおけるPCPの経験、暴露、医学教育とトレーニングに関する態度についてより詳しく知るために、Versta Researchに依頼し、1) PCP,20 2) プライマリーケアのレジデンシーを修了したばかりの医学部卒業生21 3) プライマリーケアのレジデンシーを修了したばかりの卒業生22を対象とした調査を実施した。
アルツハイマー病協会の調査
アルツハイマー病協会のプライマリ・ケア医師認知症研修調査20に参加している医師は、米国の全PCPの68%が参加しているWebMDのMedscape医師パネルを介して募集された。調査の対象となるためには、PCPは開業して2年以上経過していること、患者の直接診療に50%以上の時間を費やしていること、患者の10%以上が65歳以上であることが条件となっている。米国のPCPの総人口に合わせて、年齢、性別、診療年数、診療の種類、専門分野、地域でバランスをとった合計1000人のPCPが調査に含まれている20。
この調査では、過去 2 年以内に医学部研修を修了した一般内科、家庭科、内科の現職 PCP202 名が、WebMD の Medscape Healthcare Professional Panel を通じて、アルツハイマー病協会の「最近の医学部卒業生認知症研修調査」21 に参加するように募集された。
過去2年以内にレジデンシーを修了したPCPは、WebMDのMedscape医師パネルを通じてAlzheimer’s AssociationのRecent Primary Care Resident Dementia Training Survey22に参加するために募集された。サンプルには200人のPCPが含まれており、年齢、性別、専門、地域に基づいて、開業後2年以内のPCPの全人口にマッチングされていた22。
アルツハイマー病協会の調査によると、以下のことが明らかになった。
- PCPは、自分たちがアルツハイマー病やその他の認知症の診断とケアを提供する最前線にいることを認識している。
- PCPの半数は、医療従事者が予想される需要の増加に対応する準備ができていないと考えている。
- PCPの半数以上が、患者の紹介を受けるのに十分な専門医がいないと回答している。
プライマリーケアの医学部やレジデンシープログラムでは、アルツハイマー病やその他の認知症に関連したコースワークや患者との接触は非常に限られている。 - PCPは、アルツハイマー病やその他の認知症患者のケア、特に疾患管理と治療、スクリーニングと検査、診断に関する最新の情報を得ることに義務を感じており、そのために努力している。
- にもかかわらず、医学部やレジデント時代から認知症ケアの追加研修を受けている人は半数以下で、そのような研修を受けることに関連した課題を指摘している。
- 5人に2人近くのPCPが、患者の治療経験が最も重要な教師の1つであり、継続的医学教育(CME)コースに次いで重要であると答えている。
全体として、アルツハイマー病協会の調査結果は、重要な認知症ケアを提供する上でPCPが果たす重要な役割を強調している。また、医学部在学中やレジデンシー中に、またその後の臨床現場でも、PCPに認知症ケアのトレーニングの機会を増やす必要があることも明らかになった。
7.3.1 調査結果
患者数
アルツハイマー協会のプライマリ・ケア医師認知症ケア研修調査では、5人に4人以上のPCP(82%)が、自分が患者に認知症ケアの重要な要素を提供する最前線にいると考えていることが明らかになった。PCPは、平均して患者の40%が65歳以上であり、そのうち13%がアルツハイマー病やその他の認知症と診断されていると報告した。調査はまた、認知症の話題が患者の訪問時に頻繁に出てくることを示している。PCPの大多数(53%)は、65歳以上の患者やその家族からアルツハイマーやその他の認知症に関する質問を数日に1回以上受けており、ほぼ5人に1人(19%)は日常的に受けている(図17)。
図17 プライマリ・ケア医が 65 歳以上の患者からアルツハイマー病やその他の認知症に関する質問を受ける頻度
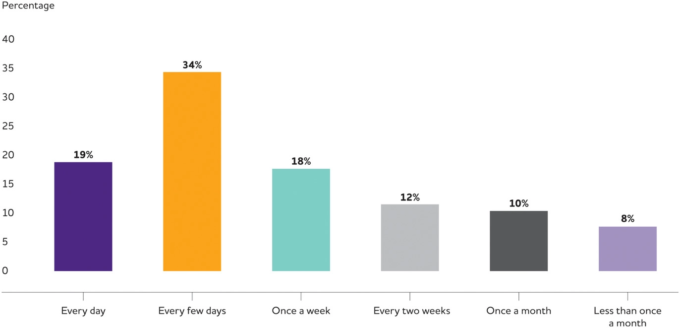
Alzheimer’s Association Primary Care Physician Dementia Training Surveyのデータから作成。
PCPは、アルツハイマー病患者の数が増加していると報告している。20 PCPはアルツハイマー病の患者数が増加していると報告している。10人のPCPのほぼ9人(87%)が、今後5年間に認知症の患者数が増加すると予想しており、3分の1(33%)は診断された患者数が「かなり」増加すると予想している。
患者の管理
認知症ケアの最前線にいることはわかっていても、調査対象となったPCPのかなりの数が、アルツハイマー病やその他の認知症の患者をケアするのに十分な準備ができているとは感じていないと報告している。4分の1以上(27%)が、アルツハイマー病やその他の認知症についての患者の質問に答えるのが気が進まないことがあると報告している。さらに、診断の大部分はPCPによって行われているにもかかわらず、10人に4人近くのPCP(39%)が、アルツハイマー病やその他の認知症の診断を個人的に行うことを快適に感じたことがない、あるいは時々しか、あるいは決してないと報告している。さらに、PCPの半数が、増加するアルツハイマー病やその他の認知症の患者をケアするために、医療従事者は「あまり準備ができていない」か「まったく準備ができていない」と答えている(図18)。
図18 医療従事者のアルツハイマー病などの認知症患者をケアするための心構え
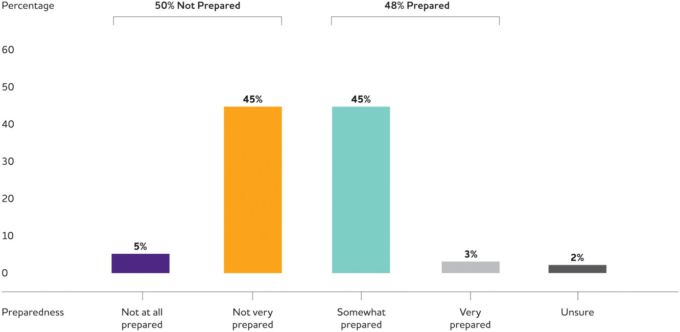
アルツハイマー病協会のプライマリ・ケア医師認知症研修調査のデータを基に作成。
患者を最適にケアするために、3分の1近くのPCP(32%)が、少なくとも月に1回は認知症患者に専門家を紹介している。しかし、ほとんどのPCP(55%)は、患者の需要に見合うだけの専門医がいないと回答している(図19)。PCPの専門医の有無については、診療所が都市部にあるか地方にあるかによってかなりの差があった。大都市のPCPの44%と大都市近郊の54%が自分の地域に十分な専門医がいないと報告しているのに対し、小都市や町のPCPの63%と農村部の71%が同じことを言っている。
図19 患者紹介のための認知症専門医の利用可能性
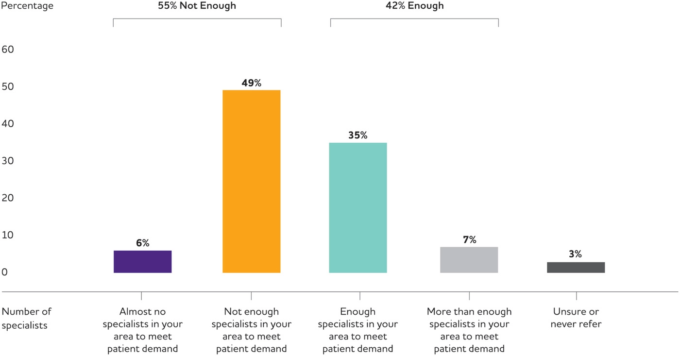
アルツハイマー病協会プライマリ・ケア医師認知症研修調査のデータを基に作成。
認知症ケアにおける医学部とレジデンシー研修
PCPの大多数(91%)は医学部でアルツハイマー病やその他の認知症の診断とケアについて少なくとも何らかのトレーニングを受けていたが、そのほとんど(66%)は “ごくわずか “であったと述べている。全PCPのほぼ4分の1(22%)は、認知症の診断とケアの研修を受けていなかった。研修を受けた78%のうち65%が「非常に少ない」と報告している。
心強いことに、この傾向は変わりつつあるようだ。最近訓練を受けたPCPのうち、認知症ケアのために医学部やレジデンシーの訓練を受けたと回答した割合は、実務経験年数の長いPCPに比べて多い。実務経験2~9年のPCPの98%が医学部で少なくとも認知症ケアの研修を受けたと回答しているのに対し、実務経験30年以上のPCPでは81%が認知症ケアの研修を受けたと回答している。同様に、2~9年勤務のPCPの85%がレジデンシー期間中に認知症のトレーニングを受けたと報告しているのに対し、30年以上勤務しているPCPの65%である。しかし、どれだけのトレーニングを受けたかにかかわらず、ほとんどのPCP(78%)は、医学部やレジデンシーでは認知症ケアのための医師を完全に準備することはできないと答えている。
新人PCPが受けている認知症トレーニングをよりよく理解するために、アルツハイマー病協会は最近の医学部とレジデンシーの卒業生を対象に調査を行った。PCP1年目と2年目の研修医を対象にした調査では、アルツハイマー病を含む認知症に特化した医学部の授業を平均41時間受けていることが明らかになった。しかし、5人に1人以上(21%)が医学部で認知症の授業を20時間未満と回答している。医学部での臨床研修では、平均20人の認知症患者を診たと報告している。
最近の研修医(現在1年目または2年目の研修医)を対象とした調査では、アルツハイマー病やその他の認知症に特化した正式なカリキュラムトレーニングを平均8時間受けていたが、4分の1(26%)は2時間未満と報告している。最近の研修医は平均して、研修期間中に50人の認知症患者を診察し、援助していた。しかし、初診時に診断されなかった10人の認知症患者の診断に関与したのは、わずか10人であった。最近の研修医のうち、認知症ケアを実践するために「非常に準備ができている」と感じているのはわずか18%であるのに対し、「やや準備ができている」、「あまりできていない」、「まったくできていない」と感じている人は72%であった。
現在の状態を維持する
新たな展開を見つける
アルツハイマー病協会の調査では、事実上すべてのPCP(99%)が認知症ケアの新展開について最新の情報を得ることが重要であると考えていることが明らかになった。同様の回答は、最近の医学部卒業者(99%)と最近の研修医(100%)にも見られた。
- 93%は、診断とケアの新しい発展に遅れないようにすることが患者への義務であると感じている。
- 92%は、患者や介護者が認知症ケアに関する最新の考え方やベストプラクティスを知ることを期待していると考えている。
- 92%は、認知症ケアは急速に進化する医療分野であり、継続的な学習とトレーニングが必要であると考えている。
さらに、調査によると、PCPの3分の2以上(69%)がアルツハイマー病やその他の認知症の診断やケアについて常に学んでいると答えており、半数(50%)が新しい開発に追いつくために多くの時間と労力を費やしていると答えていることがわかった。しかし、5人に3人以上(63%)が新しい開発に追いつくのに十分な時間がないと感じており、半数(53%)が認知症ケアの新しい開発に追いついている程度は “少し “か “全く “であると答えている。PCPは、健康関連のあらゆる領域において、時間とエネルギーを膨大に要求されているため、PCPが容易にアクセスでき、質の高いトレーニングの機会を確保することは、この分野にとって重要な課題となっている。
PCPがアルツハイマー病やその他の認知症について最新の情報を得たいと考えている最も重要な分野は、管理と治療(83%スクリーニングと検査(69%診断(64%)である。この3つの分野は、最近の医学部卒業生と最近の研修医を対象とした調査でも最も重要な分野としてランク付けされている。PCPが最新の情報を得たいと考えている分野としては、予防(49%家族支援(49%認知症の管理(46%徴候と症状(44%リスクの軽減(41%患者支援(40%看取り(31%緩和ケアとホスピス(28%他の医療提供者とのケアの調整(24%質の向上策(20%病態生理学(19%臨床試験(16%)などが挙げられている。
その他の研修の機会
最新の情報を得るために、PCPは主に認知症ケアの新展開を追いかけており、雑誌やコンテンツサマリーをスキャンして新たに発表された研究を調べたり(77%CMEをスキャンして新しいトレーニングの機会を探したり(66%)している23。24 PCPの大多数(89%)は、認知症の診断やケアの最新情報を得るためには、CMEの要件を満たすだけでは不十分であると感じており、学ぶ際には、大多数(55%)はCMEの内容よりも深く掘り下げて学ぶようにしている。
追加のトレーニングの機会について具体的に尋ねたところ、58%のPCPは、既存のトレーニングオプションの質は良いか、優れていると感じているが、トレーニングを得る上での課題も指摘されている。3分の1近く(31%)が現在のトレーニングオプションにアクセスするのが難しいと答え、半数(49%)が認知症ケアに関する継続的な教育やトレーニングのオプションが少なすぎると答えている。実際、認知症ケアについて最も学んだのは患者の治療経験であると答えたのは37%で、CMEコースから学んだと答えた40%に次ぐものであった(図20)。この結果は、PCPのためのより良い認知症トレーニングプログラムの必要性を浮き彫りにしている。PCPが認知症の診断とケアについて最も多く学んだ情報源としては、UpToDate®(32%専門誌(32%医学会議(31%研修医(29%)などが挙げられている。
図20 プライマリ・ケア医が認知症の診断とケアについて最も多く学んだのはどこか。
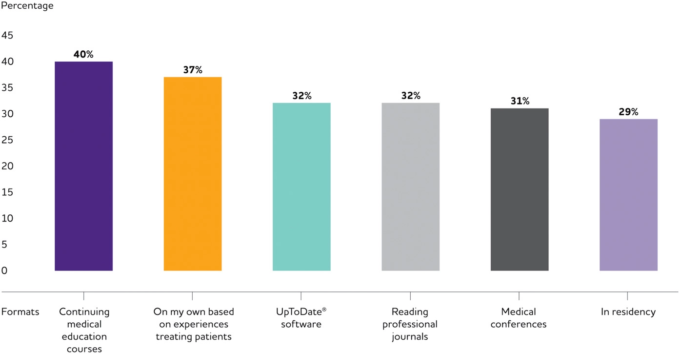
アルツハイマー病協会のプライマリ・ケア医師認知症トレーニング調査のデータを基に作成。
20 PCPが認知症ケアの追加トレーニングを受けようとした理由としては、患者人口を考慮した一般的な継続的な患者ニーズ(70%解決しようとしている特定の患者の問題やニーズ(64%最新の状態を維持するための職業上の義務(60%またはそのトピックに対する個人的または職業上の関心(53%)などが挙げられている。医師免許の要件(11%健康保険会社や他の支払者(3%または雇用者(1%)のために追加のトレーニングを追求したPCPはほとんどいません。
追加トレーニングを追求していないPCPは、時間がないから(38%アルツハイマー病やその他の認知症患者を他の医師に紹介するのが一般的だから(35%)と答えている。追加研修を受けていない人のわずか19%は、認知症患者の管理方法に自信を持っているからと答えている26。
7.4 将来の需要に応える
このアルツハイマー病協会の認知症ケアの分析と調査は、アメリカにおける認知症ケアの将来について警鐘を鳴らすべきである。この報告書は、認知症ケアの専門家とPCPのコミュニティが不足していることを示しているが、高齢化社会の需要の増加に対応するための準備が必ずしも十分ではないことを示している。
労働力不足に対処する一つの方法は、連邦政府や州政府が提供する奨学金やローン免除プログラムを利用することである。ローン返済プログラムは、農村部で開業する医師の数を増やすことと相関関係があることが研究で明らかになっており601 、整骨医学の卒業生がプライマリーケアの医師になるかどうかの決定に直接影響を与えている。医学研究所(現在は全米医学アカデミーとして知られている)による老年医療従事者に関する報告書では、「財政的支援をサービスに結びつけるプログラムは、国内の十分なサービスを受けていない 地域でサービスを提供する医療専門家の数を増やす上で効果的であった」とし、そのようなプログラムは「老年医療提供者の不足に対処するための同様の プログラムを開発するための良いモデルになる」と結論づけている476。
アルツハイマー病やその他の認知症の診断と治療に利用できるプロバイダーの数を増やすためのもう一つのアプローチは、教育資金を利用することである。例えば、米国の医学部の家庭医学科への連邦政府の資金援助は、プライマリーケアの人材拡大と関連している。604 さらに、メディケア・メディケイド・サービスセンター(CMS)による最近の実証プロジェクトでは、高度実践登録看護師(APRN)の臨床教育への資金提供により、APRN 学生の入学者数が 54%増加し、卒業者数が 67%増加したことが明らかになっている。605
専門職の労働力を強化する政策に加えて、プライマリ・ケアの能力を構築するプログラムには、連邦政府と州の支援が必要である。その一例として、ニューメキシコ大学が開発した医療従事者向けの遠隔指導プログラムであるProject ECHO® (Extension for Community Healthcare Outcomes)がある。Project ECHOは、C606型肝炎や複雑な糖尿病など、複数の疾患のプライマリケアを改善することが示されている。607 アルツハイマー病協会は、このモデルの利用拡大を通じて認知症ケアのプライマリケア能力を構築するための世界的なイニシアチブを開始している。
このギャップを埋めるためのもう一つのアプローチは、専門家以外に頼っている共同ケアや協調ケアプログラムを拡大することである。UCLAのアルツハイマー病・認知症ケアプログラムでは、認知症ケアの管理は、プライマリ・ケア医の監督下に置かれた看護師が行う。585 インディアナ州の同様の共同ケアモデルであるヘルシーエイジング・ブレインセンター(HABC)では、患者一人当たり年間3474ドルの節約になっている。HABCでは、ケアチームの一部として専門家(老年科医か行動神経科医)が含まれていたが、チームの大部分は医師ではなく、正看護師、医療助手、技師、ソーシャルワーカーが含まれていた。また、訓練を受けたナビゲーター、上級看護師、ソーシャルワーカー、薬剤師が参加するケアエコシステムに参加した認知症患者780人のうち、12ヶ月間で救急外来の受診が120件、救急車の利用が16件、入院が13件減少した。
アルツハイマー病協会はまた、アルツハイマー病やその他の認知症の早期発見・診断、これらの状態の管理、診断後のケアプランやサポートサービスなど、疾患の連続性を通して医療システムや臨床医をサポートするための様々なリソースを提供している。
医療システムや臨床医を支援するためのアルツハイマー病協会のリソースの完全なリストについては、alz.org/professionals/health-systems-cliniciansを参照のこと。
7.5 おわりに
本特別報告書は、アルツハイマー病をはじめとする認知症患者の質の高い診断とケアに対する現在および将来の需要を満たすために、医療従事者の育成が急務であることを強調している。現在および将来の専門医不足が予測されている、老年医、神経内科医、老年精神科医、神経心理学者は、患者ケアの大部分をPCPに負担させている。しかし、PCPは自分たちがこの危機の最前線にいることを認識し、質の高いケアを提供する義務を感じている一方で、医療従事者がこの問題に十分に対処する準備ができていないこと、患者の紹介を受ける専門医が不足していること、研修の機会が不足しているか、またはアクセスが困難であることを報告している。これらのニーズの深刻さから、プライマリーケアの能力を向上させながら、専門職の労働力を開発する解決策が必要とされている。
