Contents
波長・スペクトル(効果)
波長ごとの作用を、主に論文を元に簡単にまとめてみた。
研究で使われた波長に依存するので、必ずしもその波長が効果に対しての中央値となるわけではない。
(単位 nm)
紫外線C (100-280)
成層圏で吸収される
紫外線B (280-315)
成層圏のオゾンが吸収
紫外線A (315-400)
- 340 ヒトケラチノサイト・繊維芽細胞抑制 抗炎症効果
紫色 (380-450)
- 405 アポトーシスを促進 (注意)
- 410-420 用量依存的に酸化ストレス
- 415 にきび治療
- 430 がん細胞アポトーシス
ブルー (450-495)
- 453 低細胞分裂速度の低下
- 470 青の中では長波長 細胞へのダメージも少ない
- 470 ケロイドの過剰な繊維芽細胞を抑制
グリーン (495-570)
イエロー (570-590)
- 590 コラーゲンI合成の促進 肌を改善 MMP-1活性が低下(VEGF→MMPs→血管新生)
オレンジ(590-620)
- 610-650 シワの低減・肌のでこぼこを改善・コラーゲン密度が増加
レッド(620-780)
- 629 γバンド
- 620-650 発毛
- 630 アミロイド-βペプチド誘発の酸化的および炎症反応を抑制
- ROSが増加、繊維芽細胞を不活化
- 抗アポトーシスタンパク質Bcl-2の発現を増加
- メラノサイトを修復
- 633-830 真皮コラーゲンでMMPsを抑制、MMPs分解酵素活性化
- 650-660 ヘアマックス
- 655 毛髪密度が増加
- 670 DNA修復タンパク質、抗酸化酵素、分子シャペロンをコードする遺伝子の発現調節
- 688 Bバンド
- 759-771 Aバンド ミトコンドリアの活性化がない 大気中の酸素によって吸収される波長
近赤外線 (780-1400 )
- 808 中枢神経系において最も浸透する波長
- 810 Vielight 810
- 820 変形性関節症患者の痛みを緩和
- 830 骨の修復
- 850 mtor活性 筋肥大
- 900 炎症性サイトカインの産生抑制
ハンブリン博士によると、多少の違いはあっても赤色である630nm帯、遠赤外線810nm帯も、それほどLLLTの組織自体への効果に大きな違いはないらしい。いずれも同様にミトコンドリアの賦活作用がある。
そうなってくると、LLLTの波長の違いは異なる浸透度によって活性化される組織部位の違いになってくる。これはアルツハイマー病患者にとっては重要な違いとなる。
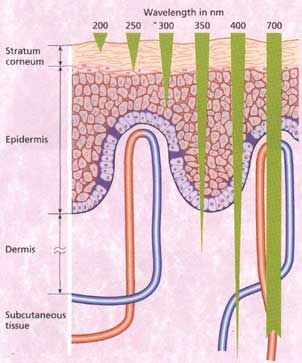
組織へ浸透する波長ウインドウ
可視光~近赤外

www.ncbi.nlm.nih.gov/pubmed/20011653
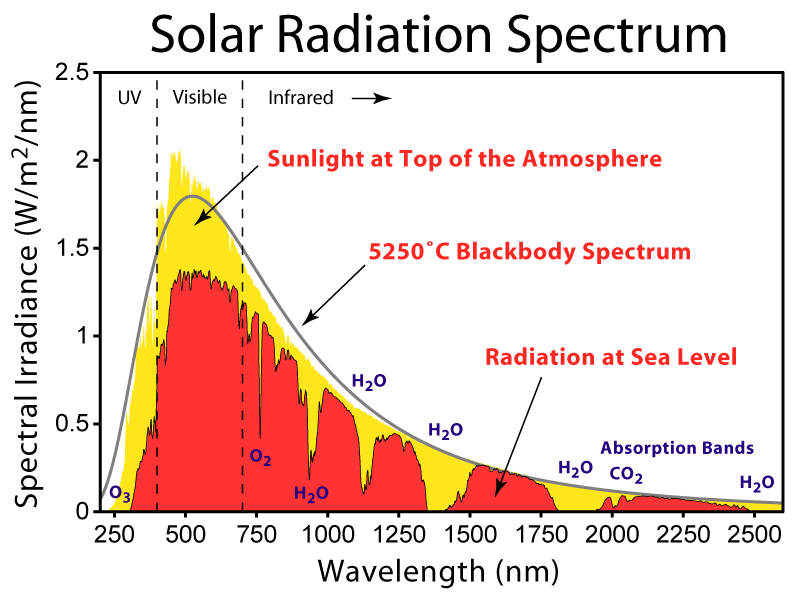
太陽エネルギーのスペクトラム

810nmよりも633nmの照射が高いBDNFを発現させる。
www.jneurosci.org/content/33/33/13505.long
波長・スペクトル(脳への浸透度)
標的までの距離
LLLT治療は、標的部位への距離の問題が常につきまとう。光が組織内部へ浸透するにつれ対数的に減衰していくため、標的細胞、標的脳部位までの距離があると治療効果が一気に減じてしまう。大雑把に言うと、仮に組織下2cmで照射エネルギーが100分の1に減衰するのであれば、4cm先だと1万分の1まで減衰する。
※実際は組織部位や頭蓋骨などによって、光の浸透度合が異なるので計算はもっとややこしい
パーキンソン病
パーキンソン病へのLLLT治療の場合、標的である脳幹まで80~100mmと照射させる浸透距離が長く、近赤外線療法の神経保護効果は限定的。
以下の論文では、パーキンソン病に対して光ファイバーの必要性が検討されている。
www.ncbi.nlm.nih.gov/pmc/articles/PMC4707222/
アルツハイマー病
ご存知のようにアルツハイマー病の場合、一般的に海馬周辺域に目立った障害が起こる。
海馬も頭部の中心に座位しており、外部から照射するだけではほとんど効果をおよぼさない。そこで照射出力をあげて影響を及ぼそうとすると、照射デバイスからより距離の近い脳領域が過剰に照射されて障害を受けてしまう問題がでてくる。
そこで、考えられたのが、鼻の奥に照射デバイスを差し込んで、そこから光を照射することで海馬や嗅内皮質までの距離を縮めようというアイディアだ。ここも、LED技術の進歩によるところが大きいが、鼻腔内に入れられるほど小さくて大きな照射量をもつLED素子が今では非常に安価な値段で入手できる。
また、アルツハイマー病は、その進行過程で皮質などにも広く障害がおよぶ一方で、皮質の障害領域にも特異性がある。そこで頭皮上の外部から直接照射することで、治療効果をもちうるのではないかとも考えられている。
波長による光浸透距離の違い

www.ncbi.nlm.nih.gov/pmc/articles/PMC5436183/
LLLT全般では、600~1070nm
波長により組織へ浸透する深さが異なってくる。
- 表面組織治療 600~700nm
- 深部の組織治療 780~950nm
808nm
毛髪促進や小じわの改善に用いられる630nm帯の赤色は、ほとんど透過しない。
人の死体頭部では、940nm、660nmと比較して808nmの波長の光が、吸収および散乱が少なくもっとも深く脳組織を浸透する。(40~50mm)
www.ncbi.nlm.nih.gov/pubmed/25772014
808nm vs 980nm
ウシ組織サンプルのレーザー光、深達距離は808nmが980nmより約1.35~1.54倍深い。距離が深くなるほど比率は縮まる。最大侵入深さは770nm~850nmの間
respondsystems.com/wp-content/uploads/2016/04/Penetration-of-808-vs-980.pdf
1000~1100nm
脳組織によって散乱特性、吸収係数は異なり、白脳、灰白質、小脳および脳幹組織(橋、視床)のすべての組織の最も深く到達する波長は、1000~1100nmの間に見出された。
www.ncbi.nlm.nih.gov/pubmed/12118601
heelspurs.com/a/led/skin_great_2005.pdf
神経系への効果に適した波長
ハンブリン博士
赤色~近赤外線 一般的には750nm~1200nmの帯域
※1200nmを超えると遠赤外線効果となり、LLLTの効果とは異なってくる。
おそらくこの間に3つのスゥィートスポットがある。
このスウィートスポットは太陽の特定の波長(スウィートスポットではない波長)が大気中で吸収されることで、生じているのだろう。
Vielight810は 810nm
Zawy氏
ベストは830nm、深達度から考えれば850nmもあたりかも。
www.instructables.com/id/LED-helmet-for-dementia-alzheimers-parkinsons/
エネルギー密度
エネルギー密度とパワー密度によって治療の有効性が大きく異なってくる。
閾値があり低すぎると治療効果は現れず、強すぎると有害な効果が利益を上回ってしまう。
脳以外の組織は、1000mw/cm2あたりが限界
脳への安全限界は 100mW/cm2 あたり ※閾値範囲が他の組織よりも狭い
ちなみに太陽のエネルギー密度はピークが100mw/cm2を超えるぐらいだが
その太陽光に含まれる近赤外線に限ると、全波長の約40%であるため30mw~40mw/cm2 あたりになる。
さらに近赤外線の中の特定の波長に絞るなら、10mw/cm2もないだろう。
閾値内であれば、基本的には単純な計算で算出できる。エネルギー密度が半分であれば、照射時間を倍にすることで、照射量と改善効果はほぼ同じとなる。
ただしエネルギー密度を高めると、浸透度は高まるため、標的部位が照射部位から離れている場合は、高出力で短時間で照射したほうが効果的である可能性がある。
一般的に低出力、長時間照射であるほど有害作用は現れにくくなる。
しかし、あまり出力が弱いと今度はデバイスを一日中つけっぱなしにしておかなければならなくなり、生活の快適さの問題がでてくるため、現実的には10~100mw/cm2あたりが、現実的な頭部への低反応レベルレーザー照射治療のエネルギー密度になるだろう。
Vielight-Infrared 810(Brain)は 14 mw/cm2
Vielightの論文資料によると、ベストな波長のコンセンサスは得られていないため、安全をとって14mwを設定しているらしい。
また、動画内で、ロー・リム博士は、個人的な考えと前置きした上で、閾値内であっても高出力は有害性が増し、改善目的には低出力側で十分でベストだと述べている。
ハンブリン博士
多くの人は過剰にLEDを浴びせすぎている。
おそらく10~20mw/cm2の間が有益性の高い領域だろう。
2mw/cm2、40mw/cm2も、効果があるだろうが、微妙だ。
パワー密度/照射量
一日4~6ジュール/cm2(組織内)が回復のためのベストな用量
100mw/cm2 1ジュール = 10秒
30mw/cm2 1ジュール ≒ 30秒
10mw/cm2 1ジュール = 100秒
頭蓋骨、組織への透過によって内部への照射量は減衰するため、実際の照射量はより多くの時間が必要。数%以下
われわれの祖先は、平均線量一日数百ジュール/cm2の太陽光を浴びていた。
ハンブリン博士
10ジュールが穏当なところだろう。100ジュールは多過ぎる。
2J/cm2でBDNFが有意に増加、
www.jneurosci.org/content/33/33/13505.long
口腔粘膜炎治療 6J/cm2
LLLTの鎮痛効果 用量反応曲線

www.ncbi.nlm.nih.gov/pmc/articles/PMC5436183/
連続波 vs 点滅(パルス)波
生化学的メリット
連続波は経頭蓋への照射には有利と考えられている。
組織の温度
パルス光は連続波と同じエネルギー密度を組織へ照射する場合、連続波よりも組織へもたらす温度上昇が引き起こされないことが示されている。
これは高出力で組織の奥深くへ照射を到達させたい場合には、パルス波が有利となる
www.ncbi.nlm.nih.gov/pubmed/16942425/
生物学的周波数との同調
生物の組織内では数十から数百Hzのなんらかの基本周波数を有している。哺乳類の脳では特定の周波数があることが知られている。
www.ncbi.nlm.nih.gov/pubmed/15011274/
目を閉じている人やリラックスしている人ではアルファ波(8〜13 Hz)が発生する。
www.ncbi.nlm.nih.gov/pubmed/15739111/
目が覚めている、警戒している、または集中している成人ではベータ波(14〜40 Hz)が発生している。
www.ncbi.nlm.nih.gov/pubmed/8047672/
デルタ波(1〜3 Hz)は主に乳児、深い眠りについた成人、または脳腫瘍のある成人に発生する。
www.ncbi.nlm.nih.gov/pubmed/19863262/
シータ波(4〜7 Hz)は、主に2〜5歳の子供、睡眠から覚醒までの間の黄昏状態、または瞑想中に発生する。
www.ncbi.nlm.nih.gov/pubmed/19626355/
光パルスの周波数と脳波の周波数との間で共鳴が生じる可能性は、パルス光を用いた経頭蓋LLLTによる結果のいくつかを説明するかもしれない。
イオンチャネルのゲート開閉
イオンチャネルがLLLTの細胞内作用に関与しているという証拠がいくつか存在する。
イオンチャネルとは、形質膜あるいは内膜系に存在する、イオンを透過させる役割を持つ膜タンパク質である。生体膜を構成する脂質二重膜はイオンをほとんど透過しないため、イオンを膜の内外に透過させるために生体機能に必須のタンパク質であり、バクテリアから高等動物まで、あらゆる細胞に発現している。
イオンチャネルを開閉するための時間スケールは数ミリ秒であることが提案されている。
www.ncbi.nlm.nih.gov/pubmed/16014709/
ミトコンドリアおよび筋細胞膜のカリウムおよびカルシウムイオンチャネルは、LLLTに対する細胞応答に関与している可能性がある。
www.ncbi.nlm.nih.gov/pubmed/15362946/
www.ncbi.nlm.nih.gov/pubmed/18651871
一酸化窒素の光解離
LLLTの作用メカニズムのひとつとして、たんぱく質結合部位から一酸化窒素が光解離するという可能性がある。このプロセスは、連続波である場合NOが同じ部位に再結合される可能性がある。パルス波は、光解離が連続波よりも数多く発生する可能性がある。
www.ncbi.nlm.nih.gov/pubmed/17066004/
比較研究
パルス波と連続波を比較した研究
9件のうち6件がパルス波が連続波よりも効果的であることがわかった。(in vivoでの創傷治療、痛み、虚血性脳卒中、)。パルス波よりも連続波がより効果的である結果を示した報告は9つのうち2つ。(創傷治癒と神経再生)
MITの研究
40Hzパルスによるガンマ波で、(マウスの目に照射)マウス海馬のアミロイドβが40~50%減少。20~80Hzの他のパルスではこの効果は見られなかった。
news.mit.edu/2016/visual-stimulation-treatment-alzheimer-1207
マウスへの外傷性脳損傷治療810nmLLLT照射 100Hzと10Hzの比較では10Hzがより脳内ATPの増加、抗うつ作用に効果的であった。連続波と100Hzでは同レベルの効果。

www.ncbi.nlm.nih.gov/pubmed/22028832/
加齢による海馬および新皮質ネットワークの振動活動の変化。高齢者では課題時のアルファ波(~10Hz)パワーに若年成人では見られなかった変化を示す。
www.ncbi.nlm.nih.gov/pubmed/26688110/
研究者の見解
ハンブリン博士
おそらく有効なパルスの値は10、20、30、40Hzの間だ。40Hzは今の時点ではギャンブル。適切なパルスは連続照射よりも効果があるだろうが、非常に大きな差ではない。
ルー・リム博士(Vielightの開発者)
40Hz ガンマ波 記憶障害、アルツハイマー病臨床試験に。
10Hz アルファ波 一般的な脳の健康
vielight.com/wp-content/uploads/2017/02/Vielight-Inventors-Notes-for-Neuro-Alpha-and-Neuro-Gamma.pdf
Zawy氏
パルス(点滅)について。
懐疑的、パルスのメリットはないという研究も多くある。オンオフの同期を同じ時間間隔で繰り返す場合、照射量が半分になってしまうため、必要量を浴びるためには倍の時間デバイスを装着しなければならないことになる。
パルスは、1~100μ秒の間が理想。さらに言えば、消灯時間の間隔を相対的に短くする。パルスの目的は、デバイスと照射皮膚の発熱を防ぎ、照射エネルギーを増量させることで浸透度を高めることができる。メリットはそれだけ。
www.instructables.com/id/LED-helmet-for-dementia-alzheimers-parkinsons/
照射角
皮膚に直接接触させて照射しているのであれば、光は細胞内で拡散するため、LEDライトの照射角はそれほど大きな影響を及ぼさないであろう。
コヒーレント
比較研究では、LEDのような単色非コヒーレント光が、表面組織の傷などの修復には向いている。
www.ncbi.nlm.nih.gov/pubmed/16144489
しかし、より深部組織になるほどレーザーのような単色非コヒーレントではない光がより効果的に作用する。多くのLLLT研究者は、コヒーレントレーザーよりも波長、パワー密度、エネルギー密度などーパラメーターが、LLLTの効果の重要な決定要因であると考えている。
www.ncbi.nlm.nih.gov/pubmed/22045511
照射レジメ
外傷性脳損傷マウスへのLLLT照射、Cの14日間連続照射したマウスのWGMTテストスコアが一番悪い。Aの4時間後に一回照射、Bの最初の三日間だけ照射のマウスの(28日後経過後)成績がほぼ同レベルの高成績。

www.ncbi.nlm.nih.gov/pubmed/23308226
www.ncbi.nlm.nih.gov/pmc/articles/PMC4189010/
論文では外傷性脳損傷の急性期に、LLLTは有効でありえる、と結ばれている。
照射面積
照射面積は照射効率と組織の浸透率に影響を及ぼしえる。
照射部位による侵入距離
光は骨で遮断されるようなイメージがあるかもしれないが、実際の光の減衰はむしろ少ない。
頭蓋では赤色~近赤外線のスペクトルで15~20%程度の減衰しかなく、光の吸収と散乱も頭蓋照射において最小限を示す。
www.ncbi.nlm.nih.gov/pubmed/20530852/
皮膚、結合組織、筋肉、骨、脊髄などの浸透度が比較的低い組織の層でも、最大28 mm光が浸透することがわかっている。
脳への透過
脳の灰白質、白質では近赤外線の波長が最も透過する。
www.ncbi.nlm.nih.gov/pubmed/18002308/
中枢神経系、末梢神経系の両方の白質部位では近赤外線、可視光線の範囲の波長は短い浸透の深さを示す。対照的に灰白質の浸透率は白質の2倍高い。
www.ncbi.nlm.nih.gov/pubmed/3683777/
10~15Wの810nmの波長の光は、子羊の頭皮からの頭蓋骨、脳組織下3cmで0.45~2.9%が透過した。
www.ncbi.nlm.nih.gov/pubmed/26346298
生物の種による差
ヒトへの850nmの波長浸透度はマウス皮質の3倍高い。
これは、組織の水分とたんぱく質の含有量の違いによって説明されている。
www.ncbi.nlm.nih.gov/pubmed/18002308/
頭部領域による光浸透距離の違い
人間の死体頭部を用いた研究では!
光の浸透が脳の解剖学的な領域によって異なることがわかった。
側頭領域 0.9%
前頭領域 2.1%
後頭領域 11.7%
www.ncbi.nlm.nih.gov/pubmed/23077622
前頭部と後頭部で10倍も差がある…
鼻腔内からの照射は距離だけでなく、組織領域による浸透性の違いもあるかもしれない。
蝶形骨
蝶形骨洞および口腔を介したPBMによる深部脳への光線療法
経頭蓋よりも20倍高い光送達。
www.ncbi.nlm.nih.gov/pubmed/25789711

cancerinfo.tri-kobe.org/pdq/summary/japanese.jsp?Pdq_ID=CDR0000258028
脳部位
脳部位に寄って異なる近赤外線の透過率
すべての組織の最も深く侵入する波長は1000~1100nmの間で見出された。
www.ncbi.nlm.nih.gov/pubmed/12118601
毛髪量・皮膚の色
MPTP障害後のアルビノマウスへの光線療法は、色素性マウスよりも有益な効果を示している。アルビノと比較して、色素性マウスでは頭蓋骨および脳を覆う体毛を通る光の透過が少ないく、体毛によって脳に達する前に光の大部分が吸収されると推定されている。
www.ncbi.nlm.nih.gov/pmc/articles/PMC3616839/
頭髪は近赤外線をほとんどブロックする。毛髪がどの程度近赤外線をブロックするのか、探してみた特にデータは見当たらなかった。
結局、自分でソーラーパワーメーターを買って、頭髪を挟んでLLLTの透過率をあてて調べてみたのだが、毛髪は近赤外線をほとんど遮断してしまうことがわかった。
毛髪促進のLLLTが効果があるのは毛髪同士の隙間から近赤外線が漏れるためであって、毛髪自体はほとんど通さない。
そのため毛髪量にもよるが、毛髪とLEDのちょっとした位置関係により10分の1から100分の1以下にまで減衰してしまう。これだと誤差が大きくて赤外線照射の量を強くして調整するということもむずかしい。
皮膚の色素沈着も脳への光の浸透を制限する可能性がある。理論的にはより高エネルギーの光を用いるか、体毛まはた毛髪を剃ることによって差を埋めることができる。坊主が理想(笑)
毛髪量がある場合、できるだけ髪をかき分けて、つむじを狙ってLEDが直に接するようにするしか方法はなさそうだ。
ビーム形状
レーザービームは密度が不均一のためジュール/cm2計算は正しい表現ではない。
ビームの不均一性が再現性を難しくしている、とのこと。
www.thorlaser.com/LLLT/calculating-LLLT-dosage.htm