Contents
Insulin Degrading Enzyme
概要
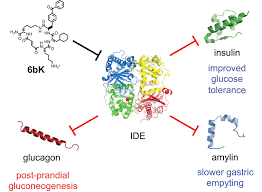
インスリン分解酵素(IDE)の多彩な機能
インスリン分解酵素(IDE)は、インスリン代謝に関与する酵素として発見された。そのため、これまでの研究もほとんどが、糖尿病の発症に関するものとして調査されている。
しかし、アミロイドβ、アミリン、グルカゴンなどのポリペプリドを分解する能力が見出されたことから、この酵素の多機能性(特に神経変性疾患)の役割が浮かび上がってきた。
最近の研究では、IDEが
- 熱ショックタンパク質
- ユビキチンプロテアソーム系の調節
- タンパク質の代謝サイクル
- 細胞ホメオスタシス
- アミロイドタンパク質の切断
- 酸化したタンパク質のユビキチン化
- 神経芽腫の細胞増殖
- ステロイドホルモンシグナル伝達経路への作用
- ヒト腫瘍抗原由来由来のMHCクラスI拘束性エピトープの産生
- 腫瘍抑制因子
などの役割を果たしている可能性があることが示唆されている。
IDEの酵素活性は金属レベルからの影響を受けることから、金属ホメオスタシス(メタロホメオスタシス)の役割も示唆されている。[R][R]
IDEのアミロイドβへの作用
IDEのアミロイドβ阻害作用
IDEは、アミロイドβモノマーのみを切断することができる。
凝集形態は切断できないが、IDEはβシートとの相互作用によりアミロイドβのフィブリル化を阻害することにより毒性効果を無効にする。[R][R][R]
アミロイドβを50%分解
インスリン分解酵素遺伝子を欠損したマウスでは、アミロイドβの分解が50%減少し、脳にアミロイドβの蓄積が生じる。[R]
アミロイドβのオリゴマー化に寄与する!?
アミロイドβのオリゴマー化の阻害は、IDEによってアミロイドβを分解する能力に加えて、断片化したアミロイドβ(フラグメント)をオリゴマー化させる可能性がある。[R]
糖質摂取によって活躍できなくなるIDE
IDEはインスリン分解酵素であるため糖質を大量摂取すると、インスリンの分解に酵素が使われてしまい、アミロイドβの分解に手が回らなくなる。
リコード法における寝る3時間前のカロリー摂取禁止はこの理由による。
ネプリライシン(NEP)とIDE遺伝子の組み合わせリスク
ネプリライシン遺伝子とインスリン分解酵素遺伝子変異の組み合わせは、そうではない個体と比べてアルツハイマー病リスクが3倍増加した。[R]

IDEの機能不全は2型糖尿病と関連
academic.oup.com/edrv/article/19/5/608/2530817
journals.plos.org/plosone/article?id=10.1371/journal.pone.0018138
www.ncbi.nlm.nih.gov/pubmed/24847884
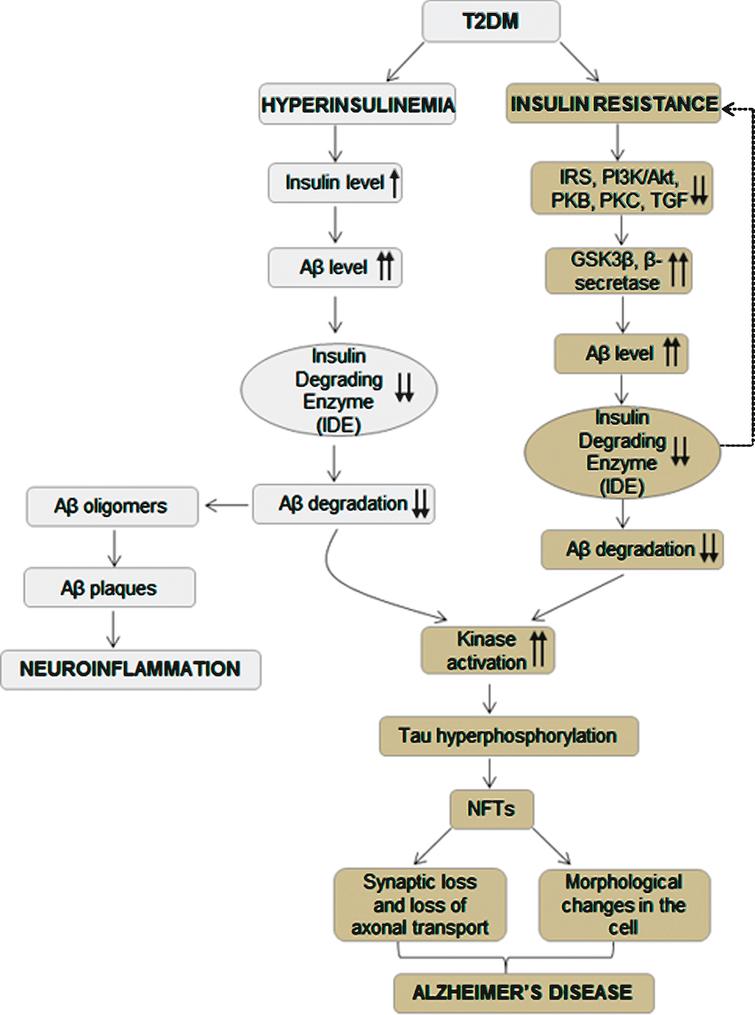
インスリン抵抗性を介したIDE低下およびアルツハイマー病発症機序
2型糖尿病
↓
インスリン抵抗性増加
↓
IRS、PI3K/Akt、PKB、PKC、TGF上昇
↓
アミロイドβ増加
↓
インスリン分解酵素(IDE)の低下
↓
アミロイドβ分解の低下 → インスリン抵抗性の増加(繰り返し)
高インスリン血症を介したIDE低下およびアルツハイマー病発症機序
2型糖尿病
↓
高インスリン血症
↓
インスリンの増加
↓
アミロイドβの増加
↓
インスリン分解酵素の低下
↓
アミロイドβ分解の低下 → アミロイドβオリゴマー → アミロイドβプラーク → 神経炎症
↓
タウの過剰リン酸化 → 神経原線維変化 → シナプス喪失、軸索障害 → アルツハイマー病
content.iospress.com/articles/journal-of-alzheimers-disease/jad150379
IDEとインスリンの相互作用
IDEはインスリンホメオスタシスの重要な要因であると考えられているが、インスリンもまたIDEレベルの維持に寄与する。
海馬ニューロンへのインスリンによる治療は、双方向のフィードバック作用によりIDEレベルを約25%増加させた。[R][R]
インスリン抵抗性と低IDEのネガティブ・フィードバック
2型糖尿病患者に見られるインスリン抵抗性は、より低いIDEレベルをもたらし、同時に2型糖尿病患の進行に寄与する高インスリン状態を維持する。
さらにインスリン受容体の脱感作を増幅させることでインスリンの低代謝サイクルをもたらす。[R]
ユビキチン-プロテアソーム系の調節
IDEの産生および活性の低下は、インスリン、アミリン、アミロイドβなどの多くの天然基質の異常調節に関連する可能性があり、その蓄積は UPSシステム全体の誤動作の原因となる。[R][R]
インスリン分解酵素は20Sプロテアソームのアロステリックモジュレーター。[R]
αシヌクレインの阻害
インスリン分解酵素(IDE)は、αシヌクレインの原繊維形成を阻害する。[R]
インスリン分解酵素IDEはαシヌクレインオリゴマーを補足し、同時にIDEタンパク質分解活性を増加させる。[R]
αシヌクレインへの結合にはIDEのデットエンドの機構が必要な前提条件であるとする仮説が存在する。
シャペロンと類似するIDE
オートファジー-リソソーム経路
アストロサイトからのIDE分泌はオートファジー-リソソーム経路を介して調節されている。[R]
「デッドエンド」シャペロン作用
IDEがデッドエンド(経路上行き着く先のない化合物)のシャペロンとして機能しているという仮説[R]
ヒートショックプロテインとの類似構造
IDEは、αシヌクレイン、アミロイドβ両方のアミロイド形成防止において、HSP(熱ショックプロテイン)の構造と非常に類似したメカニズムを有する。
熱酸化ストレスおよび栄養飢餓など様々なストレス条件下でIDE発現の誘導が示されている。[R][R]
インスリン分解酵素(IDE)の活性
ストレス(運動・サウナ、半日断食)
ヒートショックプロテイン同様、熱ストレス、酸化ストレス、栄養欠乏、DNA損傷などの生理学的ストレスはIDEレベルを顕著にアップレギュレートさせる。[R]
ハーブ・化合物
レスベラトロール
レスベラトロールのは非構造化アミロイドβ42モノマーのIDEによる分解を活性化させるin vitro[R]
ジンセノサイドRg1、Rg3
ジンセノシドRg3はネプリライシンおよびIDEの増加を促進することにより、アミロイドβ分解を促進した。[R]
ジンセノシドRg1は、PPARγをアップレギュレートさせることにより、IDE発現を増加させADマウスのアミロイドβレベルを低下させる。[R]
漢方薬 Kai Xin San
高麗人参などの混合物 Kai Xin Sanが海馬のAβ分解を促進し、IDE発現を増加させ、ラットの海馬ニューロン損傷の緩和につながった。[R]
DHA
DHAは有意に神経細胞のIDEアップレギュレーションを発現させる。[R]
薬理学的介入
スタチン
ロバスタチンによるIDE分泌の増加を介したミクログリア活性による細胞外アミロイドβペプチド分解の促進。[R]
スタチンはアストロサイトからのインスリン分解酵素の分泌を誘導する。[R]
アンドロゲン受容体アゴニスト
アンドロゲン受容体アゴニスト(ACP-105)は、マウスのIDEおよびNEPを活性させレベルの上昇を示した。
酸化窒素シンターゼ(NOS2)も、IDE、NEPの調節に関与することが見出された。
GW742(PPARデルタアゴニスト)
GW472は、ネプリライシンおよびIDE発現の増加を促進する。PPARデルタアゴニストであるGW472が、アミロイドクリアランスおよびアミロイド負荷を軽減させること可能性があることを示唆する。[R]
プロプラノロール
プロプラノロールは、β₁受容体とβ₂受容体を遮断する、アドレナリン作動性効果遮断薬。[R]
プロプラノロールはマウスのIDE、Akt、BDNF発現を促進し、タウの過剰リン酸化を減少させた。[R]
アポモルフィン
アポモルフィンはドーパミン受容体アゴニストの一種でパーキンソン病の治療などに用いられる。
アポモルフィンはIDEの活性介して細胞内のアミロイドβの分解を促進する。[R]
IDE活性因子
ソマトスタチン
ソマトスタチンは直接IDEに作用しIDEの活性を誘導させ、アミロイドβ分解を調節する。[R][R]
レプチン
レプチンはAkt経路の活性によりIDEの発現レベルの高める。[R][R]
PGC1
www.ncbi.nlm.nih.gov/pubmed/23525105
ATP
ATPによるIDE活性化[R]