Contents
Sometimes,happy memories hurt the most.
時として、幸せな記憶が一番痛みを与える。
関連記事
海馬のお勉強、個人的に興味があったものを乱雑にまとめています。
一般的な情報を知りたい方は他のサイトを見てください。
概要
海馬の特徴
海馬細胞は、他の脳部位とくらべても虚血、低酸素、無酸素、ストレスに非常に弱い。海馬はかなり不安定な脳部位。
海馬が情報を素早く情報化する能力を得るために払った代償かもしれない。
アルツハイマー病患者の海馬の神経細胞脱落は、NMDA受容体を介した興奮毒性によるものと考えられている。
海馬の記憶と学習
外の世界を認識する地図(cognitive map)が海馬の中でも形成されているものと推測されている。
海馬体の神経細胞は、さまざまに活性化されるユニットの組み合わせとして働くことで、現在の経験を内部表象している、と考えることもできる。
海馬の内部表象と、大脳皮質にあるより詳細な経験情報の相互作用によって、長期的な記憶が形成されるのだろう。
海馬体の神経細胞がある特定の情報へ選択的に反応するわけではなく、むしろ、行動のすべてを表す内象を一時的に記憶しておく「短期記憶バッファー」として働いていると考えられる。
この内部表象が後に再生されることで、ゆっくりと大脳皮質の長期的な記憶に置き換えられていくのだろう。
海馬部位
歯状回
正確には歯状回は海馬に含まれないが、一般的には歯状回と、海馬(CA1~3)を合わせて「海馬」と呼ばれる。
そこへ海馬台と嗅内野が入ると「海馬体」となる。
大人のマウスで歯状回の神経新生を促進させると、記憶の忘却がすすむ?!
歯状回のソマトスタチン細胞が活性化すると、空間的に離れた顆粒細胞を抑制する。
歯状回の主な入力は、嗅内皮質からのもの。(第Ⅱ層)
皮質下からの入力は、中隔核、乳頭体(視床下部後葉に存在する小さな脳部位)、青斑核、縫線核からのモノアミン系の投射も受けいている。
歯状回に存在する多種な神経細胞がコリン作動性の神経支配を受けているようだ。
歯状回は青斑核からノルアドレナリン性神経の強い神経支配を受けている。
出力は苔状繊維を通してCA3領域のみに投射。
苔状繊維
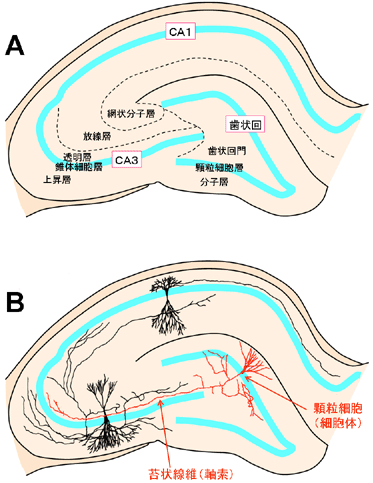
ミエリンを持たない無髄軸索、グルタミン酸を主に放出、GABAも放出するとがわかっている。
歯状回から海馬へ入力する唯一の興奮性繊維
頻回刺激による伝達物質の量が増加、増強率が数倍ある。他のシナプスは1.5倍以下
苔状繊維は生後に作られる。
海馬自体が高い可塑性を持っているが、苔状繊維はさらに高い可塑性を持っている。この高度な可塑性が神経疾患の危険因子となってしまっている。
海馬 錐体細胞層
加齢によりタウタングルが形成される順序
経嗅内野 → 嗅内野 → 海馬支脚 → アンモン角のCA1 → CA3, 4へと広がって行く。(CA2は免れる)
アルツハイマー病患者ではCA1とCA3のニューロン密度が有意に減少している。
www.studyblue.com/notes/note/n/neuro-block-3-week-2/deck/6787953
CA2とCA3の錐体細胞は、海馬の全領域へ投射を行っている。
CA1
アルツハイマー病では、まず嗅内野、海馬台、CA1に変性が見られる。
嗅内皮質のⅢ層にある神経細胞は、CA1や海馬支脚に投射。
その他からの投射場所 中隔核、扁桃体
CA1野は嗅内皮質に情報を戻す最初の海馬部位。
その意味で、歯状回やCA3、CA2とは決定的に性格が異なる。
主に内側嗅内皮質へ投射しているが、一部は外側嗅内皮質へも投射している。
これらの投射の多くは皮質第5層を標的としている
CA2
乳頭体から投射
CA1とCA3に挟まれた部位、CA2領域は誤解を与えやすい部位、名称で、解剖学的にも機能的にも海馬の他の部位とは異なる。
てんかん発作による細胞死が起こりにくい。抵抗性をもつ領域
CA2は小さな環境変化の認識[R]
健忘型MCI患者ではCA2、CA3、海馬台領域が先行して萎縮を示す。[R]
カンナビノイドCB1受容体の活性は、CA2CA3の抗炎症作用をもつ。(CB1受容体の不活性は神経病理を悪化させる)[R]
CA3
海馬のCA3領域は、
嗅内皮質のⅡ層にある神経細胞は、貫通繊維を経由して、歯状回や海馬のCA3領域に投射。 その他、内側中隔核、青班核、縫線核からも投射されている。
CA3野の特徴の一つは、錐体細胞同士が強く相互に連結しあっていること。
この再帰経路は、グルタミン酸作動性であるため、CA3回路はフィードバック興奮経路を含んでいることになる。必然的にCA3回路の挙動は不安定になる。
そもそも、CA3錐体細胞自体はバースト発火を引き起こしやすいこともあり、わずかでも興奮抑制比が崩れると、CA3回路はてんかん様発火を発する。
CA3のてんかん様発火は、CA1やその先の脳領域にまで広がっていく。実際、てんかんの多くタイプでは、CA3野のように再帰回路を含む領域で、興奮と抑制のバランスが崩壊することから生じると信じられている。
抗てんかん薬であるレベチラセタムは、海馬のCA3ニューロンの発火率を抑制、
高齢者でもCA3領域の過剰活性が見られる。
CA4
歯状回門に相当する。
場所細胞 (Place Cell)
bsd.neuroinf.jp/wiki/場所細胞 より抜粋&少し要約
・CA1野、CA3野にある錐体細胞と、歯状回にある顆粒細胞が場所細胞の特性を示す
・海馬CA1野の錐体細胞の30%~50%が、場所特異的な発火をする場所細胞である。
・場所細胞は、同じ環境では明るさと関係なく同一の場所受容野を示す。
・場所細胞の場所受容野は、同じ環境であっても内的な状態(課題の違いなど)が変化すると再配置される。
・場所細胞の発火頻度は、個体の場所、頭の向き、走る速度に依存する。
・睡眠中、特にノンレム睡眠時にも場所細胞は発火する。睡眠時や動かずじっとしている場合の場所細胞の発火パターンは場所に依存しない。
・場所受容野の大きさは、動物種により異なり、個体サイズに合わせて広がる。
・場所受容野は、出発位置から方向と歩数をもとに現在位置を推定しながら目標位置へ進んだ推定位置に対して形成される。
・蓄積される誤差は、ランドマークにより補正される。
・場所受容野は方向依存性を示す。直線走路実験の往復するさい、往路と復路で場所受容野がまったく異なる。
・場所細胞は回想記憶だけでなく、展望記憶、将来行なおうとする行動を想起するための記憶に関連している。
・場所細胞の場所受容野は、外部環境に影響されて動的かつ瞬時に再配置される。CA1野、CA3野、歯状回でその再配置度合いが変化する。
・歯状回は、最もパターン分離能力が高く、外部環境の微妙な変化によっても場所受容野の再構築が起こる。
・CA1野は、外部環境の変化に線形に対応して場所受容野の再構築が起こり、パターン完成能力が高いといえる。
・CA3野に関しては、CA1野と歯状回の中間的な反応をする。
・老齢ラット海馬CA1野の場所細胞は、若齢ラットよりも小さな場所受容野を示す。しかしCA3野では、より大きな場所受容野を示し、発火頻度も高い。 老齢ラットでは、老齢ラットの場所細胞は、すでに体験した親しんだ環境であっても、毎回異なる場所受容野を示す。
・場所細胞の場所情報は、海馬のシナプス上流にある。内側嗅内皮質に場所受容野が格子状になる格子細胞(グリッドセル)がある。海馬に障害を与えると、格子細胞の場所受容野が不安定になる。
・場所細胞は場所だけでなく、時間も表現している。遅延時間が経過すると発火する場所細胞が存在し、海馬の場所に依存しない時間細胞と呼ばれている細胞もある。
海馬と関わる部位
扁桃体
縫線核
セロトニン細胞を多く抱え、神経伝達物質であるセロトニンを分泌する。
乳頭体
障害を受けると長期記憶を形成できなくなり(前方性健忘)と記憶を思い出す(逆行性健忘)ことも難しくなる。
青班核
覚醒状態に関与
内側中隔核
記憶障害、アルツハイマー型認知症に関わる。
障害を受けると物体がどこにあるかわからなくなる。
マイネルト基底核
障害を受けると、対象物が何であるかわからなくなる。
トリシナプティック回路
嗅内野と海馬の閉回路で情報伝達
海馬傍回

海馬の周囲に存在する灰白質の大脳皮質領域。
記号の符号化、検索に重要な役割を持つ。
自然風景や、都市風景(画像でも)を観た時に高い活動を示す。
海馬傍回が損傷をすると、風景の中にある個々の物体、(人や家具など) は認識出来るが、視覚的には風景を認識出来なくなるという症状を、しばしば引き起こす。
顔の認知に対しても特異的に活動する皮質領域。
記憶のシナプス可塑性
短期可塑性
持続時間が数百msから数分続く。
短期可塑性-テタヌス後増強
連発刺激(train of stimuli)に引き続いて起こるシナプス応答の一過性の増大
長期可塑性
海馬のグルタミン酸作動性の興奮性シナプスには30分から数時間にわたって持続する長時間タイプのものも存在する。
シナプスを連発刺激するか、もしくはシナプス前細胞と後細胞を特定の時間パターンで刺激することで誘導される。
長期可塑性-長期増強
誘導相(induction phase)高頻度刺激の時間帯 LTP
LTPが一度形成されてしまえば、数週間は持続する。
発現相(expression phase)誘導相のあとの時間帯
誘導相は数秒から1分程度、発現相は数日になることも。
LTP誘導方法 ・高頻度の刺激 ・シータバースト刺激 ・適切な発火タイミング
βエンドルフィンの分泌、A10神経の活性で、長期記憶が増強する。
長期可塑性-長期抑圧
LTDの逆、シナプス応答が長期的に抑圧される現象。
LTDの発現相も30分から数時間に渡って継続する。
脱増強(depotentiation) LTPを起こしたシナプスに低頻度刺激を与えると、増強分が元に戻る現象。
多くのシナプスにおいて、LTPとLTDの形成にはNMDA受容体の活動が深く関与している。LTPの誘導には刺激されたシナプス付近で細胞内Caイオン濃度が上昇することが必須である。
これはNMDA受容体やCaチャネルを通じてCaイオンが流入することでもたらされる。[R]
ja.wikipedia.org/wiki/%E6%B5%B7%E9%A6%AC_(%E8%84%B3)
www.fujita-hu.ac.jp/ICMS/topics/ngforget/
書籍 「脳をどう蘇らせるか」 岡野栄之
以下引用抜粋
カハールのドグマ
「いったん発育期が終わると、神経系の細胞の成長や再生の源泉は非科学的に枯渇してしまう。」とみなされていた。
しかし、神経幹細胞は成体になっても、主に脳室周囲部に存在し続ける。
・20世紀終わりに、匂いを感じる嗅球と、海馬の歯状回にニューロンが作り続けられる領域があることがわかった。
・ニューロン新生部位、これ以外では通常の条件下ではニューロンが新しく作られることはない。
・神経幹細胞は他でもある。しかし、そういった神経幹細胞でなぜニューロンが作られないかというと、神経幹細胞を取り囲む環境に要因があるから。
・脳が障害を受けると、脳室周囲の神経幹細胞は、活発に分裂するようになる。しかし、効率が悪いため、新しく生まれたニューロンの90%以上がすぐに死んでしまう。
神経の再生過程で起きていること
1 通常は眠っている分裂していない内在性の神経幹細胞の増殖が誘導される。
2 内在性の神経幹細胞から生まれた、より増殖能の高いニューロンの前駆細胞の増殖が活性化 → ニューロン産生
3 前駆細胞から生まれた新生ニューロンが、ケモカインと呼ばれる化学物質の作用により、梗塞周囲へと遊走するように誘導される
4 新しく生まれてきたニューロンはそのほとんどが幼弱なまま短命に終わるが、既存のニューロンとシナプスを作ることによって、これら新生ニューロンの成熟と生存維持をはかることが起きている。
解決案 3つの組み合わ戦略
・細胞増殖因子による幹細胞や前駆細胞の増殖の誘導
※細胞増殖因子 BDNF VEGF IGF-1
・細胞誘引物質の投与による障害部位への新生ニューロンの移動の促進
・栄養因子による細胞の生存を促進する方法
※ドーパミンニューロンを作るような、内在性の神経幹細胞や前駆細胞は見つかっていない。
中枢神経系再生の三位一体アプローチ
1. 神経軸索の再生
- 薬物療法
- セマフォリン3A阻害薬 脊髄を完全に切断したラットに投与→かなり動かせるように[R]
- CSPG分解酵素[R]
- コンドロ一ナーゼABC分解酵素
2. 神経系を構成するための細胞の補充
IPS細胞移植
3. 機能回復
リハビリテーション療法
動物実験では、複数の治療法を組み合わせることが相乗的な治療効果を示す。
組み合わせることが重要! 三位一体アプローチ
海馬新生 代謝経路
・海馬神経細胞の新生 Erk経路とAkt経路、海馬細胞の新生促進には両経路の活性が必要。
・HMG-CoA還元酵素阻害剤(高脂血症治療薬)は細胞内のROSを生成、p38の活性化を高めることで、Erk、Akt経路の活性化を抑制し、アポトーシスを誘導。(FPP、GGPPの減少も含む)
・脳由来神経栄養因子であるBDNFはErk経路
・海馬をグルタミン酸の神経毒から守るにはAkt経路とGSK3βの活性抑制
※PI3K-Akt経路の活性化はがんなどの疾患と関連している。
軸索再生 促進と阻害要因
末梢神経の軸索末端は、成長円錐を形成して再生
中枢神経の軸索末端では、dystrophic endballが出現し軸索再生を阻む。
dystrophic endballは、細胞外因子であるプロテオグリカンによって誘導されている。
軸索再生促進
細胞内 シグナル伝達系 軸索再生促進
JAK-STAT系:gp130 SOCS3↓
RAF-MEK系:B-RAF MEK1↓、MEK2↓ HDAC6?
PI3K-mTOR:PTEN↓
促進因子
cAMP,ATF3,DLK-1
細胞外、軸索再生促進因子
ヘパラン硫酸、CNTF,GDNF、neurotrophin、VEGF
軸索再生阻害
細胞内 軸索再生阻害因子
PTEN,SOCS3,Rho,KLF4,L型Ca2+チャネル
細胞外 軸索再生阻害因子
ミエリン由来タンパク質:Nogo,MAG,OMgp → Rho-Rhoキナーゼ/ROCK
軸索ガイダンスタンパク質:semaphorin,ephrin,slit
プロテオグリカン:コンドロイチン硫酸,ケラタン硫酸[R]
in vivoにおいてケラタン硫酸分解酵素、コンドロイチン硫酸分解酵素の投与により軸索再生および機能の回復が促進[R]
ヒアルロニダーゼがコンドロイチン硫酸を特異的に分解する酵素[R]
海馬過剰活性のリスク
www.ncbi.nlm.nih.gov/pmc/articles/PMC5325620/
海馬活性の2つの仮説
海馬の過剰活性は有害である。
1 海馬のシナプスが(老化により)過剰活性 → アミロイドβの分泌を引きおこす
2 アミロイドβ → 海馬のニューロン活動を過剰活性化させる。
※1,2がお互いに悪循環となるケース
・海馬の活動亢進は、プラーク沈着とは無関係に起こる。(皮質ニューロンの活動亢進はアミロイド班と関連する)
・海馬活性にともなって経時的に記憶力が低下するわけではない。
・縦方向のアミロイドβの蓄積は、経時的に記憶力の低下予測につながる。
脳再生のための必要な栄養因子
- BDNF 脳由来神経栄養因子
- GDNF グリア細胞由来神経栄養因子
- NGF 神経成長因子
- NT-3 ニューロトロフィン-3
- NT-4 ニューロトロフィン-4
- GFL GDNFファミリーリガンド
- NRTN Neurturin ニュールツリン
- ARTN artemin アルテミン
- PSPN persephin ペルセフィン
海馬神経細胞新生に関わる因子
- Akt プロテインキナーゼB
- ERK 細胞外シグナル制御キナーゼ(Extracellular signal-regulated kinase)
- Nrf2 NF-E2-related factor-2
- Wnt3 ウィント3
- BDNF 脳由来神経栄養因子 Brain-derived neurotrophic factor
- GDNF グリア細胞株由来神経栄養因子 Glial-Cell Derived Neurotrophic Factor
- Sirt6 サーチュイン6
- HDAC ヒストン脱アセチル化酵素
- HDACクラス1 HDAC1、2,3,8
- HDACクラス3 SirT1~7
- PI3K PI3キナーゼ
- IGF-1 インスリン様成長因子
- オレキシンA オレキシンB
- Notch1シグナル伝達
- VEGF 血管内皮細胞成長因子
- 5-HT1A受容体
- 5-HT4受容体
- GSK3β グリコーゲン合成酵素キナーゼ3 (阻害)
- Shh ソニック・ヘッジホッグ
- ADAM10 A Disintegrin and Metalloproteinase 10、αセクレターゼ切断を増強
www.longecity.org/forum/topic/52921-best-supplements-to-stimulate-neurotrophic-factors/
BDNF・NGF組み合わせ戦略
BDNFとNGFを組み合わせた治療は、それぞれ単独で行うよりも多くの神経細胞を増殖させる。[R]

www.sciencedirect.com/topics/page/Neurturin